Журнал "Гастроэнтерология" Том 59, №4, 2025
Вернуться к номеру
Мітохондріальні інтеграції в ацинарних клітинах підшлункової залози: міжорганелярна взаємодія як ключовий фактор патогенезу гострого панкреатиту
Авторы: Чуклін С.М. (1), Чуклін С.С. (1), Бариляк Р.В. (2)
(1) - Медичний центр Святої Параскеви, м. Львів, Україна
(2) - Львівська обласна клінічна лікарня, м. Львів, Україна
Рубрики: Гастроэнтерология
Разделы: Справочник специалиста
Версия для печати
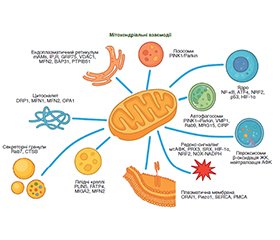
Актуальність. Мітохондрії, традиційно відомі як основні генератори АТФ, відіграють значно ширшу роль у високоспеціалізованих клітинах, зокрема в ацинарних клітинах підшлункової залози (АЦК). Вони є центральними регуляторами клітинного гомеостазу, кальцієвого обміну, окисно-відновного балансу, програмованої загибелі клітин та адаптації до стресу. Ці функції реалізуються не ізольовано, а в контексті складної міжорганелярної мережі. Особливості цих взаємодій набувають критичного значення при розвитку гострого панкреатиту (ГП) — тяжкої запальної патології з високим ризиком ускладнень і летальності. Сучасні дослідження приділяють все більше уваги концепції «мітохондріального хабу», що підкреслює інтегровану роль мітохондрій у клітинних процесах, а не лише їх функцію як ізольованих енергетичних одиниць. Метою цієї статті є аналіз та узагальнення даних щодо складної мережі міжорганелярних взаємодій мітохондрій з іншими клітинними структурами в ацинарних клітинах підшлункової залози з особливим акцентом на їхню роль у патогенезі гострого панкреатиту. Матеріали та методи. Стаття є оглядом сучасної наукової літератури, присвяченої мітохондріальним інтеграціям та їх ролі в патогенезі гострого панкреатиту. Джерела були відібрані з провідних медичних та біологічних баз даних, включаючи PubMed, Scopus та Google Scholar за 2019–2025 роки, а також до дослідження включені окремі фундаментальні публікації. Результати. Аналіз літератури підтвердив, що мітохондрії в АЦК функціонують як інтегрована частина багатокомпонентного «мітохондріального хабу», що включає динамічні взаємодії з ендоплазматичним ретикулумом, лізосомами, пероксисомами та іншими органелами. Показано, що порушення цих взаємодій є критичним фактором у розвитку ГП. Зокрема, дисфункція мітохондріально-ендоплазматичного контакту призводить до порушення кальцієвого гомеостазу та оксидативного стресу, що є ключовими подіями в ініціації панкреатиту. Також підкреслено роль порушень мітофагії та автофагії, які як взаємопов’язані процеси деградації мітохондрій та клітинних компонентів є вирішальними для підтримки клітинного здоров’я в АЦК, а їх порушення сприяє прогресуванню ГП. Виявлено, що активація прозапальних процесів в АЦК, індукована резистином, може бути пригнічена за допомогою α-ліпоєвої кислоти через активацію PPARγ, що посилює експресію HO-1 та каталази, знижуючи рівень активних форм кисню та ІЛ-6. Це свідчить про функціональну інтеграцію антиоксидантного захисту пероксисом і мітохондрій. Крім того, активація PPARγ також пригнічує NF-κB-залежну активацію альвеолярних макрофагів, знижуючи системне запалення, опосередковане екзосомами, що виділяються ушкодженими клітинами підшлункової залози. Висновки. Порушення динамічного балансу в «мітохондріальному хабі», особливо у взаємодії з ендоплазматичним ретикулумом, лізосомами та пероксисомами, є ключовим фактором у патогенезі гострого панкреатиту, сприяючи розвитку запалення, оксидативного стресу та клітинної смерті.
Background. Mitochondria, traditionally known as primary adenosine triphosphate generators, play a significantly greater role in highly specialized cells, particularly in pancreatic acinar cells (PACs). They are central regulators of cellular homeostasis, calcium metabolism, redox balance, programmed cell death, and stress adaptation. These functions are not implemented in isolation but within the context of a complex inter-organelle network. The specific characteristics of these interactions become critically important in the development of acute pancreatitis (AP), a severe inflammatory disorder with a high risk of complications and mortality. Contemporary research increasingly emphasizes the concept of the “mitochondrial hub,” which underscores the integrated role of mitochondria in cellular processes rather than just their function as isolated energetic units. The purpose of this article is to analyze and synthesize data regarding the complex network of inter-organelle interactions of mitochondria and other cellular structures in pancreatic acinar cells, with a particular focus on their role in the pathogenesis of acute pancreatitis. Materials and methods. This article is a review of current scientific literature on mitochondrial integrations and their role in the pathogenesis of acute pancreatitis. Sources were selected from leading medical and biological databases, including PubMed, Scopus, and Google Scholar, for 2019–2025, as well as selected fundamental publications. Results. Literature analysis confirmed that mitochondria in PACs function as an integrated part of a multi-component “mitochondrial hub”, which involves dynamic interactions with the endoplasmic reticulum, lysosomes, peroxisomes, and other organelles. It was shown that disruptions of these interactions are critical factors in the development of AP. In particular, dysfunction of mitochondria-endoplasmic reticulum contact sites leads to impaired calcium homeostasis and oxidative stress, which are key events in the initiation of pancreatitis. The role of dysregulated mitophagy and autophagy, interconnected processes for the degradation of mitochondria and cellular components, was also highlighted as crucial for maintaining cellular health in PACs, and their disruption contributes to AP progression. It was found that the activation of pro-inflammatory processes in PACs, induced by resistin, can be suppressed by α-lipoic acid through the activation of PPARγ, which enhances the expression of HO-1 and catalase, thereby decreasing reactive oxygen species and IL-6 levels. This indicates a functional integration of peroxisomal and mitochondrial antioxidant defense. Furthermore, PPARγ activation also inhibits NF-κB-dependent activation of alveolar macrophages, reducing systemic inflammation mediated by exosomes released from damaged pancreatic cells. Conclusions. Disruption of the dynamic balance within the “mitochondrial hub,” especially in interaction with the endoplasmic reticulum, lysosomes, and peroxisomes, is a key factor in the pathogenesis of acute pancreatitis, contributing to the development of inflammation, oxidative stress, and cell death.
мітохондрії; ацинарні клітини; гострий панкреатит; міжорганелярні взаємодії
mitochondria; acinar cells; acute pancreatitis; inter-organelle interactions
Для ознакомления с полным содержанием статьи необходимо оформить подписку на журнал.
- Iannuzzi JP, King JA, Leong JH, Quan J, Windsor JW, Tanyin–goh D, et al. Global Incidence of Acute Pancreatitis Is Increasing Over Time: A Systematic Review and Meta-Analysis. Gastroenterology. 2022 Jan;162(1):122-134. doi: 10.1053/j.gastro.2021.09.043. Epub 2021 Sep 25. PMID: 34571026.
- Trikudanathan G, Yazici C, Evans Phillips A, Forsmark CE. Diagnosis and Management of Acute Pancreatitis. Gastroenterology. 2024 Sep;167(4):673-688. doi: 10.1053/j.gastro.2024.02.052. Epub 2024 May 15. PMID: 38759844.
- Mihoc T, Latcu SC, Secasan CC, Dema V, Cumpanas AA, Selaru M, et al. Pancreatic Morphology, Immunology, and the Pathogenesis of Acute Pancreatitis. Biomedicines. 2024 Nov 17;12(11):2627. doi: 10.3390/biomedicines12112627. PMID: 39595191.
- Chen X, Zhong R, Hu B. Mitochondrial dysfunction in the pathogenesis of acute pancreatitis. Hepatobiliary Pancreat Dis Int. 2025 Feb;24(1):76-83. doi: 10.1016/j.hbpd.2023.12.008. Epub 2023 Dec 30. PMID: 38212158.
- Casanova A, Wevers A, Navarro-Ledesma S, Pruimboom L. Mitochondria: It is all about energy. Front Physiol. 2023 Apr 25;14:1114231. doi: 10.3389/fphys.2023.1114231. eCollection 2023. PMID: 37179826.
- Zong Y, Li H, Liao P, Chen L, Pan Y, Zheng Y, et al. Mitochondrial dysfunction: mechanisms and advances in therapy. Signal Transduct Target Ther. 2024 May 15;9(1):124. doi: 10.1038/s41392-024-01839-8. PMID: 38744846.
- Habtezion A, Gukovskaya AS, Pandol SJ. Acute Pancrea–titis: A Multifaceted Set of Organelle and Cellular Interactions. Gastroentero–logy. 2019 May;156(7):1941-1950. doi: 10.1053/j.gastro.2018.11.082. Epub 2019 Jan 18. PMID: 30660726.
- Picard M, Shirihai OS. Mitochondrial signal transduction. Cell Metab. 2022 Nov 1;34(11):1620-1653. doi: 10.1016/j.cmet.2022.10.008. PMID: 36323233.
- Katona M, Bartók Á, Nichtova Z, Csordás G, Berezhnaya E, Weaver D, et al. Capture at the ER-mitochondrial contacts licenses IP3 receptors to stimulate local Ca2+ transfer and oxidative metabolism. Nat Commun. 2022 Nov 9;13(1):6779. doi: 10.1038/s41467-022-34365-8. PMID: 36351901.
- Biczo G, Vegh ET, Shalbueva N, Mareninova OA, Elperin J, Lotshaw E, et al. Mitochondrial Dysfunction, Through Impaired Autophagy, Leads to Endoplasmic Reticulum Stress, Deregulated Lipid Metabolism, and Pancreatitis in Animal Models. Gastroenterology. 2018 Feb;154(3):689-703. doi: 10.1053/j.gastro.2017.10.012. Epub 2017 Oct 23. PMID: 29074451.
- Zhang J, Huang W, He Q, Deng T, Wu B, Huang F, et al. PINK1/PARK2 dependent mitophagy effectively suppresses NLRP3 inflammasome to alleviate acute pancreatitis. Free Radic Biol Med. 2021 Apr;166:147-164. doi: 10.1016/j.freeradbiomed.2021.02.019. Epub 2021 Feb 23. PMID: 33636335.
- Walter FR, Harazin A, Tóth AE, Veszelka S, Santa-Maria AR, Barna L, et al. Blood-brain barrier dysfunction in L-ornithine induced acute pancreatitis in rats and the direct effect of L-ornithine on cultured brain endothelial cells. Fluids Barriers CNS. 2022 Feb 17;19(1):16. doi: 10.1186/s12987-022-00308-0. PMID: 35177109.
- Zhou Y, Huang X, Jin Y, Qiu M, Ambe PC, Basharat Z, et al. The role of mitochondrial damage-associated molecular patterns in acute pancreatitis. Biomed Pharmacother. 2024 Jun;175:116690. doi: 10.1016/j.biopha.2024.116690. Epub 2024 May 7. PMID: 38718519.
- Zhu L, Xu Y, Lei J. Molecular mechanism and potential role of mitophagy in acute pancreatitis. Mol Med. 2024 Sep 3;30(1):136. doi: 10.1186/s10020-024-00903-x. PMID: 39227768.
- Manhas N. Computational Model of Complex Calcium Dynamics: Store Operated Ca2+ Channels and Mitochondrial Associated Membranes in Pancreatic Acinar Cells. Cell Biochem Biophys. 2025 Mar;83(1):519-535. doi: 10.1007/s12013-024-01484-6. Epub 2024 Sep 13. PMID: 39266873.
- Park MK, Ashby MC, Erdemli G, Petersen OH, Tepikin AV. Perinuclear, perigranular and sub-plasmalemmal mitochondria have distinct functions in the regulation of cellular calcium transport. EMBO J. 2001 Apr 17;20(8):1863-74. doi: 10.1093/emboj/20.8.1863. PMID: 11296220.
- Chvanov M, Voronina S, Zhang X, Telnova S, Chard R, Ouyang Y, et al. Knockout of the Mitochondrial Calcium Unipor–ter Strongly Suppresses Stimulus-Metabolism Coupling in Pancreatic Acinar Cells but Does Not Reduce Severity of Experimental Acute Pancreatitis. Cells. 2020 Jun 5;9(6):1407. doi: 10.3390/cells9061407. PMID: 32516955.
- Zhang Y, Wu Y, Zhang M, Li Z, Liu B, Liu H, et al. Synergistic mechanism between the endoplasmic reticulum and mitochondria and their crosstalk with other organelles. Cell Death Discov. 2023 Feb 9;9(1):51. doi: 10.1038/s41420-023-01353-w. PMID: 36759598.
- Liu Y, Wei Y, Jin X, Cai H, Chen Q, Zhang X. PDZD8 Augments Endoplasmic Reticulum-Mitochondria Contact and Regulates Ca2+ Dynamics and Cypd Expression to Induce Pancreatic β-Cell Death during Diabetes. Diabetes Metab J. 2024 Nov;48(6):1058-1072. doi: 10.4093/dmj.2023.0275. Epub 2024 Jul 29. PMID: 39069376.
- Li J, Qi F, Su H, Zhang C, Zhang Q, Chen Y, et al. GRP75-faciliated Mitochondria-associated ER Membrane (MAM) Integrity controls Cisplatin-resistance in Ovarian Cancer Patients. Int J Biol Sci. 2022 Apr 11;18(7):2914-2931. doi: 10.7150/ijbs.71571. eCollection 2022. PMID: 35541901.
- Liu J, Wang L, Ge L, Sun W, Song Z, Lu X, et al. Lanthanum decreased VAPB-PTPP51, BAP31-FIS1, and MFN2-MFN1 expression of mitochondria-associated membranes and induced abnormal autophagy in rat hippocampus. Food Chem Toxicol. 2022 Mar;161:112831. doi: 10.1016/j.fct.2022.112831. Epub 2022 Jan 25. PMID: 35090998.
- Pallagi P, Görög M, Papp N, Madácsy T, Varga Á, Crul T, et al. Bile acid- and ethanol-mediated activation of Orai1 dama–ges pancreatic ductal secretion in acute pancreatitis. J Physiol. 2022 Apr;600(7):1631-1650. doi: 10.1113/JP282203. Epub 2022 Feb 17. PMID: 35081662.
- Petersen OH. Specific mitochondrial functions in separate sub-cellular domains of pancreatic acinar cells. Pflugers Arch. 2012 Jul;464(1):77-87. doi: 10.1007/s00424-012-1099-6. Epub 2012 Apr 12. PMID: 22491894.
- Sastre J, Pérez S, Sabater L, Rius-Pérez S. Redox signaling in the pancreas in health and disease. Physiol Rev. 2025 Apr 1;105(2):593-650. doi: 10.1152/physrev.00044.2023. Epub 2024 Sep 26. PMID: 39324871.
- Yuan C, Xu X, Wang N, Zhu Q, Zhang J, Gong W, et al. Paeonol protects against acute pancreatitis by inhibiting M1 macrophage polarization via the NLRP3 inflammasomes pathway. Biochem Biophys Res Commun. 2022 Apr 16;600:35-43. doi: 10.1016/j.bbrc.2022.02.019. Epub 2022 Feb 8. PMID: 35182973.
- Rius-Pérez S, Pérez S, Toledano MB, Sastre J. p53 drives necroptosis via downregulation of sulfiredoxin and peroxiredoxin 3. Redox Biol. 2022 Oct;56:102423. doi: 10.1016/j.redox.2022.102423. Epub 2022 Aug 20. PMID: 36029648.
- Yang X, Zhao K, Deng W, Zhao L, Jin H, Mei F, et al. Apocynin Attenuates Acute Kidney Injury and Inflammation in Rats with Acute Hypertriglyceridemic Pancreatitis. Dig Dis Sci. 2020 Jun;65(6):1735-1747. doi: 10.1007/s10620-019-05892-0. Epub 2019 Oct 15. PMID: 31617131.
- Peng Q, Li B, Song P, Wang R, Jiang J, Jin X, et al. IDH2-NADPH pathway protects against acute pancreatitis via suppressing acinar cell ferroptosis. Br J Pharmacol. 2024 Oct;181(20):4067-4084. doi: 10.1111/bph.16469. Epub 2024 Jul 27. PMID: 39072736.
- Jin HZ, Yang XJ, Zhao KL, Mei FC, Zhou Y, You YD, et al. Apocynin alleviates lung injury by suppressing NLRP3 inflammasome activation and NF-κB signaling in acute pancreatitis. Int Immunopharmacol. 2019 Oct;75:105821. doi: 10.1016/j.intimp.2019.105821. Epub 2019 Aug 19. PMID: 31437787.
- Lee J, Lim JW, Kim H. Lycopene Inhibits IL-6 Expression by Upregulating NQO1 and HO-1 via Activation of Nrf2 in Ethanol/Lipopolysaccharide-Stimulated Pancreatic Acinar Cells. Antioxidants (Basel). 2022 Mar 8;11(3):519. doi: 10.3390/antiox11030519. PMID: 35326169.
- Ma Y, Li X, Liu Z, Xue X, Wang Y, Ma Y. HIF-1α-PPARγ-mTORC1 signaling pathway-mediated autophagy induces inflammatory response in pancreatic cells in rats with hyperlipidemic acute pancreatitis. Mol Biol Rep. 2023 Oct;50(10):8497-8507. doi: 10.1007/s11033-023-08639-3. Epub 2023 Aug 29. PMID: 37644373.
- Park MJ, Iyer S, Xue X, Bragazzi Cunha J, Gu S, Moons D, et al. HIF1-alpha Regulates Acinar Cell Function and Response to Injury in Mouse Pancreas. Gastroenterology. 2018 May;154(6):1630-1634.e3. doi: 10.1053/j.gastro.2018.01.037. Epub 2018 Feb 1. PMID: 29409830.
- Kong L, Deng J, Zhou X, Cai B, Zhang B, Chen X, et al. Sitagliptin activates the p62-Keap1-Nrf2 signalling pathway to alleviate oxidative stress and excessive autophagy in severe acute pancreatitis-related acute lung injury. Cell Death Dis. 2021 Oct 11;12(10):928. doi: 10.1038/s41419-021-04227-0. PMID: 34635643.
- Hamada S, Matsumoto R, Tanaka Y, Taguchi K, Yamamoto M, Masamune A. Nrf2 Activation Sensitizes K-Ras Mutant Pancreatic Cancer Cells to Glutaminase Inhibition. Int J Mol Sci. 2021 Feb 14;22(4):1870. doi: 10.3390/ijms22041870. PMID: 33672789.
- Vanasco V, Ropolo A, Grasso D, Ojeda DS, García MN, Vico TA, et al. Mitochondrial Dynamics and VMP1-Related Selective Mitophagy in Experimental Acute Pancreatitis. Front Cell Dev Biol. 2021 Mar 18;9:640094. doi: 10.3389/fcell.2021.640094. eCollection 2021. PMID: 33816487.
- Mareninova OA, Jia W, Gretler SR, Holthaus CL, Tho–mas DDH, Pimienta M, et al. Transgenic expression of GFP-LC3 perturbs autophagy in exocrine pancreas and acute pancreatitis responses in mice. Autophagy. 2020 Nov;16(11):2084-2097. doi: 10.1080/15548627.2020.1715047. Epub 2020 Jan 16. PMID: 31942816.
- Shen S, Li B, Dai J, Wu Z, He Y, Wen L, et al. BRD4 Inhibition Protects Against Acute Pancreatitis Through Restoring Impaired Autophagic Flux. Front Pharmacol. 2020 May 8;11:618. doi: 10.3389/fphar.2020.00618. eCollection 2020. PMID: 32457617.
- Liu W, Bi J, Ren Y, Chen H, Zhang J, Wang T, et al. Targeting extracellular CIRP with an X-aptamer shows therapeutic potential in acute pancreatitis. iScience. 2023 Jun 7;26(7):107043. doi: 10.1016/j.isci.2023.107043. eCollection 2023 Jul 21. PMID: 37360693.
- Tang H, Yu Q, Chen X, Zhang J, Guo D, Guo W, et al. Phosphoglycerate mutase 5 exacerbates liver ischemia-reperfusion injury by activating mitochondrial fission. Sci Rep. 2024 Apr 12;14(1):8535. doi: 10.1038/s41598-024-58748-7. PMID: 38609411.
- Zhu ZD, Yu T, Liu HJ, Jin J, He J. SOCE induced calcium overload regulates autophagy in acute pancreatitis via calcineurin activation. Cell Death Dis. 2018 Jan 19;9(2):50. doi: 10.1038/s41419-017-0073-9. PMID: 29352220.
- Voronina SG, Barrow SL, Simpson AW, Gerasimenko OV, da Silva Xavier G, et al. Dynamic changes in cytosolic and mitochondrial ATP levels in pancreatic acinar cells. Gastroenterology. 2010 May;138(5):1976-87. doi: 10.1053/j.gastro.2010.01.037. Epub 2010 Jan 25. PMID: 20102715.
- Mukherjee R, Mareninova OA, Odinokova IV, Huang W, Murphy J, Chvanov M, et al. Mechanism of mitochondrial permeability transition pore induction and damage in the pancreas: inhibition prevents acute pancreatitis by protecting production of ATP. Gut. 2016 Aug;65(8):1333-46. doi: 10.1136/gutjnl-2014-308553. Epub 2015 Jun 12. PMID: 26071131.
- Bruce JIE, Sánchez-Alvarez R, Sans MD, Sugden SA, Qi N, James AD, et al. Insulin protects acinar cells during pancreatitis by preserving glycolytic ATP supply to calcium pumps. Nat Commun. 2021 Jul 19;12(1):4386. doi: 10.1038/s41467-021-24506-w. PMID: 34282152.
- Zhang D, Li J, Zhao L, Yang Z, Wu C, Liu Y, et al. Mitochondrial DNA Leakage Promotes Persistent Pancreatic Acinar Cell Injury in Acute Pancreatitis via the cGAS-STING-NF-κB Pathway. Inflammation. 2025 Jun;48(3):1420-1437. doi: 10.1007/s10753-024-02132-0. Epub 2024 Aug 24. PMID: 39180578.
- Deng X, He Y, Miao X, Yu B. ATF4-mediated histone deacetylase HDAC1 promotes the progression of acute pancreatitis. Cell Death Dis. 2021 Jan 4;12(1):5. doi: 10.1038/s41419-020-03296-x. PMID: 33414424.
- Peng F, Deng X. Ubiquitin-specific protease 7 exacerbates acute pancreatitis progression by enhancing ATF4-mediated autophagy. In Vitro Cell Dev Biol Anim. 2025 Mar;61(3):320-330. doi: 10.1007/s11626-024-01009-8. Epub 2025 Jan 28. PMID: 39875698.
- Zhou L, Tan JH, Zhou WY, Xu J, Ren SJ, Lin ZY, et al. P53 Activated by ER Stress Aggravates Caerulein-Induced Acute Pancreatitis Progression by Inducing Acinar Cell Apoptosis. Dig Dis Sci. 2020 Nov;65(11):3211-3222. doi: 10.1007/s10620-020-06052-5. Epub 2020 Jan 23. PMID: 31974911.
- Lee C, Xin G, Li F, Wan C, Yu X, Feng L, et al. Calcium/P53/Ninjurin 1 Signaling Mediates Plasma Membrane Rupture of Acinar Cells in Severe Acute Pancreatitis. Int J Mol Sci. 2023 Jul 17;24(14):11554. doi: 10.3390/ijms241411554. PMID: 37511311.
- Zhao T, Fang R, Ding J, Liu Y, Cheng M, Zhou F, et al. Melatonin ameliorates multiorgan injuries induced by severe acute pancreatitis in mice by regulating the Nrf2 signaling pathway. Eur J Pharmacol. 2024 Jul 15;975:176646. doi: 10.1016/j.ejphar.2024.176646. Epub 2024 May 17. PMID: 38762157.
- Liang X, Hu C, Liu C, Yu K, Zhang J, Jia Y. Dihydrokaempferol (DHK) ameliorates severe acute pancreatitis (SAP) via Keap1/Nrf2 pathway. Life Sci. 2020 Nov 15;261:118340. doi: 10.1016/j.lfs.2020.118340. Epub 2020 Aug 26. PMID: 32860805.
- Niu X, Sun W, Tang X, Chen J, Zheng H, Yang G, et al. Bufalin alleviates inflammatory response and oxidative stress in experimental severe acute pancreatitis through activating Keap1-Nrf2/HO-1 and inhibiting NF-κB pathways. Int Immunopharmacol. 2024 Dec 5;142(Pt A):113113. doi: 10.1016/j.intimp.2024.113113. Epub 2024 Sep 13. PMID: 39276459.
- Gu R, Cui T, Guo Y, Luan Y, Wang X, Liu R, et al. Angiotensin-(1-7) ameliorates intestinal barrier dysfunction by activating the Keap1/Nrf2/HO-1 signaling pathway in acute pancreatitis. Mol Biol Rep. 2023 Jul;50(7):5991-6003. doi: 10.1007/s11033-023-08544-9. Epub 2023 Jun 3. PMID: 37269386.
- Liu Y, Cui H, Mei C, Cui M, He Q, Wang Q, et al. Sirtuin4 alleviates severe acute pancreatitis by regulating HIF-1α/HO-1 mediated ferroptosis. Cell Death Dis. 2023 Oct 21;14(10):694. doi: 10.1038/s41419-023-06216-x. PMID: 37865653.
- Gao T, Zhang H, Xu Y, He G, Ma H, Zheng C, et al. HIF-1α Enhances Intestinal Injury and Inflammation in Severe Acute Pancreatitis Through NLRP3 Inflammasome Activation. Dig Dis Sci. 2025 Feb 25. doi: 10.1007/s10620-025-08926-y. Online ahead of print. PMID: 39998719.
- Rong J, Han C, Huang Y, Wang Y, Qiu Q, Wang M, et al. Inhibition of xanthine oxidase alleviated pancreatic necrosis via HIF-1α-regulated LDHA and NLRP3 signaling pathway in acute pancreatitis. Acta Pharm Sin B. 2024 Aug;14(8):3591-3604. doi: 10.1016/j.apsb.2024.04.019. Epub 2024 Apr 24. PMID: 39220867.
- Wölk M, Fedorova M. The lipid droplet lipidome. FEBS Lett. 2024 May;598(10):1215-1225. doi: 10.1002/1873-3468.14874. Epub 2024 Apr 11. PMID: 38604996.
- Zadoorian A, Du X, Yang H. Lipid droplet biogenesis and functions in health and disease. Nat Rev Endocrinol. 2023 Aug;19(8):443-459. doi: 10.1038/s41574-023-00845-0. Epub 2023 May 23. PMID: 37221402.
- Fan H, Tan Y. Lipid Droplet-Mitochondria Contacts in Health and Disease. Int J Mol Sci. 2024 Jun 22;25(13):6878. doi: 10.3390/ijms25136878. PMID: 38999988.
- Lv J, Ji L, Wang G, Sun B, Tong J. Alcohol Aggravates Acute Pancreatitis by Impairing Autophagic Flux Through Activation of AMPK Signaling Pathway. Dig Dis Sci. 2022 Feb;67(2):524-535. doi: 10.1007/s10620-021-06870-1. Epub 2021 Feb 8. PMID: 33555515.
- Biswas S, Baruah M, Shil A, Sarkar S, Ali M, Samanta A, et al. Polarity-Driven Two-Photon Fluorescent Probe for Monitoring the Perturbation in Lipid Droplet Levels during Mitochondrial Dysfunction and Acute Pancreatitis. ACS Sens. 2023 Oct 27;8(10):3793-3803. doi: 10.1021/acssensors.3c01245. Epub 2023 Oct 10. PMID: 37815484.
- Srinivasan MP, Bhopale KK, Caracheo AA, Kaphalia L, Popov VL, Boor PJ, et al. Dysregulated pancreatic lipid phenotype, inflammation and cellular injury in a chronic ethanol feeding model of hepatic alcohol dehydrogenase-deficient deer mice. Life Sci. 2023 Jun 1;322:121670. doi: 10.1016/j.lfs.2023.121670. Epub 2023 Apr 6. PMID: 37030615.
- Farooq A, Hernandez L, Swain SM, Shahid RA, Romac JM, Vigna SR, et al. Initiation and severity of experimental pancreatitis are modified by phosphate. Am J Physiol Gastrointest Liver Physiol. 2022 Jun 1;322(6):G561-G570. doi: 10.1152/ajpgi.00022.2022. Epub 2022 Mar 16. PMID: 35293263.
- Dolman NJ, Gerasimenko JV, Gerasimenko OV, Voronina SG, Petersen OH, Tepikin AV. Stable Golgi-mitochondria complexes and formation of Golgi Ca(2+) gradients in pancreatic acinar cells. J Biol Chem. 2005 Apr 22;280(16):15794-9. doi: 10.1074/jbc.M412694200. Epub 2005 Feb 18. PMID: 15722348.
- Zierke L, John D, Gischke M, Tran QT, Sendler M, Weiss FU, et al. Initiation of acute pancreatitis in mice is independent of fusion between lysosomes and zymogen granules. Cell Mol Life Sci. 2024 May 6;81(1):207. doi: 10.1007/s00018-024-05247-7. PMID: 38709385.
- Takahashi K, Mashima H, Sekine M, Uehara T, Asano T, Sun-Wada GH, et al. Rab7 localized on zymogen granules is involved in maturation but not in autophagy or regulated exocytosis in pancreatic acinar cells. Sci Rep. 2023 Dec 12;13(1):22084. doi: 10.1038/s41598-023-49520-4. PMID: 38087030.
- Yang Y, Peng Y, Li Y, Shi T, Xu N, Luan Y, et al. Sestrin2 balances mitophagy and apoptosis through the PINK1-Parkin pathway to attenuate severe acute pancreatitis. Cell Signal. 2025 Feb;126:111518. doi: 10.1016/j.cellsig.2024.111518. Epub 2024 Nov 20. PMID: 39577789.
- Mareninova OA, Dillon DL, Wightman CJM, Yakubov I, Takahashi T, Gaisano HY, et al. Rab9 Mediates Pancreatic Autophagy Switch From Canonical to Noncanonical, Aggravating Experimental Pancreatitis. Cell Mol Gastroenterol Hepatol. 2022;13(2):599-622. doi: 10.1016/j.jcmgh.2021.09.017. Epub 2021 Oct 2. PMID: 34610499.
- Gu B, Yu W, Huang Z, Bai J, Liu S, Ren B, et al. MRG15 promotes cell apoptosis through inhibition of mitophagy in hyperlipi–demic acute pancreatitis. Apoptosis. 2025 Feb;30(1-2):149-166. doi: 10.1007/s10495-024-02034-4. Epub 2024 Nov 2. PMID: 39487311.
- Liu W, Ren Y, Wang T, Wang M, Xu Y, Zhang J, et al. Blo–cking CIRP protects against acute pancreatitis by improving mitochondrial function and suppressing pyroptosis in acinar cells. Cell Death Discov. 2024 Mar 27;10(1):156. doi: 10.1038/s41420-024-01923-6. PMID: 38538578.
- Wu SK, Wang L, Wang F, Zhang J. Resveratrol improved mitochondrial biogenesis by activating SIRT1/PGC-1α signal pathway in SAP. Sci Rep. 2024 Oct 31;14(1):26216. doi: 10.1038/s41598-024-76825-9. PMID: 39482340.
- Ali BM, Al-Mokaddem AK, Selim HMRM, Alherz FA, Saleh A, Hamdan AME, et al. Pinocembrin’s protective effect against acute pancreatitis in a rat model: The correlation between TLR4/NF-κB/NLRP3 and miR-34a-5p/SIRT1/Nrf2/HO-1 pathways. Biomed Pharmacother. 2024 Jul;176:116854. doi: 10.1016/j.biopha.2024.116854. Epub 2024 Jun 1. PMID: 38824834.
- Jin H, Zhao K, Li J, Xu Z, Liao S, Sun S. Matrine alleviates oxidative stress and ferroptosis in severe acute pancreatitis-induced acute lung injury by activating the UCP2/SIRT3/PGC1α pathway. Int Immunopharmacol. 2023 Apr;117:109981. doi: 10.1016/j.intimp.2023.109981. Epub 2023 Mar 8. PMID: 37012871.
- Lee Y, Lim JW, Kim H. α-lipoic acid inhibits cerulein/resistin-induced expression of interleukin-6 by activating peroxisome proliferator-activated receptor-γ in pancreatic acinar cells. Mol Med Rep. 2022 Aug;26(2):264. doi: 10.3892/mmr.2022.12780. Epub 2022 Jun 22. PMID: 35730599.
- Hu Q, Yao J, Wu X, Li J, Li G, Tang W, et al. Emodin attenuates severe acute pancreatitis-associated acute lung injury by suppressing pancreatic exosome-mediated alveolar macrophage activation. Acta Pharm Sin B. 2022 Oct;12(10):3986-4003. doi: 10.1016/j.apsb.2021.10.008. Epub 2021 Oct 21. PMID: 36213542.