Вступ
Інсульт залишається провідною причиною інвалідності та смертності в усьому світі, і це означає, що необхідні нові методи лікування та реабілітації [1]. Хоча рандомізовані контрольовані дослідження (РКД) вважаються золотим стандартом клінічних досліджень, їх дизайн оптимізований для внутрішньої оцінки, наприклад для окремо визначених груп пацієнтів. Отже, необхідні подальші дослідження ефективності та безпеки терапевтичних втручань у звичайних клінічних умовах.
Дослідження фази 4 після затвердження та неінтервенційні дослідження набули більшої актуальності завдяки зростанню цінності реальних доказів, доповнюючи дослідження до затвердження [2, 3], надаючи важливі дані про безпеку та ефективність у різних групах пацієнтів у звичайних клінічних умовах [4–6].
Ці дані все частіше використовуються регуляторними органами, органами з оцінки медичних технологій та платниками для сприяння прийняттю обґрунтованих рішень [7, 8]. Дослідження порівняння ефективності (ДПЕ) особливо цінні у випадках інсульту, коли гетерогенність пацієнтів та складність догляду вимагають доказів із клінічної практики [9].
Для забезпечення методологічної надійності таких досліджень було створено кілька структур. Принципи GRACE та Target Trial Emulation Framework (TTEF) надають рекомендації щодо дизайну досліджень, прозорості та аналітичної ретельності в ДПЕ [10, 11]. Вони слугують орієнтирами для побудови високоякісних досліджень, акцентуючи увагу на попередньо визначених протоколах, виборі відповідних груп порівняння, впровадженні стратегій зменшення упередженості та аналізі чутливості [12, 13]. За умови послідовного застосування принципів ДПЕ може запропонувати надійні набори даних, які доповнюють та розширюють дані з РКД [14].
Було продемонстровано, що Церебролізин, нейропептидний препарат з мультимодальною активністю, імітує активність ендогенних нейротрофічних факторів. Таким чином, він сприяє церебропротекції, нейропластичності та нейрогенезу, модулюючи відповідні шляхи передачі сигналів, такі як PI3K/Akt, Sonic Hedgehog та MAPK/ERK. Він поліпшує цілісність гематоенцефалічного бар’єра, зменшує запалення та демонструє ефективність у поліпшенні функціональних, а також когнітивних результатів у моделях інсульту [15–18]. Дослідження Церебролізину та відновлення після інсульту (CARS) продемонструвало вірогідне поліпшення рухової функції та загального результату у пацієнтів, яким проводилося лікування Церебролізином та рухова реабілітація, порівняно з групою плацебо; показник необхідної кількості пацієнтів для лікування в цьому дослідженні становив 7,1 для клінічно вірогідних змін у ранньому неврологічному відновленні [19, 20]. У пацієнтів, які страждали на нефлюентну афазію після інсульту (дослідження ESCAS), лікування Церебролізином призвело до вірогідного поліпшення відновлення мовлення та зменшення неврологічного дефіциту [21]. Метааналізи підтвердили корисний вплив Церебролізину на раннє неврологічне відновлення та безпеку препарату [22–24]. Кілька настанов рекомендують використовувати Церебролізин для нейрореабілітації після інсульту [25, 26]. З огляду на попередні результати метою нашої роботи була оцінка ефективності лікування Церебролізином у реальних умовах у пацієнтів із гострим інсультом середнього ступеня тяжкості.
Матеріали та методи
C-REGS2 було проспективним нерандомізованим відкритим обсерваційним контрольованим дослідженням ефективності, яке відповідало принципам HQCER [27] та GRACE [10], а також додатково охоплювало ключові концептуальні компоненти цільового дослідження [11]. Дослідження поєднувало структурований методологічний підхід із заздалегідь визначеними процедурами аналізу та централізованим моніторингом на основі ризику, а також сліпим впровадженням плану статистичного аналізу та бази даних аналізу незалежною центральною статистичною установою.
Усі зареєстровані пацієнти підписали інформовану згоду. Інтенсивна терапія та Церебролізин призначалися відповідно до місцевих стандартів, не змінювалися протягом дослідження та не зазнавали впливу протоколу дослідження. Супутнє застосування ліків не обмежувалося.
Щоб мінімізувати систематичну помилку та вплив різних факторів, групи пацієнтів були стандартизовані за допомогою непараметричних багаторівневих процедур стратифікації, як рекомендовано в настановах GRACE [10]. Стратифікація верхнього рівня базувалася на діапазоні від 8 до 15 балів за NIHSS [28, 29]. Враховуючи рекомендовану нижню межу включення 8,30, верхню межу технічно довелося встановити на рівні 15, щоб зберегти достатні розміри вибірки.
Для коригування даних щодо віку, наявності діабету та захворювань дрібних судин було проведено стратифікацію другого рівня за допомогою об’єднання Кохрана — Мантеля — Хензеля [28] (рис. 1). Відповідно до принципів ДПЕ для подальшої мінімізації впливу різних факторів було використано обмежений когортний дизайн шляхом виключення пацієнтів з інсультом в анамнезі або з інвалідністю (mRS > 1) [27].
Було проведено формальний непараметричний розрахунок розміру вибірки, хоча оцінки потужності були лише орієнтовними. Розрахунок було налаштовано таким чином, щоб дозволити виявлення малих відмінностей між групами з потужністю 90 %. Розрахований загальний розмір вибірки становив 1745 осіб. Щоб компенсувати звичайні неоднозначності, вибірку було збільшено в 1,15 раза до загальної кількості приблизно 2000 осіб.
Кінцеві точки
Первинною кінцевою точкою був порядковий аналіз mRS на 90-й день після інсульту. Вторинними кінцевими точками були бали за шкалою NIHSS на 21-й та 90-й дні та mRS на 21-й день. Крім того, бали за mRS аналізувалися на предмет наявності відмінного відновлення (mRS 0–1) та функціональної незалежності (mRS 0–2). Для оцінки когнітивного зниження використовували MoCA [31] на 90-й день після інсульту. Були проведені подальші аналізи чутливості, включаючи оцінку найгіршого рангу для відсутніх значень mRS у групі Церебролізину, аналіз нефатальних серйозних побічних ефектів, результат оцінки за MoCA на основі дихотомізованого IQCODE (≤ 3,3 та > 3,3) [32], проведення чи непроведення тромболізису та госпіталізації до інсультного відділення. Що стосується первинних результатів ефективності, то було проведено аналіз коваріації (ANCOVA) з коригуванням на вихідні бали NIHSS як аналіз чутливості (цільова популяція та популяція наміру включення в дослідження (Intention to Include, ITI)). Для порядкових та бінарних даних використовувалася статистика Манна — Вітні (MW) [33–35]. Оцінка переваги проводилася на основі нульової гіпотези про відсутність різниці між групами лікування, з порогами інтерпретації від меншої різниці (MW < 0,5) до більшої ймовірності (MW > 0,5).
Результати наведено у вигляді значень P, а також показників розміру ефекту MW з відповідними довірчими інтервалами [33–36]. Статистику MW також можна виразити в інших поширених показниках розміру ефекту [28, 33, 37], таких як відношення шансів (OR) або кількість пацієнтів, необхідних для лікування.
Для дихотомізованих результатів розраховувалися OR, доповнені розміром ефекту MW для міжрезультатного порівняння [33]. Аналіз безпеки оцінював смертність, побічні ефекти та серйозні побічні ефекти на основі спостережуваних випадків з використанням OR, при цьому на популяції ITI проводилися як аналізи з урахуванням додаткових факторів, так і аналізи чутливості. Для різносторонньої оцінки результатів лікування пацієнтів, що перенесли інсульт, оцінювалися як серйозні, так і незначні побічні ефекти.
Якість даних підтримувалася за допомогою системи електронної форми звіту про випадок (eCRF) із вбудованою валідацією та незалежним централізованим статистичним моніторингом. За згодою ICH E6 (R2), EMA/269011/2013 [38] план статистичного аналізу був доопрацьований та розміщений у репозиторії ISRCTN до блокування бази даних та розкриття інформації про статистику для аналізу. Детальна методологія C-REGS-2 була опублікована раніше [29].
Результати
З квітня 2018 року до грудня 2023 року у дослідженні було зареєстровано 1865 пацієнтів у 16 країнах Європи, Азії, Африки та Південної Америки. Близько 3,2 % зареєстрованих пацієнтів не відповідали критеріям включення до популяції ІТІ. З популяції ІТІ 2,0 % не відповідали критеріям включення до цільової популяції. Таким чином, 94,5 % усіх зареєстрованих пацієнтів були включені до цільової популяції, а 90,0 % зареєстрованих пацієнтів були остаточно включені до попередньо визначеного аналізу. Демографічні та вихідні характеристики проаналізованих пацієнтів наведено в табл. 1. Блок-схема дослідження подана на рис. 2.
Оцінка ефективності
Попередньо запланований аналіз даних за mRS як первинного результату з використанням показника розміру ефекту MW показав статистично вірогідну помірну або середню перевагу лікування Церебролізином порівняно з групою контролю (MW 0,6157; 95% ДІ 0,5910–0,6404; P < 0,0001; I2 = 0,0000; рис. 3).
Щодо відсутніх кінцевих балів за mRS для групи Церебролізину було проведено оцінку найгіршого рангового бала як консервативний підхід чутливості. Результати найгіршого рангового бала впевнено підтвердили первинні результати (P < 0,0001), виключаючи систематичну помилку через передчасне припинення прийому препарату.
Порядковий показник за mRS також був проаналізований щодо раннього відновлення після інсульту (21-й день), що також показало помірну або середню перевагу в групі Церебролізину (MW 0,6065; 95% ДІ 0,5811–0,6319; P < 0,0001; I2 = 0,1696).
Оцінка багаторівнево скоригованої частки пацієнтів з відмінним відновленням на 90-й день у цільовій популяції (target population, TP) (mRS 0–1, TP, OC) показала MW 0,66 (95% ДІ 0,62–0,70; PWei-Lachin < 0,0001; I2 = 0,0000), з отриманим OR [33] 2,74 (95% ДІ 2,12–3,60) на користь Церебролізину. Подібні результати були отримані для частки пацієнтів з функціональною незалежністю (mRS 0–2) з MW 0,67 (95% ДІ 0,63–0,71; PWei-Lachin < 0,0001; I2 = 0,0000) та похідним OR [33] 2,88 (95% ДІ 2,28–3,68).
/15.JPG)
/15_2.jpg)
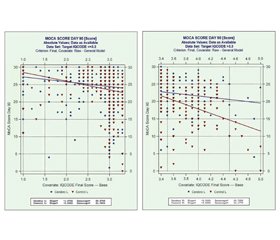
Аналіз показників за NIHSS показав невелику перевагу Церебролізину порівняно з контрольною групою (MW 0,5781; 95% ДІ 0,5561–0,6002; P < 0,0001; I2 = 0,3134; рис. 4) на 90-й день та аналогічний результат на 21-й день (MW 0,5792; 95% ДІ 0,5576–0,6008; P < 0,0001; I2 = 0,3210), що знову ж таки вказує на клінічне поліпшення стану пацієнтів, які отримували Церебролізин, вже на ранніх стадіях одужання. Аналіз шкали MoCA на 90-й день після інсульту продемонстрував невелику, але статистично вірогідну перевагу Церебролізину порівняно з контрольною групою (MW 0,5530; 95% ДІ 0,5282–0,5778; P < 0,0001; I2 = 0,0000; рис. 5). Щоб врахувати когнітивний статус до інсульту, дані MoCA були дихотомізовані, як описано раніше (IQCODE ≤ 3,3 означає, що немає ознак когнітивних порушень до інсульту, IQCODE > 3,3 свідчить про вже існуюче когнітивне зниження) [39]. Бали за MoCA на 90-й день були загалом вищими у пацієнтів з IQCODE ≤ 3,3 (MW 0,5282; 95% ДІ 0,5040–0,5524; P = 0,0222; I2 = 0,0000) порівняно з тими, у кого IQCODE > 3,3 (MW 0,5803; 95% ДІ 0,5306–0,6300; P = 0,0015; I2 = 0,0000; рис. 6). Примітно, що вплив Церебролізину на когнітивні показники був особливо вираженим у підгрупі з ознаками когнітивного дефіциту до інсульту (IQCODE > 3,3), що вказує на те, що ці пацієнти отримали найбільшу користь від лікування з точки зору показників когнітивних функцій.
Аналіз чутливості порівнював показники за mRS через 90 днів після початку інсульту у пацієнтів, яким проводився та не проводився тромболізис (рис. 7, панелі A та B). У групі цільової популяції 17,6 % пацієнтів отримували тромболізис. У групі без тромболізису (82,4 %) ефект лікування Церебролізином був порівнянним з первинним результатом (MW 0,6226; 95% ДІ 0,5943–0,6505; P < 0,0001; I2 = 0,0000; рис. 7, панель A). Слід зазначити, що в групі пацієнтів, які отримували тромболізис, лікування Церебролізином призвело до статистично вірогідної переваги над попередньо визначеною робустною процедурою Вей — Лахіна, незважаючи на значно менший розмір вибірки (MW 0,5723; 95% ДІ 0,5091–0,6354; PWei-Lachin = 0,0248; I2 = 0,3537; рис. 7, панель B).
/16.jpg)
Аналіз пацієнтів, які проходили та не проходили лікування в інсультному відділенні, показав однаковий результат. Серед пацієнтів, які не лікувалися в інсультному відділенні (34,70 %), було продемонстровано помірну або середню перевагу в групі Церебро-лізину (MW 0,6673; 95% ДІ 0,6159–0,7188; P < 0,0001; I2 = 0,0000). Пацієнти, які проходили лікування в інсультному відділенні (65,30 %), демонстрували помірну перевагу у групі Церебролізину (MW 0,5999; 95% ДІ 0,5696–0,6301; P < 0,0001; I2 = 0,0000).
Аналіз безпеки
Не було вірогідних відмінностей між групами щодо випадків смерті, серйозних побічних ефектів та нефатальних серйозних побічних ефектів (усі P ≥ 0,1). Усі аналізи проводилися в популяції наміру включення в дослідження з використанням моделі фіксованих ефектів з поправкою на тяжкість інсульту.
Обговорення
Дослідження C-REGS2 показало, що лікування Церебролізином забезпечувало вірогідне поліпшення функціонального результату через 90 днів після інсульту порівняно зі стандартним лікуванням, що узгоджується з результатами контрольованих клінічних досліджень [19–21]. Виходячи з величини ефектів та їх контрольних значень для вірогідності різниці [37], величина ефекту MW 0,6157 відповідає OR приблизно 2,03 та кількості пацієнтів, необхідних для лікування, 8,64, що свідчить про помірний ефект лікування [40].
Вторинні кінцеві точки, включаючи NIHSS на 21-й та 90-й дні, mRS на 21-й день та категорійні функціональні результати (наприклад, незалежність), продемонстрували результати, що узгоджуються з первинним аналізом. Примітно, що переваги раннього відновлення (21 день), які відповідали попереднім дослідженням [22, 41], вказують на те, що лікування Церебролізином дійсно може пришвидшити темпи відновлення після інсульту.
З огляду на схвалення Церебролізину приблизно в 60 країнах, було розпочато масштабне багатонаціональне обсерваційне контрольоване дослідження ефективності, проведене в реальних умовах. Хоча рандомізовані конт–рольовані дослідження вважаються золотим стандартом клінічних досліджень, обсерваційні дослідження демонструють значну перевагу ширшого відбору пацієнтів та підвищеної зовнішньої валідності [6]. Такі дослідження точніше відображають рутинну клінічну практику, поліпшуючи узагальнення результатів та надаючи цінний набір даних для прийняття рішень регуляторними органами та органами з оцінки медичних технологій.
Однак відсутність рандомізації, суворий відбір пацієнтів та засліплення в обсерваційних дослідженнях можуть призвести до потенційної систематичної похибки [42]. Щоб пом’якшити ці обмеження, C-REGS2 було розроблено відповідно до рекомендацій GRACE [12, 43], забезпечуючи суворі методологічні стандарти. Ключові фактори, що впливають на результати дослідження, такі як захворювання дрібних судин, попередній інсульт, попередня інвалідність, діабет та вік [44], були враховані в попередньо визначеній стратегії стандартизації [29]. Тяжкість інсульту на початковому етапі була врахована шляхом відповідної стратифікації пацієнтів для забезпечення порівнянних когорт пацієнтів [30, 45, 46]. Щоб уникнути ефектів стелі через спонтанне одужання, були включені лише пацієнти з початковим балом за NIHSS 8 і вище.
Була впроваджена централізована система моніторингу на основі ризику, що забезпечувала стабільну якість даних та ретельне спостереження за пацієнтами. Такий підхід призвів до дуже низького рівня відсіву (5,7 %) та високої частки пацієнтів, включених до остаточного аналізу (90 %), мінімізуючи потенційну систематичну похибку відсіву.
Включення понад 1800 пацієнтів з 16 країн світу забезпечує широке представництво клінічних практик, етіології інсульту та систем охорони здоров’я.
Спочатку планувалося використовувати двохетапну адаптивну процедуру за Бауером — Кене [29], але науково-консультативна рада рекомендувала безперешкодний перехід через затримку набору учасників, спричинену пандемією COVID-19. Однак аналіз чутливості, проведений із використанням первинно зазначеної процедури Бауера — Кене, підтвердив, що контроль помилок I типу було забезпечено.
Показник використання тромболізису на рівні 17,6 % (TP) у країнах-учасницях, хоча й нижчий за оптимальні порогові значення, перевищив очікування в багатьох регіонах з низьким та середнім рівнем доходу [47]. Через спостережувану різницю в частоті проведення тромболізису між групами на початковому етапі (21,4 проти 12,4 %) було проведено аналіз чутливості, заснований на принципі порівняння подібних, в якому пацієнти, яким проводився тромболізис, та пацієнти, яким він не проводився, були оцінені як окремі групи. Було показано, що Церебролізин ефективний в обох групах пацієнтів, що свідчить про те, що він пропонує варіант лікування для пацієнтів, які не отримують тромболізис (MW 0,6224, OR 2,11, Number Needed to Treat 8,2), але також може бути корисним як додаткова терапія до тромболізису. Ці результати узгоджуються з метааналізами Борнштайна та ін. [22] та Гюхта та ін. [20], які показують комбінований Number Needed to Treat 7,7 та 7,1 відповідно для клінічно вірогідних змін на ранніх стадіях NIHSS. Для подальшого підтвердження цього спостереження необхідні додаткові рандомізовані дослідження. Подібні результати були отримані для відділень інсульту та загальних лікарень, що підтверджує його роль як життєздатного терапевтичного варіанта в різних умовах гострого інсульту. Підгруповий аналіз 90-денного бала за mRS, стратифікованого за статусом тромболізу, надає чіткі докази стабільності лікування з сильнішим ефектом лікування в групі, яка не отримувала тромболізис. Завдяки конкурентній ефективності тромболізису та Церебролізину добре пояснюються менш виражені результати в групі пацієнтів з тромболізисом.
Постінсультні когнітивні порушення є поширеним наслідком інсульту та можуть суттєво вплинути на результати лікування пацієнтів з інсультом та на стан осіб, які за ними доглядають. Постінсультні когнітивні порушення найбільш поширені протягом першого року після інсульту, їх частота становить до 60 % [48]. Оцінка когнітивних функцій в постінсультному періоді за допомогою MoCA через 90 днів також показала сприятливий вплив Церебролізину, особливо у пацієнтів з підозрою на когнітивне зниження до інсульту (IQCODE > 3,3). Цей висновок добре узгоджується з попередніми дослідженнями, що демонстрували переваги Церебролізину щодо когнітивних функцій [49, 50] у різних групах пацієнтів. З огляду на цей факт подальші дослідження [51–53], спрямовані на вивчення довгострокового впливу Церебролізину на когнітивні показники у пацієнтів після інсульту, тривають, а результати очікуються у 2026 році [21, 54].
Дані щодо безпеки в дослідженні C-REGS2 узгоджувалися з результатами попередніх клінічних досліджень [23] без суттєвих відмінностей у частоті випадків смерті, серйозних побічних ефектів або нефатальних серйозних побічних ефектів між групами Церебролізину та контролю, що підкреслює сприятливий профіль переносимості препарату.
Незважаючи на свої сильні сторони, дослідження C-REGS2 має деякі обмеження, включаючи можливість залишкового поєднання факторів. Хоча в дослідженні дотримувалися принципів GRACE та застосовували передові методи стандартизації для усунення ключових негативних факторів, причинно-наслідкові висновки залишаються більш обмеженими порівняно з рандомізованими контрольованими дослідженнями. Однак основні висновки C-REGS2 відповідали попереднім рандомізованим контрольованим дослідженням, що свідчить про загальну валідність результатів. Усі аналізи чутливості узгоджувалися з первинними результатами, що підкреслює надійність набору даних. Крім того, тривалість лікування та дозування не були стандартизовані та застосовувалися відповідно до місцевих стандартів лікування, що відображає реальні умови. На завершення, ці результати позиціонують C-REGS2 як цінне доповнення до більш конт–рольованих рандомізованих досліджень, а також ще більше підкреслюють додаткову цінність лікування –Церебролізином у разі гострого та підгострого інсульту.
Список литературы
1. GBD 2019 Diseases and Injuries Collaborators. Global, regional, and national burden of stroke and its risk factors, 1990-2019: a systematic analysis for the Global Burden of Disease Study 2019. Lancet Neurol. 2021;20:795-820.
2. U.S. Food & Drug Administration. Real-world evidence. https://www.fda.gov/science-research/science-and-research-special-topics/real-world-evidence (2024, accessed 31 March 2025).
3. (CHMP/MWP) MWP. Reflection paper on use of real-world data in non-interventional studies to generate real-world evidence for regulatory purposes. Amsterdam: European Medicines Agency, 2025.
4. Moore CG, Carter RE, Nietert PJ, et al. Recommendations for planning pilot studies in clinical and translational research. Clin Transl Sci. 2011;4:332-337.
5. Colli A, Fraquelli M, Casazza G, et al. The architecture of diagnostic research: from bench to bedside — research guidelines using liver stiffness as an example. Hepatology. 2014;60:408-418.
6. Fernainy P, Cohen AA, Murray E, et al. Rethinking the pros and cons of randomized controlled trials and observational studies in the era of big data and advanced methods: a panel discussion. BMC Proc. 2024;18:16.
7. Sherman RE, Anderson SA, Dal Pan GJ, et al. Real-world evidence — what is it and what can it tell us? N Engl J Med. 2016;375:2293-2297.
8. Barnish MS, Turner S. The value of pragmatic and observational studies in health care and public health. Pragmat Obs Res. 2017;8:49-55.
9. Williamson P, Altman DG, Bagley H, et al. The COMET Handbook: version 1.0. Trials. 2017;18:280.
10. Dreyer NA, Schneeweiss S, McNeil BJ, et al. GRACE principles: recognizing high-quality observational studies of comparative effectiveness. Am J Manag Care. 2010;16:467-471.
11. Hernn MA, Robins JM. Using big data to emulate a target trial when a randomized trial is not available. Am J Epidemiol. 2016;183:758-764.
12. Dreyer NA, Velentgas P, Westrich K, et al. The GRACE checklist for rating the quality of observational studies of comparative effectiveness: a tale of hope and caution. J Manag Care Spec Pharm. 2014;20:301-308.
13. Acha V, Barefoot B, Juarez Garcia A, et al. Principles for good practice in the conduct of non-interventional studies: the view of industry researchers. Ther Innov Regul Sci. 2023;57:1199-1208.
14. Dreyer NA, Tunis SR, Berger M, et al. Why observational studies should be among the tools used in comparative effectiveness research. Health Aff. 2010;29:1818-1825.
15. Zhang C, Chopp M, Cui Y, et al. Cerebrolysin enhances neurogenesis in the ischemic brain and improves functional outcome after stroke. J Neurosci Res. 2010;88:3275-3281.
16. Chen H, Tung YC, Li B, et al. Trophic factors counteract ele–vated FGF-2-induced inhibition of adult neurogenesis. Neurobiol –Aging. 2007;28:1148-1162.
17. Teng H, Li C, Zhang Y, et al. Therapeutic effect of Cerebrolysin on reducing impaired cerebral endothelial cell permeability. Neuroreport. 2021;32:359-366.
18. Zhang L, Chopp M, Meier DH, et al. Sonic hedgehog signaling pathway mediates Cerebrolysin-improved neurological function after stroke. Stroke. 2013;44:1965-1972.
19. Muresanu DF, Heiss WD, Hoemberg V, et al. Cerebrolysin and Recovery After Stroke (CARS): a randomized, placebo-controlled, double-blind, multicenter trial. Stroke. 2016;47:151-159.
20. Guekht A, Vester J, Heiss WD, et al. Safety and efficacy of Cerebrolysin in motor function recovery after stroke: a meta-analysis of the CARS trials. Neurol Sci. 2017;38:1761-1769.
21. Homberg V, Jianu DC, Stan A, et al. Speech therapy combined with Cerebrolysin in enhancing nonfluent aphasia recovery after acute ischemic stroke: ESCAS randomized pilot study. Stroke. 2025;56:937-947.
22. Bornstein NM, Guekht A, Vester JC, et al. Safety and efficacy of Cerebrolysin in early post-stroke recovery: a meta-analysis of nine randomized clinical trials. Neurol Sci. 2017;39:629-640.
23. Strilciuc S, Vcsei L, Boering D, et al. Safety of Cerebrolysin for neurorecovery after acute ischemic stroke: a systematic review and meta-analysis of twelve randomized-controlled trials. Pharmaceuticals. 2021;14:1297.
24. Brainin M. Cerebrolysin: a multi-target drug for recovery after stroke. Expert Rev Neurother. 2018;18:681-687.
25. Beghi E, Binder H, Birle C, et al. European Academy of Neurology and European Federation of Neurorehabilitation Socie–ties guideline on pharmacological support in early motor rehabilitation after acute ischaemic stroke. Eur J Neurol. 2021;28:2831-2845.
26. Neurorehabilitation DGf. S3-Leitlinie: Rehabilitative Therapie bei Armparese nach Schlaganfall. Report no. AWMF-Registernummer 080/001, 2021. Berlin: AWMF.
27. Williams CM, Skinner EH, James AM, et al. Comparative effectiveness research for the clinician researcher: a framework for making a methodological design choice. Trials. 2016;17:406.
28. Colditz GA, Miller JN, Mosteller F. Measuring gain in the evaluation of medical technology. The probability of a better outcome. Int J Technol Assess Health Care. 1988;4:637-642.
29. Vester J, Bornstein N, Heiss WD, et al. C-REGS 2 — design and methodology of a high-quality comparative effectiveness observational trial. J Med Life. 2021;14:700-709.
30. DeGraba TJ, Hallenbeck JM, Pettigrew KD, et al. Progression in acute stroke: value of the initial NIH stroke scale score on patient stratification in future trials. Stroke. 1999;30:1208-1212.
31. Nasreddine ZS, Phillips NA, Bdirian V, et al. The Montreal Cognitive Assessment, MoCA: a brief screening tool for mild cognitive impairment. J Am Geriatr Soc. 2005;53:695-699.
32. Quinn TJ, Fearon P, Noel-Storr AH, et al. Informant Questionnaire on Cognitive Decline in the Elderly (IQCODE) for the diagnosis of dementia within community dwelling populations. Cochrane Database Syst Rev. 2014;4:CD010079.
33. Rahlfs VW, Zimmermann H, Lees KR. Effect size measures and their relationships in stroke studies. Stroke. 2014;45:627-633.
34. D’Agostino RB, Campbell M, Greenhouse J. The Mann-Whitney statistic: continuous use and discovery. Stat Med. 2006;25:541-542.
35. Kieser M, Friede T, Gondan M. Assessment of statistical significance and clinical relevance. Stat Med. 2013;32:1707-1719.
36. Munzel U, Hauschke D. A nonparametric test for proving noninferiority in clinical trials with ordered categorical data. Pharm Stat. 2003;2:31-37.
37. Rahlfs V, Zimmermann H. Effect size measures and their benchmark values for quantifying benefit or risk of medicinal products. Biom J. 2019;61:973-982.
38. ICH. Statistical principles for clinical trials. ICH topic E9. Report no. CPMP/ICH/363/96, 1998. London: European Medicines Agency (EMA).
39. Hnon H, Pasquier F, Durieu I, et al. Preexisting dementia in stroke patients. Baseline frequency, associated factors, and outcome. Stroke. 1997;28:2429-2436.
40. Davis MP, Vanenkevort E. Understanding the number needed to treat. J Pain Symptom Manage. 2024;68:e190-e193.
41. Lang W, Stadler CH, Poljakovic Z, et al. A prospective, randomized, placebo-controlled, double-blind trial about safety and efficacy of combined treatment with alteplase (rt-PA) and Cerebrolysin in acute ischaemic hemispheric stroke. Int J Stroke. 2013;8:95-104.
42. Anglemyer A, Horvath HT, Bero L. Healthcare outcomes assessed with observational study designs compared with those assessed in randomized trials. Cochrane Database Syst Rev. 2014;2014:MR000034.
43. Bryant AS, Mendelsohn AB, Viswanathan S, et al. What impacts the quality of comparative-effectiveness research: a classification and regression tree analysis using the GRACE checklist. Value Health. 2016;19:A277.
44. Johnston KC, Connors AF, Jr, Wagner DP, et al. A predictive risk model for outcomes of ischemic stroke. Stroke. 2000;31:448-455.
45. Wouters A, Nysten C, Thijs V, et al. Prediction of outcome in patients with acute ischemic stroke based on initial severity and improvement in the first 24 h. Front Neurol. 2018;9:308.
46. Heiss WD, Brainin M, Bornstein NM, et al. Cerebrolysin in patients with acute ischemic stroke in Asia: results of a double-blind, placebo-controlled randomized trial. Stroke. 2012;43:630-636.
47. Khatib R, Arevalo YA, Berendsen MA, et al. Presentation, evaluation, management, and outcomes of acute stroke in low- and middle-income countries: a systematic review and meta-analysis. Neuroepidemiology. 2018;51:104-112.
48. Ihle-Hansen H, Thommessen B, Wyller TB, et al. Incidence and subtypes of MCI and dementia 1 year after first-ever stroke in patients without pre-existing cognitive impairment. Dement Geriatr Cogn Disord. 2011;32:401-407.
49. Al-Kuraishy HM, Al-Gareeb AI, Zekry SH, et al. The possible role of cerebrolysin in the management of vascular dementia: levera–ging concepts. Neuroscience. 2025;568:202-208.
50. Guekht AB, Moessler H, Novak PH, et al. Cerebrolysin in vascular dementia: improvement of clinical outcome in a randomized, double-blind, placebo-controlled multicenter trial. J Stroke Cerebrovasc Dis. 2011;20:310-318.
51. Cramer SC, Richards LG, Bernhardt J, et al. Cognitive deficits after stroke. Stroke. 2023;54:5-9.
52. Rost NS, Brodtmann A, Pase MP, et al. Post-stroke cognitive impairment and dementia. Circ Res. 2022;130:1252-1271.
53. El Husseini N, Katzan IL, Rost NS, et al. Cognitive impairment after ischemic and hemorrhagic stroke: a scientific statement from the American Heart Association/American Stroke Association. Stroke. 2023;54:e272-e291.
54. Rosu OV. Can treatment with Cerebrolysin improve recovery after acute ischemic stroke? https://www.isrctn.com/ISRCTN88122184.
Оригінал статті опубліковано в
International Journal of Stroke 2025, Vol. 20(9), 1060–1070
/13.jpg)

/14.jpg)
/14_2.jpg)
/15.JPG)
/15_2.jpg)
/16.jpg)
/17.JPG)