Архив офтальмологии Украины Том 13, №3, 2025
Вернуться к номеру
Предиктори клінічного перебігу неоваскулярної глаукоми після оклюзії вен сітківки
Авторы: Гузун О.В., Задорожний О.С., Величко Л.М., Богданова О.В., Король А.Р.
ДУ «Інститут очних хвороб і тканинної терапії ім. В.П. Філатова НАМН України», м. Одеса, Україна
Рубрики: Офтальмология
Разделы: Клинические исследования
Версия для печати
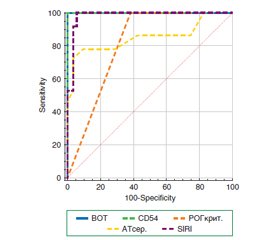
Актуальність. Оклюзія вен сітківки (ОВС) викликає ішемію та запалення внаслідок порушення перфузії сітківки та появи інтраретинальних крововиливів. Ішемія, експресія запальних цитокінів, зниження швидкості кровотоку в сітківці призводять до неоваскуляризації та розвитку неоваскулярної глаукоми (НВГ). Метою дослідження була оцінка прогностичної цінності експресії молекули міжклітинної адгезії-1 (ICAM-1/CD54) та індексу системної запальної реакції (SIRI) у пацієнтів із болючою неоваскулярною глаукомою, що виникла вторинно внаслідок ОВС. Матеріал та методи. У дослідження було включено 52 пацієнти з НВГ, вторинною до ОВС, та 36 здорових людей. Усім досліджуваним особам виконували візометрію, біомікроскопію, офтальмоскопію, гоніоскопію, вимірювання внутрішньоочного тиску (ВОТ). У зразках периферичної крові оцінювали індекс SIRI та експресію ICAM-1/CD54. Методом реоофтальмографії у всіх випадках визначали параметри внутрішньоочного об’ємного кровообігу (показник RQ). Пацієнтам з НВГ було проведено анкетування за числовою рейтинговою шкалою болю (Numericrating Scale for pain, NRS). Результати. Кількісні показники лейкоцитів (р = 0,003), нейтрофілів (р < 0,001), SIRI (р < 0,001), рівня CD54 (р < 0,001) були значно вищими, а кількість лімфоцитів (р < 0,001) була значно нижчою у пацієнтів з НВГ та ОВС. Значення показника RQ на очах з НВГ у 67,3 % пацієнтів визначалися як критичні. Були виявлені прямі кореляції (р < 0,05) між ВОТ та даними показників CD54 (rs = 0,63), SIRI (rs = 0,73), критичними показниками RQ (rs = 0,69), середнім артеріальним тиском (АТсер.; rs = 0,56), а також з інтенсивністю болю за NRS (rs = 0,79). Висновки. Було визначено, що у хворих з НВГ внаслідок ОВС комплекс показників SIRI, CD54, АТсер., RQ є предиктором тяжкості захворювання. Стан, при якому показники SIRI, CD54, АТсер. вище порогових значень (SIRI > 0,54; CD54 > 247 кл/мкл; АТсер. > 95 мм рт.ст.), а RQ ≤ 2,4 ‰ або RQ ≥ 4,3 ‰ у хворих з НВГ, вторинною до ОВС, асоційований з високим ВОТ (> 33 мм рт.ст.) та сильним очним болем за NRS.
Background. Retinal vein occlusion (RVO) induces ischemia and inflammation due to impaired retinal perfusion and the development of intraretinal hemorrhages. Ischemia, expression of inflammatory cytokines, and reduced retinal blood flow lead to neovascularization and the progression of neovascular glaucoma (NVG). The aim of this study was to evaluate the prognostic value of intercellular adhesion molecule-1 (ICAM-1/CD54) expression and the systemic inflammation response index (SIRI) in patients with painful NVG secondary to RVO. Materials and methods. The study included 52 patients with NVG secondary to RVO and 36 healthy individuals. All participants underwent visual acuity testing, biomicroscopy, ophthalmoscopy, gonioscopy, and intraocular pressure measurement. Peripheral blood samples were analyzed to determine SIRI and the ICAM-1/CD54 expression. In all cases, intraocular volumetric blood flow parameters (RQ) were measured using rheoophthalmography. Patients with NVG were additionally assessed using the Numeric Rating Scale for pain. Results. Leukocyte count (p = 0.003), neutrophils (p < 0.001), SIRI (p < 0.001), and CD54 level (p < 0.001) were significantly higher, while lymphocyte count (p < 0.001) was significantly lower in patients with NVG and RVO compared to controls. RQ in 67.3 % of NVG eyes was classified as critical. Direct correlations (p < 0.05) were found between intraocular pressure and CD54 levels (rs = 0.63), SIRI (rs = 0.73), critical RQ (rs = 0.69), mean arterial pressure (MAP) (rs = 0.56), and pain intensity on the Numeric Rating Scale (rs = 0.79). Conclusions. In patients with NVG secondary to RVO, the combined parameters SIRI, CD54, MAP, and RQ serve as predictors of disease severity. A condition characterized by SIRI, CD54, and MAP above threshold levels (SIRI > 0.54; CD54 > 247 cells/μL; MAP > 95 mmHg) and RQ ≤ 2.4 ‰ or ≥ 4.3 ‰ is associated with elevated intraocular pressure (> 33 mmHg) and severe ocular pain on the Numeric Rating Scale.
неоваскулярна глаукома; оклюзія вен сітківки; молекула міжклітинної адгезії-1; індекс системної запальної відповіді; внутрішньоочний об’ємний кровообіг
neovascular glaucoma; retinal vein occlusion; intercellular adhesion molecule-1; systemic inflammation response index; intraocular volumetric blood flow
Для ознакомления с полным содержанием статьи необходимо оформить подписку на журнал.
- Behzadian MA, Wang XL, Windsor LJ, Ghaly N, Caldwell RB. TGF-β increases retinal endothelial cell permeability by increasing MMP-9: Possible role of glial cells in endothelial barrier function. Investigative Ophthalmology & Visual Science. 2001;42(3):853-859.
- Noma H, Funatsu H, Mimura T, Harino S, Hori S. IL-6 and VEGF in macular edema with CRVO. Ophthalmology. 2009;116:87-93. https://doi.org/10.1016/j.ophtha.2008.09.034.
- Yang J, et al. Mechanistic pathogenesis of endothelial dysfunction in diabetic retinopathy: Role of VEGF and NF-κB signalling. Frontiers in Endocrinology. 2022;13:816400. https://doi.org/10.3389/fendo.2022.816400.
- Noma H, Mimura T, Tatsugawa M, Shimada K. Aqueous flare and inflammatory factors in CRVO. BMC Ophthalmology. 2013;13:78. https://doi.org/10.1186/1471-2415-13-78.
- Michelson G, Harazny J. Increased vascular resistance for venous outflow in CRVO. Ophthalmology. 1997;104:659-663. https://doi.org/10.1016/S0161-6420(97)30255-3.
- Horio N, Horiguchi M. Retinal blood flow and macular edema after radial optic neurotomy for CRVO. American Journal of Ophthalmology. 2006;141:31-34. https://doi.org/10.1016/j.ajo.2005.08.015.
- Crama N, Gualino V, Restori M, Charteris DG. Central re–tinal vessel blood flow after surgical treatment for central retinal vein occlusion. Retina. 2010;30:1692-1697. https://doi.org/10.1097/IAE.0b013e3181d8e7e8.
- Noma H, Funatsu H, Mimura T, Shimada K. Perifoveal microcirculation in RVO. Open Ophthalmology Journal. 2012;6:63-64. https://doi.org/10.2174/1874364101206010063.
- Noma H, Funatsu H, Sakata K, et al. sICAM-1 and macular edema in RVO. Graefe’s Archive for Clinical and Experimental Ophthalmology. 2010;248:1515-1518. https://doi.org/10.1007/s00417-010-1350-9.
- Noma H, Yasuda K, Mimura T, Ofusa A, Shimura M. Cytokines and retinal blood flow in CRVO. BMC Ophthalmology, 2020;20:215. https://doi.org/10.1186/s12886-020-01486-x.
- Noma H, Yasuda K, Mimura T, Suganuma N, Shimura M. Predictors for recurrence of macular edema in BRVO. Journal of Clinical Medicine. 2020;10:58. https://doi.org/10.3390/jcm10010058.
- Guzun OV, Zadorozhnyy OS, Vychuzhanin VV, Khramen–ko NI, Velichko LM, et al. A neural network model for predicting the effectiveness of treatment in patients with neovascular glaucoma associated with diabetes mellitus. Romanian Journal of Ophthalmology. 2024;68(3):294-300. https://doi.org/10.22336/rjo.2024.53.
- Guzun OV, Zadorozhnyy OS, Velychko LM, Bogdanova OV, Dumbrăveanu LG, Cuşnir VV, et al. The effect of intercellular adhesion molecule-1 and glycated haemoglobin on management of diabetic neovascular glaucoma. Romanian Journal of Ophthalmology. 2024;68(2):135-142. https://doi.org/10.22336/rjo.2024.25.
- Hawker GA, Mian S, Kendzerska T, French M. Measures of adult pain: VAS, NRS, MPQ, SF-MPQ, CPGS, SF-36 BPS, ICOAP. Arthritis Care & Research. 2011;63(Suppl 11):S240-S252. https://doi.org/10.1002/acr.20543.
- Vaidya R, Washington A, Stine S, Geamanu A, Hudson I. The IPA: A modified numerical system for pain assessment and intervention. JAAOS Global Research & Reviews. 2021;5(9):e21.00174. https://doi.org/10.5435/JAAOSGlobal-D-21-00174.
- Kolar P. Risk factors for central and branch retinal vein occlusion: A meta-analysis. Journal of Ophthalmology. 2014;2014:724780. https://doi.org/10.1155/2014/724780.
- Kazantzis D, Machairoudia G, Kroupis C, Theodossiadis G, Theodossiadis P, Chatziralli I. Complete blood count-derived inflammation indices and retinal vein occlusion. Ophthalmology and Therapy. 2022;11:1241-1249. https://doi.org/10.1007/s40123-022-00511-0.
- Wang X, Wang L, Li X, Liu S, Liu B. Characteristics of hematologic parameters in young patients with retinal vein occlusion. Ophthalmic Research. 2023;66(1):1096-1103. https://doi.org/10.1159/000531824.
- Wei L, Mao S, Liu X, Zhu C. Systemic inflammation index and mortality in CKD. Frontiers in Cardiovascular Medicine, 2024;11:1363949. https://doi.org/10.3389/fcvm.2024.1363949.
- Rayes J, Bourne JH, Brill A, Watson SP. Platelet-immune cell interactions in thromboinflammation. Research and Practice in Thrombosis and Haemostasis. 2020;4:23-35. https://doi.org/10.1002/rth2.12266.
- Zhou Y, Qi J, Liu H, Liang S, Guo T, Chen J, et al. Increased intraocular inflammation in retinal vein occlusion is independent of circulating immune mediators and contributes to retinal oedema. Frontiers in Neuroscience. 2023;17:1186025. https://doi.org/10.3389/fnins.2023.1186025.
- Papadopoulos N, et al. ICAM-1 as a therapeutic target. International Journal of Molecular Sciences. 2020;21(14):4868. https://doi.org/10.3390/ijms21144868.
- Lu M, Perez VL, Ma N, Miyamoto K, Peng HB, Liao JK, et al. VEGF increases retinal vascular ICAM-1 expression in vivo. Investigative Ophthalmology & Visual Science. 1999;40(8):1808-1812.
- Yue T, Shi Y, Luo S, Weng J, Wu Y, Zheng X. Inflammation in diabetic retinopathy: Molecular mechanisms and therapeutic implications. Frontiers in Immunology. 2022;13:1055087. https://doi.org/10.3389/fimmu.2022.1055087.
- Pham K, Parikh K, Heinrich EC. Hypoxia and inflammation: Insights from high-altitude physiology. Frontiers in Physiology. 2021;12:676782. https://doi.org/10.3389/fphys.2021.676782.
- Rohowetz LJ, Kraus CL, Koulen P. Inflammation and adhesion molecules in retinal ischemia. Experimental Eye Research. 2018;176:140-149. https://doi.org/10.1016/j.exer.2018.07.017.
- Yoshimura T, Sonoda KH, Sugahara M, et al. Comprehensive analysis of inflammatory immune mediators in vitreoretinal disea–ses. PLoS One. 2009;4(12):e8158. https://doi.org/10.1371/journal.pone.0008158.
- Wang B, Zhang X, Chen H, Koh A, Zhao C, Chen Y. Intraocular biomolecules in retinal vein occlusion: Toward potential biomarkers. Frontiers in Pharmacology. 2022;13:859951. https://doi.org/10.3389/fphar.2022.859951.
- Zhang Y, Xing Z, Zhou K, Jiang S. Predictive role of SIRI in stroke prognosis. Clinical Interventions in Aging. 2021;16:1997-2007. https://doi.org/10.2147/CIA.S339221.
- Han Y, Lin N. Systemic inflammatory response index and functional outcome after acute ischemic stroke: A meta-analysis. Neurology and Therapy. 2024;13:1431-1451. https://doi.org/10.1007/s40120-024-00645-2.
- Zhu F, Wang Z, Song J, et al. Inflammatory markers and short-term prognosis of acute ischemic stroke. Scientific Reports. 2024;14:17772. https://doi.org/10.1038/s41598-024-66279-4.
- Strieter RM, Gomperts BN, Keane MP. The role of CXC chemokines in pulmonary fibrosis. Journal of Clinical Investigation. 2007;117(3):549-556. https://doi.org/10.1172/JCI30562.
- Chono I, Miyazaki D, Miyake H, Komatsu N, Ehara F, et al. High IL-8 in aqueous humor predicts poor prognosis in glaucoma. Scientific Reports. 2018;8(1):14533. https://doi.org/10.1038/s41598-018-32725-3.
- Zadorozhnyy O, Guzun O, Kustryn T, Nasinnyk I, Chechin P, Korol A. Targeted transscleral laser photocoagulation of the ciliary body in NGV. Journal of Ophthalmology (Ukraine). 2019;4:3-7. https://doi.org/10.31288/oftalmolzh2019437.
- Guzun O, Zadorozhnyy O, Nasinnyk I, & Korol A. Efficacy of modified diode transscleral cyclophotocoagulation in painful neovascular glaucoma secondary to RVO. Journal of Ophthalmology (Ukraine). 2025;3:3-10. https://doi.org/10.31288/oftalmolzh20253310.