Журнал «Здоровье ребенка» Том 21, №1, 2026
Вернуться к номеру
Клінічний та епідеміологічний профіль токсоплазмозу в імунокомпетентних дітей: ретроспективне дослідження з лікарні третинного рівня в Індонезії
Авторы: Ayu Dewi Yuliawati, Dwiyanti Puspitasari
Faculty of Medicine, Universitas Airlangga, Surabaya, Indonesia
Dr. Soetomo General Academic Hospital, Surabaya, Indonesia
Рубрики: Педиатрия/Неонатология
Разделы: Клинические исследования
Версия для печати
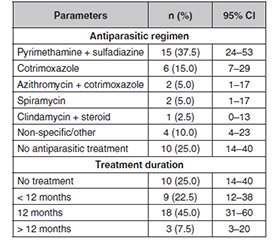
Актуальність. Токсоплазмоз — тропічна хвороба, яка є поширеною, але часто недооціненою в імунокомпетентних дітей, здебільшого через припущення про безсимптомний або самообмежувальний перебіг. Зростаюча кількість повідомлень про тяжкі прояви впродовж останнього десятиліття вимагає переоцінки потенційної захворюваності в цій популяції. Мета: описати клінічні й епідеміологічні характеристики, схеми лікування та короткострокові клінічні результати токсоплазмозу в імунокомпетентних дітей віком ≤ 18 років, які проходили лікування у медичному закладі Dr. Soetomo General Academic Hospital (Сурабая, Індонезія) у 2020–2024 роках. Матеріали та методи. Ретроспективне описове дослідження з використанням медичних записів імунокомпетентних пацієнтів (≤ 18 років) із діагнозом токсоплазмозу. Проаналізовано демографічні дані, клінічні прояви, ураження органів, діагностичні висновки, схеми лікування й короткострокові результати. Результати. У дослідження включено 40 пацієнтів, більшість були дітьми віком 0–1 рік (n = 20, 50 % [95% довірчий інтервал (ДІ): 35–65 %]), переважно хлопчиками (n = 23, 57,5 % [95% ДІ: 42–71 %]), та мали нормальний харчовий статус (n = 21, 52,5 % [95% ДІ: 37–67 %]). Органом, який уражався найчастіше, були очі (n = 25, 62,5 % [95% ДІ: 47–76 %]), що здебільшого проявлялося порушеннями зору. Серологічні тести продемонстрували позитивний результат щодо IgM із високими титрами IgG у 24 пацієнтів (60 % [95% ДІ: 45–74 %]) на підставі стандартних профілів IgM/IgG без визначення авідності IgG. Виявлено коінфекцію з іншими TORCH-збудниками, зокрема потрійну коінфекцію з цитомегаловірусом i краснухою (n = 18, 45 % [95% ДІ: 31–60 %]). У цій когорті більшість симптоматичних випадків спостерігалися в дітей із множинними TORCH-коінфекціями (72,5 %), тоді як лише невелика підгрупа мала ізольований або мінімальний токсоплазмоз (27,5 %). Найпоширенішою антипаразитарною схемою була комбінація піриметаміну із сульфадіазином (n = 15, 37,5 % [95% ДІ: 24–53 %]) протягом одного року (n = 18, 45 % [95% ДІ: 31–60 %]). Короткострокове клінічне поліпшення спостерігалося в 97,5 % випадків (n = 39 [95% ДІ: 87–100 %]) незалежно від призначення специфічної антипаразитарної терапії. Висновки. Токсоплазмоз в імунокомпетентних дітей у цьому закладі третинного рівня переважно проявлявся в немовлячому віці зі значним ураженням очей і частими TORCH-коінфекціями, що обмежує можливість пов’язувати клінічні прояви виключно з Toxoplasma gondii. Короткочасне клінічне поліпшення спостерігалося в 97,5 % випадків незалежно від призначення специфічної антипаразитарної терапії, що ускладнює причинно-наслідкову інтерпретацію ефектів лікування.
Background. Toxoplasmosis is a neglected tropical disease that is common but often underrecognized in immunocompetent children, largely due to the assumption of an asymptomatic or self-limiting course. Increasing reports of severe manifestations over the past decade necessitate a re-evaluation of potential morbidity in this population. This study aimed to describe the clinical and epidemiological characteristics, treatment patterns, and short-term clinical outcomes of toxoplasmosis in immunocompetent children aged ≤ 18 years at the Dr. Soetomo General Academic Hospital, Surabaya, Indonesia, in 2020–2024. Materials and methods. A retrospective descriptive study, using medical records of immunocompetent patients (≤ 18 years) diagnosed with toxoplasmosis. Demographic data, clinical manifestations, organ involvement, diagnostic findings, treatment regimens, and short-term outcomes were analyzed. Results. Forty patients were included, most of them were infants aged 0–1 year (n = 20, 50 % [95% confidence interval (CI): 35–65 %]), predominantly males (n = 23, 57.5 % [95% CI: 42–71 %]), and had normal nutritional status (n = 21, 52.5 % [95% CI: 37–67 %]). Eyes was the most frequent organ system affected (n = 25, 62.5 % [95% CI: 47–76 %]), primarily presenting as visual impairment. Serological patterns demonstrated positive IgM with high IgG titers in 24 patients (60 % [95% CI: 45–74 %]), based on conventional IgM/IgG profiles without IgG avidity testing. Co-infection with other TORCH pathogens was notable, particularly triple co-infection with cytomegalovirus and rubella (n = 18, 45 % [95% CI: 31–60 %]). In this tertiary referral cohort, most symptomatic cases occurred in children with multiple TORCH co-infections (72.5 %), while only a small subgroup had isolated or minimal toxoplasmosis (27.5 %). The most common antiparasitic regimen was pyrimethamine-sulfadiazine (n = 15, 37.5 % [95% CI: 24–53 %]) for a duration of one year (n = 18, 45 % [95% CI: 31–60 %]). Short-term clinical improvement was observed in 97.5 % of cases (n = 39 [95% CI: 87–100 %]), irrespective of whether specific antiparasitic therapy was administered. Conclusions. Toxoplasmosis in immunocompetent children in this setting predominantly presents in infancy, with significant ocular involvement and frequent TORCH co-infections, limiting attribution of manifestations solely to Toxoplasma gondii. Short-term clinical improvement was observed in 97.5 % of cases, irrespective of whether specific antiparasitic therapy was administered, which complicates causal interpretation of treatment effects.
токсоплазмоз; діти; імунокомпетентність; недооцінена хвороба; клінічні прояви; результати
toxoplasmosis; children; immunocompetence; neglected disease; clinical manifestations; outcomes
Для ознакомления с полным содержанием статьи необходимо оформить подписку на журнал.
- Perdana TM, Dwiputro AH, Kusuma S, Simanjuntak AMT, Wijayanto FPS. Seroprevalence of anti-Toxoplasma IgG among the human population in Indonesia: a systematic review and meta-analysis. BMC Public Health. 2025;25(1):194. doi: 10.1186/s12889-025-21317-2.
- Flegr J, Prandota J, Sovičková M, Israili ZH. Toxoplasmosis — a global threat. Correlation of latent toxoplasmosis with specific disease burden in a set of 88 countries. PLoS One. 2014;9(3):e90203. doi: 10.1371/journal.pone.0090203.
- Molan A, Nosaka K, Hunter M, Wang W. Global status of Toxoplasma gondii infection: systematic review and prevalence snapshots. Trop Biomed. 2019;36(4):898-925.
- Manwani N, Ravikumar K, Viswanathan V, Rao SM, Mahadevan A. Acquired toxoplasmosis presenting with a brainstem granuloma in an immunocompetent adolescent. Indian Pediatr. 2016;53(2):159-161.
- Lijeskić O, Štajner T, Srbljanović J, Radosavljević A, Bobić B, et al. Postnatal ocular toxoplasmosis in immunocompetent patients. J Infect Dev Ctries. 2021;15(10):1515-1522. doi: 10.3855/jidc.14824.
- Oya Y, Futami H, Nakazawa T, Ishijima K, Umemiya K, et al. Tubulointerstitial nephritis and uveitis syndrome following meningitis and systemic lymphadenopathy with persistent Toxoplasma immunoglobulin M: a case report. J Med Case Rep. 2021;15(1):482. doi: 10.1186/s13256-021-02909-z.
- Punhani P, Madan N, Kaur S, Ranga S. Toxoplasma pericarditis in an immunocompetent child: a rare case report. Asian J Res Infect Dis. 2021;7(4):1-6. doi: 10.9734/ajrid/2021/v7i430220.
- Pangracio E, de Macedo V, Alves PK. Pulmonary and renal toxoplasmosis in an immunocompetent adult patient. J Med Cases. 2023;14(2):50-53. doi: 10.14740/jmc4029.
- Singh S. Congenital toxoplasmosis: clinical features, outcomes, treatment, and prevention. Trop Parasitol. 2016;6(2):113-122. doi: 10.4103/2229-5070.190813.
- Garweg JG, Kieffer F, Mandelbrot L, Peyron F, Wallon M. Long-term outcomes in children with congenital toxoplasmosis: a systematic review. Pathogens. 2022;11(10):1187. doi: 10.3390/pathogens11101187.
- Akbari M, Azadi D, Habibi D, Khodashenas S, Shariatmadari F, Abedi B. Toxoplasmosis infection in newborn: a systematic review and meta-analysis. Adv Biomed Res. 2022;11:75. doi: 10.4103/abr.abr_24_21.
- Singh G, Tucker EW, Rohlwink UK. Infection in the developing brain: the role of unique systemic immune vulnerabilities. Front Neurol. 2022;12:805643. doi: 10.3389/fneur.2021.805643.
- Bollani L, Auriti C, Achille C, Garofoli F, De Rose DU, et al. Congenital toxoplasmosis: the state of the art. Front Pediatr. 2022;10:894573. doi: 10.3389/fped.2022.894573.
- Archana, Singh RN, Kumar V. Seroprevalence of ocular toxoplasmosis and the associated risk factors among pediatric patients. Int J Pharm Clin Res. 2024;16(5):1362-1368.
- Flegr J, Kaňková Š. The effects of toxoplasmosis on sex ratio at birth. Early Hum Dev. 2020;141:104874. doi: 10.1016/j.earlhumdev.2019.104874.
- Shapiro K, Bahia-Oliveira L, Dixon B, Dumètre A, de Wit LA, et al. Environmental transmission of Toxoplasma gondii: oocysts in water, soil and food. Food Waterborne Parasitol. 2019;15:e00049. doi: 10.1016/j.fawpar.2019.e00049.
- Gwela A, Mupere E, Berkley JA, Lancioni C. Undernutrition, host immunity and vulnerability to infection among young children. Pediatr Infect Dis J. 2019;38(8):e175-e177. doi: 10.1097/INF.0000000000002363.
- Bourke CD, Berkley JA, Prendergast AJ. Immune dysfunction as a cause and consequence of malnutrition. Trends Immunol. 2016;37(6):386-398. doi: 10.1016/j.it.2016.04.003.
- Cuffey J, Lepczyk CA, Zhao S, Fountain-Jones NM. Cross-sectional association of Toxoplasma gondii exposure with BMI and diet in US adults. PLoS Negl Trop Dis. 2021 Oct 1;15(10):e0009825. doi: 10.1371/journal.pntd.0009825.
- Yuliawati I, Nasronudin N. Pathogenesis, diagnostic and ma–nagement of toxoplasmosis. Indones J Trop Infect Dis. 2015;5(4):100-106.
- Journé A, Garweg J, Ksiazek E, Peyron F, Binquet C, Wallon M. Long-term ocular outcomes in congenital toxoplasmosis treated perinatally. Pediatrics. 2024;153(4):e2023064114. doi: 10.1542/peds.2023-064114.
- Eraghi AT, Garweg JG, Pleyer U. The role of age in ocular toxoplasmosis: clinical signs of immunosenescence and inflammaging. Front Med (Lausanne). 2024;11:1311145. doi: 10.3389/fmed.2024.1311145.
- De-la-Torre A, Mejía-Salgado G, Eraghi AT, Pleyer U. Age and ocular toxoplasmosis: a narrative review. FEMS Microbes. 2025;6:xtaf002. doi: 10.1093/femsmc/xtaf002.
- Erazo Flores BJ, Knoll LJ. Toxoplasma gondii at the host interface: immune modulation and translational strategies for infection control. Vaccines (Basel). 2025;13(8):819. doi: 10.3390/vaccines13080819.
- Galván-Ramírez ML, Soto-Hernández EE, Bojórquez-Pérez R. Coinfection of Toxoplasma gondii and other microorganisms: a syste–matic review and meta-analysis. Microorganisms. 2024;12(10):2106. doi: 10.3390/microorganisms12102106.
- Ismael R, et al. Infeksi Toxoplasma dan CMV kongenital: rekomendasi tata laksana infeksi Toxoplasma dan CMV kongenital. Jakarta: Perhimpunan Dokter Spesialis Anak Indonesia; 2016 (in Indonesian).