Международный эндокринологический журнал Том 22, №2, 2026
Вернуться к номеру
Мультимодальна оцінка гетерогенності стеатозу печінки: сегментарна МРТ-ФЖПЩ та визначення коефіцієнта затухання ультразвуку
Авторы: M.M. Zhaivoronok (1), N.V. Deresh (2), I. Sporea (3), O.B. Dynnyk (4), Feysa S.V. (5), Pushkarenko O.A. (5), O.A. Fedusenko (6), O.V. Shcherbina (1), N.M. Kobyliak (7)
(1) - Shupyk National Healthcare University of Ukraine, Kyiv, Ukraine
(2) - LifeScan Clinic, Kyiv, Ukraine
(3) - Victor Babeş University of Medicine and Pharmacy, Timișoara, Romania
(4) - Medical Center “Institute of Elastography”, Kyiv, Ukraine
(5) - Institute of Postgraduate Education and Pre-University Training, Uzhhorod National University, Uzhhorod, Ukraine
(6) - Medical Center “Doctor Lakhman”, Zaporizhzhia, Ukraine
(7) - Bogomolets National Medical University, Kyiv, Ukraine
Рубрики: Эндокринология
Разделы: Клинические исследования
Версия для печати
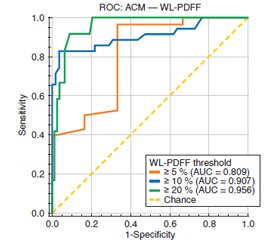
Актуальність. Метаболічно асоційована стеатотична хвороба печінки (МАСХП) є однією з провідних причин хронічного ураження цього органа у світі. Попри розвиток кількісних методів візуалізації, розподіл жиру в печінці залишається просторово гетерогенним, що може впливати на точність неінвазивних біомаркерів, зокрема визначення коефіцієнта затухання (ВКЗ) ультразвуку, при порівнянні з магнітно-резонансною томографією з оцінкою фракції жиру за протонною щільністю (МРТ-ФЖПЩ). Мета: кількісно оцінити сегментарну гетерогенність стеатозу печінки за допомогою МРТ-ФЖПЩ та з’ясувати її вплив на діагностичну точність ВКЗ в осіб із МАСХП. Матеріали та методи. У проспективне дослідження включено 116 дорослих пацієнтів (42,2 % чоловіків; середній вік 48,2 ± 13,6 року), яким проведено одномоментні дослідження печінки з МРТ-ФЖПЩ та ВКЗ ультразвуку. МРТ-ФЖПЩ виконували у всіх восьми сегментах за Couinaud для розрахунку значення по всій печінці (ФЖПЩ-ВП) та міжсегментарної варіабельності. ВКЗ (дБ/см) здійснено за стандартизованими критеріями якості. Проведено кореляційний аналіз, оцінку узгодженості (ICC, Bland — Altman) та ROC-аналіз для клінічно значущих порогів ФЖПЩ-ВП (≥ 5, ≥ 10, ≥ 20 %). Результати. Середня ФЖПЩ-ВП становила 11,0 ± 6,4 %, середня сегментарна ФЖПЩ — 11,3 ± 6,3 %. Найвищі кореляції з ФЖПЩ-ВП виявлені у сегментах VIII (ρ = 0,99) та VII (ρ = 0,98), найнижчі — у сегменті I (ρ = 0,82). ВКЗ вірогідно корелювало з ФЖПЩ-ВП (ρ = 0,63; p < 0,001), із найвищою сегментарною кореляцією в сегменті VI (ρ = 0,68). ROC-аналіз продемонстрував високу діагностичну ефективність (AUC = 0,809; 0,907; 0,956 для порогів ФЖПЩ ≥ 5, ≥ 10 та ≥ 20 % відповідно). Висновки. Стеатоз печінки при МАСХП має виражену сегментарну гетерогенність. ВКЗ демонструє тісну кореляцію та високу діагностичну точність щодо МРТ-ФЖПЩ, однак локальні відмінності можуть знижувати узгодженість. Вимірювання в кількох ділянках, особливо у задньолатеральних сегментах правої частки, підвищує відтворюваність і має бути включене до стандартизованих протоколів.
Background. Metabolic dysfunction-associated steatotic liver disease (MASLD) is highly prevalent among patients with obesity and type 2 diabetes, yet hepatic fat distribution is spatially heterogeneous. This heterogeneity may influence the performance of noninvasive diagnostic tools, including ultrasound attenuation coefficient measurement (ACM), when benchmarked against magnetic resonance imaging-proton density fat fraction (MRI-PDFF). The purpose of the study was to quantify segmental heterogeneity of hepatic steatosis by MRI-PDFF and evaluate its impact on the diagnostic accuracy of ACM in MASLD. Materials and methods. A prospective cohort of 116 adults (42.2 % men; mean age 48.2 ± 13.6 years) underwent same-episode liver MRI-PDFF and ultrasound ACM. MRI-PDFF was quantified in all eight Couinaud segments to compute whole-liver PDFF (WL-PDFF) and intersegmental heterogeneity metrics. ACM values (dB/cm) were obtained under standardized quality criteria. Correlation, agreement (intraclass correlation coefficient, Bland-Altman), and ROC analysis were performed for clinically relevant WL-PDFF thresholds (≥ 5, ≥ 10, ≥ 20 %). Results. The mean WL-PDFF was 11.0 ± 6.4 %, while mean segmental PDFF was 11.3 ± 6.3 %. Intersegmental correlations with WL-PDFF were strongest in segments VIII (ρ = 0.99) and VII (ρ = 0.98) and lowest in segment I (ρ = 0.82). ACM correlated significantly with WL-PDFF (ρ = 0.63, p < 0.001), with the highest segmental correlation in segment VI (ρ = 0.68). ROC analysis showed excellent diagnostic performance: AUC = 0.809, 0.907, and 0.956 for PDFF ≥ 5, ≥ 10, and ≥ 20 %, respectively. Conclusions. Hepatic steatosis in MASLD exhibits clinically relevant segmental heterogeneity. ACM provides strong correlation with MRI-PDFF and excellent diagnostic performance for clinically significant fat thresholds, but localized variability may weaken concordance. Multiple ROI sampling, particularly in posterior-lateral right-lobe segments, enhances agreement with whole-liver PDFF and should be incorporated into standardized protocols.
ожиріння; цукровий діабет 2-го типу; метаболічно асоційована стеатотична хвороба печінки; магнітно-резонансна томографія з оцінкою фракції жиру за протонною щільністю; затухання ультразвуку; стеатоз печінки; сегментарна гетерогенність
obesity; type 2 diabetes mellitus; metabolic dysfunction-associated steatotic liver disease; magnetic resonance imaging-proton density fat fraction; ultrasound attenuation; hepatic steatosis; segmental heterogeneity
Для ознакомления с полным содержанием статьи необходимо оформить подписку на журнал.
- Younossi ZM, Kalligeros M, Henry L. Epidemiology of metabolic dysfunction-associated steatotic liver disease. Clin Mol Hepatol. 2025;31(Suppl):32-50. doi: 10.3350/CMH.2024.0431.
- Kan C, Zhang K, Wang Y, et al. Global burden and future trends of metabolic dysfunction-associated steatotic liver disease: 1990–2021 to 2045. Ann Hepatol. 2025;30(2). doi: 10.1016/J.AOHEP.2025.101898.
- Nguyen MH, Le MH, Yeo YH, et al. Forecasted 2040 glo–bal prevalence of nonalcoholic fatty liver disease using hierarchical bayesian approach. Clin Mol Hepatol. 2022;28(4):841. doi: 10.3350/CMH.2022.0239.
- Allen AM, Lazarus JV, Younossi ZM. Healthcare and socioeconomic costs of NAFLD: A global framework to navigate the uncertainties. J Hepatol. 2023;79(1):209-217. doi: 10.1016/j.jhep.2023.01.026.
- Hernaez R, Lazo M, Bonekamp S, et al. Diagnostic accuracy and reliability of ultrasonography for the detection of fatty liver: A meta-analysis. Hepatology. 2011;54(3):1082-1090. doi: 10.1002/HEP.24452.
- Caussy C, Reeder SB, Sirlin CB, et al. Non-invasive, quantitative assessment of liver fat by MRI-PDFF as an endpoint in NASH trials. Hepatology. 2018;68(2):763. doi: 10.1002/HEP.29797.
- Ferraioli G, Barr RG, Berzigotti A, et al. WFUMB Guidelines/Guidance on Liver Multiparametric Ultrasound. Part 2: Guidance on Liver Fat Quantification. Ultrasound Med Biol. 2024;50(8):1088-1098. doi: 10.1016/j.ultrasmedbio.2024.03.014.
- Kumada T, Ogawa S, Goto T, et al. Intra-individual Comparisons of the Ultrasound-Guided Attenuation Parameter and the Magne–tic Resonance Imaging-Based Proton Density Fat Fraction Using Bias and Precision Statistics. Ultrasound Med Biol. 2022;48(8):1537-1546. doi: 10.1016/J.ULTRASMEDBIO.2022.03.019.
- Bonekamp S, Tang A, Mashhood A, et al. Spatial Distribution of MRI-Determined Hepatic Proton Density Fat Fraction in Adults with Nonalcoholic Fatty Liver Disease. J Magn Reson Imaging. 2014;39(6):1525. doi: 10.1002/JMRI.24321.
- Stine JG, Munaganuru N, Barnard A, et al. Change in MRI-PDFF and Histologic Response in Patients With Nonalcoholic Steatohepatitis: A Systematic Review and Meta-Analysis. Clinical Gastroenterology and Hepatology. 2021;19(11):2274-2283.e5. doi: 10.1016/j.cgh.2020.08.061.
- Sumida Y, Nakajima A, Itoh Y. Limitations of liver biopsy and non-invasive diagnostic tests for the diagnosis of nonalcoholic fatty liver disease/nonalcoholic steatohepatitis. World J Gastroenterol. 2014;20(2):475-485. doi: 10.3748/WJG.V20.I2.475.
- Imajo K, Toyoda H, Yasuda S, et al. Utility of Ultrasound-Gui–ded Attenuation Parameter for Grading Steatosis With Refe–rence to MRI-PDFF in a Large Cohort. Clinical Gastroenterology and Hepatology. 2022;20(11):2533-2541.e7. doi: 10.1016/j.cgh.2021.11.003.
- Dynnyk OB, Zhaivoronok MM, Kobyliak NM. Ultrasound screening of nonalcoholic fatty liver disease using an innovative attenuation coefficient measurement method for primary healthcare. Ukrainski Medychni Visti. 2022;3–4:74-75.
- Zhaivoronok MM, Dynnyk OB. Multiparametric ultrasound steatometry in hepatic steatosis: a literature review and own data. Current Aspects of Military Medicine. 2025;32(1):171-194. doi: 10.32751/2310-4910-2025-32-1-14.
- Dynnyk O, Solodovnyk O, Zakomornyi O, et al. Stratification of liver steatosis by the attenuation coefficient measurement (ACM) of the hand-held ultrasound device. Ultrasound Med Biol. 2022;48:S34-S35. doi: 10.1016/J.ULTRASMEDBIO.2022.04.105.
- Zhaivoronok M, Dynnyk O, Livkutnyk O, et al. Inter- and intraobserver variability of attenuation coefficient measurement in innovative ultrasound diagnosis of metabolic dysfunction-associated steatotic liver disease: a cross-sectional study. Front Med (Lausanne). 2025;12:1457960. doi: 10.3389/FMED.2025.1457960/BIBTEX.
- Campo CA, Hernando D, Schubert T, et al. Standardized Approach for ROI-Based Measurements of Proton Density Fat Fraction and R2* in the Liver. AJR Am J Roentgenol. 2017;209(3):592-603. doi: 10.2214/AJR.17.17812.
- Lee H, Jun DW, Kang BK, et al. Estimating of hepatic fat amount using MRI proton density fat fraction in a real practice setting. Medicine. 2017;96(33):e7778. doi: 10.1097/MD.0000000000007778.
- Fasel J, Schenk A. Concepts for Liver Segment Classification: Neither Old Ones nor New Ones, but a Comprehensive One. J Clin Imaging Sci. 2013;3(1):48. doi: 10.4103/2156-7514.120803.
- Dubinsky TJ. Evaluating Hepatic Steatosis with MRI as the Reference Standard: Different Performances of Three US Machines. Radiology. 2022;305(2):362-363. doi: 10.1148/radiol.221177.
- Kim A, Kim M, Lee CM, et al. Three segments sampling strategy for the assessment of liver steatosis using magnetic resonance ima–ging proton density fat fraction. Eur J Radiol. 2023;159. doi: 10.1016/J.EJRAD.2022.110653.
- Cao D, Li M, Liu Y, et al. Comparison of reader agreement, correlation with liver biopsy, and time-burden sampling strategies for liver proton density fat fraction measured using magnetic resonance imaging in patients with obesity: a secondary cross-sectional study. BMC Med Imaging. 2022;22(1):1-21. doi: 10.1186/S12880-022-00821-6/TABLES/8.
- Cannella R, Agnello F, Porrello G, et al. Performance of ultrasound-guided attenuation parameter and 2D shear wave elastography in patients with metabolic dysfunction-associated steatotic liver disease. Eur Radiol. 2024;35(4):2339. doi: 10.1007/S00330-024-11076-W.