Международный эндокринологический журнал Том 22, №2, 2026
Вернуться к номеру
Клінічні характеристики та прогностичні чинники низькодиференційованих карцином щитоподібної залози
Авторы: Гуда Б.Б., Тимків А.В., Остафійчук М.В., Комісаренко І.І., Гамезардашвілі І.В., Мельник М.Д.
ДУ «Інститут ендокринології та обміну речовин ім. В.П. Комісаренка НАМН України», м. Київ, Україна
Рубрики: Эндокринология
Разделы: Клинические исследования
Версия для печати
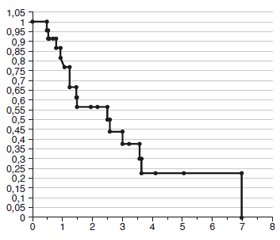
Актуальність. Низькодиференційований рак щитоподібної залози (ЩЗ) — це рідкісні інвазивні високозлоякісні карциноми, що походять з фолікулярних клітин, які гістологічно мають солідний, трабекулярний і острівцевий характер росту (або їх комбінації). На початку ХХI століття низькодиференційовану карциному (НДК) було визнано окремим варіантом та встановлено гістологічні критерії її діагностики. Попри зусилля з вивчення НДК, ці карциноми все ще становлять суттєву проблему для клініцистів та онкологів через труднощі, які пов’язані з діагностичним процесом, гострою необхідністю складної тиреоїдектомії, високою частотою рецидивів і значною летальністю від неанапластичного раку ЩЗ. Мета роботи: ретроспективний аналіз клінічних даних пацієнтів з НДК ЩЗ щодо доопераційної діагностики, характеристик пухлин, ефективності лікувальних стратегій, чинників, які можуть впливати на тривалість післяопераційного періоду життя пацієнтів та рівень їх виживаності. Матеріали та методи. Проведено ретроспективний аналіз даних 23 хворих з НДК ЩЗ, які були обстежені та прооперовані упродовж 20 років. Аналізували вік, стать хворих, розміри пухлин та їх класифікацію за системою TNM, результати цитологічних досліджень аспіратів (ТАПБ), наявність інвазії (у капсулу, кровоносні та/або лімфатичні судини пухлини, інтра- чи екстратиреоїдна), обсяг хірургічного втручання, післяопераційне лікування, стан здоров’я (пацієнти у ремісії, prolongatio morbi, померли), тривалість післяопераційного життя та рівень кумулятивної виживаності хворих. Результати. Вік більшості пацієнтів з НДК перевищував 50 років; кількісне співвідношення жінки : чоловіки є рівним. Гендерна різниця щодо основних клінічних характеристик хвороби відсутня, за винятком більшого розміру пухлин у хворих чоловічої статі і вищого ризику у них наявності інвазивних карцином. Аналіз результатів цитологічних досліджень аспіратів у хворих когорти засвідчив їх низьку діагностичну цінність у випадках НДК: за результатами ТАПБ у жодному випадку не було правильно діагностовано карциному, а 38 % пухлин були віднесені до Bethesda II–IV. 87 % хворих мали карциноми категорії Т3–T4, розмір 78 % перевищував 4 см, понад половина з них були широко інвазивними, серед метастазуючих пухлин 75 % мали метастази у латеральні лімфовузли шиї, спостерігали також випадки компресії структур, що оточують ЩЗ. Такі несприятливі клініко-патологічні характеристики обумовили високу летальність серед хворих (60,9 %), короткий термін їх життя після операції (від 5 до 84 міс., у середньому 17,7 міс.) і низький рівень їх виживаності упродовж перших 5 післяопераційних років (22,5 %). Зазначено, що більша частка смертей хворих припадала на перші 3 післяопераційні роки, з часом, що минув після видалення карциноми, кількість/відсоток летальних випадків зменшувалися. Висновки. Діагностична цінність результатів ТАПБ у доопераційній діагностиці НДК ЩЗ низька. Отримані дані дозволяють рекомендувати обов’язкове проведення хірургічного лікування у хворих віком понад 60 років з висновком Bethesda III–IV. Інвазія пухлин у межах ЩЗ, наявність метастазів у лімфатичні вузли шиї та відсутність післяопераційного променевого лікування можуть бути чинниками ризику смерті у перші роки після операції, тоді як вік хворих, розмір пухлини та екстратиреоїдна інвазія є основними прогностичними біологічними чинниками виживаності хворих з низькодиференційованим раком ЩЗ.
Background. Poorly differentiated thyroid cancer (РDTC) is a rare, invasive, highly malignant carcinoma originating from follicular cells that histologically has a solid, trabecular, and insular growth pattern (or their combinations). At the beginning of the 21st century, poorly differentiated carcinoma was recognized as a separate entity and histological criteria for its diagnosis were established. Despite efforts to study poorly differentiated carcinomas, they still pose a significant challenge to clinicians due to the difficulties associated with the diagnosis, urgent need for complex thyroidectomy, high recurrence rate, and significant lethality from non-anaplastic thyroid cancer. The purpose of the study: a retrospective analysis of clinical data of patients with РDTC regarding preoperative diagnosis, tumor characteristics, effectiveness of treatment strategies, factors that may affect the duration of the postoperative period and survival rate. Materials and methods. A retrospective analysis of data from 23 patients with PDTC who were examined and operated over a 20-year period was conducted. We analyzed the age, gender of the patients, tumor size and classification according to the TNM system, results of cytological studies of aspirates (fine needle aspiration biopsy), presence of invasion (into the capsule, blood and/or lymphatic vessels of the tumor, intra- or extrathyroidal), extent of surgical intervention, postoperative treatment, health status (patients in remission, prolongatio morbi, died), duration of postoperative life and cumulative survival. Results. The age of most patients with PDTC was over 50 years; the ratio of women to men was equal. There is no gender difference in the main clinical characteristics of the disease, except for larger tumor size in male patients and a higher risk of invasive carcinomas in them. Analysis of the results of cytological studies of aspirates showed their low diagnostic value in cases of PDTC: carcinoma was not correctly diagnosed in any case, and 38 % of tumors were classified as Bethesda II–IV. 87 % of patients had T3-T4 carcinomas, 78 % exceeded 4 cm in size, more than half of them were widely invasive; among metastatic tumors, 75 % had metastases to the lateral cervical lymph nodes, and cases of compression of structures surrounding the thyroid were also observed. Such unfavorable clinicopathological characteristics caused high mortality (60.9 %), short lifetime after surgery (from 5 to 84 months, average of 17.7 months) and low survival rate during the first 5 postoperative years (22.5 %). It was noted that most deaths occurred in the first 3 postoperative years, with the number/percentage of deaths decreasing with time after carcinoma removal. Conclusions. The diagnostic value of fine needle aspiration biopsy results in the preoperative diagnosis of PDTC is low. The data obtained allow us to recommend mandatory surgery in patients aged 60+ with a Bethesda III–IV diagnosis. Tumor invasion within the thyroid gland, presence of metastases in cervical lymph nodes, and absence of postoperative radiation therapy may be risk factors for death in the first years after surgery, while patient age, tumor size, and extrathyroidal invasion are the main prognostic biological markers of survival in patients with poorly differentiated thyroid cancer.
низькодиференційована карцинома щитоподібної залози; доопераційна діагностика; лікування; прогностичні чинники; тривалість життя; кумулятивна виживаність
poorly differentiated thyroid carcinoma; preoperative diagnosis; treatment; prognostic factors; lifetime; cumulative survival
Для ознакомления с полным содержанием статьи необходимо оформить подписку на журнал.
- Ibrahimpasic T, Ghossein R, Shah JP, Ganly I. Poorly Differentiated Carcinoma of the Thyroid Gland: Current Status and Future Prospects. Thyroid. 2019 Mar;29(3):311-321. doi: 10.1089/thy.2018.0509.
- Simoes MS, Saavedra AJ, Tallini G, Santoro M, Volante M, Pilotti S, et al. Poorly differentiated carcinoma. In: DeLellis RA, Lloyd RV, Heitz PU, Eng C (eds). World Health Organization Classification of Tumours: Pathology and Genetics of Tumours of Endocrine Organs. Lyon: IARC Press; 2004. Р. 73-76.
- Volante M, Collini P, Nikiforov YE, Sakamoto A, Kakudo K, Katoh R, et al. Poorly differentiated thyroid carcinoma: the Turin proposal for the use of uniform diagnostic criteria and an algorithmic diagnostic approach. Am J Surg Pathol. 2007 Aug;31(8):1256-64. doi: 10.1097/PAS.0b013e3180309e6a.
- Lloyd RV, Osamura RY, Kloppel G, Rosai J. WHO classification of tumours of endocrine organs. Chapter 2. Tumours of the thyroid gland; 4th ed. Lyon: IARC; 2017. Р. 65-144.
- Baloch ZW, Asa SL, Barletta JA, Ghossein RA, Juhlin CC, Jung CK, et al. Overview of the 2022 WHO Classification of Thyroid Neoplasms. Endocr Pathol. 2022 Mar;33(1):27-63. doi: 10.1007/s12022-022-09707-3.
- Xu B, Lubin DJ, Dogan S, Ghossein RA, Viswanathan K. Significance of oncocytic features in poorly differentiated thyroid carcinoma — a bi-institutional experience. Virchows Arch. 2023;482(3):479-91. doi: 10.1007/s00428-022-03422-4.
- Schipor S, Publik MA, Manda D, Ceausu M. Aggressive Thyroid Carcinomas Clinical and Molecular Features: A Systematic Review. Int J Mol Sci. 2025 Jun 10;26(12):5535. doi: 10.3390/ijms26125535.
- Tong J, Ruan M, Jin Y, Fu H, Cheng L, Luo Q, Liu Z, et al. Poorly differentiated thyroid carcinoma: a clinicianʼs perspective. Eur Thyroid J. 2022 Mar 24;11(2):e220021. doi: 10.1530/ETJ-22-0021.
- Hay ID, Bergstralh EJ, Goellner JR, Ebersold JR, Grant CS. Predicting outcome in papillary thyroid carcinoma: development of a reliable prognostic scoring system in a cohort of 1779 patients surgically treated at one institution during 1940 through 1989. Surgery. 1993;114(6):1050-7. PMID: 8256208.
- Wan Z, Wang B, Yao J, Li Q, Miao X, Jian Y, et al. Predictive factors and clinicopathological characteristics of outcome in poorly differentiated thyroid carcinoma: a single-institution study. Front Oncol. 2023 Jul 7;13:1102936. doi: 10.3389/fonc.2023.1102936.
- Alwelaie Y, Howaidi A, Tashkandi M, Almotairi A, Saied H, Muzzaffar M, et al. Revisiting the cytomorphological features of poorly differentiated thyroid carcinoma: a comparative analysis with indeterminate thyroid fine-needle aspiration samples. J Am Soc Cytopathol. 2023 Sep-Oct;12(5):331-340. doi: 10.1016/j.jasc.2023.05.002.
- Alam IS, Patel KN. Management of Poorly Differentiated Thyroid Cancer and Differentiated High-Grade Thyroid Carcinoma. Surg Clin North Am. 2024 Aug;104(4):751-765. doi: 10.1016/j.suc.2024.02.005.
- Huang J, Sun W, Zhang Q, Wang Z, Dong W, Zhang D, et al. Clinicopathological Characteristics and Prognosis of Poorly Differentiated Thyroid Carcinoma Diagnosed According to the Turin Criteria. Endocr Pract. 2021 May;27(5):401-407. doi: 10.1016/j.eprac.2020.11.008.
- Wong KS, Lorch JH, Alexander EK, Marqusee E, Cho NL, Nehs MA, et al. Prognostic Significance of Extent of Invasion in Poorly Differentiated Thyroid Carcinoma. Thyroid. 2019 Sep;29(9):1255-1261. doi: 10.1089/thy.2019.0263.
- Yuang K, Al-Bahadili H, Chang A. An Unexpected Finding of Poorly Differentiated Thyroid Carcinoma in a Toxic Thyroid Nodule. JCEM Case Rep. 2023 May 23;1(3):luad052. doi: 10.1210/jcemcr/luad052.
- Apelian S, Ismail S, Roumieh D, Saad B, Alshehabi Z. Poorly differentiated thyroid carcinoma arising from substernal goiter: a case report. Ann Med Surg (Lond). 2024 Mar 18;86(5):3020-3024. doi: 10.1097/MS9.0000000000001868.
- Gu H, Wang J, Ran W, Li G, Hu S, Zhao H, et al. Anaplastic and poorly differentiated thyroid carcinomas: genetic evi–dence of high-grade transformation from differentiated thyroid carcinoma. J Pathol Clin Res. 2024 Mar;10(2):e356. doi: 10.1002/cjp2.356.
- Ito Y, Hirokawa M, Kihara M, Takamura Y, Kobayashi K, Miya A, et al. Prognostic value of poorly differentiated carcinoma in Japa–nese Society of Thyroid Surgery in a series of papillary thyroid carcinoma patients: comparison with risk classification system in Kuma Hospital. Endocr J. 2012;59(9):817-21. doi: 10.1507/endocrj.ej12-0175.
- Januś D, Kujdowicz M, Kiszka-Wiłkojć A, Kaleta K, Taczanowska-Niemczuk A, Radliński J, et al. Ultrasound and histopathological assessment of benign, borderline, and malignant thyroid tumors in pediatric patients: an illustrative review and literature overview. Front Endocrinol (Lausanne). 2025 Jan 30;15:1481804. doi: 10.3389/fendo.2024.1481804.
- Beute JE, Silberzweig AM, Gold BS, Shaari AL, Kapustin DA, Matloob A, et al. Thyroid cancer necrosis not evident on ima–ging: A cautionary case series on poorly differentiated thyroid carcinoma diagnosed only on final pathology. Am J Otolaryngol. 2024 Jan-Feb;45(1):104054. doi: 10.1016/j.amjoto.2023.104054.
- Win TT, Othman NH, Mohamad I. Poorly differentiated thyroid carcinoma: A hospital-based clinicopathological study and review of literature. Indian J Pathol Microbiol. 2017 Apr-Jun;60(2):167-171. doi: 10.4103/IJPM.IJPM_457_16.
- Bellini MI, Biffoni M, Patrone R, Borcea MC, Costanzo ML, Garritano T, et al. Poorly Differentiated Thyroid Carcinoma: Single Centre Experience and Review of the Literature. J Clin Med. 2021 Nov 12;10(22):5258. doi: 10.3390/jcm10225258.
- Thompson LDR. High Grade Differentiated Follicular Cell-Derived Thyroid Carcinoma Versus Poorly Differentiated Thyroid Carcinoma: A Clinicopathologic Analysis of 41 Cases. Endocr Pathol. 2023 Jun;34(2):234-246. doi: 10.1007/s12022-023-09770-4.
- Agarwal S, Jung CK, Gaddam P, Hirokawa M, Higashiyama T, Hang JF, et al. PD-L1 Expression and Its Modulating Factors in Anaplastic Thyroid Carcinoma: A Multi-institutional Study. Am J Surg Pathol. 2024 Oct 1;48(10):1233-1244. doi: 10.1097/PAS.0000000000002284.
- Al Masaoudi L, Jawa Z, Alsaffar H, Al Badaai Y. Poorly Differentiated Papillary Thyroid Carcinoma in a 8-Year Old Girl: A Case Report. WCTC. 2025. Abstracts. Submission ID 72.
- Mohsen M, Hamdy O, Ramadan A, Awny Z, Zalata K, Ezat M. Poorly differentiated papillary thyroid carcinoma in a 5-year-old girl: a case report. Egypt Pediatric Association Gaz. 2024;72:10. https://doi.org/10.1186/s43054-024-00251-9.
- Gubbiotti MA, Andrianus S, Sakhi R, Zhang Q, Montone K, Jalaly JB, Baloch Z. Does the presence of capsule influence prognosis in poorly differentiated thyroid carcinoma? Hum Pathol. 2023 Jun;136:96-104. doi: 10.1016/j.humpath.2023.04.005.
- Gill SM, Hassan A, Bashir H, Shafiq W. I-131 Avid Tumor Thrombus in a Case of Poorly Differentiated Thyroid Cancer. Mol Imaging Radionucl Ther. 2023 Jun 20;32(2):178-180. doi: 10.4274/mirt.galenos.2023.81567.
- Meng X, Chang X, Qin P, Li Y, Guo Y. Risk-dependent conditional survival analysis and annual hazard rate of inflammatory breast cancer. Eur J Surg Oncol: J Eur Soc Surg Oncol Br Assoc Surg Oncol. 2023;49:106957. doi: 10.1016/j.ejso.2023.06.009.
- Liu Z, Xu Q, Xia H, Wang M. Dynamic estimates of survival of patients with poorly differentiated thyroid carcinoma: a population-based study. Front Endocrinol (Lausanne). 2024 Sep 13;15:1375274. doi: 10.3389/fendo.2024.1375274.
- Orlando G, Capella G, Vocino Trucco G, Vissio E, Metovic J, Maletta F, et al. Prognostic impact of fibrosclerotic chan–ges in non-papillary, non-anaplastic, follicular cell-derived thyroid carcinomas. Virchows Arch. 2025 Jan 23. doi: 10.1007/s00428-025-04028-2.
- Lin L, Almont T, Beaubrun M, Macni J, Pierre-Louis A, Zabulon A, et al. Overall survival of patients with thyroid cancer in Martinique (2008-2018). BMC Cancer. 2023 Aug 10;23(1):739. doi: 10.1186/s12885-023-11072-1.
- Kim JY, Myung JK, Kim S, Tae K, Choi YY, Lee SJ. Prognosis of Poorly Differentiated Thyroid Carcinoma: A Systematic Review and Meta-Analysis. Endocrinol Metab (Seoul). 2024 Aug;39(4):590-602. doi: 10.3803/EnM.2024.1927.