Международный эндокринологический журнал Том 22, №2, 2026
Вернуться к номеру
Рівень фактора росту фібробластів 19 у плазмі крові, пухлинах щитоподібної залози та метастазах
Авторы: N.Ya. Kobrynska, V.M. Pushkarev, N.I. Levchuk, O.I. Kovzun, I.I. Komisarenko, B.B. Guda, M.D. Tronko
V.P. Komisarenko Institute of Endocrinology and Metabolism of NAMSU, Kyiv, Ukraine
Рубрики: Эндокринология
Разделы: Клинические исследования
Версия для печати
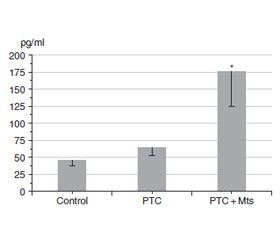
Актуальність. Ендокринна підродина фактора росту фібробластів 19 (FGF19) складається з FGF19, FGF21 та FGF23. Численні дані вказують на те, що FGF19 бере участь у канцерогенезі, епітеліально-мезенхімальному переході, утворенні метастазів і резистентності пухлини до інгібіторів. Мета: порівняти рівні FGF19 у зразках тканин фолікулярної аденоми, зоба, папілярної карциноми щитоподібної залози (ПКЩЗ), метастазів (Мтс) та умовно нормальної тканини. Матеріали та методи. Для дослідження використовували післяопераційні зразки тканини й плазми крові, отримані в хірургічному відділенні клініки ІЕМ. Кількість FGF19 визначали за допомогою наборів для імуноферментного аналізу. Результати. Рівень FGF19 у тканині фолікулярної аденоми та зоба був вищим, ніж в умовно нормальній тканині. Також спостерігалася значна різниця між нормальною тканиною і тканинами ПКЩЗ iз Мтс та без них. Важливо зазначити, що рівень FGF19 у Мтс був вищим, ніж у пухлинній тканині ПКЩЗ. У плазмі крові пацієнтів із ПКЩЗ та Мтс концентрація FGF19 значно перевищувала таку в контрольній плазмі та в крові осіб із ПКЩЗ без Мтс. У плазмі хворих із ПКЩЗ без Мтс рівень FGF19 не відрізнявся від його вмісту в крові здорових людей. Висновки. Наші дані вказують на значні відмінності в концентрації FGF19 між пухлинними тканинами ПКЩЗ і Мтс. У плазмі крові пацієнтів із ПКЩЗ та Мтс рівень FGF19 перевищував такий у контрольній плазмі й в крові осіб із ПКЩЗ без Мтс. Не було виявлено різниці між умістом FGF19 у крові хворих із ПКЩЗ без Мтс та в контрольній плазмі. Останні факти можуть бути корисними для прогнозування утворення Мтс.
Background. The endocrine subfamily of fibroblast growth factor 19 (FGF19) consists of FGF19, FGF21, and FGF23. Numerous data indicate that FGF19 is involved in carcinogenesis, epithelial-mesenchymal transition, metastasis formation, and tumor resistance to inhibitors. The purpose of the study was to compare the levels of FGF19 in tissue samples of follicular adenoma, goiter, papillary thyroid carcinoma (PTC), metastasis (Mts), and conditionally normal tissue. Materials and methods. Postoperative samples of tissue and blood plasma, obtained from the surgical department of the IEM clinic, were used for research. The amount of FGF19 was determined using enzyme immunoassay kits. Results. The level of FGF19 in the tissue of follicular adenoma and goiter exceeded the levels in conditionally normal tissue. There was also significant difference between normal tissue and РТС tissues with and without Mts. It is important to note that the level of FGF19 in metastasis was higher than in the tumor tissue of the РТС. In blood plasma of patients with PTC and Mts, the concentration of the FGF19 significantly exceeded its level in control plasma and in the blood of patients with PTC without Mts. In plasma of patients with PTC without Mts, the concentration of the FGF19 did not differ from its concentration in blood of healthy people. Conclusions. Our data indicate significant differences in the concentration of FGF19 between tumor tissues of PTC and Mts. In blood plasma of patients with PTC and Mts, the concentration of the FGF19 exceeded its level in control plasma and the concentration of FGF19 in the blood of patients with PTC without Mts. There was no difference between level of FGF19 in the blood of patients with PTC without Mts and in control plasma. The latter facts may be useful for predicting the formation of Mts.
папілярна карцинома щитоподібної залози; метастазування; фактор росту фібробластів 19
papillary thyroid carcinoma; metastasis; fibroblast growth factor 19
Для ознакомления с полным содержанием статьи необходимо оформить подписку на журнал.
- Motylewska E, Stępień T, Borkowska M, et al. Alteration in the serum concentrations of FGF19, FGFR4 and βKlotho in patients with thyroid cancer. Cytokine. 2018 May;105:32-36. doi: 10.1016/j.cyto.2018.02.013.
- Xie Y, Su N, Yang J, et al. FGF/FGFR signaling in health and disease. Signal Transduct Target Ther. 2020 Sep 2;5(1):181. doi: 10.1038/s41392-020-00222-7.
- Teng Y, Zhao H, Gao L, Zhang W, Shull AY, Shay C. FGF19 Protects Hepatocellular Carcinoma Cells against Endoplasmic Reti–culum Stress via Activation of FGFR4-GSK3β-Nrf2 Signaling. Cancer Res. 2017 Nov 15;77(22):6215-6225. doi: 10.1158/0008-5472.CAN-17-2039.
- Edirisinghe O, Ternier G, Alraawi Z, Suresh Kumar TK. Decoding FGF/FGFR Signaling: Insights into Biological Functions and Disease Relevance. Biomolecules. 2024 Dec 18;14(12):1622. doi: 10.3390/biom14121622.
- Li F, Li Z, Han Q, et al. Enhanced autocrine FGF19/FGFR4 signaling drives the progression of lung squamous cell carcinoma, which responds to mTOR inhibitor AZD2104. Oncogene. 2020 Apr;39(17):3507-3521. doi: 10.1038/s41388-020-1227-2.
- Zhang X, Wang Z, Tian L, Xie J, Zou G, Jiang F. Increased Expression of FGF19 Contributes to Tumor Progression and Cell Motility of Human Thyroid Cancer. Otolaryngol Head Neck Surg. 2016 Jan;154(1):52-8. doi: 10.1177/0194599815609534.
- Zhao H, Lv F, Liang G, et al. FGF19 promotes epithelial-mesen–chymal transition in hepatocellular carcinoma cells by modulating the GSK3β/β-catenin signaling cascade via FGFR4 activation. Oncotarget. 2016 Mar 22;7(12):13575-86. doi: 10.18632/oncotarget.6185.
- Raja A, Park I, Haq F, Ahn SM. FGF19-FGFR4 Signaling in Hepatocellular Carcinoma. Cells. 2019 Jun 4;8(6):536. doi: 10.3390/cells8060536.
- Hu L, Cong L. Fibroblast growth factor 19 is correlated with an unfavorable prognosis and promotes progression by activating fibroblast growth factor receptor 4 in advanced-stage serous ovarian cancer. Oncol Rep. 2015 Nov;34(5):2683-91. doi: 10.3892/or.2015.4212.
- Gao L, Wang X, Tang Y, Huang S, Hu CA, Teng Y. FGF19/FGFR4 signaling contributes to the resistance of hepatocellular carcinoma to sorafenib. J Exp Clin Cancer Res. 2017 Jan 9;36(1):8. doi: 10.1186/s13046-016-0478-9.
- Chen J, Shao J, Shen A, et al. Enhanced expression of FGF19 predicts poor prognosis in patients with non-small cell lung cancer. J Thorac Dis. 2021 Mar;13(3):1769-1784. doi: 10.21037/jtd-21-126.
- Chen X, Chen J, Feng W, et al. FGF19-mediated ELF4 overexpression promotes colorectal cancer metastasis through transactivating FGFR4 and SRC. Theranostics. 2023 Feb 22;13(4):1401-1418. doi: 10.7150/thno.82269.
- Zhu W, Huang M, Thakur A, Yan Y, Wu X. FGF19 promotes cell autophagy and cisplatin chemoresistance by activating MAPK signaling in ovarian cancer. PeerJ. 2023 Feb 2;11:e14827. doi: 10.7717/peerj.14827.
- Bradford ММ. A rapid and sensitive methods for the quantitation of microgram quantities of protein utilizing the principle of protein-dye binding. Anal Biochem. 1976;72(1):248-254.
- Ungefroren H, Sebens S, Seidl D, Lehnert H, Hass R. Interaction of tumor cells with the microenvironment. Cell Commun Signal. 2011 Sep 13;9:18. doi: 10.1186/1478-811X-9-18.
- Pernot S, Evrard S, Khatib AM. The Give-and-Take Interaction Between the Tumor Microenvironment and Immune Cells Regu–lating Tumor Progression and Repression. Front Immunol. 2022 Apr 13;13:850856. doi: 10.3389/fimmu.2022.850856.
- Garifulin OM, Filonenko VV, Bdzhola AV, et al. Expression of Ribosomal Protein Kinase S6 (S6K1) Isoforms in Different Types of Papillary Thyroid Carcinoma. Cytology and Genetics. 2023;57(4):305-311. doi: 10.3103/S0095452723040059.
- Zinich PP, Pushkarev VM, Bolgov MYu, Guda BB, Pushkarev VV. Molecular mechanisms of the formation of metastases. Mar–kers of metastasis in thyroid carcinoma (review literary). Endokrynologia. 2020;25(3):249-264. doi: 10.31793/1680-1466.2020.25-3.227 (in Ukrainian).
- Guda BB, Pushkarev VM, Pushkarev VV, et al. The expression and activation of extracellular signal-regulated kinase-1/2 and proli–ferating cell nuclear antigen content in normal tissue and human thyroid tumors. SM J Endocrinol Metab. 2015;1(1):1002.
- Guda BB, Pushkarev VV, Kovzun OI, Pushkarev VM, Tronko MD. PCNA expression as a marker of proliferation in benign and highly differentiated malignant tumors of the human thyroid gland (literature review and clinical case). International Journal of Endocrinology. 2019;15(4):339-43. doi: 10.22141/2224-0721.15.4.2019.174822 (in Ukrainian).
- Zinych PP, Pushkarev VM, Levchuk NI, Tronko MD. ZEB1 as a marker of metastasis in thyroid carcinomas: review of literature and own data. Mìžnarodnij endokrinologìčnij žurnal. 2024;20(7):517-528. doi: 10.22141/2224-0721.20.7.2024.1451 (in Ukrainian).
- Kobrynska N, Pushkarev V, Levchuk N, Kovzun O, Komisarenko І, Tronko M. Matrix Metalloproteinase 2 level in blood plasma, thyroid tumors and metastases. Endokrynologia. 2025;30(2):119-123. doi: 10.31793/1680-1466.2025.30-2.119.
- Kobrynska N, Pushkarev V, Levchuk N, et al. TGF-β1 level in differentiated thyroid tumors, metastases and blood plasma. Mìžnarodnij endokrinologìčnij žurnal. 2025 Jul 4;21(4):364-7. doi: 10.22141/2224-0721.21.4.2025.1560.
- Niciporuka R, Nazarovs J, Ozolins A, Narbuts Z, Miklasevics E, Gardovskis J. Can we predict differentiated thyroid cancer behavior? Role of genetic and molecular markers. Medicina (Kaunas). 2021 Oct 19;57(10):1131. doi: 10.3390/medicina57101131.