Журнал «Медицина неотложных состояний» Том 22, №3, 2026
Вернуться к номеру
Вплив гострої та хронічної гіперглікемії на обсяг та локалізацію гострого мозкового інсульту: дані комп’ютерної томографії
Авторы: Ясній О.М. (1), Тріщинська М.А. (1, 2)
(1) - Національний університет охорони здоров’я України імені П.Л. Шупика, м. Київ, Україна
(2) - Клінічна лікарня «Феофанія» ДУС, м. Київ, Україна
Рубрики: Медицина неотложных состояний
Разделы: Клинические исследования
Версия для печати
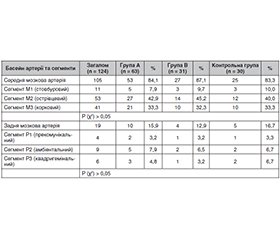
Актуальність. Гострий мозковий інсульт залишається однією з провідних причин смертності та інвалідизації у світі. Важливу роль у перебігу захворювання відіграють метаболічні порушення, зокрема цукровий діабет та гіперглікемія, які асоціюються з більш тяжким ушкодженням мозкової тканини та гіршими клінічними наслідками. Нейровізуалізація є ключовим інструментом ранньої діагностики гострого мозкового інсульту та визначення подальшої лікувальної тактики. Використання шкал ASPECTS та pc-ASPECTS дозволяє об’єктивно оцінити морфологічні зміни мозкової тканини та прогнозувати клінічний перебіг, що зумовлює актуальність вивчення впливу порушень вуглеводного обміну на характеристики ішемічного інсульту. Мета: визначити особливості нейровізуалізаційних змін при гострому мозковому інсульті залежно від стану вуглеводного обміну. Матеріали та методи. У проспективне дослідження включено 124 пацієнти з гострим ішемічним інсультом. Залежно від глікемічного статусу сформовано три групи: пацієнти з цукровим діабетом 2-го типу (n = 63), з транзиторною гіперглікемією (n = 31) та контрольна група без порушень вуглеводного обміну (n = 30). Виконано аналіз локалізації ішемічного ураження та оцінку об’єму ішемічного ядра за шкалами ASPECTS та pc-ASPECTS. Статистичну обробку здійснювали з використанням критерію χ2, p < 0,05 вважали статистично значущим. Результати. Розподіл інсульту за судинними басейнами та сегментами артерій не залежав від глікемічного статусу (p > 0,05). Найчастіше уражався басейн середньої мозкової артерії з переважанням дистальних сегментів М2 та М3. Виявлено статистично значущі відмінності за показниками ASPECTS (p < 0,001). Найвищі середні значення за ASPECTS визначені у групі транзиторної гіперглікемії (9,45), нижчі — у пацієнтів із цукровим діабетом 2-го типу (8,40) та у контрольній групі (8,50). Низькі значення за ASPECTS (≤ 6 балів) спостерігалися переважно при цукровому діабеті 2-го типу. Висновки. Глікемічний статус не впливає на топографію ішемічного ураження, однак асоціюється з його об’ємом. Хронічна гіперглікемія при цукровому діабеті 2-го типу пов’язана з більш вираженими ранніми ішемічними змінами, тоді як транзиторна гіперглікемія характеризується відносно сприятливішими нейровізуалізаційними показниками.
Background. Acute ischemic stroke remains one of the leading causes of mortality and disability worldwide. Metabolic disturbances, particularly diabetes mellitus and hyperglycemia, play a significant role in disease progression, as they are associated with more severe brain tissue injury and poorer clinical outcomes. Neuroimaging is a key tool for the early diagnosis of acute stroke and determining subsequent therapeutic strategies. The use of the ASPECTS and pc-ASPECTS enables objective assessment of morphological brain tissue changes and prediction of clinical course, highlighting the relevance of investigating the impact of carbohydrate metabolism disorders on the characteristics of ischemic stroke. Objective: to determine the features of neuroimaging changes in acute ischemic stroke depending on carbohydrate metabolism status. Materials and methods. A total of 124 patients with acute ischemic stroke were enrolled in this prospective study. According to glycemic status, they were divided into three groups: those with type 2 diabetes mellitus (n = 63), transient hyperglycemia (n = 31), and a control group without carbohydrate metabolism disorders (n = 30). The location of ischemic lesions and ischemic core volume were analyzed using the ASPECTS and pc-ASPECTS. Statistical processing was performed using the χ2 test; p < 0.05 was considered statistically significant. Results. The distribution of stroke according to vascular territories and arterial segments did not depend on glycemic status (p > 0.05). The middle cerebral artery territory was most frequently affected, with a predominance of distal M2 and M3 segments. Statistically significant differences were found in the ASPECTS among the groups (p < 0.001). The mean ASPECTS was highest in the transient hyperglycemia group (9.45), whereas lower values were found in patients with type 2 diabetes mellitus (8.40) and in the control group (8.50). Low ASPECTS (≤ 6 points) was predominantly observed in patients with type 2 diabetes mellitus. Conclusions. Glycemic status does not influence the topography of ischemic lesions but is associated with their volume. Chronic hyperglycemia in type 2 diabetes mellitus is linked to more pronounced early ischemic changes, whereas transient hyperglycemia is characterized by relatively more favorable neuroimaging parameters.
гострий мозковий інсульт; цукровий діабет; глюкоза крові; транзиторна гіперглікемія; шкала ASPECTS; шкала pc-ASPECTS; нейровізуалізація; глюкозний парадокс; лейкоареоз
acute ischemic stroke; diabetes mellitus; blood glucose; transient hyperglycemia; ASPECTS; pc-ASPECTS; neuroimaging; glucose paradox; leukoaraiosis
Для ознакомления с полным содержанием статьи необходимо оформить подписку на журнал.
- Tegegne BA, Adugna A, Yenet A, Belay WY, Yibeltal Y, Dagne A, et al. A critical review on diabetes mellitus type 1 and type 2 management approaches: from lifestyle modification to current and novel targets and therapeutic agents. Front Endocrinol (Lausanne). 2024;15:1440456. doi: 10.3389/fendo.2024.1440456.
- Su J, Luo Y, Hu S, Tang L, Ouyang S. Advances in research on type 2 diabetes mellitus targets and therapeutic agents. Int J Mol Sci. 2023;24(17):13381. doi: 10.3390/ijms241713381.
- Snarska KK, Bachórzewska-Gajewska H, Kapica-Topczewska K, et al. Hyperglycemia and diabetes have different impacts on outcome of ischemic and hemorrhagic stroke. Arch Med Sci. 2017;13(1):100-108. doi: 10.5114/aoms.2016.61009.
- Wang L, Cheng Q, Hu T, et al. Impact of stress hyperglycemia on early neurological deterioration in acute ischemic stroke patients treated with intravenous thrombolysis. Front Neurol. 2022;13:870872. doi: 10.3389/fneur.2022.870872.
- Szlachetka WA, Pana TA, Tiamkao S, et al. Impact of diabetes on complications, long term mortality and recurrence in 608,890 hospitalised patients with stroke. Glob Heart. 2020;15(1):2. doi: 10.5334/gh.364.
- Mogale NM, Ntuli TS, Chelule PK. Barriers to effective ma–nagement of type 2 diabetes mellitus in primary healthcare facilities. J Public Health Afr. 2025;16(1):1420. doi: 10.4102/jphia.v16i1.1420.
- Gieroba B, Kryska A, Sroka-Bartnicka A. Type 2 diabetes mellitus — conventional therapies and future perspectives in innovative treatment. Biochem Biophys Rep. 2025;42:102037. doi: 10.1016/j.bbrep.2025.102037.
- Bushnell C, et al. 2024 guideline for the primary prevention of stroke: a guideline from the American Heart Association/American Stroke Association. Stroke. 2024;55(3):e185-e245. doi: 10.1161/STR.0000000000000475.
- Singh A, Shadangi S, Gupta PK, Rana S. Type 2 diabetes mellitus: a comprehensive review of pathophysiology, comorbidities, and emerging therapies. Compr Physiol. 2025;15(1):e70003. doi: 10.1002/cph4.70003.
- Coutts SB, Lev MH, Eliasziw M, et al. ASPECTS on CTA source images versus unenhanced CT: added value in predicting final infarct extent and clinical outcome. Stroke. 2004;35(11):2472-2476. doi: 10.1161/01.STR.0000145330.14928.2a.
- Ouyang K, Kang Z, Liu Z, et al. Posterior circulation –ASPECTS on CT angiography predicts futile recanalization of endovascular thrombectomy for acute basilar artery occlusion. Front Neurol. 2022;13:831386. doi: 10.3389/fneur.2022.831386.
- Yoo AJ, Berkhemer OA, Fransen PSS, et al. Effect of baseline Alberta stroke program early CT Score on safety and efficacy of intra-arterial treatment: a subgroup analysis of a randomised Phase 3 trial (MR CLEAN). Lancet Neurol. 2016;15(7):685-694. doi: 10.1016/S1474-4422(16)00124-1.
- Khatibi K, Nour M, Tateshima S, et al. Posterior circulation thrombectomy-pc-ASPECT score applied to preintervention magnetic resonance imaging can accurately predict functional outcome. World Neurosurg. 2019;129:e566-e571. doi: 10.1016/j.wneu.2019.05.217.
- Lu WZ, Lin HA, Bai CH, Lin SF. Posterior circulation acute stroke prognosis early CT scores in predicting functional outcomes: a meta-analysis. PLoS One. 2021;16(2):e0246906. doi: 10.1371/journal.pone.0246906.
- Majumder D. Ischemic stroke: pathophysiology and evolving treatment approaches. Neurosci Insights. 2024;19:26331055241292600. doi: 10.1177/26331055241292600.
- Subhash A, Kumar CR, Singh NK, Krishnamurthy S, Nagabushana MV, Visweswara Reddy YJ. Stroke in patients with and without diabetes mellitus. J Clin Sci Res. 2018;7(1):7-11. doi: 10.4103/JCSR.JCSR_8_18.
- Mosenzon O, Cheng AYY, Rabinstein AA, Sacco S. Diabetes and stroke: what are the connections? J Stroke. 2023;25(1):26-38. doi: 10.5853/jos.2022.02306.