Международный эндокринологический журнал Том 22, №3, 2026
Вернуться к номеру
Метаболічно-протеомні детермінанти та імуногенетична транскриптоміка загоєння ран у пластичній і реконструктивній хірургії: когортне дослідження
Авторы: L.P. Sydorchuk (1), R.M. Gumennyi (2), A.R. Sydorchuk (3), V.L. Vasiuk (1), Sai Praveen Daruvuri (4), I.V. Batih (1)
(1) - Bukovinian State Medical University, Chernivtsi, Ukraine
(2) - Bukovinian Center for Plastic and Aesthetic Surgery (PlastArt Clinic), Chernivtsi, Ukraine
(3) - Donauklinik Neu-Ulm, Neu-Ulm, Germany
(4) - St. Mary’s General Hospital, Passaic, New Jersey, USA
Рубрики: Эндокринология
Разделы: Клинические исследования
Версия для печати
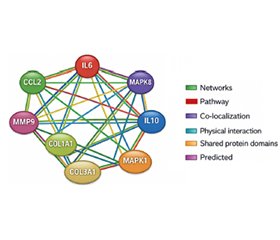
Актуальність. Періопераційний догляд та післяопераційні ускладнення, як-от порушення загоєння ран, інфекція, відторгнення клаптя або трансплантата, патологічне рубцювання, залишаються серйозною клінічною проблемою, що негативно впливає на результати лікування та задоволеність пацієнтів. Мета: оцінити транскрипційну активність генів IL6, CCL2, MAPK1, MAPK8, IL10, MMP9, COL1A1 і COL3A1, функціональних мереж та основних метаболічних й імуногенетичних шляхів, що беруть участь у загоєнні ран у пластичній та реконструктивній хірургії. Матеріали та методи. У проспективному поздовжньому когортному дослідженні взяли участь 95 жінок, які перенесли реконструктивні/пластичні хірургічні втручання. Їхній середній вік становив 35,48 ± 6,61 року (від 19 до 57). Усім жінкам проведено комплекс клінічних, демографічних, лабораторних та інструментальних обстежень. Дослідження виконували відповідно до принципів GCP, Ради Європи з прав людини та біомедицини. Транскрипційну активність генів IL6, CCL2, MAPK1, MAPK8, IL10, MMP9, COL1A1 та COL3A1 у периферичній крові підтверджено за допомогою ПЛР-чипу, специфічного для відповідних сигнальних шляхів. Функціональний зв’язок генів та білок-білкові взаємодії побудовані за допомогою програмного забезпечення GeneMANIA й програми STRING Interaction Network. Результати. Установлено 267 ген-генних взаємодій генів IL6, CCL2, MAPK1, MAPK8, IL10, MMP9, COL1A1, COL3A1 із 20 найбільш залученими генами, що реалізують свою активність переважно через наступні функціональні зв’язки: домінує коекспресія (50,06 %) та колокалізація (31,81 %), значно рідше — загальні білкові домени (8,63 %), передбачувані (5,30 %) та фізичні взаємодії (2,49 %), додаткові сигнальні шляхи (1,71 %). Центральне місце в мережі ген-генної взаємодії належить IL6, який виступає ключовим медіатором прозапальної відповіді та пов’язує імунні (CCL2, IL10), сигнальні (MAPK1, MAPK8) і матриксні (MMP9, COL1A1, COL3A1) компоненти. Ген IL10 демонструє найсильнішу експресію (майже в 3 рази) у взаємодії з геном MAPK8 (М: 2,81 (р = 0,003)), останній активує запалення, ремоделювання, а за надмірної експресії — фіброз. Висновки. Транскрипційна активність генів IL6, CCL2, MAPK1, MAPK8, IL10, MMP9, COL1A1 i COL3A1 впливає на основні метаболічні й імуногенетичні шляхи, що беруть участь у загоєнні ран у пластичній та реконструктивній хірургії.
Background. Perioperative care and postoperative complications, such as impaired wound healing, infection, flap or graft failure, pathological scarring, remain a significant clinical challenge, negatively affecting patient outcomes and satisfaction. The aim of the study is to evaluate the IL6, CCL2, MAPK1, MAPK8, IL10, MMP9, COL1A1 and COL3A1 genes’ transcriptional activity, functional networks, and major metabolic and immunogenetic pathways involved in the wound healing in plastic and reconstructive surgery. Materials and methods. Ninety-five women participated in the prospective longitudinal cohort study and underwent reconstructive/plastic surgery. Their mean age was 35.48 ± 6.61 years (from 19 to 57). All women underwent a set of clinical, demographic, laboratory and instrumental examinations. The study was conducted in accordance with the principles of the GCP, Council of European Convention on Human Rights and Biomedicine. Transcriptional activity of IL6, CCL2, MAPK1, MAPK8, IL10, MMP9, COL1A1 and COL3A1 genes in the peripheral blood was validated by pathway-specific PCR array. Functional linkage of the genes and protein-protein interaction were constructed using GeneMANIA software and the STRING Interaction Network program. Results. Two hundred and sixty-seven gene-gene interactions of the IL6, CCL2, MAPK1, MAPK8, IL10, MMP9, COL1A1, COL3A1 genes were established with the 20 most involved genes, which realize their activity mainly through the following functional linkage: co-expression (50.06 %) and co-localization (31.81 %) dominate, significantly less — common protein domains (8.63 %) and predicted (5.30 %) and physical interactions (2.49 %), additional signaling pathways (1.71 %). The central place in the gene-gene interaction network belongs to IL6, which acts as a key mediator of the pro-inflammatory response and connects immune (CCL2, IL10), signaling (MAPK1, MAPK8), and matrix (MMP9, COL1A1, COL3A1) components. IL10 gene shows the strongest expression (almost 3 times) in interaction with MAPK8 gene (М: 2.81 (р = 0.003)), the latter activates inflammation, remodeling, and with excess expression — fibrosis. Conclusions. The IL6, CCL2, MAPK1, MAPK8, IL10, MMP9, COL1A1 and COL3A1 genes’ transcriptional activity influence major metabolic and immunogenetic pathways involved in the wound healing in plastic and reconstructive surgery.
метаболізм; експресія генів; імунні маркери; протеомна активність; функціональний генетичний зв’язок; механізми; загоєння ран; пластична та реконструктивна хірургія; детермінанти
metabolism; genes expression; immune markers; proteomic activity; functional genetic linkage; mechanisms; wound healing; plastic and reconstructive surgery; determinants
Для ознакомления с полным содержанием статьи необходимо оформить подписку на журнал.
- De Simone B, Abu-Zidan FM, Saeidi S, et al. Knowledge, attitudes and practices of using Indocyanine Green (ICG) fluorescence in emergency surgery: an international web-based survey in the ARtificial Intelligence in Emergency and trauma Surgery (ARIES)-WSES project. Updates Surg. 2024;76(5):1969-1981. doi: 10.1007/s13304-024-01853-z.
- Cobianchi L, Dal Mas F, Massaro M, et al. Diversity and ethics in trauma and acute care surgery teams: results from an international survey. World J Emerg Surg. 2022;17(1):44. doi: 10.1186/s13017-022-00446-8.
- De Simone B, Abu-Zidan FM, Chouillard E, et al. The ChoCO-W prospective observational global study: Does COVID-19 increase gangrenous cholecystitis? World J Emerg Surg. 2022;17(1):61. doi: 10.1186/s13017-022-00466-4.
- Cobianchi L, Dal Mas F, Agnoletti V, et al. Time for a para–digm shift in shared decision-making in trauma and emergency surgery? Results from an international survey. World J Emerg Surg. 2023;18(1):14. doi: 10.1186/s13017-022-00464-6.
- Sen CK. Human Wound and Its Burden: Updated 2020 Compendium of Estimates. Adv Wound Care (New Rochelle). 2021;10(5):281-292. doi: 10.1089/wound.2021.0026.
- Mueller SM, Miller N, Gill J, Yu LC, Pike MD, Orgill DP. Genetic Determinants of Wound Healing: Monogenic Disorders and Polygenic Influence. Cells. 2026;15(1):74. doi: 10.3390/cells15010074.
- Smolanka II, Bagmut IY, Sheremet MI, et al. Delayed breast reconstruction with tram-flap and various modifications after radical mastectomy. J Med Life. 2021;14(6):847-852. doi: 10.25122/jml-2021-0354.
- Semianiv M, Sydorchuk L, Fedonyuk L, et al. Meta–bolic and hormonal prognostic markers of essential arterial hypertension considering the genes polymorphism AGTR1 (rs5186) and VDR (rs2228570). RJDNMD. 2021;28(3):284-91. Available from: https://www.rjdnmd.org/index.php/RJDNMD/article/view/1049.
- Almadani YH, Vorstenbosch J, Davison PG, Murphy AM. Wound Healing: A Comprehensive Review. Semin Plast Surg. 2021;35(3):141-144. doi: 10.1055/s-0041-1731791.
- Amjadian S, Fatemi MJ, Moradi S, Hesaraki M, Mohammadi P. mir-182-5p regulates all three phases of inflammation, proliferation, and remodeling during cutaneous wound healing. Arch Dermatol Res. 2024;316(6):274. doi: 10.1007/s00403-024-03079-w.
- Lin P, Zhang G, Li H. The Role of Extracellular Matrix in Wound Healing. Dermatol Surg. 2023;49(5S):S41-S48. doi: 10.1097/DSS.0000000000003779.
- Xiao Y, Qian J, Deng X, et al. Macrophages regulate healing-associated fibroblasts in diabetic wound. Mol Biol Rep. 2024;51(1):203. doi: 10.1007/s11033-023-09100-1.
- Jin C, Jin Y, Ding Z, et al. Cellular and Molecular Mechanisms of Wound Repair: From Biology to Therapeutic Innovation. Cells. 2025;14(23):1850. doi: 10.3390/cells14231850.
- Limandjaja GC, Niessen FB, Scheper RJ, Gibbs S. The Keloid Disorder: Heterogeneity, Histopathology, Mechanisms and Models. Front Cell Dev Biol. 2020;8:360. doi: 10.3389/fcell.2020.00360.
- Umeyama H, Ding J, Nguyen A, et al. The Roles of SDF-1/CXCR4, MCP-1/CCR2 and CCL5/CCR5 Chemokine Pathway in Hypertrophic Scarring. International Journal of Medical Science and Health Research. 2021;5(2):181-201. doi: 10.51505/ijmshr.2021.5215.
- Zhu S, Liu M, Bennett S, Wang Z, Pfleger KDG, Xu J. The molecular structure and role of CCL2 (MCP-1) and C-C chemo–kine receptor CCR2 in skeletal biology and diseases. J Cell Physiol. 2021;236(10):7211-7222. doi: 10.1002/jcp.30375.
- Meng XM, Nikolic-Paterson DJ, Lan HY. TGF-β: the master regulator of fibrosis. Nat Rev Nephrol. 2016;12(6):325-38. doi: 10.1038/nrneph.2016.48.
- Liu J, Wang Y, Tang C, Zhang L, Xiong S, Wang J, Dong C. TGF-β in tumor development and progression: mechanisms and therapeutics. Mol Biomed. 2026;7(1):9. doi: 10.1186/s43556-026-00403-w.
- Deshmane SL, Kremlev S, Amini S, Sawaya BE. Monocyte chemoattractant protein-1 (MCP-1): an overview. J Interferon Cytokine Res. 2009;29(6):313-26. doi: 10.1089/jir.2008.0027.
- Ma YT, Li C, Shen Y, You WH, Han MX, Mu YF, Han FJ. Mechanisms of the JNK/p38 MAPK signaling pathway in drug resistance in ovarian cancer. Front Oncol. 2025;15:1533352. doi: 10.3389/fonc.2025.1533352.
- Wagner EF, Nebreda AR. Signal integration by JNK and p38 MAPK pathways in cancer development. Nat Rev Cancer. 2009;9(8):537-49. doi: 10.1038/nrc2694.
- Yu J, Li X, Cao J, Zhu T, Liang S, Du L, et al. Components of the JNK-MAPK pathway play distinct roles in hepatocellular carcinoma. J Cancer Res Clin Oncol. 2023;149(19):17495-17509. doi: 10.1007/s00432-023-05473-9.
- Ge Q, Zhang J, Fan Z, et al. Wnt11 mediates fibroblast-smooth muscle cell interaction to promote neurogenic bladder fibrosis in rats. Commun Biol. 2026;9(1):194. doi: 10.1038/s42003-026-09647-2.
- Vandooren J, Van den Steen PE, Opdenakker G. Biochemi–stry and molecular biology of gelatinase B or matrix metalloproteinase-9 (MMP-9): the next decade. Crit Rev Biochem Mol Biol. 2013;48(3):222-72. doi: 10.3109/10409238.2013.770819.
- Nahornyi OV, Ziablitsev SV. Pathogenetic role of transfor–ming growth factor beta (TGF-β) in the mechanisms of development of diabetic nephropathy (literature review). Medical Science of Ukraine. 2025;21(1):128-139. doi: 10.32345/2664-4738.1.2025.16.
- Sydorchuk AR, Sydorchuk LP, Gutnitska AF, et al. Endothelium function regulation markers and carotid intima-media thickness in arterial hypertension depending on NOS3 (rs2070744) and GNB3 (rs5443) genes polymorphism: a prospective case-control study. Endocrine Regulations. 2022;56(2):104-114. doi: 10.2478/enr-2022-0012.
- Sydorchuk A, Sydorchuk L, Gutnitska A, et al. The role of NOS3 (rs2070744) and GNB3 (rs5443) genes’ polymorphisms in endothelial dysfunction pathway and carotid intima-media thickness in hypertensive patients. General Physiology and Biophysics. 2023;42(2):179-190. doi: 10.4149/gpb_2022060.
- Sydorchuk LP, Dzhuryak VS, Sydorchuk AR, et al. Association of lipids’ metabolism disorders with aldosterone synthase CYP11B2 (-344C/T) gene polymorphism in hypertensive patients depending on glomerular filtration rate. Pharmacology OnLine. 2020;2:230-242. Available from: https://pharmacologyonline.silae.it/files/archives/2020/vol2/PhOL_2020_2_A023_Sydorchuk.pdf.
- Rose-John S. Interleukin-6 signalling in health and disease. F1000Res. 2020;9:F1000 Faculty Rev-1013. doi: 10.12688/f1000research.26058.1.
- Barabási AL, Gulbahce N, Loscalzo J. Network medicine: a network-based approach to human disease. Nat Rev Genet. 2011 Jan;12(1):56-68. doi: 10.1038/nrg2918.
- Richards AL, Eckhardt M, Krogan NJ. Mass spectrometry-based protein-protein interaction networks for the study of human diseases. Molecular Systems Biology. 2021;17:e8792. doi: 10.15252/msb.20188792.
- Grebenciucova E, VanHaerents S. Interleukin 6: at the interface of human health and disease. Front Immunol. 2023 Sep 28;14:1255533. doi: 10.3389/fimmu.2023.1255533.
- Schumertl T, Lokau J, Garbers C. IL-6 Signaling in Immunopathology: From Basic Biology to Selective Therapeutic Intervention. Immunotargets Ther. 2025;14:681-695. doi: 10.2147/ITT.S485684.
- Chen X, Zhang J, Guo L, et al. Decoding organ fibrosis: mechanistic insights and emerging therapeutic strategies. Sig Transduct Target Ther. 2026;11:82. doi: 10.1038/s41392-025-02532-0.
- Grafanaki K, Maniatis A, Sotiropoulou V, Pasmatzi E, Tzouvelekis A. Fibrotic Disease of the Skin and Lung: Shared Pathways, Environmental Drivers, and Therapeutic Opportunities in a Changing Climate. International Journal of Molecular Sciences. 2025;26(17):8394. doi: 10.3390/ijms26178394.
- Johnson BZ, Stevenson AW, Prêle CM, Fear MW, Wood FM. The Role of IL-6 in Skin Fibrosis and Cutaneous Wound Healing. Biomedicines. 2020;8(5):101. doi: 10.3390/biomedicines8050101.
- Wu J, Chen M, Peng Z, Sun Y, Jin J. Mechanism and research progress of MAPK signaling pathway in myocardial fibrosis. Front Cardiovasc Med. 2025 Nov 21;12:1667568. doi: 10.3389/fcvm.2025.1667568.
- Wang X, Liu R, Liu D. The Role of the MAPK Signaling Pathway in Cardiovascular Disease: Pathophysiological Mechanisms and Clinical Therapy. International Journal of Molecular Sciences. 2025;26(6):2667. doi: 10.3390/ijms26062667.
- Steen EH, Wang X, Balaji S, Butte MJ, Bollyky PL, Keswani SG. The Role of the Anti-Inflammatory Cytokine Interleukin-10 in Tissue Fibrosis. Adv Wound Care (New Rochelle). 2020 Apr 1;9(4):184-198. doi: 10.1089/wound.2019.1032.
- Mayorca-Guiliani AE, Leeming DJ, Henriksen K, et al. ECM formation and degradation during fibrosis, repair, and regeneration. NPJ Metab Health Dis. 2025;3(1):25. doi: 10.1038/s44324-025-00063-4.
- Cabral-Pacheco GA, Garza-Veloz I, Castruita-De la Rosa C, Ramirez-Acuña JM, Perez-Romero BA, Guerrero-Rodriguez JF, et al. The Roles of Matrix Metalloproteinases and Their Inhibitors in Human Diseases. Int J Mol Sci. 2020 Dec 20;21(24):9739. doi: 10.3390/ijms21249739.
- Singampalli KL, Balaji S, Wang X, et al. The Role of an IL-10/Hyaluronan Axis in Dermal Wound Healing. Front Cell Dev Biol. 2020 Jul 17;8:636. doi: 10.3389/fcell.2020.00636.
- Peña OA, Martin P. Cellular and molecular mechanisms of skin wound healing. Nat Rev Mol Cell Biol. 2024;25(8):599-616. doi: 10.1038/s41580-024-00715-1.
- Wong RSY, Tan T, Pang ASR, Srinivasan DK. The role of cytokines in wound healing: from mechanistic insights to therapeutic applications. Explor Immunol. 2025;5:1003183. doi: 10.37349/ei.2025.1003183.