Международный эндокринологический журнал Том 22, №3, 2026
Вернуться к номеру
Роль фактора росту судинного ендотелію С в метастазуванні при папілярному раку щитоподібної залози
Авторы: N.Ya. Kobrynska, I.I. Komisarenko, V.M. Pushkarev, N.I. Levchuk, O.I. Kovzun, B.B. Guda, V.V. Pushkarev, M.D. Tronko
V.P. Komisarenko Institute of Endocrinology and Metabolism of NAMSU, Kyiv, Ukraine
Рубрики: Эндокринология
Разделы: Клинические исследования
Версия для печати
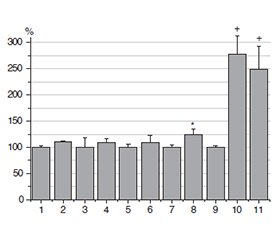
Актуальність. Система фактора росту судинного ендотелію (VEGF) включає кілька лігандів: VEGF-A, VEGF-B, VEGF-C, VEGF-D та їх рецептори: VEGFR-1, VEGFR-2 і VEGFR-3. VEGF-A переважно сигналізує через VEGFR-2, сприяючи проліферації, міграції та виживанню ендотеліальних клітин. VEGF-C та VEGF-D особливо важливі для лімфангіогенезу через VEGFR-3, що має велике значення для метастазування у лімфатичних вузлах при раку щитоподібної залози. Мета: порівняння вмісту VEGF-С у зразках умовно нормальної (УН) тканини щитоподібної залози, фолікулярної аденоми, зоба, папілярної карциноми щитоподібної залози (ПКЩЗ), метастазів (Мтс), а також у плазмі крові й мононуклеарних клітинах периферичної крові (МНКПК) пацієнтів із ПКЩЗ. Матеріали та методи. Післяопераційні зразки тканин, плазми крові та клітин були отримані в хірургічному відділенні клініки ІЕОР. Кількість VEGF визначали за допомогою наборів для імуноферментного аналізу. Результати. Рівні VEGF у доброякісних новоутвореннях не відрізнялися від таких в УН тканині. Спостерігалася вірогідна різниця між УН тканиною та тканинами ПКЩЗ без метастазів. Рівень VEGF у тканинах ПКЩЗ із метастазами був приблизно у 2,5 раза вищим, ніж в УН тканині. Високий уміст VEGF-C спостерігався в тканині з Мтс. Концентрація VEGF у тканині ПКЩЗ із Мтс перевищувала таку в тканині ПКЩЗ без метастазів більше ніж у 2 рази. У плазмі та, особливо, МНКПК пацієнтів із ПКЩЗ уміст VEGF був значно вищий за контрольні значення, але не спостерігалося відмінностей між зразками з Мтс та без них. Висновки. Рівні VEGF-С у доброякісних новоутвореннях щитоподібної залози не відрізнялися від таких в УН тканині. У тканинах ПКЩЗ із метастазами концентрації VEGF-C були значно підвищені порівняно з УН тканиною та ПКЩЗ без метастазів. Наші результати допомогли виявити значні відмінності в рівнях VEGF між тканинами ПКЩЗ із Мтс та без них, що може бути корисним для прогнозування метастатичного потенціалу пухлини. Рівень VEGF у плазмі та МНКПК може стати основою для діагностики ПКЩЗ у передопераційному періоді.
Background. The vascular endothelial growth factor (VEGF) system includes several ligands: VEGF-A, VEGF-B, VEGF-C, VEGF-D and their receptors: VEGFR-1, VEGFR-2, and VEGFR-3. VEGF-A primarily signals through VEGFR-2, promoting endothelial cell proliferation, migration, and survival. VEGF-C and VEGF-D are particularly important for lymphangiogenesis via VEGFR-3, which is highly relevant to lymph node metastasis in thyroid cancer. The aim of this study was to compare levels of VEGF in tissue samples of conditionally normal (CN) thyroid tissue, follicular adenoma, goiters, papillary thyroid carcinoma (PTC), metastasis (Mts), as well as in blood plasma and peripheral blood mononuclear cells (PBMC) of patients with PTC. Materials and methods. Postoperative samples of tissue, blood plasma, and cells were obtained from the surgical department of the IEM clinic. The amount of VEGF was determined using enzyme immunoassay kits. Results. VEGF levels in benign neoplasms did not differ from those in CN tissue. There was significant difference between CN tissue and РТС tissues without Mts. The level of VEGF-C in the РТС tissues with Mts was ~ 2.5 times higher than in CN tissues. The high level of VEGF-C was observed in the Mts tissue. The VEGF-C concentration in PTC tissue with Mts exceeded its level in the PTC tissues without Mts by more than 2 times. In plasma and, especially, PBMC of PTC patients, VEGF-C concentration significantly exceeded control levels but there were no differences between specimens with and without Mts. Conclusions. VEGF-C levels in benign thyroid neoplasms did not differ from those in CN tissue. In PTC tissues with Mts, VEGF-C concentrations were significantly elevated compared to CN and PTC tissues without Mts. Our findings reveal significant differences in VEGF concentrations between PTC tissues with and without Mts, which may be useful for predicting metastatic potential of tumor. The level of VEGF-C in plasma and PBMC can become the basis for PTC diagnosis in the preoperative period.
фактор росту судинного ендотелію С; папілярна карцинома щитоподібної залози; метастази; доброякісні новоутворення
vascular endothelial growth factor C; papillary thyroid carcinoma; metastasis; benign neoplasms
Для ознакомления с полным содержанием статьи необходимо оформить подписку на журнал.
- Tronko ND, Pushkarev VM. 30 years of the Chernobyl accident. Molecular genetic mechanisms of carcinogenesis of thyroid gland. Cytol Genet. 2016 Nov-Dec;50(6):15-22.
- Guda BB, Pushkarеv VM, Kovalenko AE, Pushkarev VV, Kovzun ОI, Tronko МD. Molecular genetic mechanisms of the pathogenesis of thyroid malignant tumors (review of literature and own data, part 1). Endokrynologia. 2019;24(1):53-65. doi: 10.31793/1680-1466.2019.24-1.53 (in Ukrainian).
- Qian B, Guo S, Zhou J, Qu X, Zhang S. Intraglandular disse–mination is a risk factor for lymph node metastasis in papillary thyroid carcinoma: a propensity score matching analysis. Gland Surg. 2021 Dec;10(12):3169-3180. doi: 10.21037/gs-21-470.
- Li Z, Wang N, Li X, et al. Thyroid cancer: From molecular insights to therapy (Review). Oncol Lett. 2025 Sep 10;30(5):520. doi: 10.3892/ol.2025.15266.
- Yang Y, Cao Y. The impact of VEGF on cancer metastasis and systemic disease. Semin Cancer Biol. 2022 Nov;86(Pt 3):251-261. doi: 10.1016/j.semcancer.2022.03.011.
- Kokkotou E, Charpidou A, Syrigos N. Predictive Value of Serum VEGF Levels in Non-Small Cell Lung Cancer: A Review. Oncol Res. 2025 Sep 26;33(10):2657-2672. doi: 10.32604/or.2025.066228.
- Vatseba TS, Sokolova LK, Pushkarev VV, et al. Activation of the PI3K/Akt/mTOR/p70S6K1 signaling cascade in the mononuclear cells of peripheral blood: association with insulin and insulin-like growth factor levels in the blood of patients with cancer and diabetes. Cytol Genet. 2019;53(6):489-493. doi: 10.3103/S0095452719060112.
- Bradford MM. A rapid and sensitive method for the quantitation of microgram quantities of protein utilizing the principle of protein-dye binding. Anal Biochem. 1976;72(1):248-254. doi: 10.1016/0003-2697(76)90527-3.
- Choi JU, Chung SW, Al-Hilal TA, et al. A heparin conjugate, LHbisD4, inhibits lymphangiogenesis and attenuates lymph node metastasis by blocking VEGF-C signaling pathway. Biomaterials. 2017 Sep;139:56-66. doi: 10.1016/j.biomaterials.2017.05.026.
- Hung CJ, Ginzinger DG, Zarnegar R, et al. Expression of vascular endothelial growth factor-C in benign and malignant thyroid tumors. J Clin Endocrinol Metab. 2003 Aug;88(8):3694-9. doi: 10.1210/jc.2003-030080.
- Yu XM, Lo CY, Chan WF, Lam KY, Leung P, Luk JM. Increased expression of vascular endothelial growth factor C in papillary thyroid carcinoma correlates with cervical lymph node metastases. Clin Cancer Res. 2005 Nov 15;11(22):8063-9. doi: 10.1158/1078-0432.CCR-05-0646.
- Yu XM, Lo CY, Lam AK, Leung P, Luk JM. Serum vascular endothelial growth factor C correlates with lymph node metastases and high-risk tumor profiles in papillary thyroid carcinoma. Ann Surg. 2008 Mar;247(3):483-9. doi: 10.1097/SLA.0b013e31815fa447.
- Gao B, Guo L, Luo D, et al. Steroid receptor coactivator-1 interacts with NF-κB to increase VEGFC levels in human thyroid cancer. Biosci Rep. 2018 Jun 12;38(3):BSR20180394. doi: 10.1042/BSR20180394.
- Xu SJ, Jin B, Zhao WJ, et al. The Specifically Androgen-Regu–lated Gene (SARG) Promotes Papillary Thyroid Carcinoma (PTC) Lymphatic Metastasis Through Vascular Endothelial Growth Factor C (VEGF-C) and VEGF Receptor 3 (VEGFR-3) Axis. Front Oncol. 2022 Jun 13;12:817660. doi: 10.3389/fonc.2022.817660.
- Buczyńska A, Kościuszko M, Krętowski AJ, Popławska-Kita A. Exploring the clinical utility of angioinvasion markers in papillary thyroid cancer: a literature review. Front Endocrinol (Lausanne). 2023 Nov 27;14:1261860. doi: 10.3389/fendo.2023.1261860.
- Buczyńska A, Kościuszko M, Adamska A, et al. Impact of nitrosative stress and endothelial damage on angioinvasive papillary thyroid cancer. Sci Rep. 2025 Jul 19;15(1):26245. doi: 10.1038/s41598-025-10982-3.
- Marini A, Chatzoglou T, Ntritsos G, et al. The Prognostic Role of Lymphatic Vessel Density in Papillary Thyroid Carcinoma: A Systematic Review and Meta-analysis. Cancer Diagn Progn. 2025 Sep 1;5(5):542-551. doi: 10.21873/cdp.10468.
- Huang J, Li Y, Xue G, et al. Value of VEGF-C, VEGF-D and VEGFR-3 levels combined with serum TSH in diagnosis of papil–lary thyroid carcinoma. Nan Fang Yi Ke Da Xue Xue Bao. 2014 Dec;34(12):1814-7, 1821.
- Zhou ZH, Cui XN, Xing HG, Yan RH, Yao DK, Wang LX. Changes and prognostic value of serum vascular endothelial growth factor in patients with differentiated thyroid cancer. Med Princ Pract. 2013;22(1):24-8. doi: 10.1159/000340051.
- Kong D, Zhou H, Neelakantan D, et al. VEGF-C media–tes tumor growth and metastasis through promoting EMT-epithelial breast cancer cell crosstalk. Oncogene. 2021 Feb;40(5):964-979. doi: 10.1038/s41388-020-01539-x.
- Banerjee K, Kerzel T, Bekkhus T, et al. VEGF-C-expressing TAMs rewire the metastatic fate of breast cancer cells. Cell Rep. 2023 Dec 26;42(12):113507. doi: 10.1016/j.celrep.2023.113507.
- Ceric S, Ceric T, Pojskic N, Bilalovic N, Musanovic J, Kucukalic-Selimovic E. Immunohistochemical expression and prognostic significance of VEGF-C in well-differentiated thyroid cancer. Acta Endocrinol (Buchar). 2020 Oct-Dec;16(4):409-416. doi: 10.4183/aeb.2020.409.
- Enokida T, Tahara M. Management of VEGFR-Targeted TKI for Thyroid Cancer. Cancers (Basel). 2021 Nov 4;13(21):5536. doi: 10.3390/cancers13215536.
- Mederle AL, Stana LG, Ilie AC, et al. Efficacy and Safety of Pazopanib in the Treatment of Thyroid Cancer: A Systematic Review. Biomedicines. 2024;12(12):2820. doi: 10.3390/biomedicines12122820.
- Mahaki H, Nobari S, Tanzadehpanah H, et al. Targeting VEGF signaling for tumor microenvironment remodeling and metastasis inhibition: Therapeutic strategies and insights. Biomed Pharmacother. 2025 May;186:118023. doi: 10.1016/j.biopha.2025.118023.
- Shi Z, Kuai M, Li B, et al. The role of VEGF in cancer angiogenesis and tumorigenesis: Insights for anti-VEGF therapy. Cytokine. 2025 May;189:156908. doi: 10.1016/j.cyto.2025.156908.
- Kobrynska NYa, Pushkarev VM, Levchuk NI, et al. Hypoxia-inducible factor-1α level in blood plasma, thyroid tumors and metastases. Problems of Endocrine Pathology. 2025;4:14-18. doi: 10.21856/j-PEP.2025.4.02.
- Kobrynska NYa, Pushkarev VM, Levchuk NI, et al. Matrix metalloproteinase 2 level in blood plasma, thyroid tumors and metastases. Endokrynologia. 2025;30(2):119-23. doi: 10.31793/1680-1466.2025.30-2.119.
- Kobrynska NYa, Pushkarev VM, Levchuk NI, et al. TGF-β1 level in differentiated thyroid tumors, metastases and blood plasma. Mìžnarodnij endokrinologìčnij žurnal. 2025;21(4):364-7. doi: 10.22141/2224-0721.21.4.2025.1560.
- Guda BB, Pushkarev VV, Kovzun OI, Pushkarev VM, Tronko MD. PCNA expression as a marker of proliferation in benign and highly differentiated malignant tumors of the human thyroid gland (literature review and clinical case). Mìžnarodnij endokrinologìčnij žurnal. 2019;15(4):339-43. doi: 10.22141/2224-0721.15.4.2019.174822 (in Ukrainian).
- Garifulin OM, Filonenko VV, Bdzhola AV, et al. Expression of Ribosomal Protein Kinase S6 (S6K1) Isoforms in Different Types of Papillary Thyroid Carcinoma. Cytology and Genetics. 2023;57(4):305-311. doi: 10.3103/S0095452723040059.
- Zinych PP, Pushkarev VM, Levchuk NI, Tronko MD. ZEB1 as a marker of metastasis in thyroid carcinomas: review of literature and own data. Mìžnarodnij endokrinologìčnij žurnal. 2024;20(7):517-528. doi: 10.22141/2224-0721.20.7.2024.1451 (in Ukrainian).
- Zinych PP, Pushkarev VM, Levchuk NI, Shelkovoy EA, Bolgov MYu. Expression of tight junction zonula occludens-1 protein in thyroid carcinomas. Endokrynologia. 2025;30(4):291-295. doi: 10.31793/1680-1466.2025.30-4.291.