Газета «Новости медицины и фармации» Инфекционные болезни, гепатология (281) 2009 (тематический номер)
Вернуться к номеру
Інтерферонотерапія хронічного гепатиту С і депресія: можливості профілактики і лікування
Із використанням α-2a- і α-2b-інтерферонів у лікуванні хворих на вірусний гепатит С пов''язане виникнення психоневрологічних ознак — від підвищеної стомлюваності та дратівливості до розвитку клініки повної депресії [1–6]. Особливі складності постають перед лікарем у випадках лікування хронічного гепатиту С у психіатричних хворих або у хворих з депресією в анамнезі.
Депресія (від depressio — придушення, гноблення) — психічний розлад, що характеризується патологічно зниженим настроєм з негативною, песимістичною оцінкою себе, свого становища в навколишній дійсності й свого майбутнього.
Згідно з міжнародною класифікацією DSM IV, для депресії характерна наявність 5 симптомів, включаючи 1 або 2 обов''язкові симптоми, упродовж не менше двох тижнів (С. Raіson et al., 2007).
Обов''язкові симптоми:
Додаткові симптоми:
Депресивна зміна настрою супроводжується моторним та ідеаторним (розумовим) гальмуванням, зниженням спонукань до діяльності, соматовегетативною дисфункцією.
Типи розладів настрою
За DSM ІV виділяють 7 класів розладів настрою:
Виникнення депресії пояснюють функціональним дефіцитом норадреналіну й серотоніну (моноамінова теорія).
Клінічні наслідки підвищення дофамінової активності
Позитивні ефекти:
Негативні ефекти:
Унаслідок дефіциту серотоніну виникають зниження лібідо, порушення апетиту, дратівливість, ажитація, суїцидальні думки.
Дефіцит норадреналіну призводить до апатії, загальмованості, порушення концентрації уваги, знесилення, утомлюваності; підвищення норадренергічної активності може викликати порушення сну й безсоння, труднощі концентрації уваги, а також серцево-судинні розлади (серцебиття, тахікардія).
Одночасна наявність дефіциту норадреналіну й серотоніну є причиною втрати інтересів, пригнічення настрою, зниження самооцінки, порушення сну, тривоги.
Фактори ризику інтерферонової депресії (за С. Raison et al., 2005):
Фактори ризику депресії під час ІFN-терапії (Raison C.L. et al. // J. Clin. Psychiatry. 2005; 66: 41-48; Capuron L. et al. // N. Engl. J. Med. 1999; 340: 1370)
Ключовий фактор ризику депресії під час ІФН-терапії — наявність симптомів депресії до або під час лікування.
Іншими факторами ризику депресії є:
Підхід до вирішення психіатричних проблем під час HCV-терапії (Schaefer M. et al. // Current Drug Abuse Reviews. 2008; 1: 177-187)
Депресія, як відомо, є одним із найбільш загальних і тяжко контрольованих явищ у пацієнтів з гепатитом С, які виникають у зв''язку з інтерферонотерапією.
Дані результатів досліджень депресій, що виникають при ІFN-терапії
Було проаналізовано 21 клінічне дослідження HCV-інфікованих пацієнтів з ІFN-асоційованою депресією. Визначення депресії, стратегія лікування і його тривалість в зазначених дослідженнях відрізнялися (рис. 1).
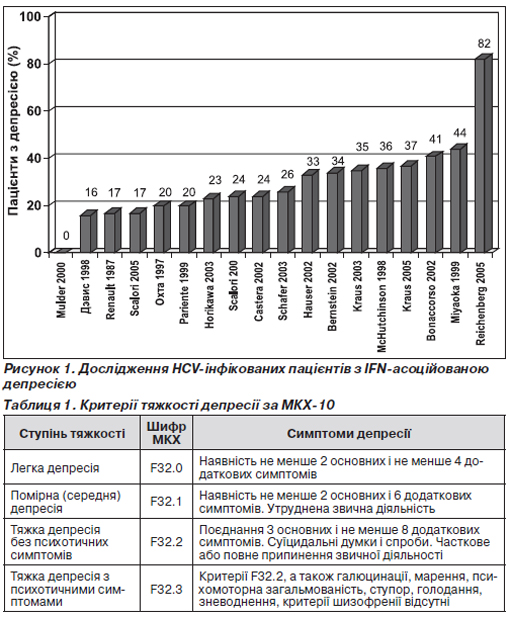
Психіатричні побічні впливи, особливо депресія, можуть спричинити необхідність зменшення дози ліків і навіть припинення лікування, що призводить до зниження кінцевої ефективності інтерферонотерапії [7, 8].
Депресія частіше зустрічається в пацієнтів із HCV порівняно з популяцією (Lang C.A. et al. // J. Pain Sym. Manage. 2006; 31: 335-344)
Критерії тяжкості депресії за МКХ-10
Корекція дози пегільованого інтерферону (pegІFN) при депресії
1. При легкому ступені корекції не потрібно, спостереження (1-й тиждень), при стабілізації — щотижневе спостереження, при нормалізації — звичайний режим спостереження, при погіршенні — зниження дози.
2. При середньому ступені тяжкості — зниження дози до 135 мкг/тиж (до 90 мкг/тиж), спостереження (1-й тиждень); при стабілізації — продовження приймання в зниженій дозі, при поліпшенні й стабілізації (1-й місяць) — звичайний режим спостереження, приймання препарату в зниженій або початковій дозі.
3. При тяжкій депресії — скасування препарату, консультація психіатра, використання антидепресантів.
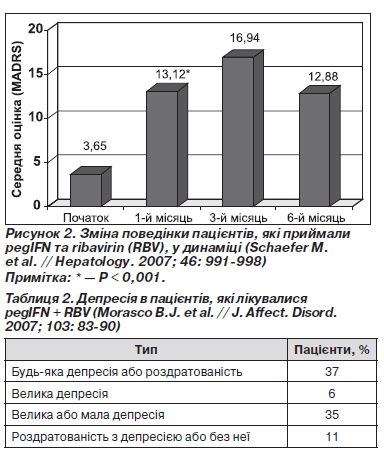
Зміна поведінки пацієнтів, які приймали pegІFN та ribavirin (RBV), у динаміці
17 пацієнтів без психічних захворювань або наркозалежності приймали pegIFN + RBV. Більшість депресивних ознак виникли протягом перших 1–3 місяців терапії (рис. 2).
На сьогодні наявність депресії в анамнезі не є протипоказанням до терапії хронічного гепатиту С, але свідчить про більшу вірогідність її розвитку в процесі інтерферонотерапії [3, 9–14]. Саме тому перед початком курсу лікування хворого на хронічний гепатит С необхідно з''ясувати, чи була депресія в минулому, та оцінити можливість її повторення.
Депресія в пацієнтів із гепатитом С унаслідок терапії рegIFN + RBV
176 HCV-інфікованих пацієнтів, які лікувались pegІFN a-2a + RBV, оцінювалися на предмет наявності депресії й дратівливості на початку й протягом терапії. Пацієнти з порушеннями поведінки були виключені (n = 30). Було виявлено високий відсоток проявів синдромів депресії та роздратованості під час лікування (табл. 2).
У країнах Європи в пацієнтів із депресією в анамнезі типовою є клінічна оцінка їх психіатричного статусу психіатром перед прийняттям рішення про терапію гепатиту С з метою оцінки потенційного ризику депресії під час інтерферонотерапії та необхідності використання антидепресантів до початку курсу лікування гепатиту.
За відсутності депресії в анамнезі та інших факторів ризику немає потреби в консультації психіатра до початку курсу інтерферонотерапії.
У штатний розклад багатьох гепатологічних центрів європейських країн введені посади фахівців (психолог, психіатр), які мають досвід роботи з HCV-інфікованими пацієнтами та беруть участь у їх лікуванні як до призначення курсу інтерферонотерапії, так і під час його проведення.
Тактика використання профілактичного курсу антидепресантів корисна в двох випадках: у пацієнтів із депресією під час попереднього курсу терапії гепатиту С [16] та в пацієнтів з ознаками депресії взагалі [17]. Проте необхідно зазначити, що вказана тактика офіційно ще не рекомендована в стандартах терапії гепатиту С і зазвичай не використовується всіма лікарями [18].
Із метою профілактики депресії та оцінки її ефективності в межах проведення клінічних досліджень у країнах Європи використовується paroxetin [15, 19]. Проте, на думку P. Marcellin (2008), поки що відсутні дані, які свідчать про більшу ефективність paroxetin порівняно з іншими антидепресантами.
Однією з частих ознак хронічного гепатиту С і його лікування є слабкість. У хворих на гепатит С, які не отримують противірусних засобів, слабкість реєструється у 86 % випадків [20]. У той же час слабкість — це одна з ключових клінічних ознак для ідентифікації депресії. Крім того, ця ознака є загальним симптомом побічного впливу інтерферонотерапії, що може проявитися незалежно від депресії та може посилитись на тривалий час [1]. Саме тому в пацієнтів зі слабкістю важливо встановити її основну причину.
Оцінка вираженості депресії та слабкості внаслідок ІФН-терапії
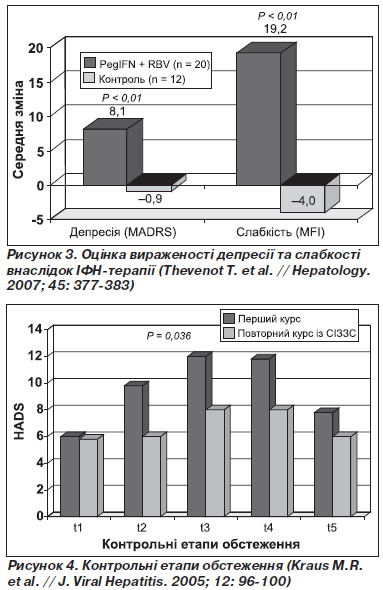 Так, наприклад, слабкість є ключовою ознакою анемії, тому необхідно оцінити рівень гемоглобіну. Якщо анемія ідентифікована як основна причина слабкості, важливо, з одного боку, зменшити значення анемії у виникненні ознак депресії і, з іншого боку, допомогти пацієнту дотримуватись оптимальних доз противірусних засобів відповідно до маси тіла.
Так, наприклад, слабкість є ключовою ознакою анемії, тому необхідно оцінити рівень гемоглобіну. Якщо анемія ідентифікована як основна причина слабкості, важливо, з одного боку, зменшити значення анемії у виникненні ознак депресії і, з іншого боку, допомогти пацієнту дотримуватись оптимальних доз противірусних засобів відповідно до маси тіла.
Як показують клінічні дослідження [21], для корекції ribavirin-обумовленої анемії ефективним виявився epoetin alfa, що призначають при зниженні рівня гемоглобіну < 10 г/дл; лікування продовжують до підвищення гемоглобіну не більше 12 г/дл [22]. За даними P. Marcellin (2008), у Франції частина фахівців не зменшують дозу ribavirin з метою збереження максимальної ефективності терапії та збільшення числа SVR; інші спочатку зменшують дозу ribavirin та спостерігають за рівнем гемоглобіну й тільки потім приймають рішення про використання epoetin alfa. Для оцінки ефективності вказаних тактичних прийомів наразі продовжуються рандомізовані клінічні дослідження.
Пацієнти з хронічним гепатитом С, окрім психіатричних хвороб, часто страждають від наркоманії. Поширеність зміни настрою, неспокою, дратівливості та психотичних синдромів збільшена у HCV-інфікованих [23]. Крім того, повідомляється про збільшення кількості хворих зі зміною настрою, виникненням депресії [24], маніїї [25, 26] cеред хворих на гепатит С під час інтерферонотерапії [27–30].
Як стверджує M. Schafer (2008), психіатричне обстеження пацієнтів повинне бути проведене досвідченими психіатрами перед призначенням противірусних засобів, тому що більшість терапевтів і гепатологів не володіють навичками виявлення певних психіатричних проблем.
Крім того, рекомендується навчити членів сім''ї, родичів та друзів хворого методам раннього розпізнавання психічних змін, що можуть виникнути під час інтерферонотерапії [31].
У більшості клінічних досліджень у США та Європі з метою попередження депресії за 2 тижні до початку інтерферонотерапії проводять лікування антидепресантами.
Попередній курс приймання селективних інгібіторів зворотного захвату серотоніну в пацієнтів з повторним лікуванням HCV
Пацієнти, у яких розвинулася велика депресія під час першого курсу ІFN-терапії, пройшли попереднє лікування селективними інгібіторами зворотного захвату серотоніну (СІЗЗС) перед повторним курсом противірусної терапії (n = 8). Прояви депресії при повторному курсі зменшилися (рис. 4).
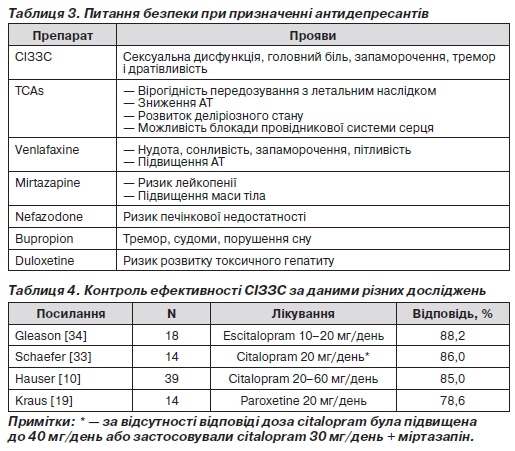
Вторинна спорідненість СІЗЗС до сигма-рецепторів
Позитивні ефекти:
Негативні ефекти:
Так, у декількох відкритих клінічних дослідженнях використовуються різні антидепресанти у хворих на хронічний гепатит С та розвитком депресії: citalopram, escitaloptram, paroxetin. І тільки в одному дослідженні наводяться дані про лікування депресії, що виникла під час інтерферонотерапії, з ефективним використанням СІЗЗС
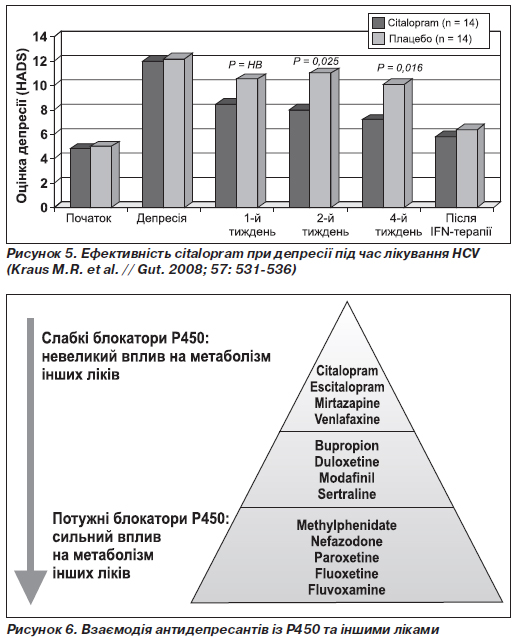
Лікування депресії, пов''язаної з HCV-терапією (Kraus M.R. et al. // Aliment. Pharmacol. Ther. 2002; 16: 1091-1099; Kra-us M.R. et al. // Gut. 2008; 57: 531-536):
— trіmіpramіne/nefazodone;
— sertralіne;
— paroxetіne;
— cіtalopram;
— плановане дослідження лікування гострих форм.
Питання безпеки при призначенні антидепресантів висвітлені в табл. 4.
Ефективність антидепресантів у пацієнтів, які отримують ІФН-терапію
Контроль ефективності СІЗЗС за даними різних досліджень подано в табл. 4.
Пацієнти із психіатричними проблемами: протягом HCV-терапії і після неї (Raison C. et al. // CNS Drugs. 2005; 19: 105-123)
Ефективність citalopram при депресії під час лікування HCV відображено на рис. 5.
Загалом, подібна ефективність спостерігається у багатьох СІЗЗС. Але paroxetin, як відомо, впливає на цитохром Р450, а тому може порушувати метаболізм інших лікарських засобів і, відповідно, збільшувати токсичний вплив на печінку.
Вибір антидепресанту: можливість взаємодії препаратів
Антидепресанти можуть взаємодіяти з ферментом P450 у печінці й, відповідно, порушувати метаболізм інших лікарських препаратів (рис. 6).
Фактори ризику виникнення порушень сприйняття при HCV-терапії
Порушення сприйняття можуть виникнути незалежно від дози противірусного препарату або тривалості HCV-терапії.
Фактори ризику:
Показники закінчення лікування, SVR і виключення з дослідження приблизно однакові як для контролю, так і для психіатричних пацієнтів
70 HCV-інфікованих пацієнтів оцінювалися за реакцією на ІFN-терапію, наявністю психіатричної хвороби та наркозалежності.
Комбінація pegІFN a-2b + RBV застосовувалася протягом 24 тижнів (генотипи 2/3) або 48 тижнів (генотипи 1/4) (рис. 7).
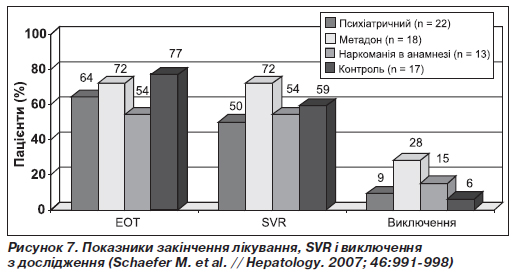
Лікування HCV-інфікованих пацієнтів із раніше існуючими психіатричними проблемами (Pariante C.M. et al. // Lancet. 1999; 354: 131-132; Schaefer M. et al. // Hepatology. 2003; 37: 443-451; Schaefer M. et al. // Hepatology. 2007; 46: 991-998)
Пацієнтів із раніше існуючими психіатричними порушеннями можна лікувати від хронічного гепатиту С.
Загалом, психіатричні пацієнти:
Висновки
HCV-пацієнти, які отримують антивірусну терапію, мають більший ризик розвитку депресії. Перед призначенням антидепресантів обов''язкова консультація психіатра. Депресія зазвичай виникає протягом 12 тижнів лікування. Ранній діагноз депресії необхідний для поліпшення прихильності до HCV-терапії. СІЗЗС ефективні для зниження симптомів депресії.
Профілактична антидепресивна терапія в цей час рекомендується тільки для пацієнтів з депресією в анамнезі. Терапія повинна бути продовжена протягом лікування ІFN та в наступні 6 місяців.
1. Raison C.L., Demetrashvili M., Capuron L., Miller A.H. Neuropsychiatric side effects of interferon-alpha: recognition and management // CNS Drugs. — 2005. — 19. — 105-123.
2. Loftis J.M., Hauser P. The phenomenology and treatment of interferon-induced depression // J. Affect. Disord. — 2004. — 82. — 175-190.
3. Raison C.L., Borisov A.S., Broadwell S.D. et al. Depression during pegylated interferon-alpha plus ribavirin therapy: prevalence and prediction // J. Clin. Psychiatry. — 2005. — 66. — 41-48.
4. Russo M.W., Fried M.W. Side effects of therapy for chronic hepatitis C // Gastroenterology. — 2003. —124. — 1711-1719.
5. Marcellin P., Lau G.K., Zeuzem S. et al. Comparing the safety, tolerability and quality of life in patients with chronic hepatitis B vs chronic hepatitis C treated with peginterferon alpha-2a // Liver Int. — 2008. — 28. — 477-485.
6. Zdilar D., Franco-Bronson K., Buchler N., Locala J.A., Younossi Z.M. Hepatitis C, interferon alfa, and depression // Hepatology. — 2000. — 31. — 1207-1211.
7. Raison C.L., Broadwell S.D., Borisov A.S. et al. Depressive symptoms and viral clearance in patients receiving interferon-alpha and ribavirin for hepatitis C // Brain Behav. Immun. — 2005. — 19. — 23-27.
8. Gaeta G.B., Precone D.F., Felaco F.M. et al. Premature discontinuation of interferon plus ribavirin for adverse effects: a multicentre survey in «real world» patients with chronic hepatitis C // Aliment. Pharmacol. Ther. — 2002. — 16. — 1633-1639.
9. Schaefer M., Schmidt F., Folwaczny C. et al. Adherence and mental side effects during hepatitis C treatment with interferon alfa and ribavirin in psychiatric risk groups // Hepatology. — 2003. — 37. — 443-451.
10. Hauser P., Khosla J., Aurora H. et al. A prospective study of the incidence and open-label treatment of interferon-induced major depressive disorder in patients with hepatitis C // Mol. Psychiatry. — 2002. — 7. — 942-947.
11. Cotler S.J., Wartelle C.F., Larson A.M., Gretch D.R., Jensen D.M., Carithers R.L. Jr. Pretreatment symptoms and dosing regimen predict side-effects of interferon therapy for hepatitis C // J. Viral Hepat. — 2000. — 7. — 211-217.
12. Gohier B., Goeb J., Rannou-Dubas K., Fouchard I., Cales P., Garre J. Hepatitis C, alpha interferon, anxiety and depression disorders: a prospective study of 71 patients // World J. Biol. Psychiatry. — 2003. — 4. — 115-118.
13. Renault P.F., Hoofnagle J.H., Park Y. et al. Psychiatric complications of long-term interferon alfa therapy // Arch. Intern. Med. — 1987. — 147. — 1577-1580.
14. Pariante C.M., Orru M.G., Baita A., Farci M.G., Carpiniello B. Treatment with interferon-alpha in patients with chronic hepatitis and mood or anxiety disorders // Lancet. — 1999. — 354. — 131-132.
15. Morasco B.J., Rifai M.A., Loftis J.M. et al. A randomized trial of paroxetine to prevent interferon-alpha-induced depression in patients with hepatitis C // J. Affect. Disord. — 2007. — 103. — 83-90.
16. Kraus M.R., Schafer A., Al-Taie O., Scheurlen M. Prophylactic SSRI during interferon alpha re-therapy in patients with chronic hepatitis C and a history of interferon-induced depression // J. Viral Hepat. — 2005. — 12. — 96-100.
17. Raison C.L., Woolwine B.J., Demetrashvili M.F. et al. Paroxetine for prevention of depressive symptoms induced by interferon-alpha and ribavirin for hepati-tis C // Aliment. Pharmacol. Ther. — 2007. — 25. — 1163-1174.
18. Larrey D., Couzigou P., Denis J. Chronic hepatitis C: management of side effects of treatment // Gastroenterol. Clin. Biol. — 2007. — 31. — 4S20-4S28.
19. Kraus M.R., Schafer A., Faller H., Csef H., Scheurlen M. Paroxetine for the treatment of interferon-alpha-induced depression in chronic hepatitis C // Aliment. Pharmacol. Ther. — 2002. — 16. — 1091-1099.
20. Lang C.A., Conrad S., Garrett L. et al. Symptom prevalence and clustering of symptoms in people living with chronic hepatitis C infection // J. Pain Symptom Manage. — 2006. — 31. — 335-344.
21. Talal A.H., Weisz K., Hau T., Kreiswirth S., Dieterich D.T. A preliminary study of erythropoietin for anemia associated with ribavirin and interferon-alpha // Am. J. Gastroenterol. — 2001. — 96. — 2802-2804.
22. Thevenot T., Cadranel J.F., Di Marti-no V. et al. A national French survey on the use of growth factors as adjuvant treatment of chronic hepatitis C // Hepatology. — 2007. — 45. — 377-383.
23. Lim J.K., Cronkite R., Goldstein M.K., Cheung R.C. The impact of chronic hepatitis C and comorbid psychiatric illnesses on health-related quality of life // J. Clin. Gastroenterol. — 2006. — 40. — 528-534.
24. Raison C.L., Borisov A.S.,
25. Constant A., Castera L., Dantzer R. et al. Mood alterations during interferon-alfa therapy in patients with chronic hepatitis C: evidence for an overlap between manic/hypomanic and depressive symptoms // J. Clin. Psychiatry. — 2005. — 66. — 1050-1057.
26. Dell''Osso L., Pini S., Maggi L. et al. Subthreshold mania as predictor of depression during interferon treatment in HCV+ patients without current or lifetime psychiatric disorders // J. Psychosom. Res. — 2007. — 62. — 349-355.
27. Dieperink E., Willenbring M., Ho S.B. Neuropsychiatric symptoms associated with hepatitis C and interferon alpha: a review // Am. J. Psychiatry. — 2000. — 157. — 867-876.
28. Capuron L., Ravaud A. Prediction of the depressive effects of interferon alfa therapy by the patient''s initial affective state // N. Engl. J. Med. — 1999. — 340. — 1370.
29. Castera L., Zigante F., Bastie A., Buffet C., Dhumeaux D., Hardy P. Incidence of interferon alfa-induced depression in patients with chronic hepatitis C // Hepatology. — 2002. — 35. — 978-979.
30. Renault P.F., Hoofnagle J.H. Side effects of alpha interferon // Semin. Liver Dis. — 1989. — 9. — 273-277.
31. Schaefer M., Mauss S. Hepatitis C treatment in patients with drug addiction: Clinical management of Interferon-alpha associated psychiatric side effects // Current Drug Abuse Reviews. — 2008. — 1. — 177-187.
32. Gleason O.C., Fucci J.C., Yates W.R., Philipsen M.A. Preventing relapse of major depression during interferon-alpha therapy for hepatitis C-A pilot study // Dig. Dis. Sci. — 2007. — 52. — 2557-2563.
33. Schaefer M., Schwaiger M., Garkisch A.S. et al. Prevention of interferon-alpha associated depression in psychiatric risk patients with chronic hepatitis C // J. Hepatol. — 2007. — 46. — 991-998.
34. Kraus M.R., Schafer A., Schottker K. et al. Therapy of interferon-induced depression in chronic hepatitis C with citalopram: a randomized, double-blind, placebo-controlled study // Gut. — 2008. — 57. — 531-536.
