Газета «Новости медицины и фармации» Маммология (298) 2009 (тематический номер)
Вернуться к номеру
Профілактика дисгормональних захворювань молочних залоз у жінок після самовільного аборту в першому триместрі вагітності
Авторы: В.К. Чайка, С.А. Ласачко, В.П. Квашенко, Донецький регіональный центр охорони материнства й дитинства.
Кафедра акушерства, гінекології та перинатології ФІПО ДонНМУ
Версия для печати
Актуальність. Частота невиношування вагітності коливається від 10 до 25 % від загальної кількості вагітностей та не має тенденції до зниження [3, 11]. Самовільне переривання вагітності негативно впливає як на психологічний, так і на гормональний баланс в організмі жінки на фоні порушень, що призвели до викидня, та високого рівня стресу [5, 11]. Після самовільного аборту (СА) як одразу, так і через деякий час виникають дисгормональні порушення, що мають негативний вплив на стан молочних залоз (МЗ), зокрема призводять до розвитку таких дисгормональних захворювань молочних залоз (ДЗМЗ), як дисплазії (мастопатії), мастодинія, галакторея, кісти та ін. [6, 12]. Дисгормональні захворювання МЖ діагностуються у 30–50 % жінок репродуктивного віку [7, 9]. У свою чергу, такі захворювання підвищують ризик злоякісних новоутворень, зокрема раку МЗ. У жінок, які мають СА в анамнезі, ДЗМЗ зустрічаються частіше у 2–3 рази, а рак МЗ — у 1,7 раза [10, 12].
У наш час більшість заходів щодо реабілітації таких жінок спрямовані на пошук факторів викидня, їх лікування та планування наступної вагітності, недостатньо уваги приділяється проблемі корегування гормональних порушень із метою профілактики ДЗМЗ. У доступній літературі з цього приводу багато уваги приділяється використанню гормональної контрацепції (ГК) як способу збереження репродуктивної функції після штучного аборту (ША) та до закінчення періоду пошуку та лікування факторів викидня (за умов виключення протипоказань) [8].
Але в жодній профілактичній схемі не приділяється уваги стану МЗ у цих жінок. Між тим є дані, що підтверджують як негативний вплив СА безпосередньо на стан здоров''я МЗ, ризик виникнення пухлин та ДЗМЗ, так і негативний вплив попередніх СА на стан лактації після вдалої реабілітації репродуктивної функції та завершення наступної вагітності пологами та народженням дитини [5]. Після СА посилюється не тільки гормональна дисфункція, але і мікроциркуляційні процеси в МЗ. Ці порушення є наслідком як проліферативних змін у паренхімі МЗ під час вагітності, що перервалася, так і гормональної дисфункції яєчників на фоні ендокринних (наприклад, захворювання або дисфункція щитоподібної залози) та інших факторів СА [5, 11]. Вагітність, а надалі й стрес, пов''язаний з її втратою, призводять до вираженого порушення гормонального балансу на всіх рівнях гіпоталамо-гіпофізарно-яєчникової системи (ГГЯС), включаючи стероїдогенез у яєчниках і секрецію пролактину (ПРЛ) в гіпофізі. Стан МЗ після СА обумовлений в основному особливостями функції яєчників та рівнем ПРЛ [7, 9].
Метою нашої роботи є дослідження необхідності, розробка та оцінка ефективності системи заходів із профілактики ДЗМЗ після СА в першому триместрі вагітності.
Матеріал та методи
Задля дослідження необхідності профілактики ДЗМЗ після СА в першому триместрі вагітності було обстежено та проанкетовано 324 пацієнтки репродуктивного віку, з числа яких у 150 протягом останніх двох років було штучне переривання вагітності та в 174 — викидень у першому триместрі.
Також обстежено 80 жінок після СА в першому триместрі вагітності. Пацієнтки були у віці від 22 до 39 років. З них сформували дві групи по 40 пацієнток. Обидві групи були порівнянними за діагнозами та віком. У групі ІІ використовували комплексні заходи профілактики ДЗМЗ за схемою, що описується нижче, а в групі І — лише ГК. Обстеження жінок проводили одразу після викидня, через 2, 6 та 12 місяців після СА.
Клінічний стан МЗ (біль та нагрубання, виділення молока або молозива) та ступінь вираженості дисгормональних порушень МЗ оцінювали за відомою шкалою Л.Н. Сидоренко шляхом огляду та пальпації [6]. Для оцінки ступеня вираженості проявів мастодинії використовували відому візуально-аналогову шкалу [1].
Ультразвукове дослідження (УЗД) щитоподібної залози (ЩЗ) та сканування МЗ виконували на апараті Siemens з використанням сірої шкали та лінійного датчика з частотою 10 МГц відповідно до загальноприйнятої методики до 10-го дня після СА, з 7-го по 14-й день менструального циклу (умовного на фоні приймання ГК) [4]. Ехоознаками дисгормональних порушень МЗ були гіпертрофія строми, розширення та деформація молочних протоків, неоднорідність структури МЗ, наявність кістозних включень та ін. За допомогою ехосканування проводили контроль стану МЗ у динаміці.
Також виконували контактну термомамографію (КТМ) — дослідження МЗ на термографі контактному цифровому ТКЦ-1 (Донецьк, свідоцтво про державну реєстрацію № 6544/2007). При цьому оцінювали загальний рівень інфрачервоного випромінювання, збіг із ділянками локалізації найбільшого болю, наявність термоасиметрій.
У разі наявності виділень із сосків здійснювали їх цитологічне дослідження.
Оцінку рівня ПРЛ та тиреотропного гормону (ТТГ) у сироватці крові проводили за імуноферментним методом із використанням стандартних наборів фірми UBI MAGIWEL та Clone Systems (США).
Результати та їх обговорення
За даними анкетування та обстеження жінок, після штучного та самовільного переривання вагітності в першому триместрі протягом двох років виявлено більшу частоту розвитку ДЗМЗ та підвищення рівня ПРЛ у жінок після СА порівняно зі станом після ША (рис. 1, 2).
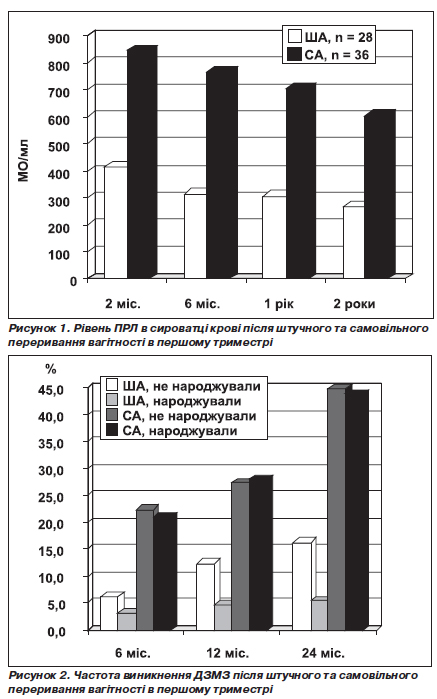
Захворювання ЩЗ було виявлено в 45,4 % жінок після СА та в 12 % жінок, які перервали вагітність за власним рішенням.
Ці дані свідчать про те, що в жінок після СА набагато більше умов для розвитку ДЗМЗ, включаючи стрес після втрати вагітності та поганий стан здоров''я (у тому числі маються на увазі фактори, що призвели до СА). Тобто ці жінки потребують додаткових заходів щодо профілактики дисгормональних порушень із боку ГГЯС та МЗ.
У перші три доби після СА ми виконували збір анамнезу, обстеження для вибору ГК. За умови виключення протипоказань приймання вибраних ГК починали в перші три доби після СА — комбіновані оральні контрацептиви, трансдермальна система, вагінальне кільце, протизаплідні таблетки прогестагенового ряду. У перші три доби після СА ми також проводили клінічне обстеження МЗ (пальпація, УЗД, КТМ).
Враховуючи позитивний вплив ГК на стан ГГЯС та МЖ після переривання вагітності, за умови виключення протипоказань ми використовували в обох групах сучасну ГК, добір якої виконували за наступними принципами:
Задля профілактики ДЗМЗ після СА в першому триместрі ми також додатково виконували такі заходи (ІІ група):
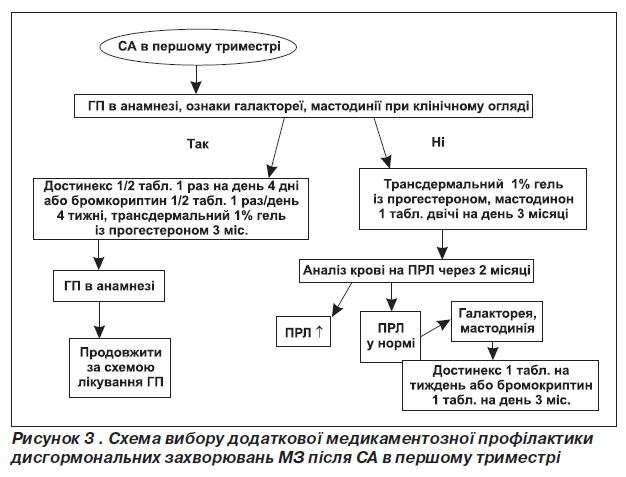
— консультація психолога або психотерапевта, у разі необхідності медикаментозної підтримки — вибір препаратів, що не призводять до підвищення ПРЛ;
Серед дофамінергічних препаратів, що нормалізують рівень ПРЛ в організмі жінки, перевагу надають саме препарату достинекс (Pfizer Inc., США), що має пролонговану дію та мінімальну кількість побічних реакцій. Достинекс включає дофамінергічну ерголінову сполуку з вираженим і тривалим пролактинзнижуючим ефектом. Препарат інгібує секрецію ПРЛ шляхом прямого стимулювання D2-дофамінових рецепторів лактотрофних клітин гіпофіза [2]. У разі відсутності гіперпролактинемії, болю та нагрубання МЗ, виділення молока або молозива вибирають з метою профілактики ДЗМЗ після СА фітопрепарат зі слабким дофамінергічним впливом: мастодинон, циклодинон («Біонорика», ФРН).
Для всіх пацієнток після СА також вибирають профілактичний захід — місцеве нанесення на кожну МЗ 1% трансдермального гелю з прогестероном прожестин («Красная Звезда», м. Харків, Україна). Гель, що містить 1% прогестерону, при трансдермальному застосуванні знижує проникність капілярів та інтенсивність циклічного набряку в сполучнотканинній стромі МЗ, а також запобігає проліферації і мітотичій активності епітелію протоків [10].
Зміни рівнів ПРЛ, наведені в табл. 1, свідчать про коливання гормональної активності після СА. У жінок ІІ групи через 6 місяців після СА і в подальшому періоді нагляду за їх здоров''ям спостерігалось відновлення показників гормонального профілю до рівня, характерного для їхніх здорових ровесниць. У жінок групи І відзначали суттєве підвищення рівня ПРЛ, що зберігалось до одного року після СА.
За результатами клінічного, цитологічного обстеження, КТМ та УЗД МЗ через 1 рік після СА відсутні ДЗМЗ у 34 (85 %) пацієнток І групи та у 13 (32,5 %) пацієнток ІІ групи. Натомість у 6 (15 %) пацієнток І групи виявили ДЗМЗ: у 5 мастодинія та в 1 дисплазія; і у 27 (67,5%) пацієнток ІІ групи: дисплазія МЗ у 8, мастодинія у 15, галакторея у 4.
Отже, частота ДЗМЗ в ІІ групі жінок, у яких застосовували запропонований комплекс заходів профілактики, знизилась на 85,0 %, а в І групі жінок, у яких використовували лише ГК, — на 32,5 %.
Клінічні приклади виконання профілактики дисгормональних захворювань МЗ після СА в першому триместрі.
Приклад 1. Хвора С., 30 років, надійшла в гінекологічну клініку після СА третьої вагітності в терміні 6 тижнів. Із анамнезу: перша вагітність була 7 років тому, пологи нормальні, грудне вигодовування дитини протягом 4 місяців. Другу вагітність перервали медичним абортом рік тому. Соматичних захворювань та коагулопатії не було. В анамнезі дані про підвищення рівня ПРЛ відсутні. Виконано УЗД ЩЗ — без патології. Рівень ТТГ у сироватці крові в нормі. Під час клінічного огляду МЗ зафіксовано скарги пацієнтки на біль та нагрубання МЗ, відзначали помірний набряк, виділення із сосків у помірній кількості (декілька крапель) молозивного характеру. На третю добу після СА призначили ГК — препарат логест за контрацептивною схемою. З метою профілактики ДЗМЗ призначили приймання дофамінергічного препарату пролонгованої дії достинекс по півтаблетки на день протягом 4 днів та трансдермальний гель із прогестероном (1%) прожестин протягом 3 місяців. Дані результатів досліджень рівня ПРЛ хворої С. занесені до табл. 2.
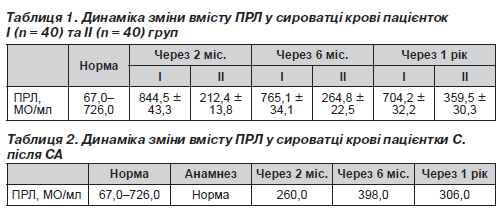
З табл. 2 видно, що рівень ПРЛ у пацієнтки С. був чітко контрольованим протягом періоду застосування профілактичних заходів. Через 2 місяці після СА він був дещо зниженим, а далі залишався в рамках норми до кінця першого року спостереження.
Стан МЗ хворої С. встановили одразу після СА, через 2 місяці, через 6 місяців та через 1 рік за допомогою клінічного огляду, методів УЗД та КТМ. Дані результатів досліджень стану МЗ хворої С. занесені до табл. 3.
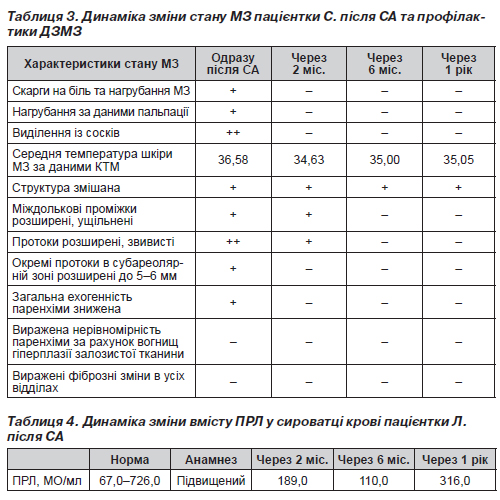
Як видно з табл. 3, вже через 2 місяці після початку виконання заходів профілактики скарг на біль та нагрубання МЗ у хворої С. не було. Через півроку відбулось поліпшення всіх показників стану МЗ у хворої С., і воно зберігалось до кінця першого року спостереження.
Приклад 2. Хвора Л., 33 років, надійшла в гінекологічну клініку після СА третьої вагітності в терміні 4 тижнів. Із анамнезу: перші дві вагітності 15 та 10 років тому перервали медичні аборти. Протягом останніх 5 років бажана вагітність не наступала, відзначали підвищення рівня ПРЛ. Обстеження головного мозку (магнітно-резонансна томографія), огляд окуліста та невролога патології не виявили. Протягом 6 місяців хвора Л. приймала ліки (бромокриптин, жанін) для корегування гормонального фону. Після відміни лікування пацієнтка Л. завагітніла в четвертому менструальному циклі. Але вагітність перервалась СА на 4-му тижні. Соматичних захворювань та коагулопатії не було. Під час огляду пацієнтка скаржилась на біль, суттєве нагрубання та набряк МЗ, виділення із сосків молозивного характеру у великій кількості. Виконано УЗД ЩЗ — без патології. Рівень ТТГ в сироватці крові в нормі. В першу добу після СА пацієнтці Л. призначили приймання достинексу по півтаблетки на день протягом 4 днів та трансдермальний гель з прогестероном (1%) прожестин протягом 3 місяців. Далі приймання достинексу продовжили по 1 таблетці двічі на тиждень упродовж 6 місяців під контролем рівня ПРЛ. З другого дня після СА призначили ГК — препарат ярина за контрацептивною схемою. Через 2 та 6 місяців перевірили рівень ПРЛ у сироватці крові. Він був у рамках норми. Приймання достинексу припинили після 6 місяців. Використання ГК продовжено з метою контрацепції. Дані результатів досліджень рівня ПРЛ хворої Л. занесені до табл. 4.
З табл. 4 видно, що рівень ПРЛ у пацієнтки Л. був чітко контрольованим протягом застосування профілактичних заходів і залишався в рамках норми до кінця першого року спостереження.
Стан МЗ хворої Л. встановили одразу після СА, через 2 місяці, 6 місяців і через 1 рік за допомогою клінічного огляду, методами УЗД та КТМ. Дані результатів досліджень стану МЗ хворої Л. занесені до табл. 5.
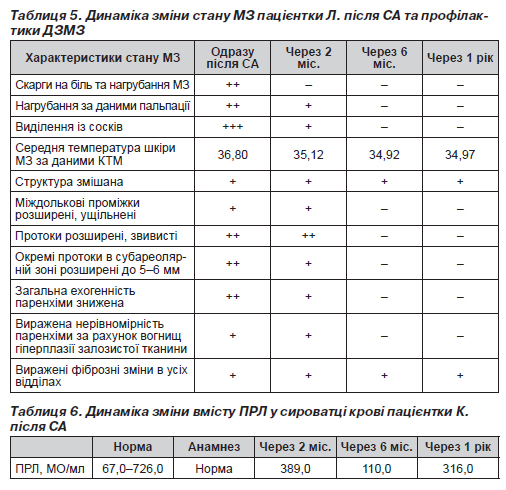
Як видно з табл. 5, вже через 2 місяці після початку виконання заходів профілактики скарг на біль та нагрубання МЗ у хворої Л. не було. Через півроку відбулось поліпшення всіх показників стану МЗ у хворої Л., і воно зберігалось до кінця першого року спостереження.
Приклад 3. Хвора К., 34 років, надійшла в гінекологічну клініку після СА третьої вагітності в терміні 6 тижнів. Із анамнезу: перші дві вагітності 5 та 7 років тому перервали медичні аборти. В анамнезі дані про підвищення рівня ПРЛ відсутні. Під час опитування та огляду одразу після СА скарг на біль та нагрубання МЗ не було, відсутні нагрубання МЗ і виділення із сосків. На третю добу після СА призначили ГК — препарат логест за контрацептивною схемою. Через 2 місяці перевірили рівень ПРЛ, що відповідав нормі. Під час огляду МЗ через 2 місяці хвора К. скаржилась на нагрубання МЗ. Відзначали суттєве нагрубання та набряк МЗ, виділення із сосків молозивного характеру в помірній кількості. Призначили дофамінергічний препарат пролонгованої дії достинекс по півтаблетки двічі на тиждень протягом 3 умовних циклів по 28 днів кожний. Приймання ГК логест продовжили з метою контрацепції. Через 6 місяців перевірили рівень ПРЛ в сироватці крові, який був у рамках норми. Дані результатів досліджень рівня ПРЛ хворої К. занесені до табл. 6.
З табл. 6 видно, що рівень ПРЛ в пацієнтки К. був чітко контрольованим протягом періоду застосування профілактичних заходів і залишався в рамках норми до кінця першого року спостереження.
Стан МЗ хворої К. встановили одразу після СА, через 2 місяці, через 6 місяців, через 1 рік за допомогою клінічного огляду, методами УЗД та КТМ. Дані результатів досліджень стану МЗ хворої К. занесені до табл. 7.
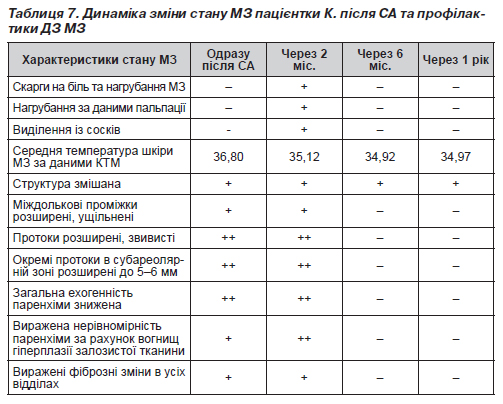
Як видно з табл. 7, через 6 місяців після початку виконання заходів профілактики скарг на біль та нагрубання МЗ у хворої К. не було. Поліпшились також всі показники стану МЗ у хворої К. Така ж картина зафіксована й через 1 рік спостереження.
Висновки
Після СА як одразу, так і через деякий час виникають дисгормональні порушення, що мають негативний вплив на стан молочних залоз, зокрема призводять до розвитку дисгормональних захворювань молочних залоз.
Розширення гормональних та клінічних діагностичних досліджень, вибір комплексу ефективних та безпечних препаратів, вибір доз та режимів їх застосування відповідно до результатів досліджень призводить до того, що ефективність комплексної профілактики ДЗМЗ після СА порівняно з використанням лише ГК підвищується з 32,5 до 85,0 %.
Заходи, проведені саме в період після викидня, мають позитивний вплив на стан МЗ на довгі місяці та роки, а надалі, після успішного завершення наступної вагітності, сприяють максимальній реалізації лактації, що має неоціненний вплив на здоров''я матері та дитини.
Впервые опубликовано в журнале
«Репродуктивное здоровье женщины», 2008, № 3, с. 134–138
1. Балашова О.И., Антоновская Я.В. Опыт применения препарата фарестон в комплексном лечении дисгормональных гиперплазий молочной железы у женщин с сохраненной менструально-овариальной функцией // Онкология. — 2004. — Т. 6, № 3. — С. 189-92.
2. Бондаренко Л.И., Иващенко Е.В. Достинекс: консервативное лечение пролактином гипофиза // Здоровье женщины. — 2005. — Т. 21, № 1. — С. 121-6.
3. Жук С.И., Чечуга С.Б. Коррекция гипергомоцистеинемии у беременных с невынашиванием // Репродуктивное здоровье женщины. — 2006. — Т. 28, № 1. — С. 42-45.
4. Озерова О.Е. Ультразвуковая маммография (дисплазия и возрастные особенности молочной железы в норме) // Акушерство и гинекология. — 2004. — № 6. — С. 58-62.
5. Квашенко В.П., Шаталова М.В. К вопросу о факторах риска развития гипогалактии у женщин с ФПН и привычным невынашиванием // Медико-социальные проблемы семьи. — 2004. — Т. 9, № 3. — С. 125-9.
6. Сидоренко Л.Н. Мастопатия: психосоматические аспекты. — Л.: Медицина, 1991. — С. 264.
7. Ласачко С.А., Квашенко В.П., Сергиенко С.Ю. Комплексный подход к ведению пациенток с гинекологическими заболеваниями и опухолевыми и дисгормональными процессами молочных желез // Збірник наукових праць асоціації акушерів-гінекологів. — К.: Інтермед, 2006. — С. 373-375.
8. Наказ МОЗ Украiни № 905 вiд 27.12.2006 «Планування сім''ї». — К., 2006. — 80 с.
9. Татарчук Т.Ф., Сольский Я.П. Эндокринная гинекология (клинические очерки). — Ч. 1. — К., 2003. — С. 147-180.
10. Тихомиров А.Л., Лубнин Д.М. Местные гормональные препараты в лечении доброкачественных заболеваний молочной железы, сопровождающихся масталгией // Русский мед. журнал. — 2000. — Т. 8, № 18. — С. 768-771.
11. Чайка В.К., Демина Т.Н. Диагностика и тактика ведения пациенток с различными патогенетическими вариантами невынашивания беременности: Метод. рекомендації. — Донецк, 2007. — 34 с.
12. Lasachko S., Chaika V., Kvashenko V. Breast cancer, mastopathy and peculiarities of the reproductive anamnesis. Problems and interrelations // XVI FIGO World Congress of Gynecology and Obstetrics: Book of Abstracts. —
