Газета «Новости медицины и фармации» Маммология (298) 2009 (тематический номер)
Вернуться к номеру
Уточняющая диагностика узловых образований молочных желез на современном уровне
Авторы: Д.А. Успенский, Н.А. Сухина, Донецкое областное клиническое территориальное медицинское объединение
Версия для печати
Диагностика узловых образований молочных желез (МЖ) является проблемой, которая может быть решена лишь за счет последовательного применения методов клинической, лучевой и морфологической диагностики. Для получения точного результата имеет значение не только использование различных способов диагностики, но и определенная их последовательность.
Первый этап диагностического алгоритма всегда следует начинать с пальпации, при которой определяется наличие или отсутствие пальпируемых уплотнений и их пальпаторные особенности: плотность, подвижность, болезненность, связь с кожей и окружающими тканями. Кроме того, определяется состояние регионарных лимфатических узлов (подмышечных, над- и подключичных), а также характер выделений из сосков.
Если пальпаторно патологических уплотнений в ткани МЖ не определено, на втором этапе диагностического поиска используют лучевые методы диагностики. В качестве таковых наибольшее распространение в настоящее время имеют УЗИ молочных желез и маммография. КТ, ПЭТ/КТ и МРТ имеют ограниченное применение в связи с их высокой стоимостью и недостаточным количеством необходимой аппаратуры в общебольничной сети.
Выбор между УЗИ и маммографией основан на возрасте пациентки и типе строения паренхимы МЖ, Общепринято, что маммографию следует применять у пациенток старше 35 лет. Однако этот возрастной барьер является условным. Качество маммографических снимков зависит от типа строения паренхимы МЖ. Чем меньше объем железы и чем плотнее паренхима, тем ниже диагностические показатели маммографии, и наоборот. На фоне плотной паренхимы невозможно выявить скопления сгруппированных микрокальцификатов и другие виды доклинических форм рака МЖ. В таких случаях лучевую диагностику следует начинать с УЗИ.
При наличие пальпируемого уплотнения в МЖ в качестве основного метода лучевой диагностики следует применять УЗИ, при котором оценивается характер уплотнения (жидкостное или тканевое), его ультразвуковые характеристики. На их основании уплотнение может быть расценено как киста (простая или атипичная), фиброаденома, олеогранулема, зона узловой гиперплазии паренхимы или рак МЖ. С практической точки зрения вызывает интерес система представления отчетов и классификации данных по лучевому исследованию молочной железы (BIRADS) Американской коллегии рентгенологов (табл. 1).
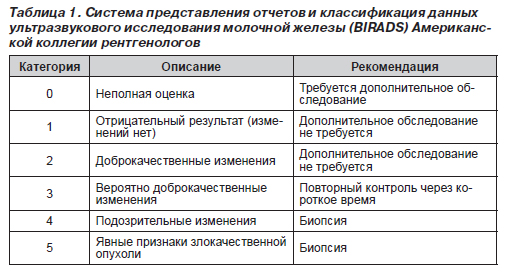
0-я категория по шкале BIRADS означает, что по данным лучевого обследования невозможно исключить или подтвердить наличие патологии МЖ. В таких случаях показано проведение дополнительных методов обследования.
1-я категория — вариант возрастной нормы МЖ, тип и структура паренхимы соответствуют возрасту, конституции и функциональному состоянию пациентки.
К образованиям 2-й категории относят типичные кисты, липомы. Пациенткам рекомендуют проходить скрининговое обследование согласно возрасту.
Впервые выявленные типичные фиброаденомы принято оценивать как образования 3-й категории. Рентгенологические изменения этой категории характерны для крупноузловой мастопатии и при наличии макрокальцификатов. Показано контрольное обследование через 3 месяца после первичного выявления изменений, в дальнейшем при стабильных размерах — 1 раз в 6 месяцев. В эту же группу относят инфильтративно-отечные формы мастита, динамический контроль за которыми проводят в процессе консервативного лечения. Если несмотря на проводимое противовоспалительное и антибактериальное лечение не отмечают положительную динамику, выявленные изменения переводят в 4-ю категорию.
Группа изменений этой категории включает атипичные кисты, внутрипротоковые опухоли, липогранулемы, фиброаденомы с усилением интра- и перитуморального кровотока и фиброаденомы, которые увеличиваются в процессе динамического наблюдения. Рентгенологические изменения 4-й категории — сгруппированные микрокальцификаты с размерами от 50 до 600 мкм. Вышеуказанные изменения требуют морфологического анализа путем выполнения пункционной биопсии (ПБ).
5-я категория по шкале BIRADS означает явные признаки рака МЖ. Показано выполнение ПБ для морфологического подтверждения диагноза по следующим причинам:
Показанием для выполнения ПБ является выявление изменений 4–5-й категории по шкале BIRADS.
Биопсию непальпируемых очагов, четко выявляемых с помощью ультразвука, а также большинства пальпируемых уплотнений лучше всего проводить под УЗ-контролем. В связи с ограничениями расстояний при использовании датчиков 7,5–10,0 МГц и более ультразвуковая навигация при выполнении ПБ наиболее эффективна при небольших или средних размерах молочной железы. Однако при выявлении микрокальцификатов и непальпируемых опухолей, которые не могут быть четко визуализированы сонографически, предпочтение отдается стереотаксической биопсии под контролем маммографа. Этот вид биопсии также имеет преимущество для морфологической верификации патологических очагов, расположенных глубоко в МЖ больших размеров при инволютивно-жировом типе строения паренхимы.
Поскольку УЗ-изображение является двухмерным, динамическая оценка линейного размера патологического очага BIRADS 3, например фиброаденомы, имеет некоторые особенности. При выполнении измерения при УЗ-обследовании необходимо четко указывать не только локализацию зоны интереса, но и плоскость сканирования, в которой осуществлен замер. Кроме того, существенное значение имеет фаза менструального цикла, в которой проводится УЗИ МЖ. В результате физиологического гормонального воздействия на ткань МЖ половых гормонов происходит некоторая циклическая диффузная гиперплазия как паренхимы, так и фиброаденомы. Этот процесс тем более выражен, чем более высока плотность содержания эстрогеновых и прогестероновых рецепторов в тканях-мишенях. Поэтому динамическое наблюдение за типичными фиброаденомами 3-й категории по шкале BIRADS следует проводить в одинаковые фазы менструального цикла, желательно на одном и том же УЗ-сканере и у одного специалиста. Физиологическое увеличение фиброаденом наблюдается при беременности и лактации, что необходимо учитывать при принятии решения о выполнении ПБ.
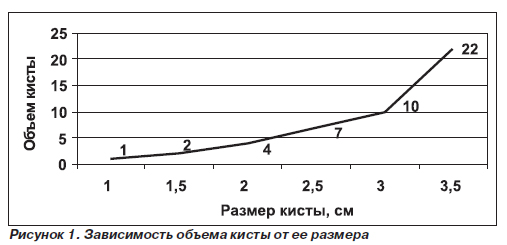
Если в процессе динамического УЗ-контроля обнаруживают увеличение линейных размеров очага, то возникает вопрос об интерпретации степени увеличения и принятии решения о выборе дальнейшей тактики ведения таких пациенток. Необходимо иметь в виду, что принципиальное значение имеет не столько увеличение линейного размера, сколько увеличение объема патологического очага. Постулат о среднем времени удвоения раковой клетки за 90–110 дней следует оценивать именно с позиции удвоения объема, но не линейного размера, который при удвоении объема увеличивается незначительно. Так, при шаровидной форме патологического очага увеличение его диаметра с 1 до
Полученные данные приведены на рис. 1.
Известно, что определение линейного размера зоны интереса является в определенной степени субъективным. Расположение датчика (радиарное или вдоль максимального размера) при исследовании одного и того же очага может приводить к различным результатам. Поэтому для более объективной оценки целесообразно выполнение бесконтрастной маммографии, при которой МЖ исследуется в стандартных проекциях и определение линейных размеров очага носит более объективный характер. Кроме того, маммография показана для выявления оккультных синхронных заболеваний МЖ.
Правильное понимание этих особенностей помогает избегать недооценки клинического значения увеличения линейных размеров зоны интереса, что особо важно с точки зрения онконастороженности. Считается, что разница в диаметре при динамическом контроле может при стабильных размерах очага достигать 2–3 мм, что является нормальной погрешностью измерения УЗ-сканеров, и вызываться физиологическими гиперпластическими изменениями паренхимы МЖ в течение менструального цикла. Поэтому увеличение линейного размера на
Тонкоигольная аспирационная или трепан-биопсия?
При необходимости морфологической верификации патологических изменений МЖ 4–5-й категории возникает вопрос о выборе метода диагностической биопсии.
В настоящее время для решения вопроса предоперационной морфологической диагностики опухолей МЖ применяются 2 вида пункционных биопсий: тонкоигольная аспирационная биопсия (ТАБ), при помощи которой получают материал для цитологического исследования, и толстоигольная, или трепан-биопсия, которая служит для получения материала для гистологического анализа. Каждый из видов пункционной биопсии имеет свои достоинства и недостатки. К достоинствам тонкоигольной аспирационной биопсии относят малую травматичность, возможность выполнения без местного обезболивания, быстроту получения цитологического заключения, крайне низкое число осложнений.
Недостатками способа являются не очень высокие точность и специфичность, невозможность определения инвазии кровеносных и лимфатических сосудов в ткани опухоли, пролиферативной активности опухолевых клеток, а также целого ряда иммуногистохимических маркеров.
Все эти данные позволяют определить гистологический анализ полученного биоптата, но трепан-биопсия является более травматичной, требует выполнения местной анестезии, имеет большее число осложнений. Кроме того, трепан-биопсия значительно дороже тонкоигольной аспирационной биопсии, поскольку для ее проведения нужны специальный биопсийный пистолет и дорогостоящие иглы. В настоящее время вопрос о том, какому методу предоперационной диагностики опухолей молочной железы следует отдавать предпочтение, остается открытым. По данным собственного исследования, несмотря на очевидные преимущества в технике проведения ТАБ по сравнению с трепан-биопсией, показатели диагностической ценности гистологического исследования выше, чем цитологического. В исследуемой группе больных число диагностических ошибок цитологической диагностики было в 4 раза больше, чем при гистологическом анализе биоптата. Сравнение диагностических возможностей цитологического и гистологического методов в предоперационной диагностике опухолей МЖ в нашем исследовании продемонстрировало значительное преимущество гистологического анализа, позволяющего в полной мере осуществить принцип «качественный диагноз — качественное лечение».
При выборе способа биопсии в случаях, когда возможно выполнение обоих методов, необходимо иметь в виду следующее:
1. Диагноз, устанавливаемый при использовании ТАБ, в лучшем случае ограничивается той группой диагнозов, которые могут быть установлены с помощью цитологического исследования. Например, ТАБ не дает возможности провести дифференциальную диагностику между внутрипротоковым раком in situ и инфильтрирующим внутрипротоковым раком, тогда как трепан-биопсия молочной железы позволяет изучить гистологию опухоли.
2. Надежная интерпретация данных ТАБ возможна лишь в небольшом количестве медицинских центров, имеющих в своем штате опытного цитолога. Небольшие и средние больницы общего профиля обычно не имеют достаточной компетентности в отношении проведения цитологических исследований для поддержания программы проведения биопсий МЖ с цитологическим исследованием получаемого материала. Патоморфологи, способные оценить гистологию молочной железы, имеются во всех больницах.
3. При проведении ТАБ обычно (с частотой до 25 %) не удается получить достаточное для постановки окончательного диагноза количество клеточного материала или данные цитоанализа не позволяют провести дифференциальную диагностику (например, между высокодифференцированной аденокарциномой и фиброаденомой с выраженной пролиферацией). Если бы окончательный диагноз основывался только на результатах цитоанализа, то у многих пациенток рак молочной железы оставался бы не идентифицированным (т.е. в большом числе случаев имелся бы ложноотрицательный результат).
В своей работе мы неоднократно сталкивались с тем фактом, что иногда при идентичной технике выполнения ТАБ от врача-цитолога мы получали информацию о недостаточном количестве клеточного материала для постановки диагноза. Анализ операционного материала и литературных данных выявил следующую закономерность. Фиброаденома как опухоль состоит из фиброзной и железистой ткани. Соотношение этих двух типов тканей в опухоли может значительно варьировать в зависимости от разных факторов, основным из которых является длительность заболевания.
Так, в «молодых» опухолях превалирует железистая ткань, при этом клеточных элементов в пунктате бывает, как правило, достаточно для цитологического исследования.
Если опухоль находится в МЖ длительно (несколько лет), то она состоит преимущественно из фиброзной ткани. При этом в ней могут откладываться соли кальция и она кальцифицируется. Цитоанализ пунктата таких опухолей затруднен из-за скудного количества материала, состоящего в основном из эритроцитов и голоядерных элементов.
Однако в отдельных случаях выполнение ТАБ является показанным, а зачастую и единственно возможным методом верификации диагноза. ТАБ МЖ следует проводить:
Кто должен выполнять ПБ?
В большинстве развитых стран (Европейский регион, США, Япония) ПБ выполняется, как правило, радиологами. Многие хирурги, владеющие ультразвуковым методом, также могут выполнять ПБ, но они делают биопсию под УЗ-контролем в самых простых случаях — при наличии пальпируемых уплотнений.
В странах постсоветского пространства биопсии традиционно являются прерогативой хирургов, онкологов, гинекологов. Формально выполнять ПБ может врач любой специальности, прошедший специальные тематические курсы. Кроме изучения вопросов, которые были рассмотрены выше, необходимо присутствие при выполнении ПБ и самостоятельное выполнение манипуляции под контролем опытного специалиста.
Основой качественной работы может быть не только методологическая база, но и личный опыт. Как бы то ни было, при любых сомнениях стоит выполнять ПБ с учетом показаний, организации и техники выполнения.
