Газета «Новости медицины и фармации» Маммология (298) 2009 (тематический номер)
Вернуться к номеру
Диагностика, варианты лечения диффузной мастопатии
Авторы: Ч.К. Мустафин, доцент, к.м.н., руководитель курса «Маммология». Кафедра радиологии ГОУ ДПО РМАПО, г. Москва, Россия
Версия для печати
Молочная железа является частью женской репродуктивной системы, развитие которой находится под сложным контролем. Ткань молочной железы является мишенью для половых гормонов — пролактина, соматотропного и плацентарных гормонов, а также гормонов других эндокринных желез, которые принимают активное участие в формировании и развитии молочных желез в пубертатном периоде, репродуктивном возрасте, во время беременности и лактации, а также в период менопаузы.
Каждый менструальный цикл организм женщины готовится к продолжению рода, а молочные железы — к выработке молока. Если не наступает беременность, в течение нескольких месяцев происходит атрофия недавно сформированных структур. На протяжении всего репродуктивного периода жизни женщины пролиферация эпителия молочных желез и его регресс идут параллельно. С прекращением менструаций ткань молочных желез подвергается инволютивным изменениям, а именно жировому перерождению.
Рак молочной железы (РМЖ) является ведущей онкологической патологией у женщин. По данным ВОЗ, в мире ежегодно заболевают раком молочной железы свыше 1 млн женщин, прогнозируется рост числа заболеваний к 2010 году до 1,45 млн.
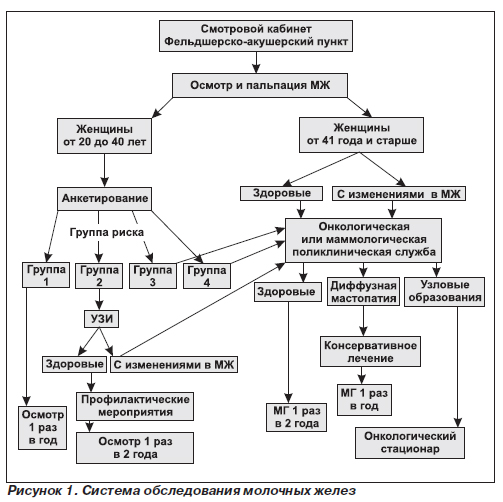
Следует отметить, что низкая выявляемость данных заболеваний на ранних стадиях зачастую обусловлена недостатком знаний в области клинической маммологии у врачей первичного звена и нередко акушеров-гинекологов, так как именно данная категория врачей является наиболее часто посещаемой женщинами.
Скрининг — массовое периодическое обследование здорового населения с целью выявления скрыто протекающего онкологического заболевания. Это прежде всего выявление доброкачественных и злокачественных опухолей молочной железы.
При профилактическом осмотре акушером-гинекологом состояние молочных желез в схему осмотра и сбора анамнеза пациентки часто не включается. Вышеперечисленное свидетельствует о том, что ранняя диагностика патологии молочной железы представляется затруднительной. Важной задачей является организация взаимодействий врачей-гинекологов и онкологов-маммологов. Участие врачей первичного звена в направлении женского населения на маммологический скрининг является важным условием снижения смертности от рака молочной железы.
Для достижения поставленной цели необходима смена приоритетов на профилактическую направленность и отбор женщин в группу риска с целью выявить онкологические заболевания на диагностической стадии.
Осмотр и пальпация — основные и доступные методы, выполняются врачом в вертикальном (с опущенными, а затем поднятыми вверх руками) и горизонтальном положении женщины. При осмотре молочной железы учитываются аномалии (добавочные молочные железы), изменение формы и объема, изменение цвета кожных покровов (наличие и степень выраженности венозного рисунка, кожные симптомы). Пальпаторно обследуют всю железу последовательно по квадрантам и область субмаммарной складки. При пальпации молочных желез определяются участки болезненных уплотнений без четких границ в виде тяжей, а также грубые железистые дольки в виде «булыжной мостовой». Довольно часто встречается локальная болезненность. Указанные изменения наиболее выражены в верхненаружных квадрантах, которые в функциональном отношении являются наиболее активными.
Доступность молочных желез для обследования и кажущаяся простота диагностики часто приводят к неправильной интерпретации результатов клинического исследования, которое зачастую проводится малоподготовленными в этом вопросе специалистами. Все это ведет как к гипо-, так и к гипердиагностике.
Основой любого лечения должна быть правильная постановка диагноза, основанная на анализе патогенетических факторов, и индивидуальный подход к терапии в каждом конкретном случае.
Поэтому мануальное обследование должно дополняться комплексным рентгенологическим, ультразвуковым (УЗИ), радиотермометрическим (РТМ-диагностикой) и другими видами инструментальных исследований.
Сразу оговоримся, что диагностику заболеваний молочных желез, как, впрочем, и заболеваний других органов и систем, проводят в специализированном медицинском учреждении онкологического или маммологического профиля. Диагноз «мастопатия» устанавливается после того, как проведено комплексное диагностические обследование, включающее клиническое исследование, маммографию, ультразвуковое исследование и др.
Основным методом объективной оценки состояния молочных желез в группе пациентов после 40 лет является маммография. Маммография — это рентгенография молочной железы без применения контрастных веществ.
Основные преимущества маммографии, используемые при диагностике заболеваний молочной железы:
Недостатки метода, ограничивающие применение:
Ультразвуковая диагностика постоянно наращивает свой потенциал благодаря совершенствованию уже имеющихся и разработке новых методик диагностики.
Исследование проводится в первую фазу менструального цикла.
Основные преимущества УЗИ молочных желез:
Недостатки УЗИ молочной железы:
Новой технологией измерения температуры тканей молочной железы и ее цифрового изображения является метод микроволновой радиотермометрии с использованием компьютеризированного диагностического комплекса (РТМ-01-РЭС), предназначенного для измерения интенсивности собственного электромагнитного излучения внутренних тканей пациента в диапазоне сверхвысоких частот, которое пропорционально температуре тканей. В отличие от известной инфракрасной термографии, которая визуализирует температуру кожных покровов, с помощью радиотермометрического метода измеряется температура тканей на глубине до
Возможность формирования цифровых изображений завоевывает всю большую популярность среди практикующих врачей. Подобно компьютеру, ставшему неотъемлемой частью повседневной жизни, цифровая обработка изображений в медицине становится дополнением классических диагностических методов, оперирующим зарегистрированным на пленке изображением.
Только комплексное обследование пациенток, осуществляемое в специализированных лечебных учреждениях, в которых работают опытные клиницисты-маммологи и имеются возможности проведения различных методов рентгенологического, УЗИ, РТМ, цитологического и других методов, позволяет квалифицированно провести необходимые медицинские мероприятия.
По данным исследователей, до 80 % опухолей молочной железы больные выявляют самостоятельно, в основном это опухоли размером около 3 и более сантиметров, при этом чувствительность метода составляет 26 %. Учитывая вышеперечисленное, можно убедиться в необходимости обучения женщин методам самообследования. Причем поскольку женщины чаще обращаются к гинекологам, онкологическая настороженность гинекологов может спасти жизнь не одной женщине, ведь имеющие гинекологическую патологию в подавляющем большинстве также страдают и патологией молочных желез. Тем более сейчас, когда гинекологи все чаще прибегают к применению гормональных препаратов, взаимодействие с маммологами-онкологами должно быть обязательным.
Проблема мастопатии является актуальной в онкологии, так как, по данным опросов, на амбулаторном приеме онколога-маммолога до 70 % больных составляют пациентки с данной патологией. Ранее мастопатию рассматривали как предраковое заболевание молочной железы. В настоящее время в целом данная патология не является предраком или стадией онкологического процесса в молочных железах, неправомочно более половины всех женщин считать страдающими предраковым заболеванием молочной железы. Однако не следует и недооценивать роль мастопатии в развитии рака молочной железы. Прежде всего в странах с высоким уровнем заболеваемости раком молочной железы высока распространенность и мастопатии; в странах с низким уровнем заболеваемости раком молочной железы значительно реже у женщин встречается и мастопатия. Неуклонный рост заболеваемости раком молочной железы в XX веке сопровождался параллельным ростом распространенности мастопатии.
Если сопоставить данные факторы риска рака молочной железы с изложенными выше причинами мастопатии, то можно обнаружить явное совпадение большинства факторов риска рака и причин мастопатии. На основании этого можно сделать заключение, что неблагоприятные факторы — генетические, репродуктивные, гормональные и обменные, внешней среды и образа жизни — приводят к развитию мастопатии и одновременно повышают риск рака молочной железы.
Дисплазия молочной железы (фиброзно-кистозная мастопатия — ФКМ) представляет собой группу гетерогенных заболеваний, характеризующихся широким спектром пролиферативных и регрессивных изменений ткани молочной железы с нарушенным соотношением эпителиального и соединительнотканного компонентов [1, 2].
Фиброзно-кистозная болезнь (ФКБ), по данным различных исследователей, выявляется примерно у 50—60 % женщин, как правило, в возрасте от 30 до 50 лет и гораздо реже у женщин в постменопаузе [2, 4, 5].
Важной причиной возникновения диспластических заболеваний молочных желез считается нарушение баланса половых стероидов — эстрогенов и прогестерона в организме женщины, в результате которого развивается относительная гиперэстрогения, что приводит к пролиферации эпителия альвеол, протоков, усилению активности фибробластов и вызывает пролиферацию соединительной ткани молочной железы [3, 6].
Прогестерон способен ограничивать влияние эстрогенов на ткань молочной железы. В зависимости от дозы и продолжительности воздействия прогестерон может потенциально видоизменять ответ как нормальных, так и раковых клеток молочной железы на разных уровнях. Таким образом, наряду со способностью прогестерона снижать экспрессию рецепторов эстрогенов данный гормон уменьшает локальный уровень активных эстрогенов, ограничивая тем самым стимуляцию пролиферации тканей молочной железы.
Подобно эстрогенам, прогестерон также опосредованно влияет на клеточную пролиферацию эпителия молочных желез — через факторы роста. Так, прогестерон повышает экспрессию ТФР-альфа (трансформирующего фактора роста) и ЭФР (эпидермального фактора роста) и снижает экспрессию TФР-бета и ИПФР-I (инсулиноподобного фактора роста). Указанные выше факторы преимущественно вырабатываются стромой молочной железы под воздействием прогестерона. Установлено, что ЭФР, ТФР-альфа и ИПФР-I вызывают пролиферацию эпителия, в то время как ТФР-бета ингибирует ее. Свои эффекты факторы роста проявляют отсроченно, а не сразу же после воздействия прогестерона, причем между самими факторами роста существуют взаимодействия, проявляющиеся изменениями их экспрессии и связи с рецепторами. Имея разнонаправленное действие на пролиферацию, индуцируемые прогестероном факторы роста, вероятно, обусловливают противоположные эффекты прогестерона на ткани. Отмечено, что избыточная экспрессия факторов роста может проявиться транзиторным возрастанием пролиферации с последующим ее ингибированием.
Недостаточно изученный гормональный статус у больных пролиферативными дисплазиями молочных желез затрудняет объяснение конкретного механизма, приводящего к развитию диспластических процессов молочных желез, а следовательно, и выбор методов коррекции этих изменений.
Основными клиническими проявлениями мастопатии являются боль или болевые ощущения в молочной железе, которые усиливаются за несколько дней до менструации и прекращаются или уменьшаются после ее окончания. Боли могут иметь различную интенсивность и характер. По мере прогрессирования заболевания боли становятся более длительными, сохраняются после окончания менструации, а иногда в течение всего менструального цикла. Иногда нарушается сон, обостряются хронические соматические заболевания, развиваются нервно-психические нарушения. Одним из проявлений диффузной мастопатии является синдром предменструального напряжения, который выражается в нагрубании желез, появлении ощущения распирания, нарастании отечности стромы, увеличении кровенаполнения, появлении уплотнений в лютеиновую фазу менструального цикла. Это результат пролиферативных изменений протоков и эпителия молочной железы под влиянием прогестерона.
Выделения из сосков встречаются у 5–6 % женщин. Они могут быть кровянистыми, серозными, молочными, гноевидными. Цвет выделений может быть самый разнообразный и чаще всего не указывает на причину возникших изменений.
Лечение диспластических заболеваний молочных желез должно проводиться с учетом:
При диффузной форме ФКБ рекомендуется:
Наиболее патогенетически обоснованно применение препаратов гестагенового ряда, при этом предпочтение отдается производным натурального прогестерона.
Хорошие результаты дает использование препарата для трансдермального применения — прожестожеля. Основной ингредиент препарата — натуральный прогестерон. Гормональные препараты, введенные подобным образом, достигают органов-мишеней, не разрушаясь в печени и не оказывая неблагоприятных системных эффектов на организм. Абсорбция прогестерона при накожном применении составляет около 10 % дозы.
Прожестожель — это гель, содержащий натуральный прогестерон в количестве
Трансдермальный способ введения гестагена позволяет воздействовать на состояние железистого эпителия и сосудистой сети, в результате чего снижается проницаемость капилляров и, следовательно, уменьшается степень отека тканей молочной железы, исчезают симптомы масталгии, а также происходит блокада циклов быстрых эпителиальных митозов, стимулируемых эстрогенами. Отсутствие системного воздействия прогестерона при трансдермальном пути введения особенно актуально для женщин старше 35 лет в связи с частым сочетанием доброкачественных заболеваний молочных желез с патологией репродуктивной системы и сопутствующими экстрагенитальными заболеваниями.
Материалы и методы
На кафедре радиологии РМАПО изучались результаты терапевтического воздействия препарата прожестожель как основного элемента терапии различных форм дисгормональных мастопатий у группы пациенток репродуктивного возраста. В исследовании обобщен материал, касающийся 150 пациенток в возрасте от 25 до 44 лет с подтвержденным диагнозом «фиброзно-кистозная мастопатия» клиническим, рентгенологическим, ультразвуковым методами диагностики, получавших монотерапию прожестожелем. Эффективность терапии оценивалась через каждые 3, 6 и 9 месяцев клиническим, ультразвуковым и радиотермометрическими методами исследования.
Для комплексного обследования больных и оценки эффективности предпринимаемого лечения фиброзно-кистозной болезни был использован ряд методов. Клиническое обследование проводилось всем пациентам и включало в себя сбор анамнеза, осмотр, пальпацию молочных желез, наличие или отсутствие в них патологических образований, выделений из млечных протоков, а также изучалась выраженность различных симптомов заболевания. Указанные критерии подверглись анализу до начала, в процессе предпринимаемого лечения и после его завершения. Проводилось комплексное маммографическое (по показаниям) и ультразвуковое исследование для исключения непальпируемых опухолевых новообразований молочных желез.
Показаниями для назначения препарата были отсутствие опухолевых образований молочных желез и жалобы, характерные для предменструального синдрома. Все пациентки данной группы при первоначальном осмотре отмечали различного рода жалобы. Боли в молочных железах, связанные с менструальным циклом, были выраженными у 150 (100 %) больных. Выделения из молочных желез наблюдались у 6 (4 %) женщин. В ходе исследования женщины получали
Через 3 месяца после начала курса лечения препаратом прожестожель анализ жалоб больных показал следующие результаты. Частота жалоб на наличие болей в молочных железах уменьшилась у 125 (83,3 %) пациенток, болевой синдром сохранился у 25 (16,7 %), однако у них было отмечено уменьшение интенсивности болевого синдрома молочных желез, который возникал лишь перед менструацией. Выделения прекратились у 4 из 6 женщин. Остальные две пациентки отмечали незначительные светлые выделения из сосков молочных желез. После 3-месячного приема препарата назначался перерыв до 3 месяцев.
Через 6 месяцев после первого курса лечения препаратом прожестожель и перерыва 3 месяца показатели были иными. Болевой синдром возобновился у 48 (32 %) пациенток. В дальнейшем в данной группе пациенток прожестожель назначался с другими традиционными препаратами. Через 9 месяцев после повторного курса лечения препаратом прожестожель у всех пациенток купировался болевой синдром, нагрубание молочных желез, отсутствовали выделения из млечных протоков. Наличие болезненности в молочных железах продолжали отмечать 6 (9 %) пациенток.
При применении геля прожестожель уже к концу 2-го месяца лечения наблюдалось значительное улучшение субъективных симптомов мастопатии у большинства пациенток — уменьшение или полное исчезновение ощущения болезненности, набухания, а также снижение плотности, тяжистости и напряжения тканей молочных желез, ослабление болезненности при пальпации. Кроме того, пациентки отмечали положительное влияние терапии на психоэмоциональное состояние — уменьшение чувства тревоги, страха, исчезновение симптомов канцерофобии, улучшение настроения.
По окончании терапии прожестожелем у всех больных уменьшились проявления мастодинии. При динамическом контроле, включавшем осмотр, УЗИ молочных желез, маммографию до и после лечения, отмечена положительная динамика. У 6 пациенток, учитывая недостаточный клинический эффект, потребовалось проведение дополнительного 3-месячного курса лечения препаратом прожестожель с переходом на непрерывный режим терапии до полного исчезновения симптомов масталгии. Побочных эффектов во время лечения препаратом не отмечено.
Таким образом, препарат прожестожель может широко применяться для лечения мастодинии как самостоятельной патологии или сопровождающей ФКМ у больных с различными эндокринными заболеваниями, что позволяет улучшить состояние молочных желез, а также, что немаловажно, качество жизни женщин, страдающих мастопатией.
Препарат прожестожель на сегодняшний день является единственным патогенетически обоснованным препаратом трансдермального применения для лечения диффузной формы мастопатии у женщин репродуктивного возрастного диапазона. При применении препарата отмечается устойчивый положительный клинический эффект и не наблюдается присущих гормональной терапии факторов риска. Немаловажен для современной женщины тот факт, что препарат прожестожель имеет следующие характеристики:
Негормональные методы лечения можно условно разделить на несколько групп:
Мастодинон применим для лечения мастопатий у женщин широкого возрастного диапазона, он является препаратом выбора, что определяется по устойчивым положительным клиническим переменам в состоянии здоровья женщин. Немаловажен для современной женщины тот факт, что прием препарата двухразовый. Эффективность, безвредность, хорошая переносимость сопровождаются выраженным ослаблением предменструального синдрома, нормализацией менструального цикла и психоэмоционального состояния у большинства пациенток, применяющих данный препарат.
Диффузный вариант мастопатии вовсе не опасен для жизни. Тем не менее оставленное без внимания и адекватного лечения, что случается весьма часто, это заболевание причиняет существенные неудобства и неприятности как страдающим этой болезнью женщинам, так и их близким. В тех же вариантах мастопатии, когда неизбежно хирургическое вмешательство, болезненное состояние пациенток, как правило, осложняется серьезными психоэмоциональными переживаниями, что нередко приводит к состоянию дистимии и даже депрессии. Оставленная без врачебного внимания мастопатия может привести к сексуальной дисгармонии, что, в свою очередь, способно утяжелить течение болезни молочных желез. Длительно существующая мастопатия является ведущим фактором риска развития рака молочной железы. Учитывая широкое распространение мастопатии среди женского населения и относительно невысокую эффективность лечения, необходимо также упомянуть о существовании проблемы экономических затрат и потерь, связанных с этим заболеванием, поэтому очевидна актуальность дальнейших исследований.
Заключение
Любые усилия по совершенствованию ранней диагностики могут быть наиболее успешны, если в качестве первого этапа будет участвовать поликлиническая служба практического здравоохранения, поскольку именно здесь происходит первое обращение человека к медицине.
Подготовка и переподготовка кадров в системе высшего последипломного медицинского образования является важнейшим направлением снижения смертности от злокачественных опухолей, в том числе рака молочной железы. Онкологическая служба, специалисты-онкологи только в условиях тесной связи с врачами общей лечебной сети в состоянии решить проблему ранней диагностики и снизить смертность от рака молочной железы. Одной из основных причин запущенности злокачественных опухолей является субъективный подход к оценке состояния молочных желез различными специалистами, субъективная оценка возможностей различных диагностических методов врачами различного профиля, что приводит к диагностическим и тактическим ошибкам, к разобщенности между врачами различных специальностей первичного звена и специализированных служб, что не позволяет реализовать достижения современного комплексного исследования. Имеющихся знаний по проблеме РМЖ у терапевтов, гинекологов, эндокринологов, хирургов, врачей ультразвуковой диагностики, рентгенологов и других лечебных специальностей оказывается недостаточно для эффективного решения организационно-диагностических задач, связанных с проблемой скрининговой диагностики заболеваний молочной железы врачами общей лечебной сети. Многообразие влияния различных органов и систем на молочную железу вызывает необходимость объединения всех смежных специалистов в решении вопросов профилактики, диагностики, лечения и реабилитации.
Кафедра радиологии РМАПО одной из первых в 1997 году начала подготовку врачей различных специальностей по вопросам диагностики и лечения заболеваний молочной железы. Накоплен опыт и к настоящему времени проведено более 60 циклов, на которых прошли подготовку более 1000 курсантов из всех областей Российской Федерации.
Учебная программа включает лекции, семинары, практические занятия, на которых наряду с медицинскими аспектами проблемы затрагиваются вопросы организации онкологической и маммологической службы, стандарты диагностики и лечения.
Общепринятый стандарт обследования пациенток включает: клинический осмотр, маммографию в сочетании с интервенционными методиками; ультразвуковое исследование; диагностическую пункцию.
Бурный технический прогресс и развитие диагностических технологий диктует необходимость разработки и оптимизации всей системы технологии диагностического процесса, включая медицинские, технические и организационные аспекты, обеспечивающие максимальную реализацию возможностей современного диагностического комплекса, позволяющие внести качественные изменения на всех уровнях управления диагностическим процессом и создать новые условия для работы врача и требований к организации труда.
Современный врач-клиницист, занимающийся диагностикой и лечением заболеваний молочной железы, должен владеть методами клинического обследования, знать гормональную регуляцию и генетический статус женского организма, оценивать семейный анамнез, выполнять или анализировать рентгенологические, ультразвуковые, радиотермометрические исследования молочной железы, производить пункционную биопсию с использованием инвазивных диагностических методик, знать основы организации маммологического скрининга. Должно быть налажено взаимодействие в первую очередь с системой онкологической помощи для решения вопроса о дальнейшей комплексной диагностике пациентов с выявленными опухолями молочных желез с последующим лечением в специализированном онкологическом стационаре.
Основной целью дополнительного профессионального образования по совершенствованию медицинской помощи при заболеваниях молочных желез является приобретение и совершенствование практических и теоретических навыков, необходимых для решения вопросов ранней диагностики, адекватного лечения, реабилитации, эффективного мониторинга и профилактики различных заболеваний молочной железы в соответствии с профилем учреждения и занимаемой врачом должностью.
На тематические циклы зачисляются врачи, прошедшие ранее специализацию или общее усовершенствование по специальности «хирургия», «гинекология», «рентгенология», «ультразвуковая диагностика» и другим лечебным специальностям, связанным с вопросами диагностики и лечения заболеваний молочных желез. Продолжительность обучения на циклах тематического усовершенствования — 1 месяц в зависимости от контингента обучающихся, цели и тематики цикла.
Для выполнения данной программы в процессе обучения используются следующие виды занятий: лекции, практические занятия, различные виды семинаров, учебные конференции, а также занятия на базах онкологических, радиологических, маммологических научно-исследовательских учреждений. После успешного окончания цикла слушатель получает удостоверение установленного образца.
Совершенствование преподавания вопросов маммологии в медицинских вузах: подготовка профессорско-преподавательского состава по онкомаммологии, онкологов-маммологов, рентгенологов, врачей УЗ-диагностики, владеющих современными интервенционными технологиями, морфологов, практических врачей широкого профиля на базе специализированных клиник, кафедрах онкологии и радиологии и созданных курсах маммологии в системе последипломного образования.
1. Бурдина Л.М. Особенности состояния молочных желез и гормонального статуса у больных с доброкачественными гиперпластическими заболеваниями внутренних половых органов // Маммология. — 1993. — № 1. — С. 4-11.
2. Демидов С.М. Гормонально-иммунологический статус при пролиферативных дисплазиях молочных желез и способы его коррекции: Автореф. дис... канд. мед. наук. — М., 1991. — 19 с.
3. Летягин В.П., Высоцкая Н.В., Легков А.А. с соавт. Лечение доброкачественных и злокачественных заболеваний молочных желез. — М.: Рондо, 1997. — 287 с.
4. Сидоренко Л.Н. Мастопатия. — Л.: Медицина, 1991. — 264 с.
5. Рожкова Н.И. Медицина и общественные организации на страже женского здоровья // Современные аспекты лечения заболеваний молочных желез. Материалы научно-практической конференции. — Москва, 2004.— С. 3.
