Газета «Новости медицины и фармации» Маммология (298) 2009 (тематический номер)
Вернуться к номеру
Рак молочной железы
Авторы: Г.В. Бондарь, И.Е. Седаков, Донецкий областной противоопухолевый центр, ДонНМУ им. М. Горького
Версия для печати
Введение
Рак молочной железы (РМЖ) занимает первое место в структуре онкологической заболеваемости женщин, а статистические данные свидетельствуют о неуклонном интенсивном росте заболеваемости данной патологией.
Цель работы — отражение современного уровня знаний, касающихся биологических особенностей течения РМЖ, его диагностики и основных принципов лечения РМЖ в мировой практике и ДОПЦ.
Заболеваемость
Структура заболеваемости злокачественными опухолями среди женского населения большинства экономически развитых стран мира, в том числе и в Украине, за последние годы претерпела серьезные изменения. Лидирующее место среди гормонозависимых опухолей органов репродуктивной системы женщин занимает рак молочной железы, составляя 53,7 случая на 100 000 населения Украины. РМЖ наиболее распространен в странах Европы (более 180 000 случаев в год) и США (более 130 000 случаев в год). Наибольший прирост случаев РМЖ наблюдается в Канаде, США, Швеции, Испании, Финляндии. В среднем число случаев регистрации РМЖ увеличивается в каждой стране на 1–2 %. Наименьшее число случаев приходится на Японию, в которой РМЖ встречается только в 12–15 случаях на 100 000 женщин.
Интересны для сравнения показатели заболеваемости и смертности от РМЖ в странах Европейского Союза (табл. 2).
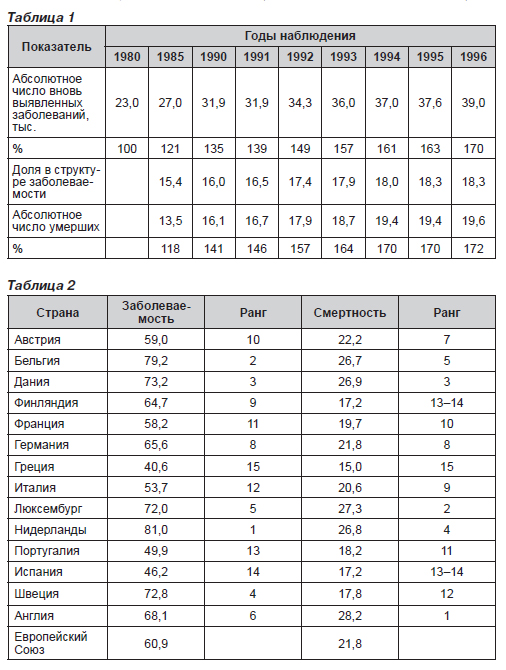
Сведения статистического сборника (канцер-регистр) по Украине относительно показателей заболеваемости РМЖ представлены в табл. 3.
Показатели смертности от злокачественных заболеваний молочной железы (МЖ) по Украине представлены в табл. 4.
По Донецкой области показатели представлены в табл. 5.
Как видно из табл. 3–5, по показателям заболеваемости и смертности Украина если и не лидирует, то и не отстает, приближаясь к уровню стран Европейского Союза (53,7 случая на 100 000 женщин). Однако с уверенностью можно утверждать, что по удельному весу запущенных форм РМЖ Украина находится на одном из первых мест (более 60 % впервые обращающихся женщин имеют III–IV стадию заболевания), и это обстоятельство объясняется как низким уровнем информированности и образованности населения, так и низким уровнем оказания специализированной медицинской помощи. Показатели Донецкого областного противоопухолевого центра относительно удельного веса запущенных форм РМЖ (III–IV стадии) и удельного веса выявленных при профосмотрах в процентном отношении за пять предшествующих лет представлены в табл. 6.
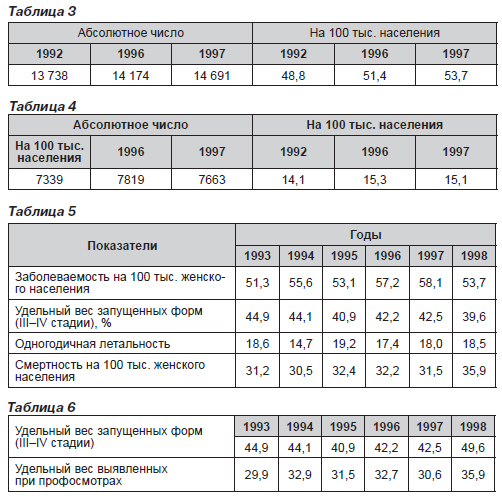
Столь неутешительные показатели требуют все более интенсивного поиска новых методов диагностики и лечения. Несмотря на то что в высокоразвитых странах выявление ранних форм РМЖ достигло значительных успехов, результаты лечения этой патологии, а соответственно и безрецидивной выживаемости, оставляют желать лучшего.
Этиология
По данным ВОЗ, основными факторами риска в развитии РМЖ являются:
1. Факторы, характеризующие функционирование репродуктивной системы организма:
2. Эндокринно-метаболические факторы, обусловленные сопутствующими и предшествующими заболеваниями:
3. Генетические факторы (носители BRCA-1 или BRCA-2 генов):
г) раково-ассоциированные генодерматозы:
4. Экзогенные факторы:
Предраковые (предшествующие) заболевания
Классификация Пантюшенко в модификации Рожковой:
Хирургическая анатомия
Молочные железы как часть репродуктивной системы женщины — сложный в анатомическом и функциональном отношении орган, претерпевающий выраженные циклические изменения. В процессе маммогенеза в нем происходит сложная перестройка структуры, достигающая своего расцвета в период беременности и лактации. По эмбрионогенезу молочная железа тесно связана с потовыми железами. Анатомически МЖ представляют сложный альвеолярно-трубчатый орган, состоящий из 15–24 долей (М.М. Авербах, 1958; Н.И. Рожкова, 1993). Каждая доля имеет конусовидную форму с вершиной у соска, окружена рыхлой соединительной тканью и небольшим количеством жировой клетчатки, частично проникающей между дольками (Н.В. Заболотская, 1993). Все выводные протоки одной железистой доли соединяются в млечный ход, который оканчивается на верхушке соска. Количество протоков может быть от 12 до 20. В молочной железе существует два вида соединительной ткани — опорная и ложевая, или мантильная (Н.И. Рожкова, 1993). Опорная ткань входит в систему поддерживающей связки Купера и расположена в основном между долями и дольками. Внутридольковые перегородки продолжаются кпереди за пределы фасциального футляра к глубоким слоям кожи в виде связок Купера. Ложевая ткань распределена между ацинусами.
МЖ кровоснабжается в основном из трех источников: внутренней грудной артерии (ветвь подключичной артерии), боковой грудной артерии (ветвь подключичной артерии) и межреберных (от 3 до 7) (Н.И. Рожкова, 1993). Венозный отток осуществляется через межреберные и внутренние грудные вены.
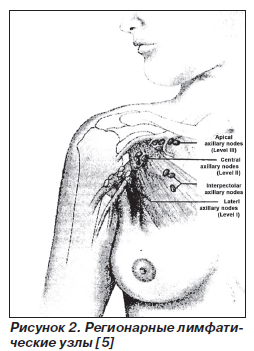
Знание путей оттока лимфы от МЖ позволяет определять направление процесса при метастазировании. Лимфа от наружных квадрантов МЖ оттекает к группе подмышечных лимфатических узлов. Подмышечные лимфатические узлы подразделяют на узлы 3 уровней (в зависимости от взаиморасположения с малой грудной мышцей). Состояние подмышечных лимфатических узлов является наиболее важным прогностическим фактором у больных РМЖ (В. Fornage, J. Lorigtin, 1989; Sacre, 1990). От внутренних квадрантов МЖ лимфоотток происходит в парастернальные лимфатические узлы. Кроме того, различают подключичный, межреберный, медиастенальный, внутрикожный, подкожный пути оттока лимфы в направлении противоположных лимфоузлов, подкожная и субфасциальная сеть лимфатических узлов в эпигастральной области, внутрикожный и кожный путь оттока по ходу внутренних и наружных ветвей верхних и нижних эпигастральных сосудов в направлении забрюшинных лимфоузлов, брюшины и яичников (Л.Ю. Дымарский, 1980; А.П. Баженова, 1983; Т.А. Пантюшенко, 1984; Fornage, Lorigaii, 1989; Sacre, 1990).
Морфофункциональной единицей МЖ являются альвеолы, величина которых изменяется в зависимости от гормональной фазы (Т.Е. Самойлова, 1986, 1987). Их стенки выстланы одним слоем железистых клеток — лактоцитов. Альвеолы, сужаясь, переходят в тонкий проток. 150–200 альвеол объединены в дольки с общим протоком более крупного диаметра. Дольки, в свою очередь, объединены в доли с более широкими протоками. Сократительный аппарат МЖ представлен клетками миотелия и гладкой мускулатуры, которые являются важным звеном нейрогормональной регуляции в период лактации.
Развитие и функция МЖ находятся под контролем эндокринной системы. Маммогенез представляет собой сложный физиологический процесс, происходящий в отдельные периоды онтогенеза (Л.М. Бурдина, 1992, 1993). По данным М.А. Анохиной (1969), Г.А. Мельниченко (1984), пролиферативные процессы в МЖ зависят от общего обмена веществ. Активная роль при этом отводится инсулину, который, включаясь в метаболизм, повышает реактивность МЖ к половым гормонам (Е.М. Самунджан и соавт., 1979). Во второй фазе пубертатного периода становление гипоталамо-гипофизарно-яичниковых связей приобретает зрелый характер, устанавливаются взаимоотношения, способствующие цикличному развитию фолликула и овуляции (Т.А. Пантюшенко, 1985;
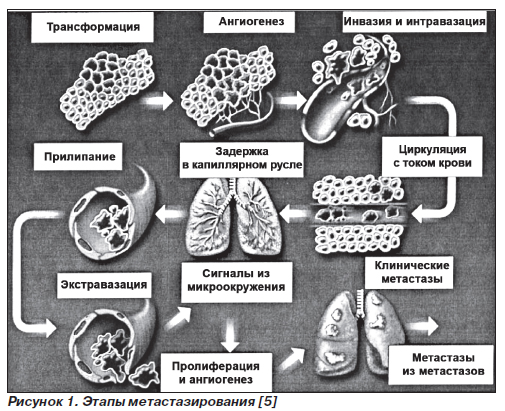
Схема развития опухоли на клеточно-генетическом уровне
Основные этапы развития опухоли и метастазирования могут быть разделены следующим образом:
1) появление одной или нескольких опухолевых клеток. Первоначально их рост обеспечивается питательными веществами путем диффузии;
2) опухолевый ангиогенез является необходимым этапом метастазирования, начинается при достижении опухолью
3) инвазия окружающей стромы;
4) интравазация, при этом до 99 % опухолевых клеток погибают;
5) задержка в капиллярном русле опухолевой клетки путем прилипания к эндотелиальным клеткам или базальной мембране капилляра;
6) экстравазация;
7) рост опухолевого узла в паренхиме, при высокой колониеобразующей способности эти метастазы могут давать начало новым метастазам, так называемым метастазам из метастазов.
Морфологические варианты, морфологическая классификация:
1. Неинфильтрирующие опухоли:
2. Инфильтрирующие:
л) рак с метаплазией (плоскоклеточного типа, веретеноклеточного типа, хондроидного и остеоидного типа, смешанного типа);
3) Болезнь Педжета соска.
Наиболее часто встречающиеся формы РМЖ и частота
1. Папиллярный рак (1 % всех случаев РМЖ) — внутрипротоковое неинвазивное новообразование, исходящее из эпителия протоков, низкой степени злокачественности, прогноз относительно благоприятный.
2. Медуллярный рак, встречается в 5–10 % наблюдений — чаще это большая объемная опухоль со слабой способностью к инвазивному росту, окруженная лимфоцитарным валом. Прогноз (по сравнению с инфильтрирующим протоковым раком) более благоприятный.
3. Воспалительный рак (маститоподобный, 5–10 %) распространяется по лимфатическим сосудам кожи, что сопровождается ее покраснением, уплотнением и рожеподобным воспалением, повышением температуры тела. Без соответствующего лечения в ряде случаев быстро прогрессирует, достаточно хорошо реагирует на селективную внутриартериальную антибиотико-химиотерапию. Относительно часто метастазирует гематогенным путем.
4. Инфильтрирующий протоковый скиррозный рак (70 %) характеризует образование гнезд и тяжей опухолей клеток, окруженных плотной коллагеновой стромой, имеет выраженную способность к инвазивному росту, характеризуется достаточно ранней манифестацией метастазов, прогноз относительно неблагоприятный.
5. Болезнь Педжета (рак соска и ареолы молочной железы) — разновидность рака молочной железы; характерно экземоподобное поражение соска. В глубоких слоях эпидермиса выявляют происходящие из эпителия апокриновых желез крупные клетки со светлой цитоплазмой. Существенное значение имеет цитологическое исследование мазка, взятого с изъязвленной поверхности. При соответствующем радикальном лечении в ранних формах прогноз относительно благоприятный.
Рецепторы стероидных гормонов являются критерием чувствительности опухолей МЖ к эндокринной терапии (РЭ, РП, РА). По состоянию эстрогеновых рецепторов (ЭРц) выделяют виды РМЖ:
1. ЭРц-позитивные опухоли чаще встречают в постменопаузе. Около 60–70 % первичных раков молочной железы характеризует наличие ЭРц.
2. ЭРц-негативные опухоли чаще встречают у больных в пременопаузе. У одной трети больных с ЭРц-негативными первичными РМЖ в последующем наблюдают развитие рецидивных ЭРц-позитивных опухолей.
Опухоли молочных желез, имеющие ЭРц-позитивный статус, являются прогностически более благоприятными.
Из других прогностических маркеров чаще применяются:
Клиническая классификация, стадии, система TNM
Отечественная классификация по стадиям
I стадия — опухоль до
IIа стадия — опухоль от 2 до
IIb стадия — опухоль тех же или меньших размеров с одиночными (не более 2) смещаемыми метастазами в подмышечные и/или парастернальные лимфоузлы на стороне поражения.
IIIa стадия — опухоль более
IIIb стадия — опухоль тех же или меньших размеров с одиночными (не более 2) ограниченно смещаемыми или множественными смещаемыми метастазами в подмышечных, подключичных, подлопаточных, парастернальных узлах на стороне поражения. Опухоль той же или меньшей степени распространения с одиночными (не более 2) смещаемыми метастазами в надключичных лимфатических узлах на стороне поражения. Метастазы в надключичной области могут сочетаться с другими регионарными метастазами.
IVa стадия — местно распространенная опухоль с наличием диссеминации по коже (сателлиты) или обширным изъязвлением, или фиксированная к грудной стенке, или с тотальным отеком МЖ. Все острые формы РМЖ — рожистоподобные, маститоподобные, панцирные. Метастазы в регионарных лимфоузлах отсутствуют.
IVb стадия — опухоль аналогичной степени местного распространения с любыми вариантами регионарного метастазирования или опухоль меньшей степени местного распространения с одиночными ограниченно смещаемыми или множественными смещаемыми надключичными и/или несмещаемыми регионарными метастазами. Опухоль любой степени местного распространения с клинически определяемыми отдаленными метастазами, в том числе лимфогенными контрлатеральными.
При наличии двустороннего поражения МЖ классификация проводится по общим принципам отдельно для каждой железы.
Классификация TNM опухоли молочной железы (ICD-0 174) изд. 6,
Правила классификации
Классификация применима только для рака. Должно быть гистологическое подтверждение диагноза. Анатомическая часть, где развивается опухоль, фиксируется, но не учитывается при классификации. В случае одновременного развития нескольких опухолей в одной железе Т-категория определятся по наибольшей. Одновременно возникшие билатеральные опухоли классифицируются отдельно. При оценке категорий Т, N и М используются следующие методы:
Дополнительные символы. Когда необходимо, могут использоваться символы у, r и С-фактор.
Анатомические части. 1. Сосок (174.0). 2. Центральная часть (174.1). 3. Верхневнутренний квадрант (174.2).
4. Нижневнутренний квадрант (174.3). 5. Верхненаружный квадрант (174.4). 6. Нижненаружный квадрант (174.5).
7. Аксиллярный отросток (174.6).
Регионарными лимфатическими узлами являются:
1. Подмышечные (на стороне поражения) и интерпекторальные (лимфатические узлы Роттера) располагаются вдоль аксиллярной вены и ее притоков и подразделяются на следующие уровни:
2. Внутренние лимфатические узлы МЖ (на стороне поражения) располагаются в эндоторакальной фасции в межреберных пространствах вдоль края грудины.
Любые другие лимфатические узлы, пораженные метастазами, включая шейные или контрлатеральные внутренние грудные лимфатические узлы, обозначаются как отдаленные метастазы М1.
TNM Клиническая классификация
Т Первичная опухоль
ТХ недостаточно данных для оценки первичной опухоли
Т0 первичная опухоль не определяется
Tis преинвазивная карцинома: интрадуктальная или лобулярная carcinoma in situ, или болезнь Педжета соска без наличия опухолевого узла.
Примечание: болезнь Педжета, при которой пальпируется опухолевой узел, классифицируется по его размерам.
Т1 опухоль до
Т2 опухоль до
Т3 опухоль более
Т4 опухоль любого размера с прямым распространением на грудную стенку или кожу
Примечание: грудная стенка включает ребра, межреберные мышцы, переднюю зубчатую мышцу, но без грудных мышц.
Примечание: воспалительная форма РМЖ характеризуется диффузным утолщением кожи с плотными краями, обычно без подлежащей пальпируемой массы. Если биопсия кожи отрицательна и нет локализованной опухолевой массы, при патологической классификации употребляется категория рТХ, а при клинической — Т4d. При оценке категории рТ определяется инвазивный компонент. Если имеется большой плоскостной компонент (до
N Регионарные лимфатические узлы
NX недостаточно данных для оценки состояния регионарных лимфатических узлов
N0 нет признаков поражения метастазами регионарных лимфатических узлов
N1 метастазы в смещаемых подмышечных лимфатических узлах(е) на стороне поражения
N2 метастазы в подмышечных лимфатических узлах, фиксированных друг с другом или с другими структурами, на стороне поражения
N3 метастазы во внутренних грудных лимфатических узлах на стороне поражения, поражение над- и подключичных гомолатеральных лимфоузлов при наличии (или без) поражения подмышечных лимфоузлов:
 М Отдаленные метастазы
М Отдаленные метастазы
MX недостаточно данных для определения отдаленных метастазов
М0 нет признаков отдаленных метастазов
М1 имеются отдаленные метастазы (включая метастазы в надключичных лимфоузлах)
Категория М1 может быть дополнена в зависимости от локализации отдаленных метастазов:
pTNM Патологическая классификация
рТ Первичная опухоль
Патологическая классификация требует исследования первичной опухоли, по краю произведенной резекции не должно быть опухолевой ткани. Если по краю резекции имеется лишь микроскопическое распространение опухолевой ткани, то случай может классифицироваться как рТ. рТ-категории соответствуют Т-категориям.
pN Регионарные лимфатические узлы
Для определения патологической классификации необходимо иссечение и исследование хотя бы нижних подмышечных лимфатических узлов (уровень 1). В подобном эксцизионном материале содержится не менее 6 лимфатических узлов.
pNX недостаточно данных для оценки состояния регионарных лимфатических узлов (узлы не удалены для исследования)
pN0 нет признаков поражения метастазами регионарных лимфатических узлов
pN1 выявлены метастазы в смещаемых подмышечных лимфоузлах(е) на стороне поражения:
pN2 метастазы в подмышечных лимфатических узлах на стороне поражения, спаянные друг с другом или другими структурами
pN3 метастазы во внутренних лимфатических узлах(е) МЖ
рМ Отдаленные метастазы
рМ-категории соответствуют М-категориям.
Резидуальные опухоли (R Классификация)
Наличие или отсутствие резидуальных опухолей после лечения обозначается символом R.
Группировка по стадиям
Примечание: прогноз больных с pN1a аналогичен прогнозу больных с pN0.
Резюме. Молочные железы
Tis In situ
T1 < 2 см:
Т2 >
Т3 >
Т4 Грудная стенка/кожа:
N1 смещаемые подмышечные лимфатические узлы — pN1
pN1а микрометастазы:
pN1b макрометастазы:
N2 фиксированные подмышечные — pN2
N3 внутренние лимфатические узлы молочной железы — pN3
Клиническая картина, основные симптомы и синдромы. Клиника ранних стадий заболевания
Клиническая картина РМЖ зависит от стадии заболевания, гистологической структуры опухоли, анатомического расположения, наличия регионарных и/или отдаленных метастазов. Основными клиническими проявлениями ранних стадий заболевания служат наличие пальпируемого уплотнения в ткани МЖ, появление болезненности в одной из желез во время менструации, дискомфорт при физических упражнениях, выделения из соска. По данным Американской ассоциации маммологов, в 96 % случаев имеются нарушения менструального цикла. В то же время клиническое обследование, анамнестические данные, осмотр МЖ, тщательно и правильно проведенная пальпация в ряде случаев превосходят другие, весьма дорогостоящие методы исследования. Так, по данным А.П. Баженовой (1985), только на основании клинических симптомов заболевания удается поставить правильный диагноз у 83,6 % больных. Тот факт, что многие женщины, не имеющие отношения к медицине, сами обнаруживают у себя небольшие опухоли, относящиеся к первой стадии заболевания, показывает, что эта задача еще легче выполнима для врача, владеющего методикой пальпации МЖ. Таким образом, клиническая диагностика РМЖ довольно эффективна. Следует лишь умело использовать ее как наиболее экономичный, массовый и легко осуществляемый метод выявления этого тяжелого заболевания.
Клиническая диагностика РМЖ основывается на ряде анамнестических сведений, данных осмотра, наличии прощупываемой опухоли и изменения лимфатических узлов. Основными жалобами больных РМЖ являются: наличие опухоли (более 70 %), патологические выделения из сосков (более 20 %), наличие отека и инфильтрации МЖ (с учетом симптома «лимонной корки» — около 30 %), боль в МЖ (до 20 %), другие симптомы (около 20 %). При изучении анамнеза необходимо выяснить сроки появления первых признаков заболевания и темп их развития, ранее выполненные операции на МЖ, замужество, семейное положение, сексуальная функция, возраст при первой беременности и первых родах, возраст появления менструальной функции, сроки ее окончания, возраст при последней беременности, число беременностей и абортов, наличие гинекологических заболеваний, указание на травмы МЖ в анамнезе, перенесенные послеродовые маститы.
Путем осмотра определяют симметричность расположения и форму МЖ, уровень стояния сосков и состояние кожных покровов. Даже при небольшой опухоли (до
При больших раковых опухолях диагностика облегчается, так как появляется ряд новых признаков:
1. Симптом умбиликации или симптом площадки.
2. Симптом Прибрама (при потягивании за сосок опухоль смещается за ним).
3. Симптом Кенига (при прижатии ладонью плашмя МЖ опухоль не исчезает).
4. Симптом Краузе (утолщение кожи ареолы вследствие поражения опухолевыми клетками лимфатического сплетения подареолярной зоны).
5. Симптом Паира (при захватывании кожи над опухолью двумя пальцами справа и слева образуется не продольная, а поперечная складчатость).
6. Ретракция и деформация соска.
7. Симптом Форже (стояние соска выше горизонтальной линии, проведенной через здоровый сосок).
8. Симптом Ри (при отведении руки на пораженной стороне до прямого угла опухоль остается неподвижной). Признак фиксации опухоли МЖ к грудной клетке.
При узловом раке пальпаторно определяется довольно четко очерченное, округлое, плотное новообразование с мелко- и крупнобугристой поверхностью, ограниченно подвижное по отношению к ткани железы в связи с инфильтрацией окружающих тканей. В случае центрального расположения опухоли при малых размерах ее отмечаются отклонение соска в сторону или его фиксация. При более распространенном процессе в результате прорастания крупных выводных протоков соска развивается симптом втяжения его.
К диффузным ракам МЖ относят первичную и вторичную отечно-инфильтративную форму. В первом случае МЖ увеличена, кожа ее пастозна и отечна. Выражены гиперемия и симптом апельсиновой корки. Выявить опухолевый узел в ткани железы часто трудно. Пальпируется инфильтрат без четких контуров, занимающий большую часть железы. Отек обусловлен блокадой лимфатических путей самой железы метастатическими эмболами или их сдавлением опухолевым инфильтратом. К данной форме ранее относили: панцирный рак, эризипелоидную или рожистую форму, маститоподобную форму.
При вторичной отечно-инфильтративной форме четко определяется опухолевый узел, но также присутствует вторичный лимфостаз, обусловленный метастазами в регионарных зонах.
Частота и закономерности лимфогенного и гематогенного метастазирования зависят от гистологической структуры опухоли, степени инвазивной активности и индивидуальных анатомических особенностей.
Диагностика, методы, эффективность. Ранняя и доклиническая диагностика. Организация скрининга
Выбор правильного лечения РМЖ возможен только при установлении верного диагноза и точной оценке степени распространенности опухолевого процесса. В настоящее время опубликовано огромное количество работ, в которых доказывается высокая эффективность таких исследований, как маммография, крупнокадровая флюоромаммография, цитологическое исследование, ультразвуковая радиоизотопная диагностика, радиоизотопная лимфосцинтиграфия, чрезгрудинная флебография, определение рецепторов, определение уровня стероидных гормонов и маркеров опухолевого роста и т.д. Несмотря на то что РМЖ относится к визуальным локализациям, его диагностика в ряде случаев бывает достаточно сложной, особенно минимальных форм рака. Е.Г. Пинхосевич, Л.Д. Линденбратен (1992) предлагают двухэтапную скрининговую систему распознавания ранних стадий РМЖ и предраковых состояний:
Ранняя диагностика РМЖ остается основной проблемой улучшения отдаленных результатов.
В литературе накоплен значительный опыт применения новых методов обследования МЖ, которые дают возможность получить изображение МЖ. Одним из ведущих является маммография (В.И. Тарутинов, 1990; В.М. Драблинский и соавт., 1991; В.Ф. Семиглазов, 1992; Н.И. Рожкова, 1993; A. Locker et а1., 1990; Goldsweing et al., 1990).
Однако, несмотря на высокую эффективность, маммография имеет ряд недостатков: невозможность дифференциальной диагностики кисты и солидного образования (О.Д. Дашмир, 1990; И.В. Лисаченко и соавт., 1990; И.Г. Панина, 1990; D. Rosner, 1981; S. Levi, 1981; M. Friedrich, 1983), лучевая нагрузка на пациента. Затруднено выявление опухоли на фоне мастопатии или при исследовании желез у молодых женщин с плотным железистым фоном, у которых железистый треугольник перекрывает тень опухоли (Н.И. Бражников, 1971). Кроме того, не всегда возможно получить изображение очагов в аксиллярной области (И.В. Лисаченко и соавт., 1990; И.Г. Панина, 1990; Adier, 1991).
Описанные недостатки рентгенологического метода побуждали внедрять в практику новые, безвредные и информативные диагностические методы, к которым относится ультразвуковой метод исследования (УЗИ) (И.А. Гиленко, 1976; Ф.Л. Аляви, 1977; И.Г. Панина, 1990; О.Д. Дашмир, 1991; R. Otto, 1993; L. Venta, 1994).
Ультразвуковое сканирование МЖ впервые провели Wild и Reid в 1952 году. Они продемонстрировали возможности УЗИ в А-режиме для дифференцировки кист и солидных образований. Ультразвуковой скрининг показан для выявления доброкачественных образований диаметром более
В случаях, когда УЗИ и маммография дополняют друг друга, точность диагностики достигает 98 %. Безвредность УЗИ делает возможность контролировать размер опухоли и лимфатических узлов после проводимого лечения.
M. Fritdrich (1983) выдеяяет 5 слоев МЖ в соответствии с эхоструктурой: кожные покровы с повышенной эхогенностью, жировая ткань с низкой интенсивностью эхосигнала, паренхима железы со смешанной эхоструктурой, ретромаммарное пространство, содержащее жировую ткань, и грудная стенка со смешанной эхоструктурой. Ультразвуковая картина неизмененной МЖ состоит из отражений от соединительной, жировой и железистой тканей (Ф.Л. Аляви, 1977; И.Г. Панина, 1989; И.И. Камалов, 1991; Н.В. Заболотская, 1993).
По литературным данным, точность ультразвуковой диагностики в выявлении РМЖ противоречива — колеблется от 58 до 90 % (F. Hall, 1985; W. Schmidt
Ультразвуковая томография на сегодняшний день является главным неинвазивным методом изображения жидкостьсодержащих объемных образований. Чувствительность метода по сводным данным составляет 94–100 % (Wild, Reid, 1952; Ciatto et al. 1991; F. Leonardi, 1993). Минимальные размеры кисты, выявляемые при УЗИ, —
Несмотря на достижения в области ранней диагностики в сфере инструментальных методов исследования, основным методом выявления ранних форм РМЖ остается пальпация, в которой ведущие маммологи отводят не второстепенную роль самопальпации. Таким образом, в обязанности специалистов, связанных с лечением заболеваний МЖ, входит разъяснительная работа по правилам, технике проведения и кратности самопальпации.
Методы диагностики:
Лечение. Краткая история, принципы
Хирургическое лечение. История хирургического лечения РМЖ берет свое начало с древних времен, однако широкое распространение метод получил после выхода работ Холстеда и Майера, которые стали основополагающими. С
В большинстве случаев применяется модифицированная радикальная мастэктомия. Операции с сохранением МЖ позволяют правильно оценить распространенность опухолевого процесса и улучшают косметический результат, однако возможность сохранения железы имеется не у всех больных. Операция может быть радикальной или паллиативной (при первично-неоперабельной опухоли, после неоадъювантного лечения или операции, предпринимаемых с целью циторедукции).
1. Удаление всей пораженной МЖ необходимо по причине многофокусности заболевания. Примерно у 30–35 % пациенток находят предраковые или раковые поражения в участках, соседних с пораженным первичной опухолью.
2. Удаление подмышечных лимфатических узлов необходимо для обеспечения радикализма и определения поражения узлов и стадии заболевания.
Виды операций:
1. Лампэктомия (секторальная резекция), лимфаденэктомия подмышечных лимфатических узлов (1-го и 2-го уровня) и послеоперационное облучение применяются при небольших опухолях (менее
2. Простая мастэктомия (операция Маддена) включает удаление МЖ с околососковым пространством совместно с удалением лимфатических узлов 1-го уровня. Показана при II стадии, преимущества заключаются в сохранении мышечных лимфатических анастомозов с верхней конечностью и сохранении большой и малой грудной мышц.
3. Модифицированная радикальная мастэктомия (операция Пэйти). Удаляют кожу вокруг железы, молочную железу, малую грудной мышцы, жировую клетчатку с лимфатическими узлами подмышечной, подключичной и подлопаточной областей. Уровень выживаемости и частота рецидивов при этой операции сравнимы с такими же при радикальной мастэктомии (операция Холстеда). Косметический дефект меньший, чем после мастэктомии по Холстеду. Реконструктивная операция — субпекторальное протезирование. Показания при II и III стадии те же, что и при модификации Маддена.
4. Радикальная мастэктомия по Холстеду. Вместе со всеми тканями, указанными выше, удаляют и большую грудную мышцу. Показана при IV стадии, когда имеется прорастание в большую грудную мышцу или грудную клетку.
5. Обширная радикальная мастэктомия включает удаление лимфатических узлов средостения. Операция показана при больших или медиально расположенных опухолях с наличием внутригрудных (парастернальных) метастазов. Высокий риск интраоперационной летальности.
6. Операции по реконструкции МЖ выполняют одновременно с мастэктомией либо вторым этапом после полного заживления первичной операционной раны. Применяются субпекторальное эндопротезирование, пластика торакодорсальными и TRAM-лоскутами.
Лучевая терапия. Применяется достаточно давно, играет важную роль в лечении РМЖ, что подтверждено многочисленными рандомизированными исследованиями. В процессе истории изменялись разовые и суммарные дозы терапии, изменяются режимы проведения лучевой терапии (ЛТ). Так, статический режим при ряде локализаций в настоящий момент считается устаревшим, в настоящий момент его заменяет ротационный режим. ЛТ делится:
1. На предоперационную. Больные РМЖ после установления диагноза получают курс предоперационной ЛТ на МЖ и зоны регионарного метастазирования.
2. Послеоперационную. Больные, перенесшие удаление опухоли и подмышечных лимфоузлов и не прошедшие курс предоперационной ЛТ, должны получать заключительную ЛТ на область МЖ лимфатических узлов (при обнаружении в них метастазов).
3. Облигатная послеоперационная. Больные РМЖ должны получать послеоперационное облучение при наличии любого из нижеперечисленных факторов риска:
4. Больные с высоким риском отдаленного метастазирования могут получать ЛТ до завершения адъювантной химиотерапии, либо ее можно проводить совместно с облучением. Послеоперационное облучение подмышечной впадины повышает риск отека верхней конечности.
Адъювантная химиотерапия. При высоком риске рецидивирования, что определяется при исследовании специфических маркеров, проводится даже при 1-й стадии заболевания. Замедляет или предупреждает рецидивирование, улучшает выживаемость больных с метастазами в подмышечные лимфоузлы, а также у части больных без подмышечных метастазов. Химиотерапия наиболее эффективна у пациенток в пременопаузе с метастазами в подмышечные лимфоузлы (наблюдают снижение 5-летней летальности на 30 %). Комбинированная химиотерапия предпочтительней монотерапии, особенно в группе больных с метастатическим РМЖ. Прием препаратов шестью курсами в течение шести месяцев — оптимальный по эффективности и по длительности метод лечения.
Схемы введения препаратов:
1. Метотрексат, циклофосфамид, 5-фторурацил.
2. Больные с высоким риском развития рецидива могут получать циклофосфамид, доксорубицин и 5-фторурацил. Эффект терапии больных с метастатическим РМЖ составляет 65–80 %.
3. Альтернативные схемы для больных с метастазирующим раком включают доксорубицин, тиоТЭФ и винбластин; высокие дозы циспластина; митомицин; внутривенные инфузии винбластина или 5-фторурацил; циклофосфамид, метотрексат и 5-фторурацил; таксол.
Использование внутрилимфатического введения химиопрепаратов, разработанного в нашем центре, позволило проводить химиотерапию в режиме непрерывной длительной внутрилимфатической инфузии, что обеспечило возможность повышения терапевтической концентрации препарата в крови при одновременном снижении частоты токсических осложнений, улучшая как непосредственные, так и отдаленные результаты лечения больных.
В 1994 году разработан и внедрен способ лечения РМЖ [8], включающий проведение адъювантной регионарной полихимиотерапии (ПХТ) в бассейне внутренней грудной артерии, который позволил уменьшить объем операции до функционально щадящей даже при местнораспространенном РМЖ (Т3–4 N1–2 M0). Активное внедрение регионарной неоадъювантной полихимиотерапии в лечении местнораспространенного первично-неоперабельного РМЖ позволило нам добиться стабилизации процесса, частичной и полного регрессирования опухоли у 84,7 % пролеченных больных, что дало возможность перевести их в операбельное состояние и выполнить радикальную мастэктомию. Катетеризацию подключичной артерии с целью проведения регионарной полихимиотерапии мы осуществляем как через ее ветви (торакоакромиальная артерия, внутренняя грудная артерия), так и через ветви плечевой артерии (глубокая артерия плеча, мышечная ветвь плечевой артерии). Концентрация химиопрепарата в опухоли при внутриартериальном введении увеличивается в два раза, а в ткани лимфатических узлов в 1,5 раза по сравнению с внутривенным введением. Во всех случаях катетеризации сосудов интраоперационно производится хроматоангиоскопический контроль правильности установки катетера. Курс внутриартериальной ПХТ начинают со второго дня после операции. Внутриартериальная ПХТ проводится по модифицированной нами схеме CMF [8, 9, 11]. Комплексное лечение больных предполагает проведение до четырех последовательных курсов селективной внутриартериальной полихимиотерапии. По данным ДОПЦ, наиболее оптимальным является введение химиопрепаратов по принципу: «один день — один препарат». При этом ежедневно в режиме непрерывной длительной инфузии с использованием дозаторов лекарственных веществ вводится 1/3 курсовой дозы каждого препарата. Длительность каждого курса составляет девять суток. Интервалы между курсами внутриартериальной полихимиотерапии составляют 3 недели.
Преимущества этого метода основаны на длительности контакта между опухолевой тканью и химиопрепаратом, при резком снижении химиотоксического действия. Также достоинством данного способа катетеризации, обеспечивающего максимальную терапевтическую концентрацию химиопрепарата в органе-мишени и в зонах регионарного метастазирования, парастернального и средостенного лимфатического коллекторов, является возможность проведения повторных курсов полихимиотерапии при отсутствии тромботических осложнений. Ближайшие и отдаленные результаты: исследования, проведенные на базе ДОПЦ, показали, что использование режима непрерывной длительной инфузии химиопрепаратов в бассейне внутренней грудной артерии у подавляющего большинства больных с запущенными формами РМЖ позволило увеличить сроки безрецидивного периода и повысить среднюю продолжительность жизни до 4,52 ± 0,60 года.
Гормонотерапия является неотъемлемой частью комплексной терапии больных РМЖ, исторически это один из относительно «молодых» методов лечения. Претерпевала различные изменения от 100% овариэктомий и адреналэктомий до почти полного забвения. В настоящий момент используется с учетом чувствительности опухоли к рецепторам стероидных гормонов.
Адъювантная гормональная терапия:
1. Подавление функций яичников облучением или овариэктомией приводит к неоднозначным результатам; в отдельных подгруппах больных отмечают продолжительные периоды улучшения состояния.
2. Гормональное лечение. Позитивный ответ на гормональную терапию вероятен при следующих условиях: длительный период без метастазирования (более 5 лет), пожилой возраст, наличие метастазов в костях, региональные метастазы и минимальные метастазы в легких, гистологически подтвержденная злокачественность 1-й и 2-й степени, длительная ремиссия в результате предшествующей гормонотерапии. Антагонист эстрогенов тамоксифен задерживает наступление рецидивов, улучшает выживаемость и предпочтительнее для больных в постменопаузе с ЭРц-позитивной опухолью. Эффективность тамоксифена более выражена у больных с ЭРц-позитивными опухолями. Препарат неэффективен либо оказывает слабое воздействие на ЭРц-негативные опухоли.
Гормональное лечение метастазирующего РМЖ
1. Гормональное лечение применяют у больных с подкожными метастазами, вовлечением в процесс лимфоузлов, наличием плеврального выпота, метастазами в кости и нелимфогенными легочными метастазами. Больным с метастазами в печень, лимфогенными метастазами в легкие, перикард и другими опасными для жизни метастазами следует проводить химиотерапию.
2. Больные с ЭРц-позитивными первичными опухолями положительно реагируют на гормональное лечение по меньшей мере в 30 % случаев. Наличие в опухоли одновременно эстрогеновых и прогестероновых рецепторов повышает лечебный эффект до 75 %.
3. Больные с неизвестным статусом гормональных рецепторов в опухолях могут реагировать на лечение гормонами при хорошо дифференцированных опухолях или при наличии интервала в 1–2 года между появлением первичной опухоли МЖ и развитием метастазов.
Следует отметить некоторые особенности применения различных видов гормонотерапии:
Качество жизни больных
Вполне естественно, что качество жизни больных РМЖ напрямую зависит от объема проведенных оперативных вмешательств и стадийности процесса. С внедрением в клиническую практику органосохраняющих операций и регионарной химиотерапии качество жизни больных существенно улучшилось. Для улучшения качества жизни больных и достижения эстетического эффекта нами разработан и внедрен в клиническую практику вариант выполнения подкожной мастэктомии с одномоментным эндопротезированием при начальных формах РМЖ.
Основные принципы хирургической, медицинской и социальной реабилитации
Сохранение МЖ, пораженной раковой опухолью, представляется в идеале тем способом лечения, который не подвергает заболевшую двойному шоку — психологическому коллапсу, обусловленному утратой женственности и утратой надежды на сохранение привычного образа жизни. Длительная клиническая практика убеждает, что инстинкт сохранения женственности у значительной части заболевших выше инстинкта самосохранения. В ряде стран введена система психосоциальной адаптации женщин, подвергшихся операциям на МЖ. Такая система включает в себя несколько этапов: внутрибольничная реабилитация, индивидуальные посещения психолога, посещение специальных клубов и пансионов, изготовление и ношение одежды, позволяющей скрыть косметические дефекты и др. В настоящий момент в маммологическом отделе ДОПЦ с больными РМЖ работает психолог, который проводит самостоятельные беседы и участвует в беседах лечащих врачей с больными. По словам больных, сам факт внимания врачей к данной проблеме вселяет веру в выздоровление и помогает наладить правильные взаимоотношения пациентки и врача.
Диспансеризация
Каждый онкологический больной подлежит диспансеризации. За каждым больным РМЖ ведется диспансерное наблюдение, для чего на каждого больного заводится контрольная карта, в которой регистрируются данные методов диагностики, диагноз, проведенное и планируемое лечение, эффективность лечения, данные контрольных осмотров и даты предстоящих осмотров. С 1995 года внедряются компьютеризированные методы диспансеризации и учета больных в маммологическом отделе ДОПЦ, что позволяет значительно сокращать время нахождения данных и оптимизировать сбор информации.
1. Справочник по онкологии / Под ред. Б.Е. Петерсона. — Москва, 1987.
2. Трапезников Н.Н., Летягин В.П., Алиев Д.А. Лечение опухолей молочной железы. — Москва, 1989.
3. Петерсон Б.Е. Хирургическое лечение злокачественных опухолей. — Москва, 1986.
4. Сидоренко Л.Н. Гормонотерапия предрака и рака молочной железы. — Москва, 1998.
5. Практическая онкология: Избранные лекции / Под ред. С.А. Тюляндина и В.М. Моисеенко. — Санкт-Петербург, 2004.
6. Способ радикальной мастэктомии. А.С. СССР №
7. Спосіб радикальної мастектомії. Патент України № 15002А, М.кл. А61В17/00, опуб. бюл. «Промислова власність» № 3. 30.06 1997, автори Г.В. Бондар, М.М. Шепляков, Ю.І. Яковець, В.М. Смирнов, І.Є. Сєдаков.
8. Спосіб лікування раку молочної залози. Патент України № 15003 А, А61В17/00, опуб. Бюл. «Промислова власність» № 3, 30.06.1997, автори Г.В. Бондар, І.Є. Седаков, І.І. Максименко.
9. Спосіб лікування раку молочної залози. Рішення про видачу патенту України від 19.06.98 за заявкою №
10. Спосіб лікування раку молочної залози. Решение о выдаче патента Украины от 19.06.98 по заявке №
11. Спосіб лікування раку молочної залози. Патент Украины № 17135, опуб. бюл. «Промислова власність» № 2 от 30.04.97, авт. Яковец Ю.И., Седаков И.Е.
12. Ariel I., Cleary J. Breast cancer. Diagnosis and treatment. —
13. Bland K.I., Copeland E.M. The Breast. —
