Газета «Новости медицины и фармации» Гастроэнтерология (304) 2009 (тематический номер)
Вернуться к номеру
Целиакия: современные аспекты проблемы
Авторы: Ю.В. Линевский, д.м.н., профессор, К.Ю. Линевская, к.м.н., доцент, К.А. Воронин, Донецкий национальный медицинский университет им. М. Горького, кафедра внутренней медицины им. А.Я. Губергрица и кафедра внутренней медицины № 2
Версия для печати
Целиакия — заболевание иммунной природы у лиц с генетически обусловленной (у носителей HLA DQ2 и DQ8) повышенной чувствительностью к различным пищевым белкам (глютену злаковых, сое, мясу тунца и др.), характеризующееся образованием в лимфоидной ткани слизистой оболочки тонкой кишки антител к соответствующим пищевым и/или ее тканевым антигенам (эндомизию, тканевой трансглутаминазе, ретикулину и др.). Различают глютенчувствительную целиакию (ГЦ) и другие редко встречающиеся формы целиакии (соевая, коллагеновая, неклассифицируемая, гипогаммаглобулинемическая).
Клиническую картину заболевания под названием Diathesis coeliacus или Morbus coeliacus описали в I столетии новой эры Aretaios Kappadozien и Aurelian. В последующем эту патологию именовали «интестинальным инфантилизмом» (Ch.A. Herther, 1908) и «идиопатической стеатореей» (Т.Е. Тайзен, 1932).
В.К. Дик (1950) впервые связал причину заболевания у детей с употреблением хлеба. Положительный эффект от исключения из пищевого рациона хлебных злаков (G. Mc. Iver, J. French, 1952) и утверждение W. Dicke, H.A. Weijers и J.H.van de Kamer (1953) о связи заболевания с глютеном (растворимой в алкоголе фракцией белка пшеницы) послужило основанием для названия указанной патологии «глютенчувствительной целиакией», «глютеновой энтеропатией» или «глютеновой болезнью».
Внешнее сходство этого заболевания с тропической спру, но отсутствие при последней эффекта от исключения из рациона продуктов из злаковых дало основание именовать настоящую патологию «нетропическим спру».
Отсутствие эффекта от исключения из рациона продуктов из злаковых у ряда больных с клиническими признаками целиакии (рефрактерная целиакия или спру) привело к выделению в дальнейшем прочих разновидностей целиакии, обусловленных непереносимостью других продуктов, содержащих белок (соя, мясо индейки, тунец и др.). Таким образом, целиакия без установления причины является синдромом. При исключении известных по этиологии разновидностей целиакии ее принято обозначать как неклассифицируемую целиакию. Выделены коллагеновая и гипогаммаглобулинемическая целиакия (спру).
По данным Всемирной гастроэнтерологической ассоциации (WGO) и Всемирной организации дигестивной эндоскопии (ОМЕD), целиакия встречается не менее чем у 1 % населения (2005) с ежегодным увеличением заболеваемости [8].
В повседневной лечебной практике в основном диагностируются относительно редко встречающиеся случаи целиакии, протекающие с синдромом нарушенного всасывания (СНВ). Ежегодно типичная целиакия, подтвержденная биопсией, устанавливается у 2–13 человек на 100 000 взрослого населения. Несравненно чаще имеют место случаи целиакии, протекающие без симптомов мальабсорбции, но с аутоиммунными проявлениями или малосимптомные. Эти разновидности заболевания диагностируются относительно редко, что создает обманчивое впечатление о целиакии как редкой патологии. В Европе на один случай выявленной целиакии встречаются 7–10 невыявленных. Подтверждением роли генетических факторов в развитии ГЦ является ее частота у близких родственников около 1 : 10, тогда как в общей популяции частота манифестных типичных форм заболевания варьирует от 1 : 1000 до 1 : 6000 населения [6].
Этиология и патогенез
Наследование происходит по ауто-сомно-доминантному типу с неполной пенетрантностью. Эта патология не-обязательно наблюдается у обоих монозиготных близнецов. Конкордантность наблюдается в 70–78 % [8].
Обнаружен короткий (33-mer) пептид, входящий в состав глютена, который, по-видимому, повреждает щеточную кайму мембран эпителия тонкой кишки с развитием воспалительной реакции желудка и поджелудочной железы [17]. Этот пептид индуцирует синтез Т-клеток.
Повреждение слизистой оболочки тонкой кишки характеризуется у многих больных развитием атрофии ее ворсин и компенсаторной гиперплазии крипт. При распространенном поражении тонкой кишки — выраженной атрофии ворсин — развивается СНВ. Образование аутоантител к компонентам поврежденной слизистой тонкой кишки и может быть причиной внекишечных проявлений заболевания. Они во многих случаях могут доминировать в клинической картине заболевания, когда симптомы поражения тонкой кишки выражены слабо или вообще отсутствуют. Этим объясняется возможность манифестации ГЦ в виде атипичных форм (железодефицитная анемия, бесплодие, инсулинзависимый диабет, остеопороз и др.), когда структура ворсин слизистой оболочки тонкой кишки может оставаться практически нормальной. При этом единственным признаком заболевания может быть только качественное и количественное изменение межэпителиальных лимфоцитов (МЭЛ) в поверхностном эпителии [11, 13]. Именно им принадлежит важная роль в распознавании пептидов глиадина.
Лимфоциты вызывают пролиферацию и дифференцировку плазматических клеток, продуцирующих антитела к глиадину (АГА). Взаимодействие глиадина с тканевой трансглутаминазой ведет к образованию антител к последней (АТТГ). Развитие местной иммунной реакции в слизистой оболочке тонкой кишки сопровождается увеличением продукции α-интерферона, провоспалительных цитокинов, ФНО-α, которые повреждают кишечный эпителий [14, 16].
В числе инициаторов клеточного иммунного ответа, аналогичного воздействию глютена, может быть аденовирус серотипа 14, имеющий сходную с пептидами глиадина последовательность аминокислот [12].
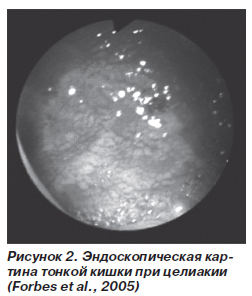
Таким образом, ГЦ развивается в результате иммунного ответа на глиадин в лимфоидной ткани слизистой оболочки тонкой кишки, обусловленного генетическим дефектом (наличие HLA-DQ2 и -DQ8). Однако лишь у небольшой части больных формируется классическая гиперрегенераторная атрофия слизистой оболочки тонкой кишки с СНВ. У большинства больных изменения в слизистой оболочке затрагивают ограниченный участок тонкой (двенадцатиперстной) кишки или наблюдаются незначительные изменения (углубление крипт и/или увеличение количества МЭЛ).
Патоморфология в зависимости от выраженности чувствительности к глютену может варьировать от минимальной, характеризующейся увеличением количества МЭЛ, особенно в криптах, до выявления прочих классических признаков в виде атрофии ворсин с наличием глубоких крипт в слизистой оболочке тонкой (двенадцатиперстной) кишки (гиперрегенераторная атрофия). Отмечается снижение высоты энтероцитов и лимфоплазмоцитарная инфильтрация собственной пластинки слизистой оболочки. Количество бокаловидных энтероцитов уменьшено. Возможно выявление увеличенного количества эозинофилов и тучных клеток. В собственной пластинке нередко выявляется интерстициальный фиброз.
Клиника
Характер и выраженность клинических проявлений ГЦ определяет степень чувствительности слизистой оболочки тонкой кишки к глютену и выраженности иммунной реакции с образованием антител к глиадину, эндомизию, ретикулину и тканевой трансглутаминазе.
В результате повреждения слизистой оболочки тонкой кишки могут развиваться синдромы нарушенного переваривания и всасывания пищи. Возможна манифестация заболевания внекишечной аутоиммунной патологией.
Развитие синдрома нарушенного переваривания связано как со снижением продукции кишечных ферментов атрофированной слизистой оболочкой тонкой кишки, так и со снижением внешнесекреторной функции поджелудочной железы и сократительной функцией желчного пузыря за счет угнетения выработки холецистокинина-панкреозимина атрофированной слизистой двенадцатиперстной и тощей кишки.
Уменьшение содержания в проксимальных отделах тонкой кишки доли конъюгированных желчных кислот и увеличение свободных желчных кислот способствует формированию синдрома ее избыточного бактериального обсеменения.
Клинические проявления, связанные с поражением слизистой оболочки тонкой кишки, характеризуются признаками, свойственными синдрому нарушенного переваривания пищи. В их числе потеря массы тела, поносы с полифекалией, замазкообразным или жидким с гнилостным запахом, светлым, пенистым калом с остатками непереваренной пищи, которые выявляются визуально (лиентерея) и/или при микроскопическом исследовании кала (нейтральный жир, непереваренные мышечные волокна, зерна крахмала), метеоризм, урчание в животе. Отмечаются признаки плохой переносимости лактозы, характеризующиеся усилением метеоризма, урчания в животе, диареей после употребления молока, увеличением содержания водорода в выдыхаемом воздухе после нагрузки лактозой. Метеоризм может быть следствием избыточного бактериального обсеменения тонкой кишки, о чем свидетельствует увеличение содержания водорода в выдыхаемом воздухе натощак (> 15 ppm).
В числе признаков синдрома нарушенного всасывания пищи, помимо потери массы тела, — различной степени выраженности слабость, снижение трудоспособности, многочисленные гиповитаминозные проявления и трофические нарушения. Трофические нарушения характеризуются потерей тургора, сухостью и шелушением кожи, изменением формы, истончением, расслоением, поперечной исчерченностью и ломкостью ногтей, гипопротеинемическими отеками на стопах и голенях, развивается остеопороз. При выраженном дефиците кальция могут наблюдаться судороги. В числе возможных гиповитаминозных проявлений ангулярный хейлит, глоссит (язык малиново-красный со сглаженными сосочками), снижение сумеречного зрения, гингивит, кровоточивость десен, парестезии, себорейный дерматит или пеллагроидная (грязновато-коричневая) окраска кожных покровов, особенно в области физиологических складок, астения, признаки эндокринной недостаточности (полиурия, никтурия, полидипсия, признаки гипотиреоза, гипотония, импотенция, аменорея).
Может наблюдаться бледность кожных покровов и головокружение на почве анемии в связи с нарушенным всасыванием железа (микроцитарная, гипохромная), витамина В12 и фолиевой кислоты (макроцитарная, мегалобластная, гиперхромная). Особенностью железодефицитной анемии при ГЦ является резистентность к терапии препаратами железа.
У больных ГЦ часто выявляется оксалурия.
При манифестации заболевания в детском возрасте могут отмечаться признаки отставания в физическом и умственном развитии.
Живот увеличен в размере, часто распластан («лягушачий»). При пальпации выявляется болезненность в околопупочной области, урчание и плеск в слепой кишке и по всей ободочной кишке.
Следует отметить частую полиорганность поражения пищеварительной системы при ГЦ. Она выражается в сопутствующем лимфоцитарном гастрите, который отличается от классического лимфоцитарного гастрита отсутствием макроскопических признаков в виде узелков, утолщения складок и эрозий, часто сопровождается ГЭРБ, лимфоцитарным колитом. Хотя прямая связь последнего с повышенной чувствительностью к глютену не подтверждена серологическими исследованиями [4]. У больных ГЦ в связи с гиперпродукцией гастрина и повышенной кислотообразующей функцией желудка имеется риск развития язвенной болезни.
Установлена возможность поражения печени по типу стеатоза, стеатогепатита и даже цирроза у больных ГЦ [18].
У лиц с ГЦ возможно наличие иммуноассоциированных болезней (сахарного диабета 1-го типа, аутоиммунного гепатита, аутоиммунного тиреоидита, первичного билиарного цирроза печени и др.) и генетически ассоциированных болезней (герпетиформного дерматита Дюринга, рецидивирующего афтозного стоматита, гипогаммаглобулинемии и др.). Поэтому ГЦ может длительно протекать под маской различных аутоиммунных заболеваний.
Таким образом, ГЦ — многоликое заболевание, что объясняется разной чувствительностью больных к глиадину, выраженностью иммунной реакции, протяженностью и степенью поражения тонкой кишки.
Диагностика ГЦ базируется на обнаружении увеличения содержания в крови антител к α-глиадину (α-АГА), эндомизию (АЭМА), ретикулину (АРА) и тканевой трансглутаминазе (АТТГ) в классах ИГА и ИГG. ИГА является ранней реакцией иммунокомпетентных клеток слизистой оболочки тонкой кишки на антиген. Антитела класса ИГG образуются позже, после формирования иммунного ответа и сохраняются длительное время. К последнему тесту следует прибегать у лиц с селективным дефицитом ИГА.
По данным отдела патологии тонкой кишки ЦНИИ гастроэнтерологии (Москва), специфичность определения ИГА α-АГА, АРА и АЭМА составляет соответственно 84,6; 94,2 и 98,1 %, а чувствительность — 90,6; 87,5 и 100 % [4]. Таким образом, наиболее чувствительным и специфичным оказалось определение антител к эндомизию. В пользу ГЦ могут свидетельствовать значения исследования в крови ИГА АГА > 15 МЕ/мл, АТТГ > 8 МЕ/мл, АРА АЭМА ≥ 1 : 40.
По данным О.Ю. Губской [1], наибольшую ценность в серодиагностике ГЦ имеет комплексное иммуноферментное определение антител к дезаминированным пептидам глиадина и человеческой тканевой трансглутаминазе (ДПГ/чТТГ), чувствительность к которой составляла 100 %. Чувствительность к АТТП составляла 86,7 %. Наименее чувствительным оказалось определение АГА (70 %).
Тесты с определением АЭМА и АТТГ считаются строго специфичными для ГЦ.
Вместе с тем окончательный диагноз ГЦ должен быть подтвержден гистологическим исследованием биоптатов слизистой тонкой (двенадцатиперстной) кишки [7]. Это исследование является золотым стандартом в диагностике ГЦ.
В 1992 году M.N. Marsh предложил классификацию по стадиям (степени) патоморфологических изменений в слизистой оболочке тощей (двенадцатиперстной) кишки, которую следует использовать при оценке гистологических препаратов ее биоптатов [15]. При этом следует особо отметить важность правильной ориентации биоптатов при изготовлении гистологических препаратов (должна быть выполнена вертикальная ориентация ворсин к срезу с помощью бинокулярной лупы или стереоскопического микроскопа). Тангенциальные срезы не позволяют дать им правильную оценку.
Возможно проведение генетического тестирования на выявление HLA-DQ2 и -DQ8, которые оказались весьма специфичными в диагностике ГЦ. Однако почти у 30 % населения имеются DQ2 гаплотипы [15]. Поэтому типирование на HLA-DQ2 и -DQ8 малоспецифично [10].
Для оценки всасывательной функции тонкой кишки могут использоваться абсорбционные тесты.
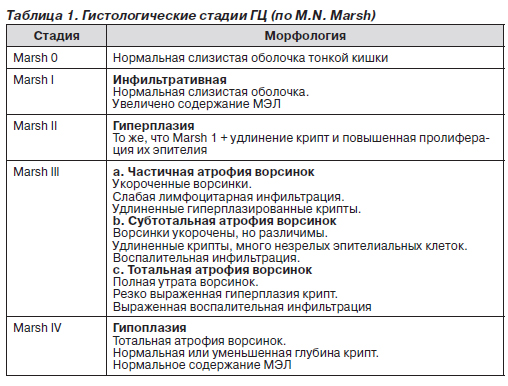
Заслуживает внимания алгоритм диагностики ГЦ [3].
Дифференциальная диагностика ГЦ должна проводиться с другими формами целиакии (соевая, неклассифицируемая, коллагеновая, гипогаммаглобулинемическая), при которых наблюдаются клинические проявления, подобные ГЦ. Однако при этом отсутствует эффект от аглютеновой диеты (АГД), в крови не выявляются АГА.
При соевой целиакии отмечается регрессия клинических проявлений и морфологических изменений слизистой оболочки тонкой кишки при длительном исключении из пищевого рациона продуктов, содержащих сою.
В случае неклассифицируемой целиакии (спру) возможно улучшение состояния больных и обратное развитие морфологических изменений в слизистой оболочке тонкой кишки при длительном исключении из рациона некоторых белковых продуктов (куриные яйца, куриное мясо, тунец). Может отмечаться положительный эффект от лечения глюкокортикоидами или иммуносупрессантами (азатиоприн, циклоспорин).
При коллагеновой целиакии (спру) в биоптатах слизистой оболочки тонкой кишки под базальной мембраной эпителиоцитов обнаруживается разрастание коллагеновой ткани. Рентгеновское исследование тонкой кишки может выявлять узловую лимфоидную гиперплазию на почве вторичного иммунодефицита.
При гипогаммаглобулинемической целиакии (спру) отмечается снижение содержания в сыворотке крови иммуноглобулинов, особенно ИГА, выражен синдром избыточного бактериального обсеменения тонкой кишки, в биоптатах ее слизистой оболочки резко снижено количество плазматических клеток, собственная пластинка слизистой обильно инфильтрирована лимфоцитами. Она образует скопления в виде лимфатических фолликулов. В связи со снижением иммунитета у больных часто имеются множественные инфекции.
Помимо рефрактерной ГЦ, отсутствие эффекта от лечения может быть обусловлено с наличием сопутствующих заболеваний (непереносимость лактозы, чрезмерный бактериальный рост в тонкой кишке, микроскопический колит, панкреатическая недостаточность), энтеропатиями, связанными с Т-клеточной лимфомой, недостаточным исключением из рациона глютенсодержащих продуктов.
Классификация ГЦ
Предложено различать типичную, латентную, рефрактерную, атипичную и бессимптомную формы ГЦ [5].
Типичная форма характеризуется развитием в раннем детском возрасте при переводе детей на специальное питание, содержащее глютен.
Латентная форма проявляется в зрелом возрасте. До этого ГЦ протекает субклинически (отставание в физическом развитии, анемия, признаки гиповитаминоза).
Рефрактерная (торпидная) форма характеризуется тяжелым течением и отсутствием эффекта от обычного лечения. Ремиссия возможна лишь при использовании глюкокортикоидных препаратов.
 Атипичная форма верифицируется преобладанием в клинической картине внекишечной симптоматики, обусловленной иммунными нарушениями (аутоиммунный тиреоидит, миокардит, сахарный диабет 1-го типа, первичный билиарный цирроз печени, аутоиммунный гепатит, синдром Шегрена, ревматоидный артрит, васкулит, фиброзирующий альвеолит, нейропатия, полимиозит и др.) или СНВ (геморрагии, анемия, остеопороз, отеки, маленький рост, задержка полового развития, артралгии, дефекты зубной эмали, облысение, депрессия, бесплодие и др.).
Атипичная форма верифицируется преобладанием в клинической картине внекишечной симптоматики, обусловленной иммунными нарушениями (аутоиммунный тиреоидит, миокардит, сахарный диабет 1-го типа, первичный билиарный цирроз печени, аутоиммунный гепатит, синдром Шегрена, ревматоидный артрит, васкулит, фиброзирующий альвеолит, нейропатия, полимиозит и др.) или СНВ (геморрагии, анемия, остеопороз, отеки, маленький рост, задержка полового развития, артралгии, дефекты зубной эмали, облысение, депрессия, бесплодие и др.).
Бессимптомная форма характеризуется отсутствием клинических проявлений и выявляется с учетом отдельных отклонений, свойственных ГЦ, при целенаправленном использовании соответствующих иммунных тестов и гистологическом исследовании биоптатов слизистой оболочки тонкой (двенадцатиперстной) кишки в группах риска (у лиц с аутоиммунными болезнями, ассоциированными с ГЦ, и генетически связанными с ГЦ заболеваниями). К ним относятся больные железодефицитной анемией, сахарным диабетом 1-го типа, лица с отставанием в физическом и психическом развитии, страдающие рецидивирующим афтозным стоматитом, дефектами зубной эмали, бесплодием, невынашиванием беременности, остеопорозом, герпетиформным гепатитом Дюринга, гипогаммаглобулинемией, деменцией, синдромом Дауна, периферической нейропатией, депрессией, аутизмом, шизофренией, близкие родственники больных ГЦ и др. Большинство больных ГЦ имеют именно эту форму заболевания. В целом скрытая и другие атипичные формы ГЦ встречаются приблизительно в 10 раз чаще типичной формы ГЦ.
 Осложнения ГЦ: метаболические нарушения в виде динамической (паралитической) кишечной непроходимости на почве гипокалиемии и метаболической кардиомиопатии, эрозивно-язвенный дуоденит с возможным развитием перфораций, кровотечений, септицемия (энтерогенный сепсис), злокачественные образования тонкой кишки (лимфома, аденокарцинома и др.).
Осложнения ГЦ: метаболические нарушения в виде динамической (паралитической) кишечной непроходимости на почве гипокалиемии и метаболической кардиомиопатии, эрозивно-язвенный дуоденит с возможным развитием перфораций, кровотечений, септицемия (энтерогенный сепсис), злокачественные образования тонкой кишки (лимфома, аденокарцинома и др.).
Лечение
Основным лечением является строгая пожизненная АГД. Из рациона необходимо исключить продукты, содержащие глютен. В их числе пшеница, рожь, ячмень, овес (часто загрязнен глютеном), полба, камут, спельта, трикаль, продукты и блюда, приготовленные с использованием соответствующих компонентов (крупа, мука и др.): все виды макаронных изделий, выпечки, хлопья, мюсли, овощи в кляре или панированные в муке, йогурт с солодом, злаками, мясо и рыба, панированные в муке или приготовленные с соусами, содержащими муку, сельдь маринованная, хлебный квас, растворимый и суррогатный кофе с примесью ячменя или ячменного солода, соус бешамель.
Разрешаются продукты, не содержащие глютен: рис, кукуруза, пшено, гречка, каштаны, молоко и молочные продукты (творог, кефир, натуральный йогурт, сыры), мясо, рыба и рыбные консервы в собственном соку, крабы, креветки, устрицы без соусов и пряностей, яйца, овощи и фрукты, орехи, консервированные и свежие бобовые (горох, фасоль, бобы, чечевица, соя), газированные напитки (кока-кола, фанта и др.), фруктовые соки и нектары, листовой чай, кофе в зернах, алкогольные напитки (вино белое, красное, розовое, игристое, сухое, коньяк, бренди, ром, джин, текила, кальвадос), мед, сахар, мармелад, фруктоза, растительные масла и маргарин, сливочное масло, свиное сало, уксус, соль, перец сладкий, пряности.
Приводим характеристику АГД, разработанную в конце 70-х годов ХХ в. в Центральном научно-исследовательском институте гастроэнтерологии (Москва) проф. Н.И. Екисениной [2].
В диете соблюдается принцип механического и химического щажения желудочно-кишечного тракта, исключаются продукты и блюда, увеличивающие бродильные процессы. Ограничиваются вещества, стимулирующие секрецию желудка, поджелудочной железы, продукты, неблагоприятно влияющие на функциональное состояние печени. Диета также является гиполактозной.
Кулинарная обработка. Все блюда готовят на пару или варят. В зависимости от функционального состояния кишечника пища дается в протертом виде (в периоды поносов) или без специального измельчения (при нормализации стула).
Химический состав и энергетическая ценность. Белков
Перечень рекомендуемых блюд. Можно употреблять хлебобулочные изделия и блюда из рисовой, кукурузной и гречневой муки (печенье, оладьи, блины, лепешки, рисовые и кукурузные хлопья). При невозможности их получения количество углеводов в диете обеспечивают за счет блюд из круп (гречневая, рисовая, кукурузная), сахара, а в периоды ремиссии заболевания также фруктов (вареных или сырых, в зависимости от переносимости).
Супы. На слабом мясном или рыбном бульоне с мясными или рыбными фрикадельками, кнелями, яичными хлопьями, рисом, мелко нашинкованными овощами (картофель, морковь, цветная капуста, кабачки, тыква).
Блюда из мяса и рыбы. Нежирные сорта мяса и рыбы, птицы без кожи (говядина, крольчатина, курятина, мясо индейки, лещ, треска, хек, ледяная рыба, карп, путассу, минтай и др.) в отварном виде или паровые, нежные сорта мяса, птица — куском, рубленая говядина без хлеба или с добавлением сваренного до полуготовности риса.
Блюда и гарниры из овощей. Овощные пюре из картофеля, моркови, кабачков, тыквы, отварная цветная капуста.
Блюда и гарниры из круп. Каши на воде с добавлением 1/3 молока, протертые (гречневая, рисовая, кукурузная). Пудинги паровые из перечисленных круп.
Блюда из яиц. Омлеты паровые.
 Сладкие блюда, сладости, фрукты, ягоды. Кисели, желе, муссы, протертые компоты из сладких сортов ягод и фруктов (яблоки, груши, малина, черника, земляника, клубника, черемуха, айва), печеные яблоки и груши. Варенье и джемы из перечисленных выше ягод и фруктов. Снежки, меренги. Сахар.
Сладкие блюда, сладости, фрукты, ягоды. Кисели, желе, муссы, протертые компоты из сладких сортов ягод и фруктов (яблоки, груши, малина, черника, земляника, клубника, черемуха, айва), печеные яблоки и груши. Варенье и джемы из перечисленных выше ягод и фруктов. Снежки, меренги. Сахар.
Молоко, молочные продукты и блюда из них. Творог некислый, свежий в натуральном виде и в блюдах: паровые пудинги с крупами и овощами, перечисленными выше, творожные пудинги с добавлением рисовой муки вместо пшеничной. При хорошей переносимости кефир, простокваша, молоко и сливки с чаем в небольшом количестве (
Соусы. Молочный соус, приготовленный на рисовой муке, фруктовые соусы.
Напитки. Чай, отвар шиповника, сладкие фруктовые и ягодные соки пополам с горячей водой.
Жиры. Масло сливочное добавлять в готовые блюда, всего до
Закуски. Сыр неострый, заливные рыба, мясо, птица, язык отварной, вымоченная сельдь (1 раз в неделю).
Во многих странах на упаковке продуктов риска присутствует маркировка об отсутствии глютена — международный логотип, принятый Европейским союзом, в виде перечеркнутого колоса, производятся специальные безглютеновые продукты (хлеб, макаронные изделия и др.).
Продукты риска, которые можно употреблять лишь после проверки на отсутствие глютена: готовые супы, колбасные изделия, сладости, мороженое, крахмал, сироп глюкозы и солод, картофельные чипсы, картофельное пюре быстрого приготовления, попкорн, каша из кукурузной муки, цукаты, готовые овощные блюда, готовые молочные напитки, фруктовый йогурт, взбитые сливки, кремы и пудинги, плавленый сыр, сыр с плесенью, молочные продукты с пониженным содержанием жира, готовые мясные и рыбные блюда, соусы, консервы с соусами, фруктовые соки с мякотью, ликеры, сахарная пудра, джем, плиточный шоколад, готовые смеси для коктейлей, горячего шоколада, кофе, шоколадные конфеты и шоколадный крем, какао-порошок, карамель, искусственные подсластители (порошок, таблетки, жидкость), готовые соусы, бульонные кубики, пряное масло, разрыхлитель теста, глазури, желатин, жевательные резинки.
При тяжелой белковой недостаточности показано парентеральное введение белковых препаратов (плазма, альбумин и др.) и смесей аминокислот (аминосол, аминоплазмаль, гидролизат казеина и др.). Использование последнего целесообразно дополнять назначением анаболических стероидных препаратов (феноболил, ретаболил и др.), способствующих синтезу белка. Возможно внутривенное введение жировых эмульсий (липофундин и др.).
При водно-электролитных нарушениях вводят внутривенно панангин (20 мл) и глюконат кальция (10 мл 10% р-ра), разведенный в 250 мл 5% глюкозы. При метаболическом ацидозе показано дополнительное внутривенное введение бикарбоната натрия и сернокислой магнезии, а при метаболическом алкалозе — хлористого кальция, хлористого калия и сернокислой магнезии.
Целесообразно использование витаминов группы А, В, D, Е, К, никотиновой кислоты, преимущественно парентерально.
Для подавления аутоиммунных механизмов важно использовать глюкокортикоидные препараты (преднизолон, метилпреднизолон и др.). Они способствуют быстрому наступлению ремиссии.
С целью купирования диареи уместно использование вяжущих (отвар коры дуба, корня лапчатки, корки граната, ольховых шишек, ягод черники и др.), обволакивающих и адсорбирующих средств (смекта, дерматол, неоинтестопан, полипефан и др.), а также средств, подавляющих моторику кишечника (лоперамид, имодиум).
Для устранения избыточного бактериального роста в кишечнике показаны антисептики (интетрикс, энтерофурил, фуразолидон, бисептол и др.), пробиотики (бактисубтил, энтерожермина, энтерол 250, лациум, линекс, бифиформ, биогая, лацидофил, лактовит форте
Для устранения метеоризма используются ветрогонные средства (отвар семян укропа) и пеногасители (эспумизан).
Возможно использование препаратов, содержащих комбинацию веществ, тормозящих перистальтику кишечника, и пеногасителей (метеоспазмил, лофлатил и др.).
Улучшению переваривания пищи способствуют препараты, содержащие пищеварительные ферменты (креон, панзинорм и др.).
1. Губская О.Ю. Целіакія: поширеність, особливості клінічного перебігу, діагностика, лікування та одужання хворих: Автореф. дис… д-ра мед. наук. — Київ, 2009. — 31 с.
2. Екисенина Н.И. Лечебное питание при заболеваниях кишечника // Справочник по диетологии. — М.: Медицина, 1981. — С. 235-251.
3. Парфенов А.И., Сабельникова Е.А., Крумс Л.М. Глютенчувствительная целиакия и профилактика аутоиммунных и онкологических заболеваний (передовая) // Тер. арх. — 2007. — № 2. — С. 5-8.
4. Парфенов А.И., Крумс Л.М., Сабельникова Е.А. и др. Микроскопический колит — причина торпидного течения целиакии // Тер. арх. — 2005. — № 2. — С. 80-81.
5. Парфенов А.И., Крумс Л.М., Сабельникова Е.А. Современная концепция, дефиниция и классификация целиакии // Мат-лы V съезда Научного общества гастроэнтерологов России. — М.: Анахарсис, 2005. — С. 473-475.
6. Парфенов А.И. Целиакия. Эволюция представлений о распространенности, клинических проявлениях и значимости этиотропной терапии. — М.: Анахарсис, 2007. — 376 с.
7. Collin P., Vilska S., Heinonen P.K. et al. Infertility and coeliac disease // Gut. — 1944. — Vol. 39. — P. 382-384.
8. Dudy C., Rostom A., Sy R. et al. The prevalence of celiac disease in average-risk and at-risk western European population: A systematic review // Gastroenterol. — 2005. — Vol. 128, № 4, suppl. 1.
9. Greco L., Romino R., Cofo J. et al. The first large population based twin study of celiac disease // Gut. — 2002. — Vol. 50. — P. 624-628.
10. Hoffenberg E.J., MacKenzie T., Barriga K.J. et al. A prospective study of the incidence of childhood celiac disease // J. Pediatr. — 2003. — Vol. 143. — P. 308-314.
11. Jarvinen T.T., Collin P., Kasmussen M. et al. Villous tip interepithelial lymphocytes as markers of early-stage celiac disease // Scand. J. Gastroenterol. — 2004. — Vol. 39. — P. 428-433.
12. Kagnoff M.F., Austrin R.K., Hubert J.J. et al. Possible role for a human adenovirus in the pathogenesis of celiac disease // J. Exp. Med. — 1984. — Vol. 160. — P. 1544-1557.
13. Kakar S., Nehra V., Murray J.A. et al. Significance of interaepithelial lymphocytosis in small bowel biopsy samples with normal mucosal architecture // Am. J. Gastroenterol. — 2003. — Vol. 98. — P. 2027-2033.
14. Kaukinen K., Maki M., Partanen J. et al. Coeliac disease without villous atrophy: revision of this criterial // Dig. Dis. Sci. — 2001. — Vol. 46 (4). — P. 879-887.
15. Marsh M.N. Mucosal pathology in gluten sensitivity // Coeliac disease. —
16. Salvati V.M., MacDonald T.T., Bajaj-Elliott M. et al. Interleikin 18 and associated markers of T-helper cell type 1 activity in celiac disease // Gut. — 2002. — Vol. 50. — P. 186-190.
17. Shan L., Mollerg O., Parrot J. et al. Structural basis for gluten intolerance in celiac sprue // Science. — 2002. — Vol. 297. — P. 2275-2279.
18. Volta V., De Franceshi L., Molinaro N. et al. Frequency and significance of anti-gliadin and anti-endomisial antibodies in autoimmune hepatitis // Dig. Dis. Sci. — 1998. — Vol. 43. — P. 2190-2195.