Газета «Новости медицины и фармации» Гастроэнтерология (304) 2009 (тематический номер)
Вернуться к номеру
Возможности флавоноидных изомеров силимарина в лечении заболеваний печени
Авторы: Ю.В. Линевский, д.м.н., профессор, К.Ю. Линевская, к.м.н., доцент, К.А. Воронин, Донецкий национальный медицинский университет им. М. Горького, кафедра внутренней медицины им. А.Я. Губергрица, кафедра внутренней медицины № 2
Версия для печати
Основным патогенетическим фактором при диффузных воспалительных заболеваниях печени является окислительный стресс, который сопровождается токсическим воздействием свободных радикалов на мембрану гепатоцитов с ее повреждением (вплоть до некроза), активацией звездчатых клеток печени, увеличением продукции коллагена. Редукция печеночных клеток в конечном итоге ведет к формированию цирротического процесса в печени, угрозе развития печеночной недостаточности.
Поэтому важная роль в лечении хронических гепатитов и циррозов печени принадлежит гепатопротекторам — лекарственным средствам, действие которых направлено на восстановление и поддержание функциональной активности гепатоцитов и репаративно-регенераторных процессов в печени.
В лечении указанной патологии печени важное место занимают гепатопротекторы растительного происхождения.
Одним из наиболее популярных источников сырья для получения соответствующих лекарственных средств является расторопша пятнистая (Silybum marianum), известная также под названием «чертополох молочный», или «святой чертополох», который принадлежит к семейству астровых. В народе это растение известно как марьин татарник. За свои лечебные свойства он получил название «подарок Девы Марии» (О. Мазуренко, 2009). Римский натуралист Плиний Старший (I век до н.э.) характеризует чертополох молочный как «прекрасное средство, очищающее желчь». Имеется упоминание об этом растении в трактате Диоскорида «Materia medica».
С давних пор расторопша используется во многих странах в лечении заболеваний печени. Ее главным действующим началом является силимарин, состоящий из флавоноидных изомеров. В их числе силибинин (50–60 %), изосилибинин (около 5 %), силикристин (20 %), силидианин (около 10 %), таксифолин (около 5 %) и другие. Таким образом, главным действующим началом силимарина является силибинин.
Биологические эффекты силимарина и их механизмы представлены в табл. 1.
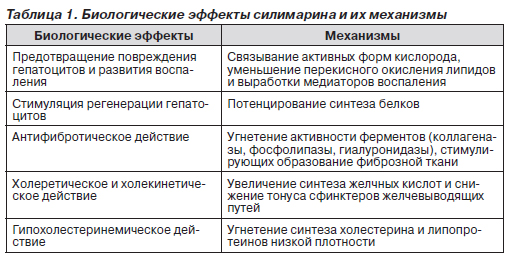
Приведенные в табл. 1 сведения свидетельствуют о неоспоримом лечебном действии силимарина, направленном на ограничение воспалительного процесса в печени и повреждения гепатоцитов, предотвращение развития фиброзной ткани и восстановление паренхимы печени (В.Т. Ивашкин и др., 2003).
Положительное влияние силимарина на течение воспалительного процесса и развитие цирроза печени подтверждено многочисленными клиническими наблюдениями.
У больных с отравлением бледной поганкой (452 чел.) смертность в группе леченных силибинином была вполовину меньшей в сравнении с группой, получавшей стандартное лечение без использования флавоноидных соединений (E.B. Keffe, 1999).
По данным гистологического исследования биоптатов печени у больных хроническим гепатитом использование силимарина в сравнении с группой больных, получавших плацебо, показало несомненный положительный эффект (E. Kiesewetter et al., 1977).
Отмечена отчетливая положительная динамика клинических проявлений при лечении 2637 пациентов с алкогольной болезнью печени (Albrecht et al., 1992). В пользу этого свидетельствуют также сводные данные 11 слепых исследований динамики биохимических показателей цитолитического синдрома у пациентов с алкогольной болезнью печени при курсовом использовании силимарина (F. Di Mario et al., 1981; H.A. Salmi, S. Sarna, 1982; J. Feher et al., 1989).
Данные о положительном влиянии силимарина на морфологические изменения в печени у пациентов с алкогольной болезнью печени получены при биопсиях до курсового использования указанного лекарственного средства и после него (H.A. Salmi, S. Sarna, 1982).
Использование силимарина у больных сахарным диабетом и циррозом печени способствовало уменьшению потребности в инсулине (M. Velussi et al., 1997).
Частота госпитализаций больных циррозом печени по поводу его осложнений оказалась существенно меньшей в группе лиц с указанной патологией, леченных силимарином, в сравнении с группой больных, получавших плацебо (A. Pares et al., 1998).
По данным биопсии печени и результатам вскрытий умерших частота эпителиом печени у больных циррозом печени оказалась вполовину меньшей у больных, леченных с использованием силимарина (E. Kiesewetter et al., 1977).
Таким образом, силимаринсодержащие препараты заслуживают внимания в лечении гепатитов и циррозов печени.
В числе силимаринсодержащих препаратов — препарат Карсил® фармацевтической компании Sopharma. Препарат содержит основное действующее начало силимарина — силибинин. Выпускается в виде драже по 35 мг и капсул (Карсила® форте), содержащих 90 мг силибинина.
Препарат Карсил® рекомендуется при поражении печени легкой и средней степени по 1–2 драже и при тяжелом поражении по 2–3 драже 3 раза в сутки, а Карсил® форте соответственно по 1 капсуле 1–2 раза и 3 раза в сутки. В возрасте от 5 до 12 лет препарат Карсил® дозируется из расчета 5 мг/кг массы тела, разделенных на 2–3 приема в течение суток.
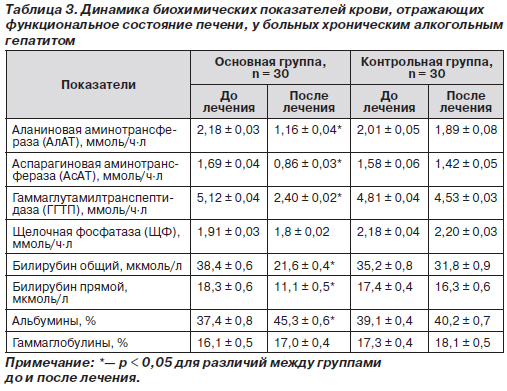
Приводим анализ динамики клинических проявлений (табл. 2) и лабораторных показателей (табл. 3) состояния печени через 3 недели терапии у двух групп больных хроническим алкогольным гепатитом со слабой и умеренной активностью. Основная группа больных получала препарат Карсил® на фоне базисной терапии, контрольная группа — только базисное лечение.
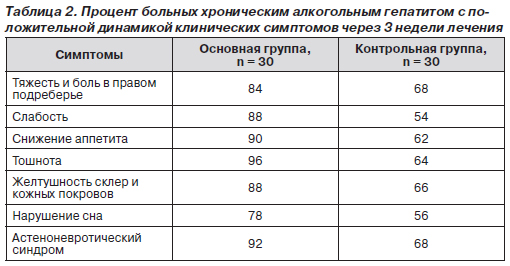
Данные табл. 2 свидетельствуют о более выраженной положительной динамике клинических симптомов хронического гепатита у больных, леченных с использованием препарата Карсил®.
Данные табл. 3 также свидетельствуют о положительном воздействии курсового использования препарата Карсил® у больных хроническим алкогольным гепатитом на показатели синдрома цитолиза (АлАТ, АсАТ, билирубин), что связано с его антиоксидантным действием. Выявлено увеличение синтетической функции печени при использовании препарата Карсил®. Об этом свидетельствовало увеличение содержания альбуминов в сыворотке крови. В группе больных, получавших Карсил®, отмечено снижение содержания ГГТП. При отсутствии воздействия препарата Карсил® на уровень ЩФ сыворотки крови динамика ГГТП указывала на уменьшение выраженности под влиянием препарата Карсил® повреждения печени, вызванного алкоголем.
Таким образом, использование у больных хроническим алкогольным гепатитом препарата Карсил® способствовало регрессированию клинических проявлений заболевания и улучшению лабораторных показателей состояния печени.
С учетом изложенного выше Карсил® может использоваться при токсических поражениях печени, после перенесенного острого гепатита, при стеатозе печени алкогольного и неалкогольного генеза, хронических гепатитах и циррозах печени, а также с целью защиты печени при массивной медикаментозной терапии с применением антибиотиков, противогрибковых, противовирусных препаратов, гормональных контрацептивов, гиполипидемических средств (статинов), при лечении сахарного диабета.
1. Мазуренко О. Гепатотропные препараты: синергия опыта и инноваций // Здоров''я України. — 2009. — №12/1. — С. 1-3.
2. Ивашкин В.Т., Лапина Т.Л. и др. Рациональная фармакотерапия органов пищеварения. — М.: Литтера, 2003. — 1046 с.
3. Albrecht M., Frerick H., Kuhn U. et al. Die Therapie toxischer Leberschaden mit Legalon // Z. Klein. Med. — 1992. — V. 47. — Р. 87-92.
4. Di Mario F., Farini R., Okolicsanyi L. et al. Die Wirkimg von Legalon auf die Leberfunktionsproben bei Patienten mit alkoholbedingter Lebererkrankung, Doppelblindstudier // De Ritis F., Csomos G., Braatz R. Der toxisch-metabolische Leberschaden. —
5. Feher J., Deak G., Muzes G. et al. Silymarin kezeles majvedo hatasa idult alkoholos majbetegsegben // Orv. Hetil. — 1989. — V. 130. — Р. 2723-2727.
6. Keeffe E.B. Chapter VII Acute hepatitis // Dale DC, editor. Scientific American Medicine SAM-CD Connected. Copyright © 1999, Healtheon/WebMD, March 1999.
7. Kiesewetter E., Leodolter I., Thaler H. Ergebnisse zweier Doppelblindstudien zur Wirksamkeit von Silymarin bei chronischer Hepatitis // Leber Magen Darm. — 1977. — V. 7. — Р. 318-323.
8. Pares A., Planas R., Torres M. et al. Effects of silymarin in alcoholic patients with cirrhosis of the liver: results of a controlled, double-blind, randomized and multicenter trial [see comments] // J. Hepatol. — 1998. — V. 28. — Р. 615-621.
9. Salmi H.A., Sarna S. Effect of silymarin on chemical, functional, and morphological alterations of the liver. A double-blind controlled study // Scand. J. Gastroenterol. — 1982. — V. 17. — Р. 517-521.
10. Velussi M., Cernigoi A.M., De Monte A. et al. Long-term (12 months) treatment with an anti-oxidant drug (silymarin) is effective on hyperinsujinemia, exogenous insulin need and malondialdehyde levels in cirrhotic diabetic patients // J. Hepatol. — 1997. — V. 26, № 4. — Р. 871-879.
