Газета «Новости медицины и фармации» Кардиология (305) 2009 (тематический номер)
Вернуться к номеру
Ведение пациента с постоянной формой фибрилляции предсердий. По следам рекомендаций Рабочей группы по нарушениям сердечного ритма Ассоциации кардиологов Украины 2009 г.
Авторы: Н.И. Яблучанский, Медицинский факультет Харьковского национального университета им. В.Н. Каразина
Версия для печати
Постоянная фибрилляция предсердий (ПФП) является одной из важных клинических проблем, когда сталкиваются интересы пациента и врача и далеко не всегда удается быстро найти наилучше возможное решение, удовлетворяющее обе стороны.
С ПФП связаны риск тромбоэмболических осложнений, наиболее часто манифестирующих нарушениями мозгового кровообращения, от транзиторных ишемических атак до ишемического инсульта, развитие и прогрессирование сердечной недостаточности, сложные комбинированные нарушения сердечного ритма и, как результат, более высокая опасность внезапной смерти, снижение качества и уменьшение продолжительности жизни.
С развитием заболевания, а точнее с момента его диагностики — ибо немало случаев, когда ПФП, как и другие формы фибрилляции предсердий, является врачебной находкой, — оно становится проблемой для образованного пациента и, вовлекая в свои орбиты психофизиологический фактор, по образному выражению Д.Д. Плетнева, становится болезнью («Болезнь начинается с того момента, когда нарушается собственное «Я»).
Мой учитель, с некоторого возраста «сосуществовавшая» с ПФП и ушедшая в мир иной совсем по иным обстоятельствам, более всего беспокоилась именно по этому поводу, помня о риске ее смертельных осложнений (Учитель проф. Н.И. Яблучанского — директор Института терапии АМН Украины, Герой Cоциалистического Труда, Герой Украины, академик Л.Т. Малая). Проводя научные конференции и требуя от докладчиков четкого следования регламенту, мои выступления она обычно предваряла замечанием: «А вы, миленький, можете говорить, сколько считаете нужным».
Я никогда не злоупотреблял ее любезностью, четко следовал регламенту, стараясь, однако, по возможности, максимально полно осветить свое понимание проблемы и свое же отношение к существующим стандартам.
Буду стараться не злоупотребить любезностью и здесь, но тем не менее…
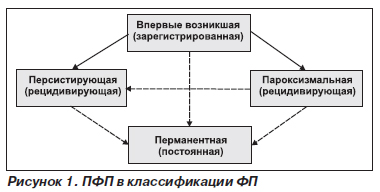
В ПФП «вливаются» остальные формы фибрилляции предсердий (рис. 1). Можно спорить в отношении точности и полноты схемы, но на то она и схема, чтобы отражать наиболее важные моменты реального положения вещей.
В соответствии с рекомендациями Рабочей группы по нарушениям сердечного ритма Ассоциации кардиологов Украины
Цели ведения ПФП с поправками на доказательную медицину могут быть сформулированы следующим образом:
Поправки на доказательную медицину исключительно важны, ибо грош цена частному достигнутому результату, если за ним последует снижение качества и возрастет риск сокращения продолжительности жизни пациента.
Также абсолютно важен контроль основного заболевания, если оно неизлечимо, так как в природе и развертывании ПФП наиболее часто «повинны» если не его интимные механизмы, то механизмы его осложнений — на все 100 %. Но об этом немного позже.
Обычно в целях лечения ПФП профилактика тромбоэмболий ставится перед контролем ЧЖС, так как не редкость нормосистолическая или нормокардитическая ЧЖС с адекватными частотоадаптивными реакциями на стресс, а за тромбоэмболическими осложнениями тенью следуют ранняя инвалидизации и вообще «прерванный полет». Я же ставлю контроль ЧЖС перед профилактикой тромбоэмболий только потому, что когда в соответствии с требованием принципа быстродействия приходится решать неотложно именно эти задачи, которые должны предшествовать задачам профилактики тромбоэмболий.
Цели и критерии успешности контроля ЧЖС при ПФП определяются так:
Из критериев видно, что они предполагают увеличение ЧЖС при физической нагрузке и ограничивают его при умеренной нагрузке 120 сердечными сокращениями в минуту.
Из критериев видно также, что при ПФП постулируется сохранение у большинства пациентов адаптивных реакций ЧЖС на стресс. Этот момент является важным, так как часто проходит мимо внимания врача. Но многие пациенты с ПФП не жалуются на одышку при стрессе именно в силу этих обстоятельств, и она начинает «преследовать» их только с развитием сердечной недостаточности (СН), в том числе обусловленной самой ФП (аритмогенной). Другая возможная причина появления одышки при стрессе — избыточные терапевтические вмешательства, когда не просто достигается целевая ЧЖС покоя, но и одновременно с этим подавляются ее адаптивные реакции.
В контроле ЧЖС врач должен не просто добиться ее целевых уровней, но и сохранить, а в оптимуме — и улучшить адаптивные реакции на стресс.
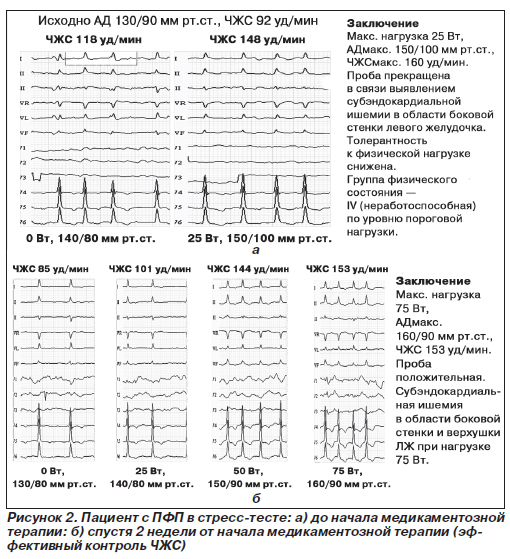
На рис. 2 (а, б) представлены результаты стресс-теста у пациента с ПФП до и спустя 2 недели после качественно подобранной терапии. До начала терапии он показывает низкую, а на ее высоте — достаточную адаптированность к стрессу по реакциям ЧЖС. Субэндокардиальная ишемия в области боковой стенки и верхушки ЛЖ, которая и стала причиной остановки стресс-теста, наступила только при нагрузке 75 Вт.
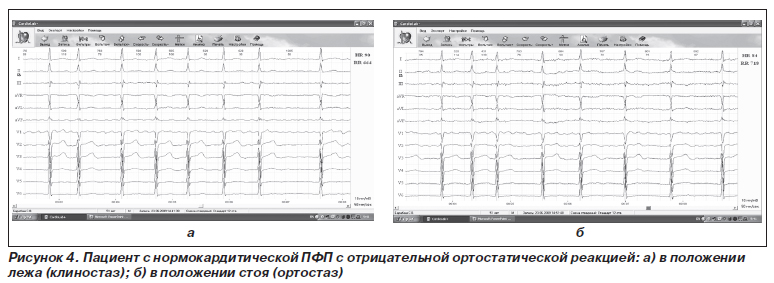
Сразу замечу, что, к счастью, далеко не у всех пациентов с ПФП приходится решать задачи контроля ЧЖС и для многих из них излишняя активность врача в этом отношении просто вредна. Пример такой активности показан на рис. 3 (а, б), в данном случае, к счастью, при резком снижении ЧЖС не удалось «задавить» ее адаптивных реакций на стресс, и при переходе из положения лежа в положение стоя (активный ортостатический тест) она возросла на 10 сокращений в минуту — с 45 до 55.
Точно так же, как многие пациенты не требуют вмешательства в ЧЖС и ее адаптивные реакции на стресс, клиника преподносит врачу далеко не простые диагностические задачи, когда вовсе не очевидно, как решить задачу контроля ЧЖС. Для примера привожу ЭКГ одного пациента последовательно в положениях лежа (рис. 4а) и стоя (рис. 4б) — активном ортостатическом тесте, когда он дает неправильную отрицательную реакцию ЧЖС на ортостаз, и вместо того, чтобы увеличиться, она уменьшается. Кстати, замечу, что, как показала одна из моих сотрудниц Л.А. Мартимьянова, частота обратных ортостатических реакций у пациентов с фибрилляцией предсердий такая же, как и у пациентов с синусовым ритмом. В приведенном примере задача контроля ЧЖС решена терапевтическими методами, но схему не привожу, так как индивидуальный случай требует своей индивидуальной схемы. Наш пример не может быть обобщен.
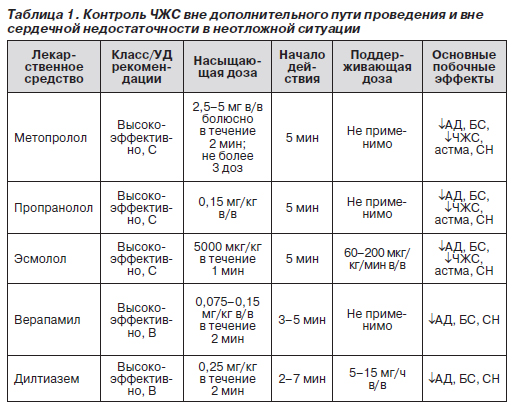
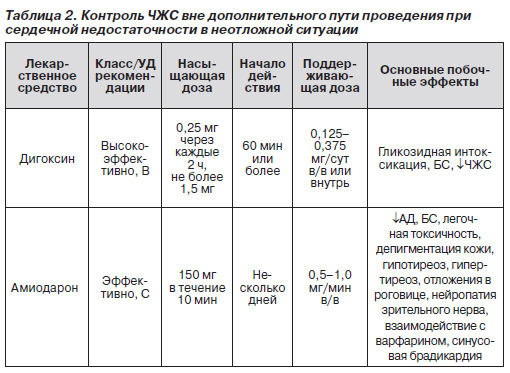
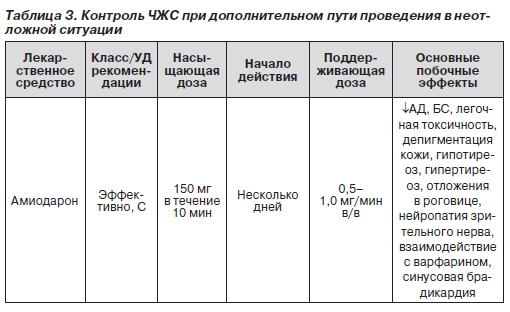
В табл. 1–3 представлены адаптированные национальными рекомендациями перечни лекарственных препаратов и схем их использования при контроле ЧЖС в неотложной ситуации, соответственно, вне дополнительных путей проведения и СН, при СН вне дополнительных путей проведения и при имеющихся дополнительных путях проведения. СН и дополнительные пути проведения резко ограничивают возможный перечень. Если принять во внимание, что в соответствии с последними национальными рекомендациями по ведению пациентов с СН к ней отнесена и асимптотическая дисфункция левого желудочка (АДЛЖ), и мне, например, не известно ни одного случая фибрилляции предсердий, при которых бы не было тех или иных признаков АДЛЖ, получается, что перечень из табл. 1 на практике имеет мало шансов на использование.
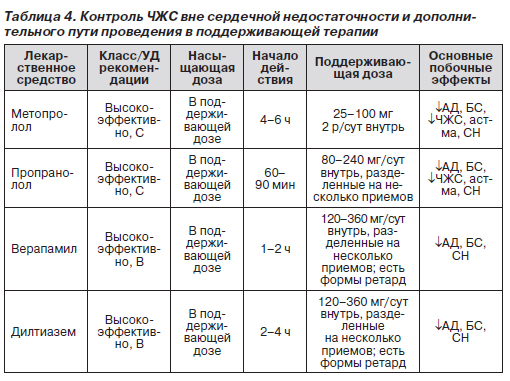
Адаптированные национальными рекомендациями перечни лекарственных препаратов при контроле ЧЖС в поддерживающей терапии построены по тому же принципу и учитывают наличие или отсутствие дополнительных путей проведения и СН (табл. 4–6). Отличия состоят только в выпавшем из списка эсмололе и других схемах использования. Как и в первом случае, СН и дополнительные пути проведения резко ограничивают возможный перечень лекарственных препаратов. Высказанные замечания касательно АДЛЖ, естественно, в равной мере приложимы и к случаю поддерживающей терапии.
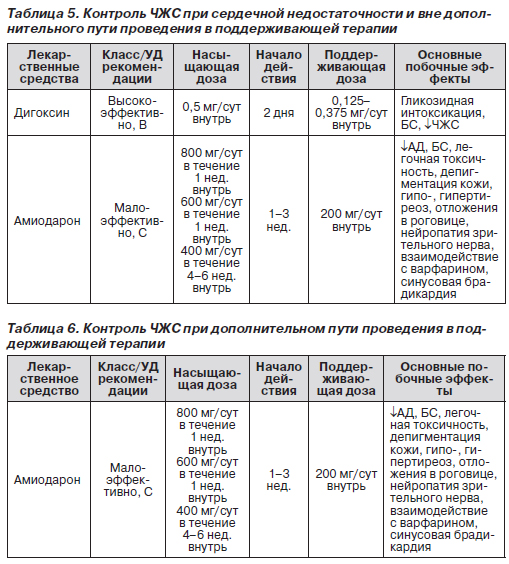
У читателя при ознакомлении с табл. 1–6 могут возникнуть вопросы по ограниченным спискам лекарственных препаратов как в неотложном контроле ЧЖС, так и при поддерживающей терапии. Одна из возможных причин — необъятное не объять, и составители рекомендаций просто не учли весь возможный их перечень. Что это так, в частности, следует из табл. 7, где даются рекомендации по выбору лекарственных препаратов при контроле ЧЖС в соответствии с предсуществующими патологическими состояниями, в том числе и как возможными причинными, в развитии фибрилляции предсердий. В табл. 7 приводятся препараты, отсутствующие в табл. 1–6.
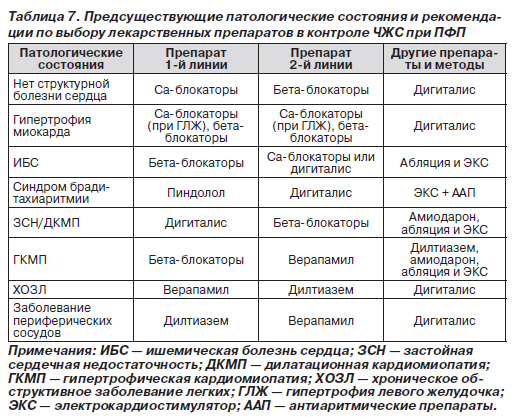
Замечу по ходу, что ниже этот список я существенно расширю, и для этого расширения имеются серьезные основания.
С антиаритмическими препаратами связан риск осложнений, в том числе аритмических, и побочных явлений, как и с всякими иными лекарственными препаратами (табл. 8). Многих из них удается избежать при тщательном интервьюировании пациента до и на этапах контроля ЧЖС.
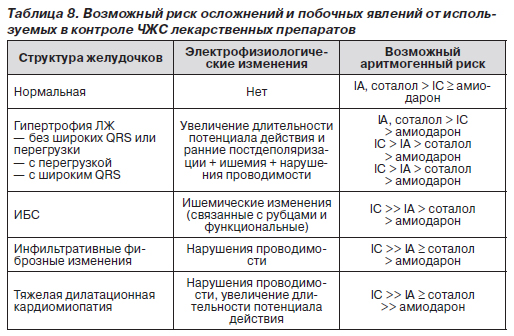
Если терапевтические вмешательства оказываются неэффективными и контроля ЧЖС достичь не удается, используются интервенционные, в том числе, в настоящее время наиболее часто, абляция атриовентрикулярного узла и имплантация водителя ритма. Показаниями для этих вмешательств являются выраженная вариабельность желудочкового ритма, брадикардия и тахикардия в покое, а также бради- и чрезмерные тахикардитические реакции на стресс. Важно помнить об ограничениях конкретно абляции атриовентрикулярного узла с имплантацией водителя ритма — необходимость в постоянной антикоагулянтной терапии, утрата атриовентрикулярного проведения и пожизненная зависимость от искусственного водителя ритма.
Блокаторы бета-адренергических рецепторов с внутренней (собственной) симпатомиметической активностью (ацебутолол, пиндолол, талинолол) при бради-тахиаритмии могут быть альтернативой абляции атриовентрикулярного узла с установкой электрокардиостимулятора. Они могут использоваться в монотерапии и в сочетании с дигоксином, но в последнем случае требуется тщательный контроль ЧЖС с мониторированием ЭКГ.
Всем пациентам с ПФП показана антиагрегантная и антикоагулянтная терапия, преследующая целью профилактику тромбоэмболий. На сегодня основными средствами такой терапии являются ацетилсалициловая кислота и варфарин, в принятии решения об использовании которых основываются на шкале CHADS2 — Cardiac failure, Hypertension, Age, Diabetes, Stroke. У пациента подсчитывается суммарное число баллов по имеющимся признакам (симптомам и синдромам) в соответствии со шкалой и по суммарному числу баллов оценивается риск тромбоэмболических осложнений. В соответствии с риском назначается терапия (табл. 9–11).


Не нужно быть семи пядей во лбу, чтобы, посмотрев на табл. 11, сделать однозначный вывод: подавляющему большинству пациентов с ПФП показана антикоагулянтная терапия и, значит, они должны принимать варфарин. Если мы все еще продолжаем иметь много транзиторных ишемических атак и ишемических инсультов у пациентов с фибрилляцией предсердий, то только потому что либо нуждающемуся в варфарине он не назначается, либо нуждающийся в варфарине не получил убедительных доводов врача о неуклонной необходимости регулярного приема этого препарата и просто в один момент перестал его принимать по той или иной причине.
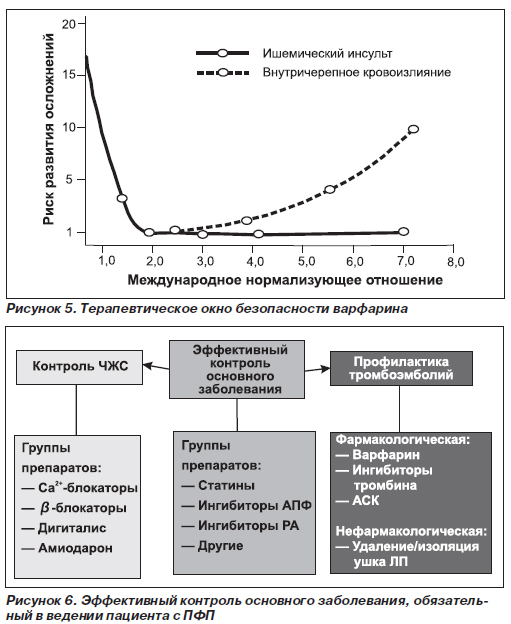
Есть «тонкое обстоятельство» лечения варфарином — Сцилла тромбоэмболических осложнений и Харибда кровотечений, между которыми узкая зона безопасности. Чтобы упредить появление кровотечений, необходимо «держать» терапевтическое окно, которое для варфарина — 2,0–3,0 МНО (рис. 5). Очевидно, что при принятии решений о назначении варфарина необходимо также четко контролировать отсутствие у пациента противопоказаний для антикоагулянтной терапии.
Первого октября
Терапия эта получила такое название потому, что предлагается в ведении пациентов с фибрилляцией предсердий использовать вместо антиаритмических препаратов или, правильнее, в дополнение к ним лекарственные средства других, вышеперечисленных, групп.
Я бы согласился назвать эти предложения «терапией против течения», если бы не мое «но». Суть этого «но» в том, что фибрилляция предсердий, и ПФП не исключение, в большинстве случаев — клинический синдром при ряде заболеваний, многие из которых как раз и лечится лекарственными препаратами поименованных фармакотерапевтических групп. Более того, по моему убеждению, даже так называемая идиопатическая фибрилляция предсердий в своем большинстве, если другой причины точно нет, чаще всего является атеросклеротической или, на худой конец, в том числе атеросклеротической, когда без лекарственных препаратов перечисленных групп не обойтись.
Здесь, получается, я обосновываю обязательный в ведении пациента с ПФП эффективный контроль основного заболевания (рис. 5), который, естественно, должен находиться в полном соответствии с состоянием здоровья пациента, а не с громадьем симптомов и синдромов, которые мы можем найти у него.
Приоритетами, важно напомнить и себе, в эффективном контроле основного заболевания всегда являются здоровый образ жизни и образование (медицинским персоналом по болезни) пациента, следование лучшим стандартам лечения, командный стиль работы и тесное сотрудничество с пациентом.
Что касается лучших стандартов лечения, весьма интересно, скоро ли придет время, когда все рекомендации, например пересмотр рекомендаций
В самом начале статьи в числе целей ведения ПФП с поправками на доказательную медицину последними я указал повышение качества и продолжительности жизни пациента.
Это и есть самая важная двуединая неделимая цель ведения любого пациента, и ПФП — частный случай, ибо грош цена другим целям, если они не обеспечивают достижения этой.
На повышение качества и продолжительности жизни пациента должны ориентироваться все методы, а что касается ПФП, их остается только повторить: