Газета «Новости медицины и фармации» 5(311) 2010
Вернуться к номеру
Больовий синдром та його корекція у ранньому післяопераційному періоді
Авторы: В.М. Короткий, професор, І.В. Колосович, д.м.н. Національний медичний університет імені О.О. Богомольця, м. Київ
Версия для печати
Як це не дивно звучить, біль є одним із найкорисніших «винаходів» природи, оскільки саме він негайно сигналізує про небезпеку, що загрожує організму з боку патологічних факторів. Не менш корисні ефекти антагоністичної протибольової системи організму, що підвищує поріг больового відчуття, швидко відволікаючи нас від переживання болю й переключаючи на інші, корисніші заняття, тоді як біологічний процес репарації ушкоджених тканин ще продовжується. Проте при порушенні рівноваги між функціонуванням ноцицептивної й антиноцицептивної систем біль стає патологічним і приносить тільки страждання. Особливо це питання актуальне для пацієнтів хірургічного профілю (до операції, у ранньому післяопераційному періоді). Так, згідно з даними ряду авторів, від вираженого больового синдрому в післяопераційному періоді страждають від 30 до 75 % пацієнтів [6, 8].
В основі патофізіологічної класифікації болю (ноцицептивний, невропатичний, психогенний) лежить послідовність формування больового відчуття на різних рівнях трьохнейронної ноцицептивної системи: перший нейрон — периферичний больовий рецептор; другий — спіноталамічний; третій — таламокортикальний. Короткотривалі патологічні ефекти болю включають: 1) емоційне та фізичне страждання пацієнта; 2) порушення сну; 3) небажані реакції серцево-судинної системи та зростання споживання кисню; 4) небажані реакції з боку шлунково-кишкового тракту (ШКТ); 5) поверхневе дихання із зменшенням дихального об''єму, зниження екскурсії діафрагми, послаблення кашльового рефлексу; 6) зниження фізичної активності пацієнта.
Основною в лікуванні болю є терапія, що застосовується залежно від інтенсивності та вираженості болю (ступінчасте знеболювання), або терапія, що діє на основний механізм розвитку болю. Лікарські засоби, що використовують для ліквідації болю, можна поділити: 1) на засоби центральної дії (опіоїдні анальгетики, неопіоїдні препарати з анальгетичною активністю, препарати змішаної дії тощо); 2) лікарські засоби периферичного типу (місцеві анестетики; ненаркотичні анальгетики з групи пропіонової кислоти, саліцилатів тощо); 3) інші засоби для знеболювання (блокатори серотонінових рецепторів; β-адреноблокатори; міорелаксанти тощо). У ранньому післяопераційному періоді для знеболювання хворих найбільш часто застосовують опіоїдні анальгетики. Ефективне лікування болю повинно включати в даному випадку: адекватний вибір препарату, адекватну початкову й наступні дози для підтримання достатньої концентрації у плазмі, за необхідності — комбінацію з ненаркотичними анальгетиками, слід урахувати можливі побічні ефекти та умови, в яких буде застосовуватися препарат. Основними проблемами лікування опіоїдами є труднощі в дозуванні для досягнення оптимального дозозалежного співвідношення ефективності та небажаних реакцій, що спостерігаються під час їх застосування. Корисні ефекти опіоїдів — седація, анальгезія, атараксія, центральне пригнічення кашлю (в окремих випадках). Негативні ефекти: надмірна седація; нудота та блювання; затримка сечі; висипання на шкірі, кропивниця або свербіж; запори внаслідок дисфункції жовчовивідних шляхів, парезу ШКТ; депресія дихального центра (при передозуванні) та порушення серцевої діяльності.
Провідну роль у механізмі формування запального ноцицептивного болю при ушкодженні тканин відіграють цикл арахідонової кислоти та його кінцеві продукти — потужні медіатори запалення й болю: простагландини, тромбоксан і простациклін. Ключову позицію в цьому циклі займає фермент циклооксигеназа (ЦОГ), що ініціює метаболізм арахідонової кислоти до вищезазначених медіаторів. На сьогодні ідентифіковані дві ізоформи ферменту — ЦОГ-1 та ЦОГ-2, кожна з яких відіграє специфічну роль у різних фізіологічних процесах. ЦОГ-1 продукується постійно, проявляє функціональну активність структурного («housekeeping», конститутивного) ферменту, експресується в більшості клітин, регулює продукцію простагландинів, забезпечує нормальне (фізіологічне) функціонування клітин організму. ЦОГ-2 є індукованою формою ферменту, бере участь як у патологічних (запальні процеси), так і фізіологічних (синтез простагландинів, репаративні процеси, регуляція гормонального фону у чоловіків і жінок, функції нирок, цитопротекторна антитоксична дія, боротьба з стресом) процесах організму. Уміст ЦОГ-2 збільшується під впливом прозапальних цитокінів і пригнічується протизапальними медіаторами (кортизол) і цитокінами (інтерлейкін-4). В останні роки була відкрита ще одна ізоформа ЦОГ — ЦОГ-3, що локалізується переважно в клітинах кори головного мозку й блокується парацетамолом, метамізолом і фенацетином. Її роль у фізіології болю ще вивчається.
Саме ЦОГ є основною молекулярною мішенню для нестероїдних протизапальних препаратів (НПЗП), що, згідно з рекомендаціями ВООЗ, використовуються на всіх рівнях ступінчастої терапії болю. Зазначені лікарські засоби застосовуються упродовж більше ніж двох століть, на сьогодні відомі понад 70 НПЗП, що мають різноманітну хімічну структуру. У лікуванні післяопераційного больового синдрому НПЗП використовують самостійно або в комбінації з опіатами та місцевими анестетиками. Основною перевагою застосування НПЗП є опіоїдзберігаючий ефект, що дає можливість не тільки уникнути характерних ускладнень, які супроводжують знеболювання наркотичними анальгетиками, а й швидше активізувати пацієнта, скоротити строки госпіталізації та зменшити витрати на стаціонарне лікування. НПЗП показали високу ефективність у лікуванні післяопераційного болю в гінекології, ортопедії, стоматології, торакальній та абдомінальній хірургії та хірургії хребта.
НПЗП поділяють на такі класи: 1) селективні інгібітори ЦОГ-1 (ацетилсаліцилова кислота в низьких дозах); 2) неселективні інгібітори ЦОГ-1 і ЦОГ-2 (більшість сучасних НПЗП); 3) селективні інгібітори ЦОГ-2 (німесулід, мелоксикам); 4) специфічні інгібітори ЦОГ-2 (коксиби); 5) стереоселективні НПЗП (декскетопрофен).
Лімітуючим фактором використання неселективних інгібіторів ЦОГ є відносно велика частота ускладнень, навіть у разі їх короткотривалого застосування, що пов''язано з пригніченням ЦОГ-1 (артеріальна гіпертензія, периферичні набряки, інтерстиціальний нефрит, гастропатія, дезагрегація тромбоцитів, підвищена кровоточивість). Основні механізми розвитку ускладнень при застосуванні неселективних НПЗП такі: 1) пригнічення синтезу простагландинів (Е2, І2), що призводить до розвитку ускладнень із боку травного тракту, порушення регуляції клубочкової фільтрації, секреції реніну; 2) пригнічення фагоцитозу; 3) пригнічення синтезу тромбоксану А2 (порушення агрегації тромбоцитів, підвищення кровоточивості);
4) пригнічення циклооксигеназної активності (гіперпродукція лейкотрієнів із розвитком реакції гіперчутливості негайного типу). Механізм ураження травного тракту також пов''язаний із зменшенням кровотоку в слизовій оболонці та порушеннями її трофіки, змінами базового рН шлункового соку та адгезії нейтрофілів. Мають значення також прямий токсичний вплив препаратів та генетичні фактори.
НПЗП-індуковані побічні ефекти з боку ШКТ поділяють на 3 основних типи: симптоматичні (біль у животі, нудота, диспепсія тощо); ураження слизової оболонки ШКТ, що виявляються при ендоскопічному або рентгенологічному дослідженнях, і тяжкі ускладнення (перфоративна виразка, кровотеча) [2]. Побічні ефекти, що розвиваються при прийомі ЦОГ-неселективних препаратів, у 34–46 % хворих проявляються шлунковою і кишковою диспепсією, у 15 % — ендоскопічно підтвердженими виразками та ерозіями шлунка та дванадцятипалої кишки, у 1,7 % — перфораціями та кровотечами [5]. Антитромбоцитарні ефекти НПЗП широко дискутуються, особливо це стосується монотерапії, однак застосовувати ці препарати в ряді країн протипоказано в разі одночасного прийому навіть низьких доз гепарину.
Останнім часом у періопераційному знеболюванні досить широко застосовують селективні та специфічні інгібітори ЦОГ-2. За фармакологічною дією вони відрізняються від традиційних НПЗП тільки коефіцієнтом селективності блокування ЦОГ-2 щодо ЦОГ: німесулід — 0,15, целекоксиб — 0,1, рофекоксиб — 0,004 (індометацин — 33,0, кетопрофен — 2,0) [1]. Однак, згідно з результатами ряду рандомізованих подвійних сліпих клінічних досліджень, було зареєстровано підвищення частоти виникнення тромботичних серцево-судинних ускладнень (інфаркт міокарда та інсульт) внаслідок тривалого вживання ряду специфічних інгібіторів ЦОГ-2 (13–15 випадків на 10 000). Розвиток тромбозів пов''язувався з дисбалансом синтезу протромбогенних (тромбоксан) та антитромбогенних (простациклін) простагландинів.
На сьогодні відсутні переконливі дані, які б довели, що використання селективних інгібіторів ЦОГ-2 у хворих із виразковим анамнезом є безпечнішим порівняно із застосуванням класичних НПЗП. Згідно з дослідженням F. Chan і співавт. (2002), у якому порівнювалася частота рецидивів кровотечі на фоні прийому целекоксибу 400 мг/добу або диклофенаку 100 мг/до-
бу в поєднанні з омепразолом 20 мг/добу, частота рецидивів становила 4,9 % в основній і 6,4 % у контрольній групі (різниця невірогідна) [7]. При аналізі результатів клінічних досліджень CLASS та VIGOR кількість ускладнень, пов''язаних із виразками травного тракту, при прийомі целекоксибу та рофекоксибу була однаковою з неселективними НПЗП [3]. Крім того, у рекомендованих дозах знеболюючий і протизапальний ефекти селективних інгібіторів ЦОГ-2 слабкіші за очікувані, а при застосуванні високих доз втрачається їх селективність.
Досить важливим питанням післяопераційного знеболювання є мультимодальна або збалансована анальгезія, що передбачає комбіноване застосування анальгетичних медикаментозних засобів і методів для досягнення синергічної дії разом зі зменшенням небажаних ефектів завдяки зниженню доз препаратів і різниці у характеристиці небажаних ефектів кожної з її складових. Слід зазначити, що НПЗП є компонентом на всіх етапах мультимодальної анальгезії. Причому найбільший інтерес викликають опіоїдзберігаючі комбінації опіатів та НПЗП або НПЗП і місцевих анестетиків. Комбіноване застосування опіатів та НПЗП, які діють синергічно (за типом потенціювання дії: 1 + 1 > 3), є ефективнішим, ніж приймання препаратів кожної групи окремо (уникнення звикання, використання меншої дози кожного препарату, підвищення антиноцицептивного потенціалу, зменшення частоти й вираженості побічних ефектів опіатів).
Отже, ідеальний НПЗП повинен мати високий терапевтичний потенціал, добру переносимість, короткий час напіввиведення, високий терапевтичний індекс, низький відсоток побічних реакцій.
Серед НПЗП найбільш виражений знеболюючий ефект виявляє кетопрофен. Згідно з даними M. Potarius та співавт. (1993), внутрішньовенне введення кетопрофену в дозі 200 мг/добу дозволяє на 40 % знизити потребу в опіоїдах після операції порівняно з плацебо. За загальною безпекою препарат займає третє місце, а за найменшою частотою побічних ефектів — друге місце серед НПЗП. Кетопрофен складається з двох стереоізомерів. Аналізуючи позитивні й негативні сторони даного лікарського засобу, Caldwell та співавт. (1996) показали, що тільки правообертаючий енантіомер кетопрофену декскетопрофен (S(+)-кетопрофен) може блокувати ЦОГ, справляючи потужний знеболювальний ефект, тоді як неактивний лівообертаючий ізомер збільшує токсичність і метаболічне навантаження дози. У гострому експерименті на тваринах із використанням рацемічної форми кетопрофену й декскетопрофену трометамолової солі було показано, що частота гострого виразкового ураження при використанні стереоселективного декскетопрофену в 5 разів нижча порівняно з рацемічною його формою [9].
На фармацевтичному ринку України представлений декскетопрофен виробництва Berlin-Chemie — Дексалгін. Препарат взаємодіє з ЦОГ у 5 разів активніше, ніж рацемічний кетопрофен, і в 100 разів активніше, ніж його лівообертаючий ізомер. Препарат блокує проведення больових імпульсів як на периферії (пригнічення збудження нервових закінчень), так і у ЦНС (переривання больового імпульсу), знижує продукцію прозапальних і альгогенних цитокінів у ЦНС, що значно підвищує анальгетичний потенціал препарату. Додаткові механізми дії дексалгіну: 1) проникає через гематоенцефалічний бар''єр завдяки високій ліофільності; 2) діє центрально на рівні задніх стовпів спинного мозку — деполяризація нейронів; 3) селективно блокує рецептори NMDA (N-метил-D-аспартату), які беруть участь у модуляції больового імпульсу; 4) прямо і швидко діє на трансмісію болю. Унікальність препарату полягає в його властивості здійснювати блокаду ЦОГ на усіх трьох рівнях передачі болю (периферичний, сегментарний (спинний мозок) та центральний).
Під нашим спостереженням знаходився 51 хворий: 27 пацієнтів із гострою хірургічною патологією (12 — із гострим апендицитом, 9 — із гострим калькульозним холециститом, 6 — із защемленою грижею), які надійшли до стаціонару в ургентному порядку, а також 24 пацієнти із хронічною патологією (хронічний калькульозний холецистит (12 хворих), зовнішні грижі живота різної локалізації (9 хворих), у тому числі післяопераційні (3 хворі)).
Знеболюючі засоби (у тому числі НПЗП) до операції, окрім премедикації (перевагу надавали сібазону), нами не використовувалися з кількох причин:
1) «змазування» клінічної картини гострої хірургічної патології може негативно впливати на перебіг операції; 2) на нашу думку, збільшення часу кровотечі під впливом НПЗП може бути серйозною проблемою під час оперативного втручання, особливо міні-інвазивного, коли усунення підвищеної кровоточивості потребує додаткових маніпуляцій та подовжує втручання. У разі прийому НПЗП хворим на догоспітальному етапі планове оперативне втручання виконували через 1–2 доби після його відміни, а при систематичному прийомі аспірину — через 5 діб. Оперативні втручання з приводу защемленої грижі без ознак некрозу кишки проводили під місцевою анестезією; втручання лапаротомним доступом, а також лапароскопічні операції — під ендотрахеальним наркозом, із приводу неускладнених гриж та гострого апендициту — під спінальною анестезією.
У післяопераційному періоді залежно від характеру втручання, виду анестезії хворі протягом 1–3 діб за показаннями парентерально отримували Дексалгін (100–150 мг/добу) — 1-ша група, кетопрофен (100–150 мг/добу) — 2-га група, морфін (0,03 г/добу) — 3-тя група. НПЗП призначали не раніше ніж через 8 годин після виконання лапароскопічних втручань, оскільки впродовж цього часу існує реальна небезпека розвитку післяопераційної кровотечі. Хворим із супутніми захворюваннями ШКТ із метою профілактики розвитку ускладнень на фоні застосування НПЗП, згідно з чинними рекомендаціями [3], призначали противиразкові препарати — інгібітори протонної помпи у стандартних дозах або аналоги простагландинів (мізопростол 0,4–0,8 мг/добу).
Результати лікування хворих із застосуванням НПЗП засвідчили, що потреби у призначенні наркотичних анальгетиків після оперативних втручань, проведених під місцевою та спінальною анестезією, не було. Усі хворі після лапароскопічного втручання на жовчному міхурі при вираженому больовому синдромі додатково отримували фентаніл (морфін викликає спазм сфінктера Одді). Застосування мультимодальної терапії в цієї категорії хворих дозволило зменшити потребу в наркотичних анальгетиках утричі. Таким чином, було підтверджено тезу про те, що НПЗП потенціюють дію наркотичних анальгетиків. Необхідність у додатковому знеболюванні наркотичними анальгетиками після великих «відкритих» оперативних втручань на органах черевної порожнини на фоні застосування НПЗП становила 45,5 % випадків у 1-й та 2-й групах. Це були хворі, прооперовані з приводу гострого деструктивного холециститу на фоні розлитого перитоніту, защемленої грижі, ускладненої гангреною кишки, та післяопераційних гриж великих розмірів на фоні тяжкого спайкового процесу в черевній порожнині. Однак і в даної групи хворих потреба в наркотичних анальгетиках зменшилась удвічі.
Було встановлено, що максимальний анальгетичний ефект настає через 30 хв після парентерального введення Дексалгіну (для порівняння: через 90 хв після введення кетопрофену, через 60 хв — морфіну). Максимальна тривалість анальгезії в кожній групі після першого введення становила відповідно для 1-ї та 2-ї груп — 8 годин, для 3-ї — 5 годин. Дексалгін показав свою високу ефективність у хворих похилого та старечого віку, поріг больової чутливості яких вищий. Використання наркотичних препаратів у даної вікової групи небезпечне високим ризиком депресії дихального центру та порушеннями серцевої діяльності.
Побічні ефекти, що виникли при застосуванні знеболюючих засобів, та їх частота відображені в табл. 1.
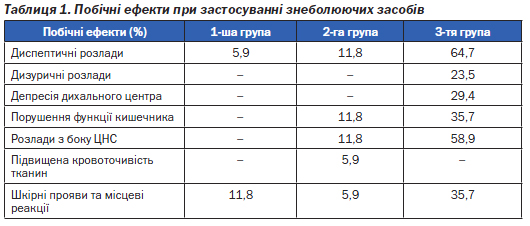
Отже, як видно з табл. 1, найбільша частота побічних реакцій зареєстрована у хворих, які отримували морфін. Це перш за все були диспептичні розлади у вигляді нудоти та блювання, збільшення терміну післяопераційного парезу кишечника, дизуричні розлади, надмірна седація пацієнта, а також депресія дихального центра. Також були зареєстровані шкірні прояви у вигляді висипань на шкірі, свербіж, в одному випадку — кропивниця. Застосування кетопрофену супроводжувалося нудотою у частини хворих, метеоризмом, шкірними висипаннями, а також головним болем. Підвищену кровоточивість із післяопераційної рани зареєстровано в одного пацієнта. Прийом Дексалгіну у частини хворих супроводжувався розвитком диспептичних розладів (нудота), а також місцевих реакцій (больовий синдром у місці введення препарату). Встановлено, що застосування Дексалгіну в мультимодальній терапії на 25 % знижує ризик та частоту побічних ефектів від наркотичних анальгетиків (із боку ЦНС, дихання, функції кишечника тощо).
Таким чином, стереоселективні НПЗП показали високу ефективність у лікуванні післяопераційного болю після різних оперативних втручань, особливо в пацієнтів старшої вікової групи. Застосування Дексалгіну дозволяє швидко та на тривалий час досягати бажаного анальгетичного ефекту за рахунок блокади ЦОГ на усіх трьох рівнях передачі болю. Препарат має високий ступінь безпеки. Застосування його у складі мультимодальної терапії після великих «відкритих» оперативних втручань дозволило вдвічі зменшити потребу в наркотичних анальгетиках, а після міні-інвазивних втручань — утричі та на чверть знизити їх негативний вплив на організм хворого.
1. Застосування специфічних інгібіторів ЦОГ-2 у периопераційному знеболенні: методичні рекомендації МОЗ України // Здоров''я України. — 2009. — № 4, 6–8, 11, 13–14.
2. Насонов Е.Л. Нестероидные противовоспалительные препараты (Перспективы применения в медицине). — М., 2000. — 262 с.
3. Свінцицький А.С. Актуальні питання діагностики та лікування гастропатій, зумовлених нестероїдними протизапальними препаратами // Здоров''я України. — 2007. — № 20/1. — С. 76-77.
4. Стороженко О.Н. Ингибиторы ЦОГ-2: истинное преимущество или активная реклама // Международный журнал медицинской практики. — 2005. — № 2. — С. 25-29.
5. Цурко В.В., Егоров И.В. Вертеброгенная боль: место нестероидных противовоспалительных средств в патогенетической терапии // Фарматека. — 2009. — № 4. — С. 49-55.
6. Carr D., Goudas L. Acute pain // Lancet. — 1999. — V. 353. — P. 2051-2058.
7. Chan F., Hung L., Suen B. Celecoxib versus diclofenac and omeprasole in reducing the risk of recurrent ulcer bleeding in patients with arthritis // N. Engl. J. Med. — 2002. — V. 347. — Р. 2104-2110.
8. Chauvin M. Postoperative patient management. Pain after surgical intervention // Presse Med. — 1999. — V. 28. — P. 203-211.
9. Wechter W.J., Mccracken J.D., Kantonci D., Murray E.D., Quiggle D., Leipold D., Gibson K., Mineyama Y., Liu Y. Mechanism of enhancement of intestinal ulcerogenity of S-aryl propionic acids by their R enantiomers in rats // Dig. Dis. Sci. — 1998. — V. 43. — P. 1264-1274.
