Газета «Новости медицины и фармации» Неврология (316) 2010 (тематический номер)
Вернуться к номеру
Эффективность ибупрофена при мигрени: рандомизированное плацебо-контролируемое исследование
Авторы: Joseph R. Codispoti, Mary Jane Prior, Min Fu, Clare M. Harte, Edward B. Nelson, Fort Washington, PA, USA
Версия для печати
Мигрень является, как правило, наследственным симптомокомплексом, включающим периодические приступы с выраженной головной болью, которым может предшествовать аура и которые сопровождаются тошнотой, рвотой, фотофобией, фонофобией и функциональной недееспособностью. Несмотря на то что причины мигрени не вполне ясны, она относится к категории довольно распространенных заболеваний: в США от нее страдают 24 млн человек в возрасте старше 12 лет [1]. Приблизительно 18 % женщин и 6 % мужчин сообщают о том, что они имеют один или несколько приступов мигрени в течение года; причем 50 и 59 % из них соответственно сообщают о наличии одного или нескольких приступов мигрени в течение месяца [1]. Социальное и экономическое влияние острой мигрени может быть довольно большим, поскольку она влечет за собой пропуск рабочих и учебных дней и негативно влияет на профессиональную и повседневную деятельность. Та или иная степень нетрудоспособности наблюдается более чем у 80 % больных с мигренью, варьируя от нарушения способности выполнять работу или повседневную деятельность до необходимости соблюдения постельного режима [1, 2]. В частности, было установлено, что 50 % женщин и 31 % мужчин, страдающих от мигрени, пропускают 3 и более рабочих дня в течение года вследствие обострения заболевания [2].
Использование безрецептурных анальгетиков для лечения мигрени достаточно распространено. Национальный опрос, проведенный в
Ибупрофен является эффективным, хорошо переносимым НПВС, который в США более 25 лет был доступен как рецептурное средство и вот уже более 15 лет используется как безрецептурный препарат. Ибупрофен — производное пропионовой кислоты с обезболивающими, противовоспалительными и антипиретическими свойствами. Механизм его действия, как и многих других НПВС, понятен не до конца, но может быть связан с ингибированием простагландинсинтетазы. Ибупрофен в течение многих лет использовался для лечения различных состояний, сопровождающихся болью, включая головную боль, зубную боль, артрит, менструальные боли и т.п. Сегодня в США в инструкции к ибупрофену указано, что для ослабления головной боли при мигрени больной должен принять 200 или 400 мг препарата.
Настоящее исследование было проведено с целью сравнить эффективность и безопасность ибупрофена в дозе 200 мг и ибупрофена в дозе 400 мг с плацебо и между собой при лечении умеренных и тяжелых головных болей при мигрени.
Методы
Дизайн исследования
Настоящее двойное слепое плацебо-контролируемое исследование, включавшее амбулаторных пациентов, было выполнено 15 исследователями на базе 17 клинических центров США. Исследование было одобрено Комиссией по биомедицинской этике, все пациенты дали письменное информированное согласие на участие в нем.
Критерии включения пациентов в исследование были следующими: 1) мужчины или женщины в возрасте 18 лет или старше; 2) наличие в анамнезе мигрени по крайней мере умеренной степени тяжести (по шкале: нет головной боли, легкая, умеренная или тяжелая головная боль), соответствующей диагностическим критериям мигрени с аурой или без нее Международного общества головной боли [10]; 3) соответствие критериям мигрени после заполнения полуструктурированного опросника для диагностики головной боли (Форма клинической оценки головной боли при мигрени — Innovative Medical Research, Балтимор, Мэриленд); 4) частота приступов мигрени не менее 1 эпизода в течение 2 месяцев, но не более 6 эпизодов в течение 1 месяца (при расчете частоты ориентировались на год, предшествовавший включению пациентов в исследование); 5) лечение предыдущих приступов мигрени с помощью безрецептурных препаратов; 6) возможность дифференцировать головную боль мигренозного характера от интервальной (связанной с мышечным напряжением) головной боли; 7) включение женщин, находящихся в менопаузе или использующих эффективную форму контрацепции не менее 3 месяцев до включения в исследование.
Критерии исключения пациентов из исследования: 1) наличие тяжелой, ограничивающей трудоспособность мигрени, при которой более 50 % приступов требуют соблюдения постельного режима или прекращения выполнения повседневной деятельности; 2) более 20 % приступов мигрени сопровождались рвотой; 3) любые другие типы головной боли, которые затрудняют дифференцировку от мигренозной боли; 4) наличие в анамнезе головных болей вследствие другой патологии или связанных с травмой головы или шеи; 5) наличие в анамнезе злоупотребления алкоголем, наркозависимости или значительных психических расстройств в течение 12 месяцев, предшествовавших включению в исследование; 6) наличие в анамнезе клинически значимых заболеваний почек и печени; неконтролируемой гипертензии; наличие клинически значимой ишемической болезни сердца, нестабильной в течение последних 6 месяцев; эпиприступов, церебральной ишемии, инфаркта, геморрагий или других заболеваний центральной нервной системы; нарушений обмена веществ, гипогликемии или диабета; злокачественных новообразований в течение последних 5 лет; активного туберкулеза; хирургических операций на желудочно-кишечном тракте, которые могут влиять на абсорбцию, метаболизм или экскрецию исследуемого препарата; 7) наличие в анамнезе аллергии или повышенной чувствительности к ибупрофену, аспирину или другим НПВС; 8) регулярное использование в настоящее время НПВС, аспирина или анальгетиков (более 15 дней в месяц) за исключением низких (325 мг/день или меньше) доз аспирина для профилактики сердечно-сосудистых заболеваний; 9) если пациенты ранее уже принимали участие в нашем исследовании, либо недавно (в течение 1 года до включения в настоящее исследование) участвовали в исследовании мигренозной головной боли под руководством McNeil, либо были участниками любого другого исследования лекарственных средств (в течение 30 дней до включения в настоящее исследование).
Пациенты продолжали принимать те лекарственные средства, которые они использовали до включения в исследование (включая препараты, используемые для профилактики мигрени). Без медицинской необходимости им не назначали каких-либо изменений в диете, физической активности или образе жизни. Хронический прием лекарственных средств, которые могли быть использованы в том числе и для профилактики мигрени — β-адреноблокаторы, эрготамины, избирательные ингибиторы обратного захвата серотонина, блокаторы кальциевых каналов — разрешали в том случае, если доза препаратов была стабилизирована в исходных условиях и не менялась во время исследования. В течение 90 дней исследования пациенты не должны были на постоянной основе принимать какие-либо препараты, которые могли влиять на количественную оценку обезболивающего эффекта (например, ацетаминофен, аспирин (за исключением низких доз аспирина ≤ 325 мг/день), ибупрофен и другие НПВС). Эпизодический прием обезболивающих средств был разрешен во время нашего исследования, за исключением 12-часового интервала, предшествующего приему тестируемого препарата. В это же время пациенты не должны были принимать противорвотные или другие лекарственные средства, которые могли повлиять на количественную оценку обезболивающего эффекта.
Каждый пациент с помощью компьютерного рандомизационного кода McNeil (размер блоков — 6) был последовательно распределен к получению лечения двойным слепым методом (каждый пациент получил блистер с таблетками и специальной кодовой меткой, состоящей из двух идентичных половин). Препараты доставляли в исследовательский центр после того, как убеждались в соответствии пациентов критериям включения в исследование и получали от них письменное информированное согласие на участие в нем. Одна из половинок кодовой метки отрывалась от блистера и прикреплялась к дневнику пациента.
Пациенты всех трех выделенных групп лечения получали блистер, содержащий две таблетки, которые были идентичными по цвету, размеру и форме. Пациенты были «слепы» к получаемому лечению в течение всего периода исследования. Ни пациенты, ни исследователи, ни лица, непосредственно вовлеченные в мониторинг исследования и просмотр данных, не знали о получаемом виде лечения до тех пор, пока коды не были рассекречены и данные не были проанализированы.
Пациенты были случайным образом распределены в одну из трех групп, получавших однократно ибупрофен 200 мг, ибупрофен 400 мг или плацебо. Пациенты получали две таблетки, предназначенные для использования в течение 90 дней исследования.
При возникновении эпизода мигрени пациенты должны были самостоятельно принять препарат. Однако перед этим им следовало убедиться, что это был именно эпизод мигрени. Для этого им необходимо было ответить на серию вопросов, охватывающих ключевые пункты диагностических критериев мигрени Международного общества головной боли; эти вопросы были помещены на обложке дневника пациентов. Если было установлено, что головная боль соответствует критериям мигрени, пациенты принимали тестируемый препарат и записывали в дневник дату и время приема. Эффективность и безопасность препарата оценивали спустя 0,5; 1; 1,5; 2; 3; 4; 5 и 6 ч после его приема.
При необходимости пациентам разрешали для купирования приступа мигрени применять заведомо эффективное лекарственное средство, однако просили по возможности не использовать его в первые 2 ч после приема тестируемого препарата. В качестве заведомо эффективного средства могли выступать любое обезболивающее средство или любой другой препарат, которые использовались больными ранее для эффективного купирования приступов мигрени. Пациентов просили иметь их в достаточном количестве, поскольку в рамках исследования они не выдавались. Пациентам напоминали, что тестируемый препарат мог содержать до 400 ибупрофена и что во время приема они не должны были превышать максимально допустимую безрецептурную суточную дозу ибупрофена — 1200 мг/день.
Пациенты оценивали и записывали в дневник следующую информацию: исходная характеристика мигрени (наличие ауры — локализация, качество, характер и сходство мигрени с типичной мигренью); исходная интенсивность боли и ее изменение в ходе исследования (0 — нет боли, 1 — легкая, 2 — умеренная, 3 — выраженная); исходная выраженность симптомов, сопутствующих мигрени (тошнота, рвота, чувствительность к свету, чувствительность к звуку), и ее изменение в ходе исследования (0 — нет симптома, 1 — легкая, 2 — умеренная, 3 — выраженная); исходная способность выполнять работу/повседневную деятельность (функциональная дееспособность) и изменение этого параметра в ходе исследования (0 — нормальная, 1 — немного нарушена, 2 — умеренно нарушена, 3 — значительно нарушена); ослабление боли во время исследования (0 — нет ослабления, 1 — немного ослаблена, 2 — умеренно ослаблена, 3 — значительно ослаблена, 4 — полностью ослаблена); появление любых побочных эффектов во время исследования. Пациенты также оценивали и записывали свое общее впечатление от принимаемого препарата спустя 6 ч после его приема, при этом использовали следующую шкалу: 0 — плохое, 1 — посредственное, 2 — хорошее, 3 — очень хорошее, 4 — отличное впечатление. Пациенты, которые выбывали из исследования, сразу же фиксировали информацию о симптомах и общем впечатлении от принимаемого препарата до самолечения другим (заведомо эффективным) препаратом.
Пациенты повторно посещали центр исследования спустя 72 ч после приема тестируемого препарата. Исследовательский коллектив проверял дневники, заполненные пациентами, на предмет наличия всей необходимой информации и уточнял любые из сообщенных побочных эффектов.
Оцениваемые параметры
В исследовании были две первичные конечные точки: количество пациентов, у которых наблюдалось уменьшение интенсивности боли от тяжелой и умеренной в исходных условиях до легкой боли или ее отсутствия спустя 2 ч после приема тестируемого препарата; разница в интенсивности боли спустя 2 ч относительно исходного уровня. Эти конечные точки были оценены как для всех пациентов, так и для пациентов, стратифицированных по исходной интенсивности боли.
Кроме того, в исследовании было оценено несколько вторичных конечных точек: разница в тяжести симптомов, связанных с мигренью (тошнота, фотофобия, фонофобия и функциональная недееспособность), между исходными значениями и 0,5–6 ч исследования; количество пациентов, у которых симптомы, связанные с мигренью, полностью исчезали ко 2-му и 6-му часу исследования; количество пациентов, у которых интенсивность боли ослаблялась до легкой или боль вовсе прекращалась к 6-му часу исследования; разница в интенсивности боли между исходными значениями и 0,5–6 ч исследования; количество пациентов без боли на 2-й и 6-й час исследования; общее впечатление пациентов от принимаемого препарата; сумма разниц в интенсивности боли относительно исходного уровня, взвешенная по интервалам времени (СРИБ); сумма баллов ослабления боли, взвешенная по интервалам времени (СБОБ); частота использования другого заведомо эффективного препарата к 6-му часу исследования; частота развития рвоты в течение 6 ч исследования.
Статистические методы
Требуемый размер выборки оценили по пилотным данным с помощью параметрических методов. Оказалось, что 600 пациентов (по 200 пациентов в каждой группе лечения) будет достаточно, чтобы между группами, получающими лечение ибупрофеном в дозе 200 мг и ибупрофеном в дозе 400 мг, и между группами, получающими лечение ибупрофеном в дозе 200 мг и плацебо, выявить 15% разницу в количестве пациентов, у которых в течение 2 ч исследования интенсивность мигренозной боли уменьшится до легкой степени или же боль полностью прекратится. При этом α-уровень принимали равным 0,05 (двусторонний), мощность — 80 %.
Демографические и исходные характеристики между группами лечения в случае непрерывных переменных сравнивали с помощью однофакторного дисперсионного анализа, в случае дихотомических переменных — с помощью критерия хи-квадрат. Для того чтобы сравнить частоты развития побочных эффектов, использовали точный критерий Фишера.
Для анализа эффективности лечения, назначенного в начале исследования, выполняли три парных сравнения: ибупрофен 200 мг и плацебо, ибупрофен 400 мг и плацебо, ибупрофен 200 мг и ибупрофен 400 мг. Все статистические критерии, описанные ниже, применяли к каждой из сравниваемых пар при α-уровене, равном 0,05 (двусторонний).
Критерий Кохрана — Мантеля — Ханзеля для общей взаимосвязи, стратифицированный по исходному уровню интенсивности боли, был использован для парных сравнений одной из первичных конечных точек исследования — количества пациентов, у которых в течение 2 ч исследования интенсивность мигренозной боли уменьшалась до легкой степени или же полностью прекращалась. Этот же критерий был использован для выполнения подобных сравнений применительно к другим интервалам времени. Для анализа другой первичной конечной точки исследования — разницы в интенсивности боли спустя 2 ч лечения относительно исходного уровня — был применен трехфакторный дисперсионный анализ (вид терапии, исходная интенсивность боли, исследователь); парные сравнения между группами лечения выполняли с помощью критерия наименьшей значимой разницы Фишера.
Количество пациентов, у которых боль полностью исчезала, анализировали с помощью критерия Кохрана — Мантеля — Ханзеля для общей взаимосвязи, стратифицированного по исходному уровню интенсивности боли. Разницу в интенсивности боли в других точках времени, отличных от 2 ч, и СРИБ анализировали точно так же, как это было сделано для 2 ч. Для анализа ослабления боли в каждой точке времени использовали двухфакторный дисперсионный анализ (вид терапии, исследователь); СБОБ анализировали аналогичным образом.
Для пациентов, у которых исходно имелись симптомы, сопутствующие мигрени (тошнота, фотофобия, фонофобия и функциональная недееспособность), разницу в тяжести этих симптомов относительно исходного уровня для каждой точки времени в течение 6 ч исследования анализировали точно так же, как и разницу в интенсивности боли (см. выше), за тем исключением, что в дисперсионную модель вместо исходной интенсивности головной боли включали исходную тяжесть каждого отдельного симптома. Парные сравнения между группами лечения по количеству пациентов, у которых тошнота, фотофобия, фонофобия и функциональная недееспособность полностью исчезли, в каждой точке времени были выполнены с помощью критерия Кохрана — Мантеля — Ханзеля для общей взаимосвязи, стратифицированного по исходному уровню каждого симптома. Частоту рвоты за весь период исследования сравнивали с помощью точного критерия Фишера.
Парные сравнения между группами лечения по общему впечатлению пациентов от принимаемого препарата выполняли с помощью расширенного критерия Кохрана — Мантеля — Ханзеля со средними модифицированными ридит-баллами, стратифицированными по исходному уровню интенсивности боли. Частоту приема другого, заведомо эффективного средства в течение 6 ч исследования анализировали с использованием критерия Кохрана — Мантеля — Ханзеля, стратифицированного по исходному уровню интенсивности боли.
Результаты
Пациенты
В общей сложности с марта 1998 по июль
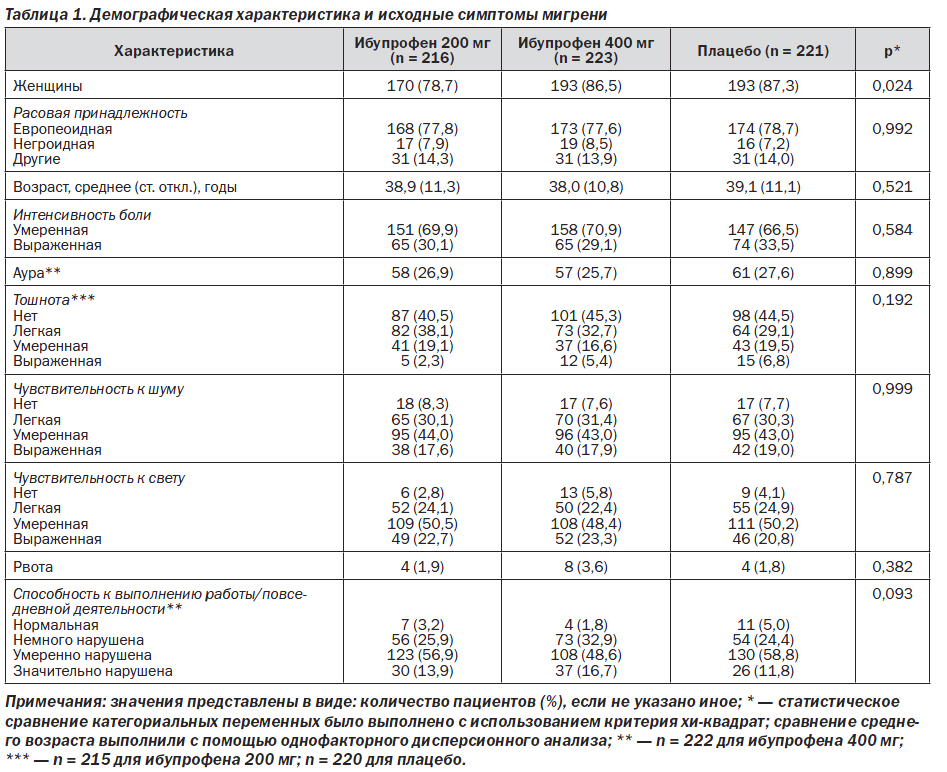
В табл. 1 представлены демографические характеристики всех пациентов, включенных в анализ (при его выполнении ориентировались на изначально назначенное лечение). Раса и возраст были сравнимы во всех трех группах. Средний возраст пациентов составил 38,6 года, 515 пациентов (78,0 %) отнесли себя к европеоидной расе. Среди пациентов, включенных в исследование, женщин было 556 (84,2 %). Это согласуется с тем фактом, что мигрень чаще встречается у женщин, нежели у мужчин. При сравнении выделенных групп больных по полу были обнаружены статистически значимые различия (р = 0,024); в группе с ибупрофеном 200 мг наблюдался более низкий процент женщин (78,7 %), чем в двух других группах. Данное различие было расценено как не имеющее клинического значения.
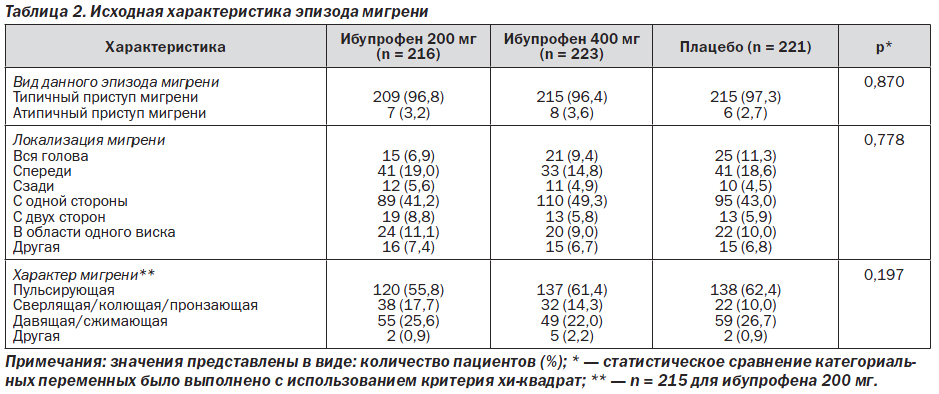
Между группами не было статистически значимых различий в исходных симптомах мигрени (табл. 2). Исследуемые пациенты имели умеренные и тяжелые мигренозные боли и значительные функциональные нарушения. В общей сложности 30,9 % пациентов имели выраженную интенсивность боли и 26,7 % сообщили о наличии ауры во время данного эпизода мигрени. В исходных условиях тошнота наблюдалась у 56,5 % пациентов, чувствительность к шуму — у 92,1 %, чувствительность к свету — у 95,8 %, рвота — у 2,4 %. Способность работать или выполнять повседневную деятельность была умеренно или значительно нарушена у 68,9 % пациентов. Как следует из табл. 2, 96,8 % пациентов расценили свой эпизод мигрени как имеющий типичное для мигрени течение. Другие исходные характеристики данного приступа мигрени не различались между выделенными группами больных и также представлены в табл. 2.
Влияние на ослабление и интенсивность боли
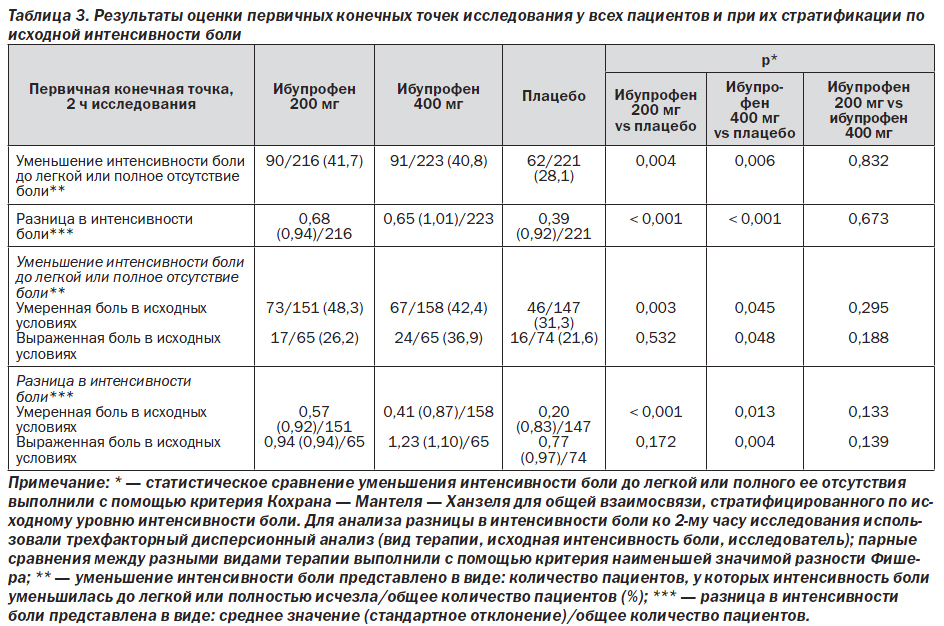
В табл. 3 представлена информация о достижении первичных конечных точек у всех пациентов, а также у пациентов, стратифицированных по исходной интенсивности головной боли. Достоверно (p ≤ 0,006) большее количество пациентов, получавших ибупрофен 200 мг и ибупрофен 400 мг, сообщили о наличии легкой боли или о полном отсутствии боли ко 2-му часу исследования (41,7 и 40,8 % соответственно) по сравнению с плацебо (28,1 %). Достоверных различий между группами с разными дозами ибупрофена обнаружено не было. Из табл. 3 видно, что аналогичные результаты были получены и в отношении средней разницы в интенсивности боли спустя 2 ч по сравнению с исходным уровнем.
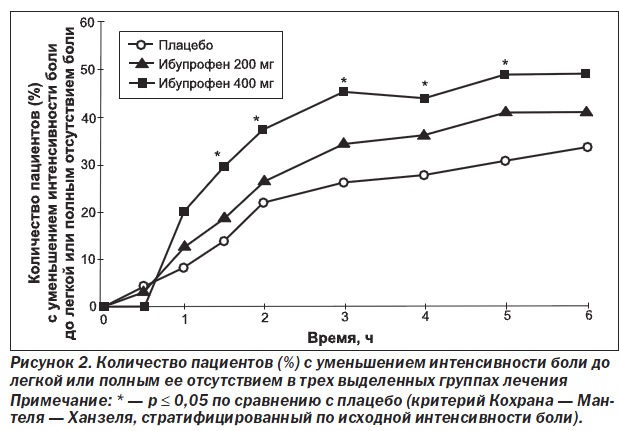
На рис. 2 для каждого интервала времени представлено количество пациентов, у которых интенсивность боли была уменьшена до легкой или боль полностью отсутствовала. Рис. 2 свидетельствует о том, что разница, отмечаемая между группами с ибупрофеном и плацебо, была статистически достоверной начиная с 1,5 ч и удерживалась таковой в течение всего 6-часового периода.
Статистически достоверные различия между группами с ибупрофеном и плацебо в отношении средней разницы в интенсивности боли наблюдались начиная с 1 ч после приема препаратов (данные не представлены).
Результаты оценки первичных конечных точек исследования для пациентов, стратифицированных по исходной интенсивности боли, также представлены в табл. 3. Результаты, полученные для пациентов с умеренной интенсивностью головной боли в исходных условиях (69,1 % от общего количества пациентов) были аналогичны тем, которые были получены для всей популяции пациентов.
Как свидетельствуют данные, представленные в табл. 3 и на рис. 3, результаты оценки первичных конечных точек у пациентов с выраженной интенсивностью боли в исходных условиях (30,9 % от общего количества пациентов) отличались от тех, которые были получены для всей популяции больных. Ибупрофен в дозе 400 мг был статистически эффективнее в улучшении первичных конечных точек исследования по сравнению с плацебо, в то время как ибупрофен в дозе 200 мг не был лучше плацебо. Достоверно (р = 0,048) большее количество пациентов с выраженной интенсивностью мигренозной боли в исходных условиях, получавших ибупрофен в дозе 400 мг, сообщили об ослаблении боли до легкой или полном ее исчезновении ко 2-му часу исследования (36,9 %) по сравнению с теми пациентами, которые получали плацебо (21,6 %). Аналогично средняя разница в интенсивности боли спустя 2 ч относительно исходного уровня при лечении пациентов с исходно выраженной интенсивностью боли была достоверно (р = 0,004) выше в группе с ибупрофеном 400 мг (1,23) по сравнению с группой, получавшей плацебо (0,77).
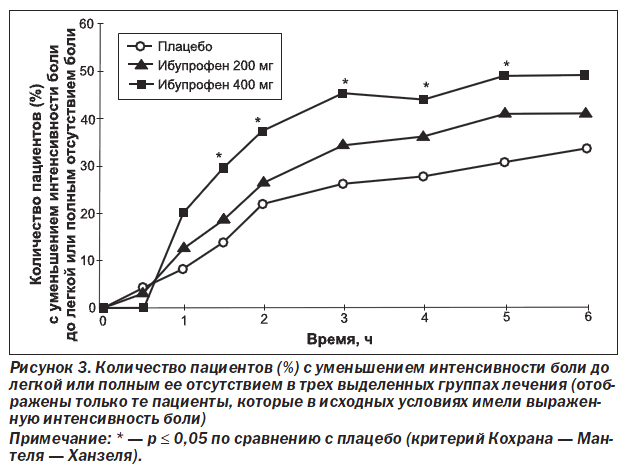
Среди пациентов с исходно выраженной интенсивностью боли результаты оценки обеих первичных конечны точек исследования были численно выше в группе с ибупрофеном 400 мг по сравнению с ибупрофеном 200 мг; однако эти различия не были статистически значимыми. Так, например, между группами с ибупрофеном 400 мг и ибупрофеном 200 мг наблюдалась 11% разница в уменьшении интенсивности боли до легкой или полном ее исчезновении.
Влияние на симптомы, связанные с мигренью, и другие вторичные конечные точки
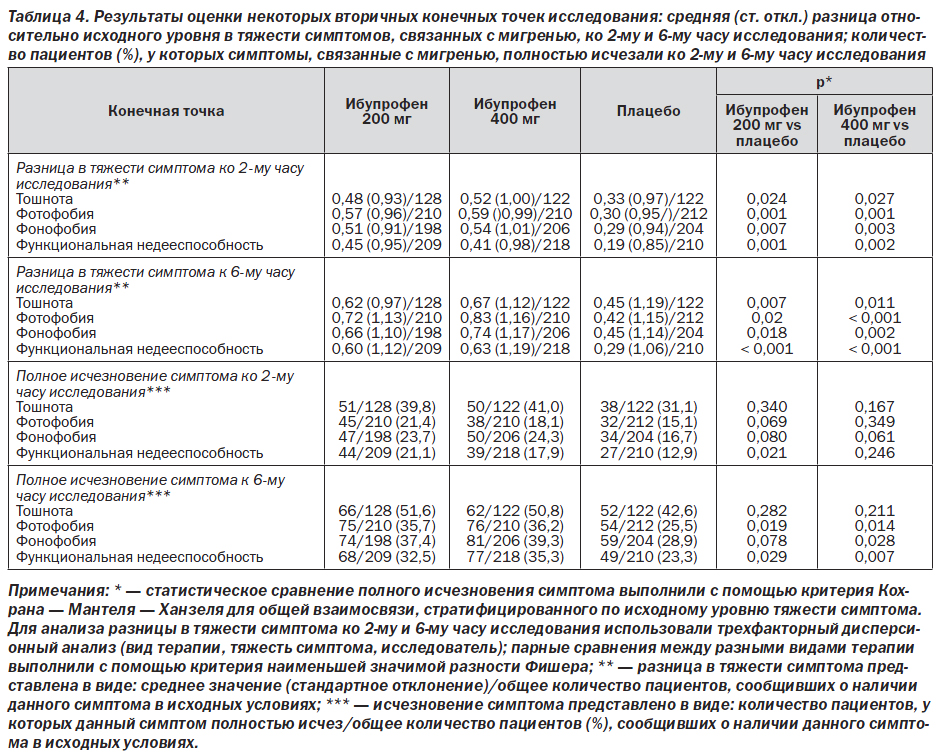
Сравнение выделенных групп больных по средней разнице относительно исходного уровня в тяжести симптомов, связанных с мигренью (тошнота, фотофобия, фонофобия, функциональная дееспособность), спустя 2 и 6 ч после приема тестируемых препаратов представлено в табл. 4.
В этот анализ были включены только те пациенты, которые имели данные симптомы в начале исследования. Пациенты, принимавшие любую дозу ибупрофена, при сравнении с пациентами, принимавшими плацебо, всегда имели достоверно большее среднее снижение тяжести симптомов, связанных с мигренью, на 2-й и 6-й час исследования (р ≤ 0,027). Однако между двумя дозами ибупрофена по этим конечным точкам исследования достоверных различий обнаружено не было.
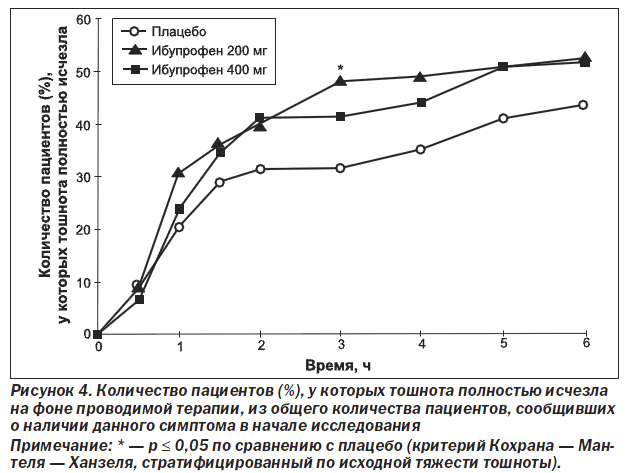
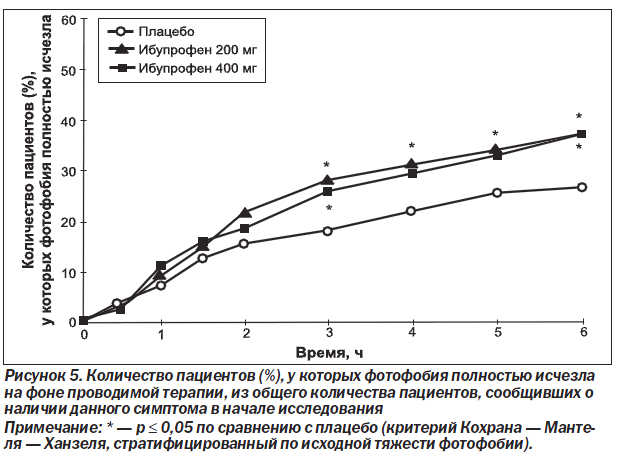
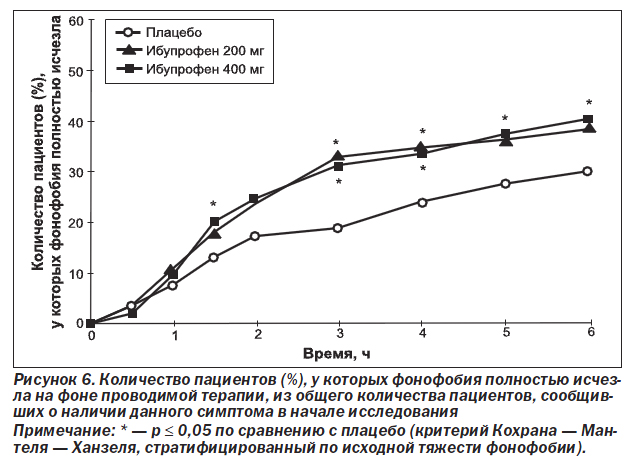
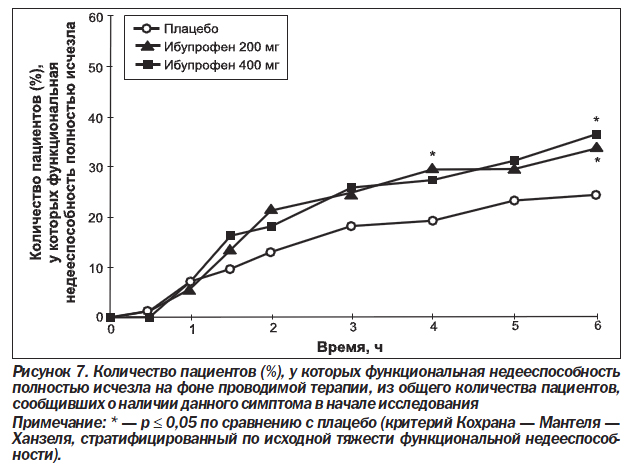
Количество пациентов, у которых симптомы, связанные с мигренью, полностью исчезали ко 2-му и 6-му часу исследования, также было проанализировано для тех пациентов, которые имели эти симптомы в исходных условиях (табл. 4). Результаты, полученные для данных конечных точек, были сопоставимы с результатами, полученными для средних изменений относительно исходного уровня в тяжести симптомов, связанных с мигренью. Большее количество пациентов, получавших ибупрофен 200 мг или ибупрофен 400 мг, сообщали о полном исчезновении симптомов, связанных с мигренью, по сравнению с пациентами, получавшими плацебо. При этом количество пациентов, сообщавших о полном исчезновении фотофобии и функциональной недееспособности, было достоверно (р ≤ 0,029) выше в обеих группах с ибупрофеном по сравнению с плацебо к 6-му часу исследования. Для тошноты и фонофобии на 2-й и 6-й час и для фотофобии и функциональной недееспособности на 2-й час количество пациентов, сообщающих об исчезновении симптомов, было всегда больше (в ряде случаев это достигало статистической значимости) в группе пациентов, получавших любую из доз ибупрофена, по сравнению с теми пациентами, которые получали плацебо. Между двумя группами пациентов, получавших разные дозы ибупрофена, не было обнаружено статистически достоверных различий в симптомах, связанных с мигренью, на 2-й и 6-й час исследования. На рис. 4–7 графически отображено количество пациентов, сообщающих об исчезновении симптомов, связанных с мигренью, в течение всего времени исследования. Хотя наблюдаемые различия не всегда достигали статистической значимости, они все же подчеркивают преимущество лечения ибупрофеном по сравнению с плацебо во все отметки времени, начиная с 1,5–2 ч исследования.
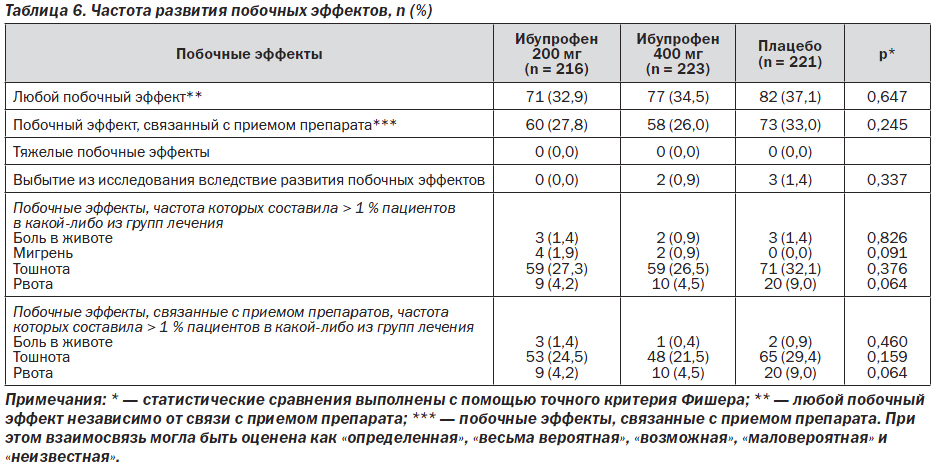
В табл. 5 представлены результаты оценки всех остальных вторичных конечных точек исследования.
По ним не было обнаружено статистически достоверных различий между двумя группами пациентов, получавших ибупрофен. Зато достоверно (p ≤ 0,003) большее количество пациентов, получавших ибупрофен 200 мг или ибупрофен 400 мг, сообщали об уменьшении интенсивности боли до легкой или о полном ее прекращении к 6-му часу исследования (45,8 и 48,9 % соответственно) по сравнению с теми пациентами, которые получали плацебо (31,7 %). Аналогично разница в интенсивности боли между исходными значениями и показателями к 6-му часу исследования была достоверно (p < 0,001) большей у пациентов, принимавших ибупрофен 200 мг или ибупрофен 400 мг (0,84 и 0,88 соответственно), по сравнению с теми пациентами, которые получали плацебо (0,47). Эти данные указывают на то, что положительный эффект ибупрофена, выявленный на 2-м часу исследования, продолжал поддерживаться в течение всех 6 ч исследования. Достоверно (р ≤ 0,031) большее количество пациентов, получавших ибупрофен в любой дозе, сообщали об отсутствии боли на 2-й и 6-й час исследования по сравнению с теми пациентами, которые получали плацебо. Как следует из табл. 5, сопоставимые результаты о превосходстве ибупрофена были сообщены и для других вторичных конечных точек, включая среднее общее впечатление пациентов от принимаемого препарата, среднюю СРИБ и СБОБ, частоту использования другого, заведомо эффективного препарата к 6-му часу исследования и частоту развития рвоты в течение 6 ч исследования.
Выбывание пациентов из исследования и безопасность
В общей сложности из исследования выбыли 280 пациентов (42,4 %), получавших тестируемые препараты. Все пациенты, кроме 8, рано выбыли из исследования в связи с необходимостью приема другого, заведомо эффективного лекарственного средства. Другие причины, которые привели к прекращению участия пациентов в исследовании, включали развитие рвоты в течение 30 мин после приема тестируемого препарата (n = 3) и развитие побочных эффектов (n = 5). У всех 5 пациентов (2 в группе с ибупрофеном и 3 в группе с плацебо), выбывших из исследования вследствие развития побочных эффектов, развивалась или тошнота, или рвота — возможные проявления мигрени.
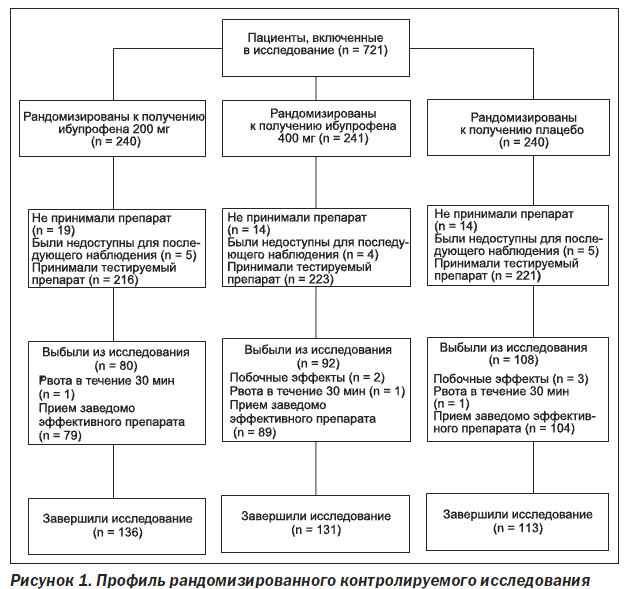
Как следует из табл. 6, между тремя группами лечения не было статистически достоверных различий в частоте сообщаемых побочных эффектов; всего об их развитии сообщили 34,8 % пациентов.
Ни в одном случае не было сообщено о развитии тяжелых побочных эффектов. Наиболее частыми побочными эффектами были нарушения со стороны желудочно-кишечного тракта (в основном тошнота и рвота), о чем сообщили 31,7 % пациентов; при этом достоверных различий между тремя группами лечения обнаружено не было (р = 0,370). В табл. 6 представлены только те побочные эффекты, которые наблюдались не менее чем у 1 % пациентов в какой-либо из групп лечения.
Комментарии
В настоящее большое рандомизированное двойное слепое плацебо-контролируемое исследование были включены амбулаторные пациенты с головной болью вследствие мигрени умеренной и выраженной степени тяжести. Было показано, что ко 2-му часу лечения ибупрофен в статистически достоверно большей степени, нежели плацебо, ослабляет мигренозную боль, о чем свидетельствуют результаты оценки двух первичных конечных точек исследования — количества пациентов с болью легкой интенсивности или полным отсутствием боли и средней разницы в интенсивности боли относительно исходного уровня. Статистически достоверные различия в пользу преимущества обеих доз ибупрофена над плацебо для средней разницы в интенсивности боли были обнаружены спустя 1 ч терапии, а для пациентов с болью легкой интенсивности или полным ее отсутствием — спустя 1,5 ч терапии. Причем различия продолжали быть достоверными до окончания исследования (до 6 ч терапии). Было также показано, что ибупрофен статистически достоверно более эффективен, чем плацебо, в отношении всех клинически значимых вторичных конечных точек исследования, отражающих ослабление боли.
Результаты настоящего исследования свидетельствуют о том, что улучшение симптомов, связанных с мигренью (тошнота, фотофобия, фонофобия, функциональная недееспособность), сопутствует ослаблению мигренозной боли. Уменьшение средней тяжести симптомов, связанных с мигренью, было статистически достоверно более выраженным при использовании обеих доз ибупрофена по сравнению с плацебо начиная с 1,5–2 ч лечения. Различия продолжали быть достоверными до 6-го часа исследования. Результаты, касающиеся количества пациентов, у которых симптомы, связанные с мигренью, полностью исчезали, также свидетельствовали в пользу преимущества ибупрофена (хотя и не всегда достигали уровня статистической значимости). Тот факт, что средняя тяжесть симптомов уменьшалась умеренно, связан со значительным числом пациентов, у которых симптомы были легкими в исходных условиях. Так, исходно количество легких симптомов варьировало от 24,8 % для фотофобии до 58,9 % для тошноты. Поскольку основным критерием включения пациентов в исследование было наличие в исходных условиях головной боли умеренной или выраженной интенсивности, то исходная тяжесть симптомов, связанных с мигренью, могла варьировать от их полного отсутствия до выраженной тяжести. Поскольку у тех пациентов, которые имели легкую выраженность симптомов в исходных условиях, она могла быть снижена только до полного отсутствия симптомов, это могло смещать общее снижение в средней тяжести симптомов к меньшим средним изменениям.
Данные нашего исследования показывают, что ибупрофен эффективен при обоих уровнях исходной интенсивности головной боли. Результаты, полученные для пациентов с исходно умеренной головной болью (69,1 % от общего количества пациентов) в отношении первичных конечных точек исследования, были подобны тем результатам исследования, которые были получены на всей популяции больных: обе дозы ибупрофена были статистически достоверно эффективнее плацебо, в то время как эффективность их между собой достоверно не различалась. У пациентов с исходно выраженной интенсивностью головной боли ибупрофен в дозе 400 мг был статистически достоверно эффективнее плацебо в отношении первичных конечных точек исследования, в то время как ибупрофен в дозе 200 мг не был. Результаты, полученные для пациентов с выраженной интенсивностью мигренозной боли, подтверждают более высокую эффективность от использования при этом состоянии ибупрофена в дозе 400 мг по сравнению с ибупрофеном в дозе 200 мг. Это согласуется с той информацией, которая указана в инструкции к использованию ибупрофена при мигрени (США): пациенты должны принимать от 200 до 400 мг препарата.
В ходе исследования не было обнаружено достоверных различий в частоте развития побочных эффектов среди трех групп лечения. В целом о развитии побочных эффектов сообщили 34,8 % пациентов. Не было сообщено ни об одном серьезном побочном эффекте. Ибупрофен хорошо переносится и в течение многих лет на безрецептурной основе использовался для лечения различных болевых состояний, включая головную боль, зубную боль, артрит, менструальные боли и т.д.
Результаты исследования могут быть распространены на большой сегмент больных, страдающих мигренью. Из исследования были исключены только те больные, у которых наблюдалась тяжелая, ограничивающая трудоспособность мигрень с более чем 50 % приступов, требующих соблюдения постельного режима или прекращения выполнения повседневной деятельности, а также больные, у которых 20 % приступов мигрени сопровождались рвотой. Фактически 30,9 % больных исходно имели выраженную интенсивность головной боли. Кроме того, хотя у многих пациентов сопутствующие мигрени симптомы были легкой степени, у ряда пациентов они были более тяжелыми: у 8,6 % наблюдалась выраженная тошнота, у 23,3 % — выраженная фотофобия, у 19,7 % — выраженная фонофобия, у 14,6 % — выраженное нарушение функциональной дееспособности.
Наши результаты согласуются с данными других исследований мигрени, в которых тестировали такие однокомпонентные анальгетики, как ацетаминофен [8] и ибупрофен [11, 12]. Несмотря на трудности, возникающие при сравнении лечебных эффектов между разными исследованиями, хочется отметить, что наблюдаемый в нашем исследовании лечебный эффект — разница в количестве пациентов, у которых интенсивность боли становилась легкой или боль полностью прекращалась ко 2-му часу лечения — между группой с ибупрофеном 200 мг и группой с плацебо (13,6 %), группой с ибупрофеном 400 мг и группой с плацебо (12,7 %) был аналогичен лечебному эффекту, о котором сообщено в аннотации к одному из других рандомизированных плацебо-контролируемых исследований ибупрофена при мигрени: между группой с ибупрофеном 400 мг и плацебо — 14 %, между ибупрофеном 600 мг и плацебо — 16 % [11]. В другом рандомизированном плацебо-контролируемом исследовании было обнаружено, что лечебный эффект между ибупрофеном 200 мг и плацебо составил 14 %, а между ибупрофеном в дозе 400 мг/600 мг и плацебо — 22 % [12]. Процитированные здесь данные указывают на нецелесообразность увеличения дозы ибупрофена более 400 мг при лечении мигрени.
При наличии надлежащей инструкции однокомпонентный, хорошо переносимый, самостоятельно принимаемый препарат, эффективно устраняющий головную боль при мигрени, является весьма полезным и желанным продуктом для соответствующей категории больных. Безрецептурный ибупрофен представляет собой альтернативу безрецептурным комбинированным препаратам, используемым для лечения мигрени, которые в дополнение к ацетаминофену содержат аспирин и кофеин (последние два ингредиента активно избегаются рядом пациентов).
Таким образом, результаты настоящего исследования свидетельствуют о том, что однократная доза ибупрофена является эффективной и хорошо переносится при лечении головной боли вследствие мигрени. Препарат оказывает сопоставимое влияние на первичные и вторичные конечные точки исследования, отражающие ослабление боли. Также важно отметить, что ибупрофен оказывает положительное влияние на симптомы, связанные с мигренью, — тошноту, фотофобию, фонофобию и функциональную недееспособность (хотя эти эффекты и не всегда достигают статистической значимости).
Оригинал статьи «Efficacy of Nonprescription Doses of Ibuprofen for Treating. Migraine Headache. A Randomized Controlled Trial» опубликован в журнале «Headache», 2001, Volume 41, Issue 7
Перевод к.м.н. А.В. Савустьяненко