Газета «Новости медицины и фармации» Неврология (316) 2010 (тематический номер)
Вернуться к номеру
Эффективность габапентина при дискогенной пояснично-крестцовой радикулопатии
Авторы: О.С. Левин, д.м.н., проф., И.А. Мосейкин, Российская медицинская академия последипломного образования, г. Москва
Версия для печати
Пояснично-крестцовая радикулопатия — один из наиболее тяжелых вариантов вертеброгенных болевых синдромов, который характеризуется особенно интенсивной и стойкой болью, обычно сопровождающейся резким ограничением подвижности [1, 5, 27]. Примерно у трети пациентов с радикулопатией интенсивная боль, ограничивающая трудоспособность, сохраняется более 6 нед. Неудивительно, что, хотя на долю радикулопатии приходится около 5 % случаев боли в спине, именно она является одной из самых частых причин стойкой утраты трудоспособности [1, 3, 4, 25].
Основной причиной пояснично-крестцовой радикулопатии является грыжа межпозвонкового диска, реже (как правило, в более пожилом возрасте) она вызвана сдавлением корешка в области латерального кармана, межпозвонкового отверстия при спондилезе вследствие формирования остеофитов, гипертрофии суставных фасеток, связок или иных причин [2, 4, 5, 25]. Стойкое поддержание болевого синдрома при грыже может быть связано не столько с компрессией корешка, сколько с вторичными нейрофизиологическими и обменными процессами, которые запускаются внедрением диска в эпидуральное пространство и воздействием высвобождаемого из пульпозного ядра материала на нервную ткань [5]. По данным клинико-нейровизуализационных сопоставлений, интенсивность боли не коррелирует со степенью протрузии диска или механической деформацией корешка. Как показывают экспериментальные данные, ключевую роль в развитии корешковой боли могут играть и воспалительные изменения в компримированном корешке и (что особенно важно) в спинномозговом ганглии [27]. Итогом являются ирритация, интра- и экстраневральный отек корешка или блокада проведения по нему. Важную роль играют и изменения нейрофизиологических характеристик нервных волокон, нейронов спинномозговых ганглиев и задних рогов спинного мозга [1, 3, 5].
Клинически пояснично-крестцовая радикулопатия характеризуется стойкой или пароксизмальной интенсивной болью, хотя бы эпизодически иррадиирующей в дистальную зону дерматома (например, при приеме Лассега), выраженным мышечно-тоническим синдромом, нередко сопровождающимся сколиотической деформацией позвоночника, изменением чувствительности (болевой, температурной, вибрационной и др.) в соответствующем дерматоме, снижением или выпадением сухожильных рефлексов, замыкающихся через соответствующий сегмент спинного мозга, гипотонией и слабостью мышц, иннервируемых данным корешком [4, 5].
У большинства пациентов с дискогенной радикулопатией консервативная терапия позволяет добиться существенного ослабления и регрессирования болевого синдрома, и лишь в сравнительно небольшой части случаев неосложненной дискогенной радикулопатии, характеризующихся особенно интенсивным стойким болевым синдромом, резким ограничением подвижности, резистентностью к консервативной терапии, показано оперативное вмешательство. В недавно опубликованном исследовании [20] было отмечено, что, хотя раннее оперативное лечение при дискогенной радикулопатии приводит к более быстрому ослаблению боли, в дальнейшем (спустя полгода, год и 2 года) оно не имеет каких-либо преимуществ перед консервативной терапией и не снижает риск хронизации боли. С другой стороны, более позднее оперативное лечение по эффективности не уступает более раннему [20].
Что касается консервативной терапии дискогенной радикулопатии, то она подвергается обоснованной критике [4, 9, 10]. Дело в том, что традиционно применявшаяся и до сих пор популярная тракция поясничного отдела оказалась неэффективной в контролируемых исследованиях [10]. Было установлено [6], что эпидуральные блокады с кортикостероидами хотя и могут способствовать ослаблению боли, оказывают лишь кратковременный эффект. Оказалась несостоятельной и практика длительного постельного режима: при радикулопатии, как и при других вариантах боли в спине, более быстрое возвращение к повседневной активности предупреждает хронизацию боли [25].
Основой консервативной терапии остаются НПВС, миорелаксанты и некоторые другие нелекарственные методы, главным образом воздействующие на ноцицептивный компонент боли, в том числе массаж, лечебная гимнастика, воздействие на миофасциальный синдром, некоторые приемы мануальной терапии и т.д. [4, 10]. Тем не менее эффективность подобной терапии ограничена и не позволяет в значительном числе случаев достаточно быстро купировать свойственный радикулопатии интенсивный болевой синдром, что может быть условием более быстрого восстановления. Это заставляет искать дополнительные возможности усилить обезболивающий эффект, прежде всего за счет методов, действующих на невропатический компонент боли [7, 21].
Учитывая смешанный характер болевого синдрома при дискогенной радикулопатии, включающего ноцицептивный, невропатический, а часто и психогенный компонент, воздействие на невропатический компонент боли представляется весьма перспективным [7, 8, 13]. Тем не менее до сих пор эффективность средств, традиционно применяемых при невропатической боли (антиконвульсанты, антидепрессанты и другие), у пациентов с болью в спине остается недостаточно доказанной [10].
В частности, предметом дискуссий остается целесообразность применения антиконвульсантов у больных с радикулопатией и болью в спине в целом. Антиконвульсанты проявили себя как действенное средство лечения болевого синдрома при краниальных невралгиях, постгерпетической невралгии, полиневропатии. Однако данные исследований их эффективности у больных с болью в спине противоречивы. Такая противоречивость результатов во многом предопределяется гетерогенностью и многообразием вариантов боли в спине, вариабельностью их механизмов и, возможно, различными сроками начала лечения.
Целью настоящего исследования явилась оценка эффективности широко применяемого в последнее десятилетие для лечения болевых синдромов антиконвульсанта габапентина у пациентов с дискогенной пояснично-крестцовой радикулопатией в зависимости от сроков начала лечения.
Материал и методы
В исследование были включены 25 пациентов (14 женщин и 11 мужчин) с дискогенной радикулопатией.
Диагноз радикулопатии устанавливался при наличии корешкового болевого синдрома (иррадиация боли в дистальную часть дерматома: спонтанная и/или при приеме Лассега) плюс как минимум один симптом выпадения: снижение (выпадение) соответствующего сухожильного рефлекса, снижение болевой, температурной (холодовой), тактильной или вибрационной чувствительности в зоне дерматома либо слабость мышц, иннервируемых данным корешком.
Наличие грыжи диска соответствующей локализации устанавливалось при помощи КТ или МРТ пояснично-крестцового отдела. В исследование вошли 14 пациентов с радикулопатией L5 и 11 пациентов с радикулопатией S1. Средний возраст больных составил 46,8 ± 9,1 года. Выраженность болевого синдрома при оценке по ВАШ колебалась от 5 до 9 баллов (в среднем 7,5 балла).
Критериями исключения были наличие опухолевого, инфекционно-воспалительного или иного заболевания позвоночника, требующего специфического лечения, выраженная деформация позвоночника, компрессия спинного мозга, другие сопутствующие неврологические заболевания, психиатрические заболевания, серьезные или нестабильные соматические заболевания (тяжелые заболевания печени, сердечно-сосудистой системы, легких или почек, декомпенсированный сахарный диабет, онкологические заболевания).
Больные были разделены на 2 группы: в 1-ю группу вошли 12 пациентов с длительностью обострения болевого синдрома не более 1 мес., во 2-ю группу — 13 пациентов с длительностью обострения более 1 мес. Соответственно, в 1-й группе лечение габапентином было начато в течение 1-го месяца обострения, во 2-й группе — спустя 1 мес. и более от начала обострения.
С 1-го по 12-й день Габапентин назначался в возрастающей дозе. Начиная с 13-го дня пациенты принимали препарат в дозе 1800 мг. В отсутствие улучшения в течение последующих 2 нед. доза могла быть увеличена до 3600 мг в сутки. Общая длительность исследования составила 8 нед. В обеих группах пациентам, помимо габапентина, была назначена стандартная терапия, включавшая НПВС, ЛФК, физиотерапию и массаж. В течение предшествующей недели и в ходе всего исследования пациентам не назначались миорелаксанты, витамины группы В, антидепрессанты, другие антиконвульсанты, лечебные блокады.
Между группами не было значимых различий по полу, возрасту, проводимой терапии, включая дозу НПВС.
Ни один из пациентов ранее не подвергался оперативному вмешательству. Средняя доза габапентина в 1-й группе оказалась 2110 ± 370 мг в сутки, во 2-й группе — 2200 ± 395 мг/сутки.
Для оценки эффективности габапентина использовалась шкала общего клинического впечатления (CGI), предусматривавшая следующие градации: ухудшение, отсутствие изменений, минимальное улучшение, умеренное улучшение, значительное улучшение.
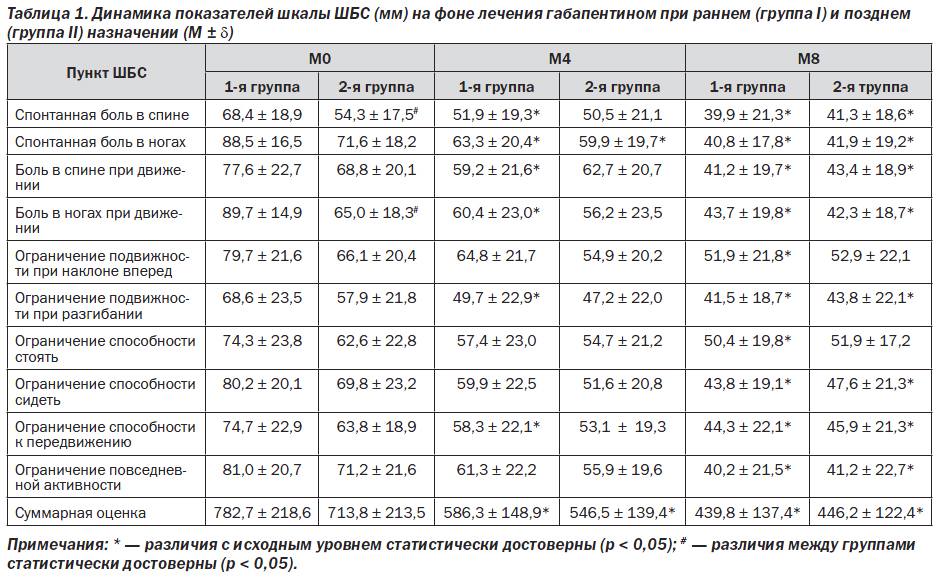
Шкала боли в спине (ШБС), устроенная по принципу визуальной аналоговой шкалы (ВАШ), предусматривала оценку больными следующих симптомов: спонтанной боли в спине, в ногах, боли при движении в спине и ногах, ограничение подвижности при наклоне вперед и при разгибании, ограничение способности сидеть, стоять, ограничение способности передвижения и повседневной активности; больной оценивал выраженность каждого из этих симптомов, отметив ее точкой на отрезке в
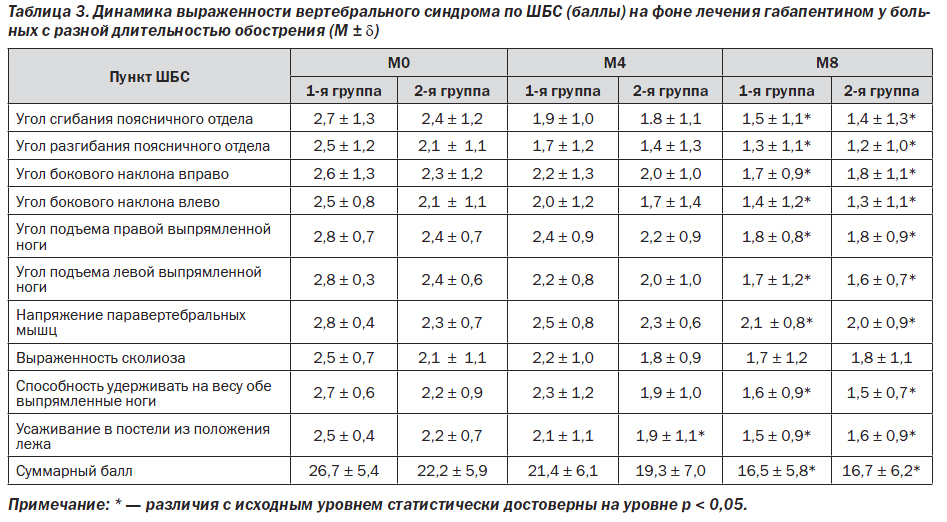
Шкала вертебрального синдрома, представляющая собой модификацию шкалы G. Waddel и соавт. [3, 25], предусматривала оценку по 4-балльной системе (от 0 до 3 баллов) 10 показателей: угла сгибания и разгибания поясничного отдела, угла бокового наклона вправо и влево, угла подъема выпрямленной правой и левой ноги, напряжения паравертебральных мышц и выраженности сколиоза, способности удерживать на весу обе выпрямленные ноги, усаживания в постели из положения лежа; суммарная оценка колебалась от 0 до 30 баллов.
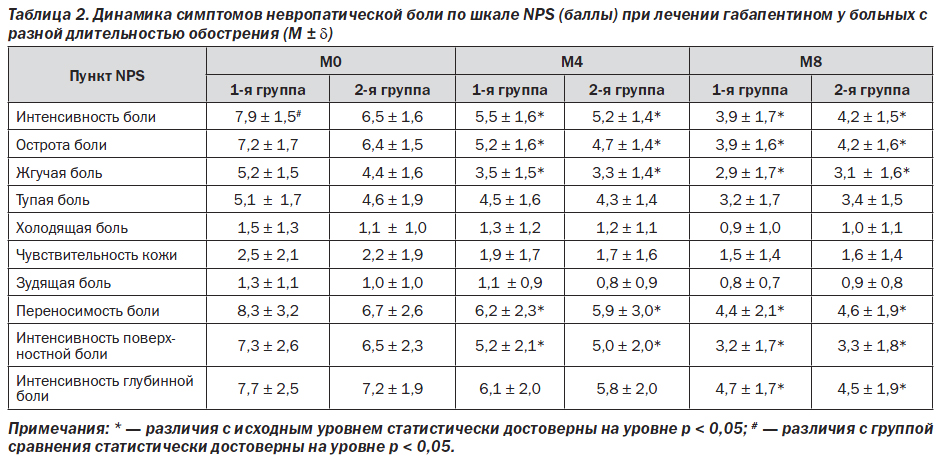
Шкала невропатической боли (NPS) [12], позволяющая оценивать выраженность 10 характеристик болевого синдрома: интенсивность, остроту, выраженность жгучей, тупой, холодящей и зудящей боли, чувствительность кожи в зоне боли, переносимость боли, интенсивность поверхностной и глубинной боли.
Оценка состояния больных проводилась в момент включения в исследование (МО), на 4-й (М4) и 8-й неделе (М8). Первичной конечной точкой явилась динамика болевого синдрома и ограничения подвижности, оцениваемых с помощью ШБС, по отношению к исходному уровню. Дополнительно оценивались динамика вертебрального синдрома, невропатических характеристик боли, степень улучшения по шкале CGI, а также различия в динамике симптомов в зависимости от сроков начала терапии габапентином.
Статистическая обработка проводилась с использованием дискриптивных методов и модели ANOVA. Оценка изменения показателей в сравнении с исходным уровнем и контрольной группой проводилась с помощью t-теста (уровень достоверности р < 0,05). Статистическая обработка осуществлялась с помощью стандартного программного пакета Statistica 6.
Результаты
К концу исследования оценка по ШБС достоверно снизилась в обеих группах (табл. 1). К 4-й неделе суммарная оценка по ШБС в 1-й группе снизилась в среднем на 25 %, во второй группе — на 23 %, к концу 8-й недели суммарная оценка по ШБС снизилась в 1-й группе на 44 % по сравнению с исходным уровнем, а во 2-й группе — на 37 %. В первые 4 нед. применения габапентина в группе с более ранним назначением препарата отмечена более быстрая положительная динамика боли в спине (как спонтанной, так и при движении) и степени ограничения способности к передвижению. К концу 8-й недели исследования в обеих группах достоверная положительная динамика отмечена по следующим показателям ШБС: спонтанная боль в спине и ногах, боль в спине и ногах при движении, ограничение разгибания и способности сидеть, ограничение способности к передвижению и повседневной активности.
Отмечалась тенденция к более высокой эффективности раннего назначения габапентина (в течение 1-го месяца после начала обострения) в сравнении с его поздним назначением. В результате показатели 2-й группы, которые исходно были ниже, чем показатели 1-й группы, к концу 8-й недели с ними сравнялись (рис. 1).
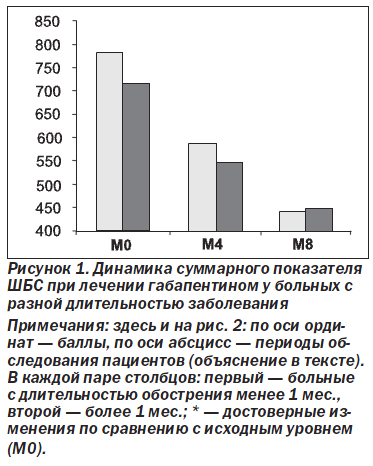 Оценка симптомов невропатической боли с помощью шкалы NPS (табл. 2) показала, что при лечении габапентином в обеих группах отмечена положительная динамика таких параметров боли, как ее острота, интенсивность, в том числе жгучей, поверхностной и глубинной боли, а также переносимость боли. При этом, если исходно в первой группе показатели невропатической боли были выше (достоверная разница отмечена только по общей интенсивности боли), то к концу 4-й и особенно 8-й недели показатели в обеих группах сравнивались, что свидетельствует о более быстром регрессировании боли в 1-й группе.
Оценка симптомов невропатической боли с помощью шкалы NPS (табл. 2) показала, что при лечении габапентином в обеих группах отмечена положительная динамика таких параметров боли, как ее острота, интенсивность, в том числе жгучей, поверхностной и глубинной боли, а также переносимость боли. При этом, если исходно в первой группе показатели невропатической боли были выше (достоверная разница отмечена только по общей интенсивности боли), то к концу 4-й и особенно 8-й недели показатели в обеих группах сравнивались, что свидетельствует о более быстром регрессировании боли в 1-й группе.
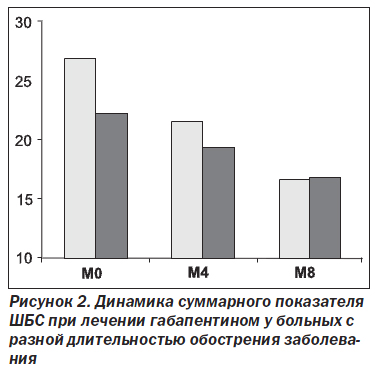
Выраженность вертебрального синдрома к концу 8-й недели снизилась в обеих группах примерно в равной степени (табл. 3). Тем не менее и по данным показателям тенденция к более высоким оценкам в 1-й группе к концу исследования нивелировалась, и соответствующие показатели в обеих группах оказались близки (рис. 2).
По данным шкалы CGI, при раннем применении габапентина к концу 8-й недели исследования значительный эффект отмечен у 3 пациентов (25 % пациентов, вошедших в исследование), удовлетворительный (умеренный эффект) — у 4 (34 %), минимальное улучшение — у 2 (16 %), отсутствие улучшения — у 3 (25 %). При позднем начале лечения габапентином значительный эффект отмечен у 2 (17 %) больных, удовлетворительный — у 4 (34 %), минимальное улучшение — у 4 (34 %), отсутствие эффекта — у 3 (26 %). Таким образом, при раннем применении габапентина клинически значимый результат отмечен у 59 % пациентов, тогда как при более позднем его назначении — у 51 % пациентов. На эффективность терапии не влияют возраст, исходная интенсивность боли, наличие симптомов выпадения, выраженность вертебрального синдрома.
 В ходе исследования отмечена хорошая переносимость габапентина. Сонливость отмечена у 2 (8 %) пациентов, головокружение — у 2 (8 %), легкая отечность ног — у 1 (4 %). Показатели переносимости габапентина были сходны в обеих группах.
В ходе исследования отмечена хорошая переносимость габапентина. Сонливость отмечена у 2 (8 %) пациентов, головокружение — у 2 (8 %), легкая отечность ног — у 1 (4 %). Показатели переносимости габапентина были сходны в обеих группах.
Обсуждение
Полученные результаты подтверждают эффективность и безопасность габапентина в лечении невропатического компонента боли у больных с дискогенной пояснично-крестцовой радикулопатией. Более того, они свидетельствуют в пользу целесообразности возможно более раннего назначения габапентина после развития болевого эпизода.
Исходное состояние пациентов с длительностью болевого эпизода более 1 мес. по целому ряду параметров (выраженности болевого синдрома, степени ограничения подвижности) было более благоприятным, чем у пациентов с относительно недавним развитием болевого синдрома, что, вероятно, отражает частичное регрессирование симптомов под влиянием предшествовавшей консервативной терапии или естественного хода событий. Однако к концу исследования по большинству оценивавшихся параметров состояние пациентов обеих групп сравнялось, что может отражать более быстрое последующее регрессирование симптомов при раннем начале лечения габапентином. Вряд ли это можно объяснить тенденцией к спонтанному восстановлению, свойственной определенной части случаев радикулопатии, поскольку в этом случае более благоприятное течение скорее можно было бы ожидать у пациентов с большей длительностью обострения.
Применение средств, воздействующих на α2δ-субъединицу кальциевых каналов, прежде всего габапентина, у больных с радикулопатией представляется особенно перспективным в свете экспериментальных данных, которые показывают, что при повреждении нерва (перевязке или пересечении спинномозговых корешков или седалищного нерва) у крыс в результате up-регуляции развивается гиперэкспрессия α2δ-субъединицы кальциевых каналов в клетках спинного мозга и спинномозговых ганглиев, что коррелирует с явлениями аллодинии [18]. Можно предполагать, что аналогичный процесс происходит и вследствие сдавления спинномозгового корешка грыжей диска. Селективно связываясь с α2δ-субъединицей кальциевых каналов, габапентин тормозит высвобождение возбуждающих нейромедиаторов и тем самым блокирует передачу болевых импульсов на уровне задних рогов, а возможно, и на более высоких уровнях ЦНС [8, 22]. В силу этого более раннее применение габапентина может противодействовать развитию центральной сенситизации и формированию «болевой памяти», поддерживающих болевой синдром, и тем самым способствовать его регрессированию [8].
К настоящему времени проведен ряд клинических исследований эффективности габапентина при боли в спине. Так, Н. Hansen [14] в открытом исследовании, включавшем 80 пациентов с болью в спине, отметил при назначении габапентина в дозе от 900 до 2400 мг в сутки уменьшение болевого синдрома в среднем на 46 %. J. Rosenberg и соавт. [22] также установили положительное влияние габапентина на невропатические болевые синдромы. По данным М. Saracoglu и соавт. [23], габапентин был полезен у пациентов с болями в спине, сохраняющимися после операционного лечения, обеспечивая стойкое ослабление болевого синдрома. Но G. МсCleane [19] в плацебо-контролируемом исследовании, включавшем 62 пациента с люмбоишиалгией, отметив на фоне приема габапентина в дозе до 1200 мг в сутки в течение 6 нед. уменьшение иррадиации боли в ногу и боли при движении, не установил ослабления боли в пояснице, улучшения подвижности или снижения потребности в анальгетиках. К. Yildrim и соавт. [26] в 2-месячном плацебо-контролируемом исследовании, включавшем 50 пациентов с хронической радикулопатией, показали, что прием габапентина в дозе 900–3600 мг в сутки способствует уменьшению интенсивности и иррадиации боли, ограничения сгибания и нарушений чувствительности. Таким образом, результаты К. Yildrim и соавт. (2003) наиболее близки к полученным нами данным.
Что касается других антиконвульсантов, то их эффективность при боли в спине изучена недостаточно. Так, в одном из исследований [16] показано, что топирамат (в средней дозе 200 мг в сутки) способствует уменьшению боли при хронической радикулопатии на 20 %, но ценой высокой частоты побочных эффектов (86 %), в результате закончили исследование лишь 16 (26 %) пациентов из 42, вступивших в него. В небольшом открытом исследовании [11] показан пороговый терапевтический эффект ламотриджина при боли в спине, однако и в этом исследовании отмечена высокая частота побочных явлений. Лишь в одном небольшом открытом исследовании [17] у пациентов с ишиалгией исследована эффективность карбамазепина. На сегодняшний день нет также доказательных исследований, подтверждающих эффективность прегабалина, окскарбазепина, вальпроевой кислоты при пояснично-крестцовой радикулопатии или других вариантах боли в спине [10].
Вариабельность результатов упомянутых исследований эффективности антиконвульсантов при боли в спине может объясняться, по крайней мере частично, гетерогенностью исследуемых групп больных и различными сроками назначения препаратов после появления или обострения болевого синдрома. Особенностью проведенного нами исследования являются относительная гомогенность исследуемой популяции больных (включались только пациенты с клиническими и нейровизуализационными признаками дискогенной радикулопатии, несомненно имеющие невропатический компонент боли), комплексность в оценке эффективности препарата и, что представляется особенно важным, оценка влияния времени назначения препарата на его эффективность.
Вместе с тем следует предостеречь от экстраполяции полученных результатов на всю группу пациентов с болью в спине, у большинства из которых невропатический компонент боли отсутствует (так называемая «аксиальная боль в спине»). В последние годы некоторые авторы, основываясь на результатах, полученных с помощью специальных опросников, высказывают мнение о том, что невропатический компонент может быть представлен более широко, чем это считалось ранее, в том числе в тех случаях хронической боли в спине, где нет признаков вовлечения спинномозговых корешков. Между тем опросники для выявления невропатической боли следует рассматривать лишь как скрининговый инструмент, в силу недостаточной специфичности они не могут считаться методом окончательной диагностики невропатической боли, которая, в соответствии с современными, более строгими критериями, требует клинического и/или инструментального подтверждения поражения невральных структур, в данном случае — спинномозговых корешков или ганглиев (например, снижение болевой, температурной, особенно холодовой, тактильной или вибрационной чувствительности в соответствующем дерматоме либо электрофизиологических признаков вовлечения корешка) [15, 24].
В заключение следует подчеркнуть, что наше исследование следует рассматривать как предварительное, поскольку небольшое число пациентов и открытый характер ограничивают доказательность его результатов. Тем не менее полученные данные могут свидетельствовать о перспективности раннего применения габапентина при дискогенной радикулопатии.
1. Веселовский В.П. Практическая вертеброневрология и мануальная терапия. — Рига, 1991. — 30-145.
2. Левин О.С. Диагностика и лечение неврологических проявлений остеохондроза позвоночника // Consilium medicum. — 2004. — 6. — 547-554.
3. Левин О.С. Современные подходы к диагностике и лечению боли в спине. — М., 2006. — 62.
4. Поднуфарова Е.В. Боль в пояснично-крестцовой области: диагностика и лечение // Рус. мед. журн. — 2004. — 10. — 581-584.
5. Попелянский Я.Ю., Штульман Д.Р. Боли в шее, спине и конечностях // Болезни нервной системы / Под ред. Н.Н. Яхно, Д.Р. Штульман. — М.: Медицина, 2001. — 293-316.
6. Аrтоп С., Argoff С., Samuels J. et al. Use of epidural steroid injections to treat radicular lumbosacral pain // Neurology. — 2007. — 68. — 723-729.
7. Baron R., Binder A. How neuropathic is sciatica? The mixed pain concept // Orthopade. — 2004. — 33. — 568-575.
8. Baron R. Mechanisms of disease: neuropathic pain // Nat. Clin. Pract. Neurol. — 2006. — 2. — 95-106.
9. Bogduk N., McGuirk B. Medical management of acute and chronic low back pain. —
10. Chang V., Gonzalez P., Akuthota V. Evidence-informed management of chronic low back pain with adjunctive analgetics // Spine J. — 2008. — 8. — 21-27.
11. Eisenberg E., Damunini G., Hoffer E. et al. Lamotrigin for intractable sciatica // Eur. J. Pain. — 2003. — 7. — 485-491.
12. Galer B.S., Jensen M.P. Development and preliminary validation of a pain measure specific to neuropathic pain: neuropathic pain scale // Neurology. — 1997. — 48. — 332-338.
13. Gorman D.J., Кат Р.А., Brisby H. et at. When is spinal pain «neuropathic»? // Orthop. Clin. N. Am. — 2004. — 35. — 73-84.
14. Hansen H. Use of gabapentin in the management of low back pain // South Med. J. — 1997. — 90, Suppl. 1.
15. Jensen M.P., Dworkin R.H., Gammaitoni A.R. et al. Assessment of pain quality in chronic neuropathic and nociceptive pain clinical trials with neuropathic pain scale // J. Pain. — 2005. — 6. — 98-106.
16. Khoromi S., Patsalides A., Parada S. et al. Topiramate in chronic lumbar radicular pain // J. Pain. — 2005. — 6. — 829-836.
17. Lovell J. Carbamazepine and sciatica // Aust. Fam. Physician. — 1992. — 21. — 784-786.
18. Luo Z.D., Calcutt N., Higuera E. et al. Injury type-specific calcium channel α2δ-l subunit up-regulation in rat neuropathic pain models correlates with antiallodynic effects of gabapentin // J. Pharmacol. Exper. Ther. — 2002. — 303. — 1199-1205.
19. McCleane G.J. Does gabapentin have an analgesic effect on background, movement and referred pain? A randomised, double-blind, placebo controlled study // Pain Clin. — 2001. — 13. — 103-107.
20. Peul W.C., van den Hout W.B., Brand R. et at. Prolonged conservative care versus early surgery in patients with sciatica caused by lumbar disc herniation: two year results of a randomised controlled trial // BMJ. — 2008. — 336. — 1355-1358.
21. Rathwell J. Rational use of interventional modalities for the treatment of pain of spinal origin. Pain 2008-Updated review. —
22.
23. Saracoglu M., Nacir В., Gene H. The Efficacy of Gabapentin in Patients with Failed Back Surgery // J. Musculoskeletal. Pain. — 2006. — 13, Issue 4. — 27-32.
24. Treede R.-D., Jensen T.S., Campbell J.N. et al. Neuropathic pain. Redefinition and a grading system for clinical and research purposes // Neurology. — 2008. — 70. — 1630-1635.
25. Waddel G. The back pain revolution. —
26. Yildirim K., Sisecioglu M., Karatay S. et al. The effectiveness of gabapentin in patients with chronic radiculopathy // Pain. Clin. — 2003. — 15. — 213-218.
27. Zhang J.-M., Munir M. Radicular Low Back Pain What Have We Learned from Recent Animal Research? // Anesthesiology. — 2008. — 108. — 5-6.