Газета «Новости медицины и фармации» Гастроэнтерология (323) 2010 (тематический номер)
Вернуться к номеру
Гастроезофагеальна рефлюксна хвороба і вагітність
Авторы: І.М. Скрипник, д.м.н., професор, Г.С. Маслова. Кафедра внутрішніх хвороб та медицини невідкладних станів факультету післядипломної освіти, Вищий державний навчальний заклад України «Українська медична стоматологічна академія», м. Полтава
Версия для печати
Гастроезофагеальну рефлюксну хворобу (ГЕРХ) більшість вчених вважають хворобою третього тисячоліття, що зумовлено наявністю чіткої тенденції до збільшення її поширеності в усьому світі. Так, у розвинених країнах Європи та США на періодично виникаючу печію скаржаться до 20–40 % дорослого населення [10, 22]. Проте лише 2 % із них лікуються з приводу рефлюкс-езофагіту. Провідним симптомом ГЕРХ є печія — відчуття болю пекучого характеру в нижній загрудинній або епігастральній ділянці, що виникає після їжі під час фізичного навантаження з нахилами тіла вперед або в положенні лежачи і зумовлений надходженням вмісту шлунку та дванадцятипалої кишки у стравохід. Відчуття хворим печії більше двох разів на тиждень значно збільшує ймовірність ГЕРХ і, безумовно, негативно впливає на якість життя. Проте менша частота симптому печії і навіть повна його відсутність не виключає ГЕРХ [1, 14, 20].
Печія є однією із найбільш поширених скарг у жінок в період вагітності, її відчувають від 30–50 % вагітних [9] до 80 % [15, 16]. Її частота і вираженість змінюється із збільшенням строку вагітності. Так, за даними С.Г. Буркова [1], Е.А. Ушкалової [14], у першому триместрі вагітності відчуття печії спостерігається у 50 % жінок, в другому — у 25 %, в третьому — у 10 % жінок. J.M. Marrero [18] при обстеженні 607 вагітних, навпаки, зазначив збільшення інтенсивності і частоти виникнення печії із збільшенням терміну гестації: у першому триместрі на печію скаржились 22 % вагітних, в другому — 39 %, у третьому — 72 %. У переважної більшості жінок печія вперше з''являється саме на фоні вагітності і зникає після її завершення. Частина лікарів вважають «печію вагітних» симптомом вагітності, який не потребує особливої уваги й лікування. Хоча печія під час вагітності може бути тривалою, інтенсивною, здатна значно погіршувати якість життя пацієнток. Також слід пам''ятати, що у жінок із ГЕРХ вагітність внаслідок свого впливу на шлунково-кишковий тракт (ШКТ), значно посилює прояви рефлюкс-езофагіту. Отже, визначення тактики ведення вагітних із ГЕРХ потребує особливої уваги.
ГЕРХ як самостійна нозологічна одиниця була визнана у жовтні 1997 року у м. Генваль (Бельгія) на міжнародному міждисциплінарному конгресі гастроентерологів та ендоскопістів. Термін «ГЕРХ» замінив термін «рефлюкс-езофагіт», введений в 1946 році Еллісоном. Згідно з Генвальським консенсусом, існують дві форми ГЕРХ (ендоскопічно позитивна і ендоскопічно негативна), розроблені чіткі рекомендації щодо діагностики й лікування ГЕРХ у країнах Європи. В 1999 році ГЕРХ була внесена до Міжнародної класифікації хвороб Х перегляду:
Під ГЕРХ розуміють хронічне рецидивуюче захворювання, яке зумовлене ретроградним надходженням у стравохід шлункового або дуоденального вмісту, що призводить до виникнення характерних симптомів (печія, біль за грудиною, дисфагія) та зниження якості життя пацієнтів незалежно від наявності або відсутності ушкоджень слизової оболонки (СО) стравоходу. Наявність симптому печії 2 рази на тиждень і більше дозволяє запідозрити у хворого ГЕРХ.
Етіологія і патогенез ГЕРХ
Виникненню ГЕРХ сприяють стрес, фізична праця та фізичні вправи з нахилами вперед, підвищена вага тіла, паління, вагітність, приймання медикаментозних засобів (нітрати, антагоністи кальцію, β-адреноблокатори, спазмолітики, антидепресанти, кофеїн, пероральні контрацептиви, нестероїдні протизапальні засоби і т.д.), продукти харчування (кава, шоколад, жирна й гостра їжа, алкогольні напої, фруктові соки і т.д.).
До основних етіологічних чинників розвитку ГЕРХ зараховують:
Недостатність нижнього сфінктера стравоходу (НСС) є основною причиною рефлюксу шлункового та дуо-денального вмісту до стравоходу. За нормальних умов він виникає рідко, на короткий період часу одноразово терміном не більше 5 хвилин, а сумарно не перевищує 1 годину на добу (5 % загального часу доби). Отже, більшість часу у стравоході спостерігаються нормальні показники рН 5,5–7,0. Патологічним прийнято вважати рефлюкс шлункового та дуоденального вмісту у стравохід, якщо у порожнині стравоходу рН < 4 спостерігається понад 4 години. В нормі тиск у НСС складає 20,8 ±
Другим важливим фактором у виникненні ГЕРХ є агресивні компоненти шлункового та дуоденального вмісту (жовчні кислоти, лізолецитин), що за умов порушення кліренсу і резистентності слизового бар''єру стравоходу призводять до розвитку у його СО запально-деструктивних процесів [2, 4].
Таким чином, у патогенезі ГЕРХ велике значення має не тільки рівень закислення стравоходу, а й фактори його захисту: адекватний стравохідний кліренс і резистентність СО. Під кліренсом стравоходу розуміють його здатність усувати зрушення внутрішньостравохідного рН у кислий бік, що здійснюється за рахунок двох механізмів: перистальтичної хвилі і нейтралізуючої дії слини, до складу якої входять муцин, епідермальний фактор росту, безмуцинний протеїн, простагландин Е2. За нормальних умов у відповідь на рефлюкс шлункового або дуоденального вмісту у стравохід відбувається збільшення продукції слини за допомогою стравохідно-слинних рефлекторних шляхів. На початкових стадіях ГЕРХ підвищується продукція слини, що змінюється зниженням її синтезу і відповідно недостатністю нейтралізуючої функції слини, зменшується синтез муцину, безмуцинного протеїну, епідермального фактора росту при збереженій концентрації простагландину Е2 [2, 4].
Резистентність СО стравоходу забезпечується трьома рівнями захисту: передепітеліальним, епітеліальним, пост-
епітеліальним. Передепітеліальний рівень представлений шаром щільного захисного слизу із достатнім вмістом іонів гідрокарбонату, який здатний нейтралізовувати йони водню. До епітеліального рівня належить шар епітеліальних клітин, нормальне функціонування яких прямо пропорційно залежить від дотримання рН 7,3–7,4 внутрішньоклітинно. Недостатня ефективність передепітеліального рівня захисту призводить до зсуву рН у кислий бік з порушенням міжклітинних зв''язків та руйнуванням епітеліоцитів. На цьому етапі включається активна проліферація базальних клітин СО стравоходу, яка перешкоджає виникненню виразкових дефектів. Відновлення епітелію стравоходу не можливо без адекватного кровопостачання СО. Тобто саме мікроциркуляторне русло забезпечує постепітеліальний рівень захисту, що впливає на резистентність СО стравоходу [4, 10].
Патогенетичні механізми розвитку печії при вагітності
Під час вагітності внаслідок гормональної перебудови значно збільшується концентрація жіночих статевих гормонів, особливо прогестерону, який чинить релаксуючу дію на гладкі м''язи, в тому числі й ШКТ. Відмічається зниження тонусу НСС, що відповідно сприяє рефлюксу вмісту шлунку і дванадцятипалої кишки у стравохід [3]. R. Nagler, H.M. Spiro [19] під час манометрії стравоходу в 39 вагітних (20 відчували печію, 19 не відчували печії) виявили зниження тонусу НСС у 11 (55 %) жінок із симптомом печії і у 4 (21 %) жінок без симптомів. Причиною гіпотонії НСС автори вважають зростання рівня естрогенів і прогестерону.
Під впливом гормонів гестації також відбувається зниження чутливості хеморецепторів до серотоніну й гістаміну на всьому протязі ШКТ, що призводить до зменшення активності його перистальтики, у тому числі й стравоходу [5]. Крім цього, на фоні збільшення розмірів матки зростає внутрішньочеревний тиск. Таким чином, провідними механізмами виникнення рефлюксу шлункового й дуоденального вмісту у стравохід є вплив прогестерону на НСС і амплітуду перистальтичних хвиль, а також зростання внутрішньочеревного тиску [9]. Відповідно інтенсивність суб''єктивного відчуття печії наростає поряд із збільшенням терміну гестації. Слід пам''ятати, що вагітність провокує загострення уже існуючих хронічних запальних захворювань ШКТ (гастрит, панкреатит, холецистит та інші), які можуть впливати на розвиток симптому печії.
Класифікація
У Генвальському консенсусі (1997) запропоновано виділяти дві форми ГЕРХ: ендоскопічно позитивну ГЕРХ та ендоскопічно негативну, або неерозивну ГЕРХ (НЕРХ).
Монреальським консенсусом (2005) визначена класифікація клінічних проявів ГЕРХ [10]:
Стравохідні симптоми:
Позастравохідні симптоми:
Найбільш зручною у щоденній практиці є клінічна класифікація:
З метою оцінки тяжкості езофагіту при ендоскопічному дослідженні користуються Лос-Анджелеською класифікацією, згідно з якою виділяють A, B, C і D стадії ураження:
При проведенні ендоскопічного дослідження хворим із симптомами ГЕРХ ерозивно-виразкові ураження СО стравоходу виявляються лише у 30–50 % пацієнтів. Таким чином, за даними різних досліджень, у спектрі ГЕРХ ерозивна форма захворювання складає приблизно 35 %, неерозивна — 60 % і стравохід Барретта — 5 % [10].
Доведено, що причиною розвитку ерозивної форми ГЕРХ є тривале закислення вмісту стравоходу (до 50 рефлюксів за добу). Слід відмітити, що не існує залежності між інтенсивністю симптоматики ГЕРХ і ступенем ураження СО при ендоскопічному дослідженні. Проте саме ерозивна форма часто прогресує й призводить до розвитку ускладнень, таких як пептична виразка стравоходу, кровотеча, стриктури стравоходу та стравохід Барретта.
На відміну від ерозивної форми ГЕРХ, неерозивна зумовлена не патологічною дією хлористоводневої кислоти на СО стравоходу, а підвищеною чутливістю стравоходу до кислоти, тому, незважаючи на вираженість клінічної симптоматики, НЕРХ не має схильності до прогресування і розвитку ускладнень [10].
Діагностика ГЕРХ
На даний час не існує єдиного загальновизнаного золотого стандарту діагностики ГЕРХ. Першим етапом діагностики повинно бути опитування пацієнта, збір анамнезу й об''єктивне обстеження. Необхідно звернути увагу на вік, сімейний анамнез за ГЕРХ і раком стравоходу, на наявність тривожних симптомів: дисфагію, одинофагію, зниження маси тіла, анемію, ознаки шлунково-кишкової кровотечі, нудоту, блювоту.
За рекомендаціями міжнародних консенсусів, за відсутності тривожних симптомів у пацієнтів віком до 40 років за умов тривалості симптому печії до 5 років езофагогастродуоденоскопію можна не проводити. Проте на підставі виявлення печії мінімум два рази на тиждень протягом 4–8 тижнів і більше повинен виставлятись попередній діагноз ГЕРХ. Після цього лікар повинен призначити емпірично лікування інгібіторами протонної помпи (ІПП) у повній терапевтичній дозі.
Методи діагностики ГЕРХ [10]
Неінвазивні:
Таким чином, вагітним, що скаржаться на печію, за умови відсутності тривожних симптомів не рекомендовано проведення інвазивних методів.
Лікування
Базисним лікуванням ГЕРХ, як і всіх кислотозалежних захворювань, є тривала кислотосупресивна терапія з використанням препаратів груп ІПП, Н2-блокаторів гістамінових рецепторів (Н2-БГР), антацидів, прокінетиків.
Існує дві стратегії лікування хворих на ГЕРХ — step up і step down. Терапія step up передбачає призначення спочатку більш слабких протикислотних препаратів з переходом за необхідністю на більш потужні, а терапія step down — перехід від більш потужних кислотосупресивних препаратів до більш слабких (табл. 1).
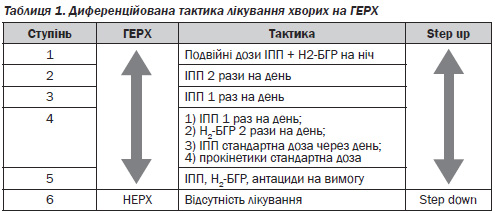
Основною умовою для загоєння ерозивних уражень СО стравоходу є дотримання правила Белла — підтримка рН > 4 всередині стравоходу протягом 18 годин і більше. Даним вимогам відповідають лише ІПП. Отже, для ерозивних форм ГЕРХ рекомендується стратегія step down: лікування розпочинають з призначення ІПП у подвійній дозі з додатковим використанням Н2-БГР за наявності епізодичного кислотного прориву.
При лікуванні вагітних із симптомами печії складність полягає в тому, що за етичними обставинами не існує мультицентрових рандомізованих контрольованих досліджень щодо впливу ІПП і Н2-БГР на організм вагітної жінки і плода. Проводились окремі когортні дослідження фармацевтичними компаніями. Таким чином, рекомендації з призначення останніх двох груп препаратів при вагітності базуються на даних FDA (Food and Drug Administration (США)).
За ступенем безпечності FDA розподіляє всі лікарські засоби на п''ять категорій: A, B, C, D та X. Дані FDA базуються на системній біодоступності препаратів, а також імовірності викликати вроджені вади розвитку в людини або тварин. ІПП і Н2-БГР віднесені FDA до категорії B — лікарські засоби, що приймались обмеженою кількістю вагітних і жінок дітородного віку без яких-небудь доказів їх впливу на частоту вроджених аномалій або пошкоджуючої дії на плід. Проте призначення ІПП тваринам (кролики, пацюки) у дозах, які у 16–18 разів вищі за ті, що призначаються людям, не показало змін фертильності і тератогенної дії на плід [3].
Рекомендації з лікування ГЕРХ під час вагітності (штат Аризона):
Рекомендації щодо модифікації способу життя у вагітних, на наш погляд, слід доповнити наступними положеннями:
При відсутності ефекту від зміни стилю життя і дієти необхідно розпочати приймання антацидів. Виходячи з власного досвіду, можна рекомендувати призначення алюмінієво-магнієвих антацидів, враховуючи їх високий профіль безпеки (альмагель нео, фосфалюгель, ма-алокс). Антациди адсорбують як хлористоводневу кислоту та пепсин, так і солі жовчних кислот та лізолецитин [7]. За рахунок утворення захисної плівки на поверхні шлунка, стимуляції продукції простагландинів антациди сприяють підвищенню секреції слизу, покращенню мікроциркуляції, тобто виявляють цитопротекторну дію. Рівне співвідношення алюмінію гідроксиду й магнію гідроксиду в даних препаратах швидко усуває печію, біль в епігастральній ділянці, не викликаючи побічних ефектів. Наявність у складі альмагелю нео симетикону усуває здуття живота, що досить часто турбує вагітних внаслідок синдрому надлишкового бактеріального росту. Альмагель нео, маалокс, фосфалюгель приймають по 10–15 мл через 1 годину після їжі 3 рази на добу і 4-й раз — перед сном. Можливе приймання антацидів у режимі «за вимогою» не більше 4 разів на добу.
Подібний до антацидів механізм дії мають препарати на основі альгінової кислоти (гевіскон), які не впливають на кислотопродукцію [8], утворюючи на поверхні СОШ щільну гель-плівку, до складу якої входить джерело СО2 — калію гідрокарбонат та кальцію гідрокарбонат, який зв''язує молекули альгінату. Саме утворення захисного бар''єра, відтворення необхідних умов для секреції простагландинів забезпечують цитопротективний ефект [13], утримання рН на рівні 4 протягом 4,5 години і більше. S.W. Lindow et al. [17] у відкритому багатоцентровому дослідженні довели високу ефективність та безпечність використання альгінатного препарату гевіскону форте з метою усунення відчуття печії та регургітації у вагітних. Призначати доцільно гевіскон форте у дозі 10 мл/добу у режимі «на вимогу».
За умов відсутності ефекту від антацидів та альгінатів доцільно додати до лікування Н2-БГР. Найбільшу ефективність та профіль безпеки серед Н2-БГР має препарат третього покоління — фамотидин, який на відміну від Н2-БГР І та ІІ покоління є високо-селективним антисекреторним засобом, має значно більшу активність (у 40 разів активніший за циметидин та у 8–10 разів активніший за ранітидин) та тривалістю дії (до 12 годин) [4, 10]. Головною перевагою фамотидину порівняно з препаратами його групи можна вважати практично повну відсутність взаємодії з системою цитохрому Р450, завдяки чому він не впливає на взаємодію лікарських засобів [6]. Також він не знижує активності алкогольдегідрогенази у печінці, не збільшує рівень пролактину, не викликає антиандрогенного ефекту. Фамотидин досить добре переноситься пацієнтами. Побічні ефекти у вигляді незначних шлунково-кишкових розладів, головного болю, висипання на шкірі спостерігаються у 0,43 % випадків [2, 4]. Рекомендується призначати фамотидин 20 мг за 40 хвилин до їжі ввечері або 2 рази на добу (за відсутності ефекту від одноразового приймання).
При виражених симптомах ГЕРХ, які значно знижують якість життя пацієнток, рекомендовано призначати ІПП пантопразол — оригінальний ІПП ІІ покоління, який має суттєві переваги перед препаратами своєї групи. Пантопразол діє дистально на рівні рецепторів, завдяки чому він пригнічує як базальну, так і стимульовану секрецію хлористоводневої кислоти незалежно від природи стимулятора (ацетилхолін, гістамін, гастрин). Активна його форма — циклічний сульфенамід — у канальцях парієтальних клітин ковалентно зв''язується з цистеїнами у ферментній системі Н+/К+-АТФази. Підвищення кислотності після приймання пантопразолу відбувається лише за рахунок нового утворення протонної помпи, а не в результаті руйнування сполучення дисульфід-скорочуючими речовинами. Отже, повне відновлення кислотності відбувається через 46 годин, на відміну від інших ІПП (для ланзопразолу цей період складає 15 годин, для омепразолу та рабепразолу — 30 годин), що забезпечує тривале (24 години) пригнічення секреції хлористоводневої кислоти навіть при прийманні один раз на добу [7, 11, 12, 21]. Крім цього, пантопразол є високоселективним ІПП з максимальною дією у кислому середовищі, при рН < 3 (при більш високих значеннях рН залишається неактивним), тому препарат впливає безпосередньо на секреторні парієтальні клітини і не призводить до розвитку небажаних біологічних ефектів. Важливо, що пантопразол відзначається високою хімічною стабільністю, навіть при нейтральному рН [21]. Особливістю саме пантопразолу є його властивість утворювати ковалентні зв''язки як з цистеїном 813, так і з цистеїном 822. Зв''язок з цистеїном 822 є стабільним і не руйнується глутатіоном [21]. За результатами досліджень останніх років [6, 11, 12], пантопразол сприяє попередженню некротичного ураження СО за рахунок підсилення захисних властивостей слизу. Це відбувається завдяки збільшенню продукції протективних простагландинів, збільшенню доступності радикалів сульфгідрилу та скороченню тривалості антиоксидантного стресу на рівні слизової. Висока ефективність та профіль безпеки пантопразолу дозволяє вважати його препаратом вибору при лікуванні ГЕРХ у вагітних. Рекомендовано призначати пантопразол в дозі 40 мг за 40 хвилин до їжі вранці.
Таким чином, печія є одним із найпоширеніших симптомів вагітності, інтенсивність якого посилюється із збільшенням терміну гестації і значно знижує якість життя пацієнток. Печія може виникати на фоні вагітності вперше, а також бути проявом ГЕРХ, що існувала до вагітності. За відсутності тривожних симптомів розпочинати лікування слід із зміни стилю життя і принципів харчування вагітної, і лише за неефективності даної тактики переходити до медикаментозного лікування, користуючись стратегією step up.
1. Бурков С.Г. Гастроезофагеальная рефлюксная болезнь у женщин в период беременности // Гинекология. — 2001. — Т. 6, № 5. — С. 12-15.
2. Гастроэнтерология и гепатология: диагностика и лечение / Под ред. А.В. Калинина, А.И. Хазанова. — М.: Миклош, 2007. — 602 с.
3. Давыдова Ю.В., Булик Л.М. Современные подходы к лечению гастроэзофагеальной рефлюксной болезни при беременности // Сучасна гастроентерологія. — 2009. — № 4(48). — С. 69-72.
4. Дегтярева И.И. Клиническая гастроэнтерология. — М.: МИА, 2004. — 616 с.
5. Елохина Т.Б., Тютюнник В.Л. Гастроэзофагеальная рефлюксная болезнь при беременности // Эксперим. и клин. гастроэнтерология. — 2009. — № 3. — С. 93-97.
6. Карпов О.И. Фармакоэкономика язвенной болезни: взгляд из Санкт-Петербурга // Эксперим. и клин. гастроэнтерология. — 2003. — № 3. — С. 13-16.
7. Кендзерская Т.Б., Христич Т.Н., Хухлина О.С., Каневская Л.В., Гайдичук В.С. Гастроэзофагеальная рефлюксная болезнь: старая проблема — новые аспекты // Острые и неотложные состояния в практике врача. — 2008. — № 2. — С. 8-18.
8. Линевский Ю.В., Линевская К.Ю., Воронин К.А. Синдром дисфагии: диагностика и лечение // Новости медицины и фармации. — 2008. — № 264. — С. 28-36.
9. Онучина Е.В., Горобец Э.А., Рожанский А.А., Цуканов В.В. Симптомы гастроэзофагеальной рефлюксной болезни у беременных // Лечащий врач. — 2010. — № 2. — С. 88-90.
10. Передерий В.Г. Кислотоза-висимые заболевания. Современные подходы к диагностике, лечению и ведению больных с ГЭРБ, пептическими язвами, НПВП-гастропатиями, функциональной диспепсией и другими гиперсекреторными состояниями / В.Г. Передерий, С.М. Ткач, Ю.Г. Кузенко, С.В. Скопиченко. — К., 2008. — 425 с.
11. Скрипник І.М., Малик Л.В. Раціональний вибір інгібітора протонної помпи при лікуванні кислотозалежних хвороб з позицій високої ефективності та безпечності // Сучасна гастроентерологія. — 2008. — № 4. — С. 48-51.
12. Скрипник І.М., Гопко О.Ф. Стан резистентності слизового бар''єра гастродуоденальної зони у хворих на виразкову хворобу та шляхи її корекції // Гастроентерологія: Міжвід. зб. — Дніпропетровськ, 2008. — Вип. 41. — С. 97-103.
13. Успенський Ю.П., Барышни-кова Н.В., Пахомова И.Г. Клинические перспективы использования препаратов на основе альгиновой кислоты в лечении гастроэзофагеальной рефлюксной болезни // Рос. журн. гастроэнтерол., гепатологии, колопроктологии. — 2009. — Т. 19, № 2. — С. 79-84.
14. Ушкалова Е.А. Лечение гастроэзофагеального рефлюкса у беременных женщин // Гинекология. — 2001. — Т. 3, № 3. — С. 89-90.
15. Bor S., Kitapcioglu G., Dettmar P., Baxter T. Association of heartburn during pregnancy with the risk of gastrophageal reflux disease // Cksn. Gastroenterol. Hepatol. — 2007. — № 5. — P. 1035-1039.
16. Dowswell T., Neilson J.P. Interventions for heartburn in pregnancy // Cochrane Database Syst. Rev. — 2008. — № 8. — CD007065.
17. Lindow S.W., Regnell P., Sykes J., Little S. An open-label, multicentre study to assess the safety and efficacy of a novel reflux suppressant (Gaviscon Advance) in the treatment of heartburn during pregnancy // Int. J. Clin. Pract. — 2003. — Vol. 3. — P. 175-179.
18. Marrero J.M., Goggin P.M., de Caestecker J.S. et al. Determination pregnancy heartburn // Br. J. Obstet. Gynaecol. — 2002. — Vol. 99. — P. 731-734.
19. Nagler R., Spiro H.M. Heartburn in late pregnancy manometric: studies of esophageal motor function // J. Clin. Invest. — 1991. — Vol. 40. — P. 956-970.
20. Richter J.E. Gastroesophageal reflux disease during pregnancy // Gastroenterol. Clin. North. Am. — 2003. — Vol. 32. — P. 235-261.
21. Sachs G., Shin J.M. et al. The gastric H-K-ATPase as a drug target past, present and future // Clin. Gastroenterology. — 2007. — Vol. 52. — P. 226-242.
22. Stanghellini V. Management of gastroesophageal reflux disease // Drug Today (Bars). — 2003. — Vol. 39. — P. 15-20.
