Газета «Новости медицины и фармации» Гастроэнтерология (323) 2010 (тематический номер)
Вернуться к номеру
Дієтотерапія при автоімунних ураженнях печінки
Авторы: Г.А. Анохіна, д.м.н., професор
Кафедра гастроентерології, дієтології та ендоскопії
Національної медичної академії післядипломної освіти ім. П.Л. Шупика, м. Київ
Версия для печати
Для автоімунного гепатиту характерним є ураження багатьох органів та систем, безперервно прогресуючий перебіг захворювання. Однією із особливостей автоімунного гепатиту є розвиток недостатності надниркової залози. Проблема посилюється також внаслідок того, що глюкокортикоїди є препаратами вибору при автоімунних гепатитах, а їх застосування, у свою чергу, підсилює недостатність надниркової залози. Прийом глюкокортикоїдів викликає цілий ряд метаболічних змін в організмі, призводить до порушень вуглеводного обміну, навіть до розвитку стероїдного цукрового діабету, викликає остеопороз, сприяє порушенню водно-сольового обміну [7–9]. Усі ці особливості перебігу захворювання та порушення обмінних процесів слід враховувати при призначенні дієтичного харчування.
Мета дієтотерапії при автоімунних гепатитах:
Хімічний склад дієти. Квота білку повинна становити 1,2–1,6 г на
Серед компонентів їжі, що активно впливають на перебіг запального процесу, у тому числі автоімунних реакцій, є жири. Жири — це великий клас органічних сполук, що мають різноманітні, часто прямо протилежні впливи. Змінюючи вміст жирів певних класів у харчуванні можна активно впливати не тільки на обмін речовин, але й на процеси запалення. Біологічне значення жирів зумовлене тим, що вони є носіями таких життєво необхідних для організму речовин, як поліненасичені жирні кислоти (ПНЖК), жиророзчинні вітаміни, фосфоліпіди, стерини. Біологічна роль жирів залежить від жирнокислотного складу та наявності інших компонентів — фосфоліпідів, вітамінів тощо. На сьогодні виділяють декілька класів жирних кислот, які входять до харчових жирів: насичені (міристинова, пальмітинова, стеаринова та ін.), мононенасичені (олеїнова — омега-9), поліненасичені (арахідонова, лінолева — омега-6 та ейкозапентаєнова і докозагексаєнова — омега-3) жирні кислоти. ПНЖК усіх класів відрізняються довгим вуглецевим ланцюжком, тому вони не можуть потрапити в мітохондрії та окислюватися так, як окислюються коротко- та середньоланцюжкові жирні кислоти. ПНЖК також не входять у структуру тригліцеридів — основних ліпідів людського жиру. ПНЖК локалізуються в клітинних мембранах, виконуючи там надзвичайно важливу біологічну функцію — регуляторну. Від співвідношення ПНЖК у клітинних мембранах залежать властивості мембран та реакція клітини на різноманітні фактори [1–3, 7, 8].
Важливим показником біологічної цінності жиру є співвідношення окремих жирних кислот. Оцінку харчових жирів та олій проводять, порівнюючи їх із гіпотетичним ідеальним жиром. Вимогою до ідеального жиру є відношення жирних кислот родин ω-6 : ω-3 — 4 : 1. Порівняння більшості жирів та олій показало, що жодний харчовий жир не відповідає вимогам ідеального жиру, особливо якщо враховувати той факт, що найчастіше люди вживають один із видів рослинних олій. В Україні найбільш популярною є соняшникова олія (близько 80 % усіх олій), багата на омега-6 жирні кислоти, звідси стає зрозумілим значний жирнокислотний дисбаланс раціону українців. Серед інших джерел омега-3 жирних кислот найбільш доступним є риба.
Уміст основних жирних кислот у жирах та оліях наведений в табл. 1.
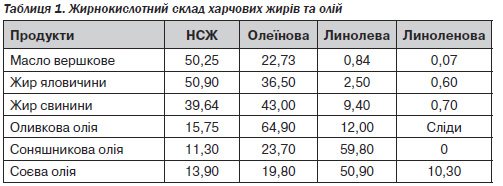
Важливою в харчуванні є квота жиру, що становить фізіологічну норму. Особливе значення має жирнокислотний склад жирових продуктів. При цьому перевагу віддають жирам тваринного походження, кількість рослинних олій має бути мінімальною, особливо жирів, що містять омега-6 жирні кислоти. Відомо, що омега-6 жирні кислоти служать джерелом синтезу запальних простагландинів. Необхідно знати, що сучасні продукти харчування містять багато прихованих омега-6 жирних кислот — це різні легкі масла, маргарин, жири, що використовують у кулінарній промисловості. Навіть вершкове масло 72,5% жирності має значну домішку рослинних олій. При призначенні дієти пацієнтам слід про це повідомити. Як жир краще використовувати сметану, вершки, а також жир, що міститься в м''ясі, рибі [8].
Квота омега-3 жирних кислот має бути збільшеною, оскільки омега-3 жирні кислоти є джерелом протизапальних простагландинів. У раціоні хворих з автоімунними ураженнями печінки щоденно повинні бути продукти, багаті на омега-3 жирні кислоти, — це глибоководні риби (оселедець, скумбрія, лосось, тунець, сардини). Найкраще вживати рибу в сирому вигляді, використовуючи для знищення мікробів соління, заморожування, а потім готувати страви з додаванням спецій, соусів. Деякі рослини, такі як зерна льону, чорної смородини, теж містять омега-3 жирні кислоти, так звані ейкозаноїди — ейкозапентаєнову, докозагексаєнову та докозапентаєнову кислоти. Якщо є необхідність призначення капсул риб''ячого жиру чи лляного масла, то слід додатково призначити вітамін Е. Найкращим джерелом протизапальних простагландинів є стеридонова кислота, що міститься в маслі зерен чорної смородини [1, 6].
При автоімунному гепатиті особливу увагу слід приділяти стану надниркової залози та використати всі можливості дієтичного харчування для покращення її функції та зниження негативних впливів імуносупресивної терапії, зменшення запального процесу. Кора надниркової залози синтезує ряд стероїдних гормонів, вихідною речовиною для утворення яких є холестерин. Для нормального функціонування кори надниркової залози важливим є достатнє забезпечення організму повноцінним білком, холестерином, лецитином, вітамінами А, Е, С, вітамінами групи В, особливо пантотеновою кислотою. Вітаміни Е, С та пантотенову кислоту при автоімунних захворюваннях слід вживати в лікувальних дозах, що в десятки разів перевищують рекомендовані дози для здорових [1, 5, 6].
Серед гормонів кори надниркової залози найбільш важливими при автоімунних захворюваннях є глюкокортикостероїди, що активно впливають на всі метаболічні процеси в організмі. Глюкокортикостероїди в печінці підсилюють синтез РНК, утворення білка, синтез ензимів, відкладання глікогену, активують ферменти синтезу сечовини. Усі ці метаболічні ефекти глюкокортико-стероїдів покращують функціональний стан печінки. При надмірному надходженні глюкокортикостероїди підвищують синтез глюкози в печінці, стимулюють процеси глюконеогенезу, зменшують утилізацію глюкози м''язами та виступають антагоністом щодо інсуліну. Призначення глюкокортикостероїдів може призвести до розвитку цукрового діабету [7, 8].
Протизапальна дія глюкокортикостероїдів обумовлена їх здатністю пригнічувати синтез фосфоліпази А2 і цим самим зменшувати доступ арахідоновї кислоти для синтезу запальних простагландинів та лейкотрієнів, подібна дія виявлена в омега-3 жирних кислот. Глюкокортикостероїди діють на цілий ряд органів та систем в організмі. При надмірному надходженні вони знижують синтез білку в м''язах, викликають катаболізм білка та знижують утилізацію глюкози, викликають демінералізацію кісток, викликаючи остеопороз, втрату кальцію з сечею. Вони також пригнічують резорбцію кальцію з кишечника, виступають антагоністом вітаміну D3. Надмірне надходження глюкокортикостероїдів може викликати зміни психічного стану пацієнтів, порушення з боку органів травлення — підвищення шлункової секреції, утворення ерозивно-виразкових уражень.
Відомо, що автоімунний гепатит — це хронічне захворювання, при якому глюкокортикостероїди, як правило, призначають довічно. Постійне, тривале вживання глюкокортикостероїдів із лікувальною метою, з одного боку, є виправданим з огляду на позитивний вплив глюкокортикостероїдів на печінку та запальні процеси, з іншого боку, чим довший прийом глюкокортикостероїдів, тим більш виражені зміни з боку кори надниркової залози та нижчий синтез власних гормонів, а також частіше розвиваються побічні ефекти.
Харчування хворих на автоімунний гепатит повинно містити достатню кількість холестерину та лецитину. Ідеальним продуктом для таких хворих є яєчний жовток, бажано яєць курей, яких тримають у домашніх умовах. Яєчні жовтки тоді багаті на холестерин, лецитин, вітамін А та інші компоненти, необхідні для відновлення кори надниркової залози та синтезу глюкокортикостероїдів. Крім цього, яєчний жовток — джерело вітаміну D3, що необхідний для профілактики остеопорозу. Важливою є правильна кулінарна обробка. Найкращим є сирий жовток, що можна використовувати для приготування яєчно-молочного коктейлю, гоголю-моголю та інших страв.
Відомо, що на фоні глюкокортикоїдної терапії в пацієнтів може збільшуватися маса тіла. Середню кількість вуглеводів у хворих слід регулювати залежно від маси тіла та порушень вуглеводного обміну. У харчуванні хворих мають переважати продукти з низьким глікемічним індексом — листяні овочі, страви із цільних круп.
У хворих на автоімунний гепатит при проведенні глюкокортикостероїдної терапії порушується водно-сольовий обмін, спостерігається затримка води в організмі, підсилюється виведення калію з сечею. Для поповнення калієвого балансу рекомендуємо овочеві соки, особливо картопляний, картоплю, запечену в шкірці. Для приготування страв можна використовувати концентрований відвар овочів, багатих калієм. Для цього подрібнені картоплю, капусту, корінь петрушки, селеру, моркву, перець та інші овочі заливають холодною водою, варять 20–30 хвилин, потім настоюють та проціджують. Отриманий відвар додають при приготуванні супів, а також соусів.
Для відновлення кори надниркової залози хворим необхідно додатково призначати вітаміни А, Е, каротиноїди, вітамін С (краще L-форму з біофлавоноїдами), вітаміни групи В та пантотенову кислоту в дозі 50 мг на добу, омега-3 жирні кислоти. Якщо недоступні естерифіковані форми вітаміну С, то аскорбінову кислоту необхідно приймати невеликими дозами упродовж усього дня. Тоді найкраще аскорбінову кислоту додавати до напоїв — соків, компоту тощо й уживати збагачені напої протягом дня. Вітамін С без біофлавоноїдів може виявляти проантиоксидантні властивості, тому доцільно вживати рослинні гепатопротектори, що багаті на біофлавоноїди та попереджують негативну дію аскорбінової кислоти [1, 6–9].
Для попередження остеопорозу рекомендований прийом вітаміну D3 в невеликих дозах, особливо в зимовий період. Улітку, коли пацієнт має можливість перебувати на свіжому повітрі, від додаткових прийомів вітаміну D3 можна відмовитися. Відомо, що гіпервітамінози вітамінів А та D3 мають негативні впливи, тому доза цих вітамінів повинна бути невеликою та не перебільшувати 3000 мг або 1,5 мг чистого ретинолу упродовж 3 тижнів. У випадках гіповітамінозу вітаміну А дозу можна збільшити до 5000 МО на добу. Більш безпечно призначати каротиноїди — бета-каротин, лікопен тощо. Добрим джерелом каротиноїдів є оранжевий гарбуз та червона морква (12 та 9 мг на
Доза вітаміну D3 може складати від 150 до 1000 МО залежно від вираженості остеопорозу. Високі дози вітаміну D3 слід призначати тільки взимку упродовж 2–3 місяців, найбільш оптимальною в цей період є доза 400–450 МО; у період пізньої осені на ранньої весни дозу необхідно зменшити, а в літні місяці можна відмовитися від додаткового прийому вітаміну D3. Вищих доз вітаміну D3 потребують пацієнти, яким призначають глюкокортикостероїди у високих дозах. Продуктами, багатими на вітамін D, є печінка тунця, тріски, палтуса, кита, а також оселедець, лосось, сардини, молоко, вершкове масло. Одним з ідеальних харчових джерел вітаміну D3 є яєчні жовтки домашніх курей, крім цього, на відміну від продуктів моря, вони є більш доступним продуктом харчування. При призначенні вітаміну D3 бажано додатково призначати магній у дозі до 1000 мг на день на весь період вживання цього вітаміну [1, 6].
Для попередження та лікування остеопорозу у хворих на автоімунний гепатит рекомендоване призначення препаратів кальцію (краще збалансованих за вмістом усіх компонентів, особливо магнію, вітаміну С). Важливою є достатня кількість вітаміну С. Вітамін С є необхідним для утворення колагену, обміну таких важливих для кісток амінокислот, як лізин та пролін. Пролін утворюється з амінокислоти лізину тільки в присутності вітаміну С.
З метою зменшення циркулюючих імунних комплексів та автоімуноагресії рекомендовано проводити ентеральну детоксикацію організму харчовими продуктами. Для цього рекомендуємо вживання продуктів, багатих на пектин (овочеві пюре з гарбуза та моркви, гарбуза, моркви та яблук, печений гарбуз, печені буряки, соки із м''якоттю), березовий сік, морквяно-яблучний, огірковий та інші овочеві та фруктово-овочеві соки.
До автоімунних уражень печінки відносять також первинний біліарний цироз печінки (ПБЦ) та первинний склерозуючий холангіт (ПСХ), для яких характерним є порушення утворення та екскреції компонентів жовчі. Уміст жовчі, яка надходить у просвіт дванадцятипалої кишки, зменшується, що порушує травлення жирів, усмоктування жирних кислот, фосфоліпідів, жиророзчинних вітамінів, солей кальцію.
Для ПБЦ та ПСХ характерним є значне порушення ліпідного обміну. У крові збільшується концентрація всіх класів ліпідів, часто з''являються ксантелазми на шкірі, спостерігається зростання в крові концентрації міді. Порушення всмоктування вітаміну D3 та кальцію призводить до розвитку остеопорозу, сухості шкіри та слизових. Зниження всмоктування вітаміну А спричиняє порушення органу зору, а вітаміну К — підвищену кровоточивість слизових. При ПБЦ у патологічний процес часто втягуються інші органи та системи, зокрема нирки, органи травлення розвиваються міопатія, нейропатія, ендокринні ураження.
При ПСХ важливу роль у прогресуванні захворювання відіграє бактеріальна інфекція. Про роль бактеріального фактора свідчить висока частота поєднання ПСХ із неспецифічним виразковим колітом, для якого характерний високий ступінь підвищення кишкової проникності. Кишкова стінка стає легко проникною для бактерій, бактеріальних токсинів, токсичних жовчних кислот, продуктів розпаду, що слід враховувати при призначенні харчування.
Дієтичне харчування при ПБЦ та ПСХ повинно бути направлене на декілька механізмів, що мають значення для розвитку цих захворювань: на нормалізацію мікробіоценозу кишечника та зменшення проникності кишкової стінки; підвищення антиоксидантного захисту; корекцію обмінних порушень, покращення відтоку жовчі.
Нормалізація мікробіоценозу кишечнику сприяє не тільки зменшенню токсичного навантаження на печінка, але й кількості пептидів, які є подразниками імунної системи, що підсилює імунопатологічні реакції та підтримує імунне запалення. Крім цього, покращення мікробного пейзажу кишечника зменшує вміст гепатотоксичних вторинних жовчних кислот та сприяє нормалізації холатоутворюючої функції, що важливо для холестатичних уражень печінки.
Нормалізація мікробіоценозу кишечника здійснюється за рахунок призначення збалансованої дієти, уникання вживання одноразово великої кількості одноманітної їжі, особливо білкових продуктів, використання в харчуванні пробіотиків та пребіотиків та ферментних препаратів.
Харчування повинно відповідати перетравлюючим можливостям шлунково-кишкового тракту та не викликати метеоризму та розладів випорожнення. Метеоризм, як правило, є ознакою надмірної мікробної контамінації, викликаної підвищенням умісту в кишечнику харчового субстрату для розмноження бактерій. Якщо в пацієнта має місце зниження шлункової та панкреатичної секреції, то з дієти необхідно виключити страви, що складно перетравлюються, багаті грубими харчовими волокнами, жирами. У дієті використовують нежирні сорти м''яса — це курятина, телятина, нежирна свинина, кролятина, а також рибу. При приготуванні страв використовують фруктові соки, багаті на органічні кислоти, — гранатовий, лимонний, вишневий, горобинний, яблучний укус, пряні трави — м''яту, кріп, петрушку тощо, які мають здатність послаблювати пептидні зв''язки та покращувати травлення. Порції повинні бути невеликі за об''ємом, знімати відчуття голоду, тяжкості та дискомфорту.
Харчові продукти мають виражені нормалізуючі властивості щодо облігатної мікрофлори та бактеріо-статичні й бактеріоцидні — щодо умовно-патогенної та патогенної мікрофлори. Найбільш фізіологічним є відновлення мікробіоценозу кишечника природним шляхом за рахунок покращення харчування корисної мікрофлори. Відомо, що все живе потребує харчування. Від того, яким буде вміст кишечника, залежить, яка мікрофлора буде переважати. Для живлення біфідумбактерій та молочнокислих паличок важливими компонентами є фруктоолігосахариди, на які багаті деякі овочі: гарбуз, морква, буряк, ієрусалимський артишок, цибуля тощо. Крім того, що харчові волокна, особливо пектини, позитивно впливають на кишкову мікрофлору, вони дуже добре перетравлюються кишковою мікрофлорою з утворенням коротколанцюжкових жирних кислот — ацетату, бутирату, пропіонату. Середньо- та коротколанцюжкові жирні кислоти ефективно використовуються в енергетичних процесах, не викликають жирової інфільтрації печінки.
Наступним важливим моментом при призначенні харчування хворим на автоімунні захворюваннями печінки є зменшення процесів перекисного окислення ліпідів, запальної реакції та захист клітинних мембран та інших структур від дії продуктів вільнорадикального окислення.
Хворим на ПБЦ та ПСХ слід додатково призначати жиророзчинні вітаміни А, Е, К, D, препарати кальцію. Найбільш доцільним є застосування вказаних компонентів із препаратами урсодезоксихолевої кислоти — урсофальком. Прийом жиророзчинних вітамінів, препаратів кальцію, омега-3 жирних кислот, лецитину одночасно з урсофальком буде сприяти засвоєнню вказаних інгредієнтів та їх надходженню в організм хворих.
1. Барабой В.А. Биоантиоксиданты. — К.: Книга плюс, 2006. — 460 с.
2. Курята А.В., Фролова А.Е. Перспективы применения Омега-3 ПНЖК у пациентов с сердечно-сосудистыми заболеваниями и хронической почечной недостаточностью // Здоровье Украины. — 2008. – № 6(187). — С. 61.
3. Мазур И.А., Чекман И.С., Беленичев И.Ф. Метаболитотропные препараты. — Запорожье, 2007. — 304 с.
4. Мартынов А.И., Чельцов В.В. Омега-3 полиненасыщенные жирные кислоты в кардиологической практике: Метод. рекомендации. — 2007. — № 2, 4. — 16 с.
5. Мартинчик А.Н., Маев И.В., Янушевич О.О. Общая нутрициология: Учеб. пособие. — М.: МЕДпресс-информ, 2005. — 388 с.
6. Ребров В.Г., Громова О.А. Витамины и микроэлементы. — М., 2003. — 647 с.
7. Смолянский Б.Л., Лифляндс-кий В.Г. Диетология: Новейший справочник для врачей. — СПб.: Сова; М.: Эскимо, 2004. — 816 с.
8. Чарльз В., Ван Вэй Ш., Кэрол Айертон-Джонс. Секреты питания. — М.: Бином, 2006. — 311 с.
9. Харченко Н.В., Анохіна Г.А. Сучасні аспекти дієтотерапії захворювань органів травлення. — К., 2005. — 156 с.
