Международный неврологический журнал 1 (39) 2011
Вернуться к номеру
Молекулярно-генетические и некоторые биохимические аспекты болезни Паркинсона
Авторы: Маджидова Ё.Н., Халимова Х.М., Раимова М.М., Матмурадов Р.Ж., Фахаргалиева С.Р., Жмырко Е.В., Кафедра нервных болезней Ташкентской медицинской академии, Институт генетики и экспериментальной биологии растений АН РУз, г. Ташкент, Узбекистан
Рубрики: Неврология
Версия для печати
Проведен молекулярно-генетический анализ на наличие ассоциаций с болезнью Паркинсона (БП) полиморфизмов генов GSTM1 (нулевая аллель), GSTT1 (нулевая аллель) у представителей узбекской национальности и определение содержания нейронспецифической енолазы (НСЕ) в сыворотке крови больных болезнью Паркинсона. Всего исследовано 190 образцов ДНК, в том числе 140 образцов ДНК больных БП и 50 образцов ДНК здоровых лиц из группы контроля. Биохимическое исследование проведено у 35 пациентов с длительностью заболевания от 1 года до 15 лет. Анализ полиморфизма генов GSTT1 и GSTM1 выявил значительную гетерогенность по частотам нулевых и ненулевых генотипов у больных БП и здоровых лиц: у больных доля нуль-генотипов гена GSTT1 на 52 % выше, и по гену GSTM1 на 45,1 % выше, чем у здоровых лиц. Повышенный уровень НСЕ отмечался в 69 % случаев БП, чаще у больных со смешанной и акинетико-ригидной формой заболевания.
Болезнь Паркинсона, гены детоксикации, GSTT1, GSTM1, нейронспецифическая енолаза.
Болезнь Паркинсона (БП) — одно из наиболее часто встречающихся нейродегенеративных заболеваний пожилого и старческого возраста. В связи с увеличением средней продолжительности жизни населения болезнь Паркинсона, несомненно, оказывает влияние на показатели качества жизни населения и приводит к значительным социально-экономическим потерям [1–3].
Предположения о причине возникновения этой болезни различны. Согласно современным взглядам, около 10 % всех случаев болезни Паркинсона имеют наследственную моногенную основу, тогда как абсолютное большинство пациентов представлены спорадической формой БП мультифакториальной природы [4–10]. Определен целый ряд генов предрасположенности к болезни Паркинсона (гены систем клеточной детоксикации и антиоксидантной защиты GSTT1, GSTM1, GSTP1, гены транспорта и метаболизма дофамина, митохондриальный геном и другие), носительство неблагоприятных аллельных вариантов которых достоверно повышает риск заболевания [11–15]. Результаты вышеописанных исследований показывают высокую вариабельность частоты встречаемости полиморфизма генов-кандидатов в развитии болезни Паркинсона у представителей разных популяций.
В последние годы появились научные исследования по изучению нейрон-специфической енолазы (НСЕ) при заболеваниях, сопряженных с вовлечением в патологический процесс нервной ткани, где количественное определение белка в сыворотке крови дает ценную информацию о степени выраженности повреждения нейронов и нарушении общей целостности гематоэнцефалического барьера (ГЭБ). В их числе инсульты, эпилепсия, травмы головного мозга. НСЕ может быть индикатором гибели нейронов, и определение его в крови больных паркинсонизмом может быть дополнительным диагностическим маркером. С этих позиций представляет интерес изучение диагностической значимости НСЕ у больных с болезнью Паркинсона.
Учитывая немаловажную роль системы детоксикации в нейтрализации вредных веществ, поступающих в организм, поиск генетических маркеров индивидуальной чувствительности людей, подвергающихся воздействию вредных веществ, на основе анализа полиморфизма генов ферментов биотрансформации ксенобиотиков представляется актуальным.
Цель исследования: при помощи комплексного анализа клинических, молекулярно-генетических и биохимических данных изучить факторы, определяющие развитие болезни Паркинсона.
Методы исследования
Исследования проведены на кафедре нервных болезней Ташкентской медицинской академии (ТМА) и в Центре геномных технологий ИГиЭБ растений.
Проведен тщательный клинико-анамнестический и молекулярно-генетический анализ данных 140 больных болезнью Паркинсона. В качестве контрольной группы молекулярно-генетический анализ был проведен у 50 больных хронической ишемией мозга без признаков паркинсонизма сопоставимого возраста. При отборе конкретных лиц учитывали их национальную принадлежность — все пациенты являются лицами узбекской национальности в возрасте от 30 до 80 лет, с клинической картиной болезни Паркинсона. Коллекция материалов была проведена у неродственных лиц. Группу сравнения составили 50 лиц, не страдающих данной патологией.
Диагностика паркинсонизма и его нозологической формы проведена согласно критериям банка головного мозга общества болезни Паркинсона Великобритании (Gibb, Lees, 1988). В случае необходимости для окончательной дифференциальной диагностики нозологической формы паркинсонизма проведено нейровизуализационное (КТ, МРТ) исследование.
Клиническая оценка состояния больных включала исследование неврологического и соматического статуса с объективизацией имеющихся неврологических нарушений с помощью шкалы Hoehn & Yahr в модификации Lindvall (1988), Tetrud & Langston (1989), I–III подшкал унифицированной шкалы оценки проявлений паркинсонизма UPDRS (S. Fahn et al., 1987).
Молекулярно-генетические исследования
Данная часть исследований проведена в Центре геномных технологий (ЦГТ) при Институте генетики и экспериментальной биологии растений (ИГиЭБР) Академии наук Республики Узбекистан (АН РУз). В рамках исследования был проведен анализ на наличие ассоциаций с болезнью Паркинсона: полиморфизма генов GSTM1 (нулевая аллель), GSTT1 (нулевая аллель) у представителей узбекской национальности (сравнение состояний генотипа по исследуемым полиморфизмам больных и здоровых по болезни Паркинсона). Материалом для ДНК служила венозная кровь из локтевой вены объемом 1 мл.
Выделение ДНК проводилось по стандартному протоколу выделения ДНК с использованием набора реагентов Diatom™ DNA Prep 200 (производство ООО «Лаборатория ИзоГен»).
Супернатант с ДНК далее подвергался непосредственно генотипированию путем ПЦР-амплификации. Типирование образцов ДНК по генам GSTM1 и GSTT1 проводили с использованием двух пар специфических олигонуклеотидных праймеров с участками генов GSTM1 (F: 5’-tgs-ttc-acg-tgt-tat-gga-ggt-tc; R: 3’-gtt-ggg-ctc-aaa-tat-acg-gtg-g) и GSTT1 (F: 5’-ggt-cat-tct-gaa-ggc-caa-gg; R: 3’-ttt-gtg-gac-tgc-tga-gga-cg). ПЦР-анализ проводили с использованием набора реагентов для ПЦР-амплификации ДНК GenePak™ PCR Core (производство ООО «Лаборатория ИзоГен»).
Гомозиготность по нулевым аллелям (0/0) генов GSTM1 и GSTT1 определяли по отсутствию на электрофореграммах фрагментов размером 131 и 114п.н. соответственно. Наличие этих фрагментов свидетельствовало о присутствии по крайней мере одной нормальной (без делеции) копии генов (гомо- и гетерозиготы, +/+ и +/0). Нулевые аллели генов GSTM1 и GSTT1 свидетельствовали, в свою очередь, о предрасположенности объекта к БП. Для определения размера фрагментов ДНК использовался маркер с начальной отметкой 100 п.н.
Содержание НСЕ в сыворотке крови больных определялось методом иммуноферментного анализа, выполняемого с помощью специфических тест-систем, разработанных на основе соответствующих моноклональных антител, на анализаторе «ALISA» согласно инструкции, прилагаемой к набору. Забор пробы крови осуществлялся из локтевой вены утром натощак в лаборатории ЦП № 2 МСО при МЗ РУз. Данное исследование проведено у 35 пациентов, в том числе у 17 (48,57 %) женщин и 18 (51,42 %) мужчин с длительностью заболевания от 1 года до 15 лет.
В последующем проводилась сравнительная оценка результатов анализов НСЕ у больных по полу, возрасту, а также в зависимости от формы, стадии, темпа прогрессирования заболевания.
Результаты и их обсуждение
Был проведен анализ на наличие ассоциаций БП с нулевыми аллелями генов системы детоксикации ксенобиотиков GSTM1 и GSTT1, кодирующих две формы фермента глутатионтрасферазы — m и q соответственно. ГSТ являются важным компонентом системы биотрансформации, и их дефицит может привести к накоплению веществ, стимулирующих развитие заболевания и участвующих в реализации патогенеза БП.
В группе больных БП частота встречаемости 0/0 полиморфизма для гена GSTM1 составила 57,1 % (80 больных); а для гена GSTТ1 — 60 % (84 больных); частота встречаемости «+» полиморфизма генов GSTM1 и GSTТ1 — 42,9 и 40 % соответственно, тогда как в группе здоровых лиц частота встречаемости 0/0 полиморфизма составила для гена GSTM1 — 12 % (6 больных); для гена GSTТ1 — 8 % (4 больных); частота встречаемости «+» полиморфизма генов GSTM1 и GSTТ1 — 88 и 92 % соответственно (рис. 1).
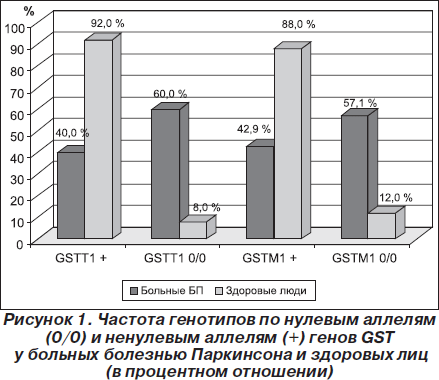
Анализ полиморфизма генов GSTT1 и GSTM1 выявил значительную гетерогенность по частотам нулевых и ненулевых генотипов у больных БП и здоровых лиц (рис. 2). Так, у больных доля нуль-генотипов гена GSTT1 на 52 % выше, чем у здоровых лиц; и по гену GSTM1 на 45,1 % выше, чем у здоровых лиц.
Поскольку ферменты GSТ играют важную роль в системе детоксикации, можно предполагать, что генотоксические промежуточные метаболиты, возникающие на первой стадии детоксикации, из-за отсутствия ферментов второй фазы (GSТ) не утилизируются, а воздействуют непосредственно на дофаминпродуцирующие клетки черной субстанции, провоцируя или ускоряя их дегенерацию.
Таким образом, независимо от того, какие именно патогенетические механизмы развития БП связаны с ферментами системы детоксикации, нет сомнения в том, что мутации в обоих генах GSТ, приводящие к потере активности соответствующих ферментов, можно рассматривать как фактор генетического риска развития БП.
Следующей задачей нашего исследования являлось сопоставление результатов анкетирования с данными молекулярно-генетического исследования. Данные сопоставления показали, что нулевые генотипы вышеизученных генов по сравнению с ненулевыми чаще встречались у лиц с более ранним дебютом заболевания, характеризовались более быстрыми темпами прогрессирования и развернутой картиной заболевания. Однако проведенное на данном этапе исследование является еще незавершенным. Нами проведено санитарно-гигиеническое исследование с использованием анкетного опросника по типу случай-контроль, где в качестве контрольной группы выступают лица, сопоставимые по возрасту и полу, не имеющие болезни Паркинсона. Также проводится рандомизация больных и здоровых по факту наличия или отсутствия воздействия неблагоприятных средовых факторов с последующим генофенотипическим сопоставлением. Результаты данных исследований будут представлены позже.
Результаты проведенного исследования содержания НСЕ в сыворотке крови больных с БП показали повышение уровня НСЕ у 24 (68,5 %) из 35 больных (>25нг/мл). Повышенное содержание НСЕ отмечалось у 58,3 % мужчин и 41,7 % женщин. Наиболее высокие показатели НСЕ определялись на начальных этапах заболевания. Были выявлены более высокие показатели уровня нейронспецифической енолазы у больных с быстрым темпом развития заболевания по сравнению с медленным и умеренным темпами развития. Как было описано выше, нейронспецифическая енолаза является основным маркером повреждения нервной ткани. В связи с этим более высокие показатели содержания нейронспецифической енолазы в сыворотке крови на начальных этапах заболевания и при более быстрых темпах прогрессирования, по-видимому, показывают большую степень выраженности повреждения клеток черной субстанции.
Больные были разделены на 3 подгруппы в зависимости от формы заболевания: больные со смешанной формой — 28 (80 %) человек, с дрожательной формой— 4 (11,4 %) человека, и с акинетико-ригидной формой— 3 (8,6 %) человека. Из 3 подгрупп только у больных с дрожательной формой БП колебание уровня НСЕ было в пределах нормы — от 11 до 15,3нг/мл. Полученные результаты также подтверждают мнение многих исследователей (Галиева Г.Ю., 2008, Карякина Г.М., 2007 и др.) о том, что концентрация НСЕ может служить маркером более распространенных повреждений нервных клеток, что имеет место при акинетико-ригидной и смешанной формах, по сравнению с дрожательной. Таким образом, выявленное в данном исследовании повышение концентрации нейронспецифической енолазы в сыворотке крови у больных болезнью Паркинсона свидетельствует о патогенетической роли данного фермента в течении заболевания.
Выводы
1. Тестирование полиморфных вариантов генов детоксикации GSTM1, GSTT1 позволяет достаточно объективно оценить индивидуальный риск БП и, таким образом, внести серьезный вклад в предиктивное тестирование этого тяжелого, распространенного заболевания.
2. «Нулевые» генотипы генов GSTM1, GSTT1 ассоциируются с более ранним дебютом заболевания, более быстрыми темпами прогрессирования и развернутой картиной заболевания.
3. Повышенный уровень НСЕ отмечается в 69 % случаев у больных с БП, чаще встречается у больных со смешанной и акинетико-ригидной формой заболевания, и у больных с быстрыми темпами прогрессирования заболевания.
4. Показатель НСЕ может использоваться как один из дополнительных методов диагностики и прогноза клинического течения БП.
1. Артемьев Д.В., Яхно Н.Н. Этиология и патогенез болезни Паркинсона // Рус. мед. журнал. — 2001. — № 9. — С. 4-9.
2. Багыева Г.Х. Клинико-генетический и биохимический анализ болезни Паркинсона: механизмы предрасположенности, экспериментальные модели, подходы к терапии: Автореф. дис… д-ра мед. наук. — Москва, 2009. — 48 с.
3. Байтимеров А.Р. Эпидемиологическое и клинико-генетическое изучение болезни Паркинсона в Республике Башкортостан: Автореф. дис… канд. мед. наук. Уфа, 2007. — 22 с.
4. Гилязова И.Р. Молекулярно-генетическое изучение болезни Паркинсона в Башкортостане // Автореф. дис… канд. биол. наук. — Уфа, 2004. — 24 с.
5. Джурич Г., Иллариошкин С.Н., Светел М. и др. Влияние комбинированных полиморфизмов в генах CYP2D6, PON1 и apoE на риск развития болезни Паркинсона // Сборник I Национального конгресса по болезни Паркинсона и расстройствам движений. — Москва, 2008. — С. 357.
6. Иллариошкин С.Н. Молекулярные основы болезни Паркинсона // Сборник I Национального конгресса по болезни Паркинсона и расстройствам движений. — Москва, 2008 — С.8-17.
7. Иллариошкин С.Н., Джурич Г.М., Багыева Г.Х. и др. Генетическая предрасположенность к болезни Паркинсона// Материалы V съезда Российского общества медицинских генетиков, часть II // Мед. генетика. — 2005. — № 5. — С.196.
8. Загоровская Т.Б., Иллариошкин С.Н., Слонимская П.А. идр. Клинико-генетический анализ ювенильного паркинсонизма в России // Журнал неврол. и психиатр. — 2004. — № 8. — С.66-72.
9. Якимовский А.В., Пушнова Е.А., Ахмедова С.Н., АвтономовВ.В. Молекулярно-генетические и токсико-экологические основы этиологии и патогенеза болезни Паркинсона (паркинсонизма)// Журнал невропатол. и психиатр. — 1997. — №4.— С.69-73.
10. Пчелина С.Н., Якимовский А.Ф., Шварц Е.И. Наследственные основы болезни Паркинсона (обзор) // Медицинская генетика. — 2003. — № 9. — С. 411-425.
11. Chan D.K.Y., Woo J., Ho S.C. et al. Genetic and environmental risk factors for Parkinson’s disease in a Chinese population // J. Neurol. Neurosurg Psychiatry. — 1998. — 65. — 781-784.
12. De Michele G., Filla A., Volpe G. et al. Environmental and genetic risk factors in Parkinson's disease: a case-control study in southern Italy // Mov. Disord. — 1996 Jan. — 11 (1). — 17-23.
13. Dick F.D., De Palma G., Ahmadi A. Geoparkinson study group. Environmental risk factors for Parkinson's disease and parkinsonism: the Geoparkinson study // Occup. Environ. Med. — 2007 Oct. — 64(10). — 666-72.
14. Evangelou E., Maraganore D.M., Ioannidis J.P. Meta-analysis in genome-wide association datasets: strategies and application in Parkinson disease // PLoS ONE. — 2007. — 2:e196.
15. Gasser T. Genetics of Parkinson's disease // J. Neurol. — 2001 Oct. — 248 (10). — 833-40.
