Международный эндокринологический журнал 2 (34) 2011
Вернуться к номеру
Немедикаментозная профилактика и восстановительная коррекция поздних осложнений климактерического синдрома у женщин
Авторы: Королевская Л.И., ФГУ «Российский научный центр восстановительной медицины и курортологии Росздрава», г. Москва, Россия
Рубрики: Эндокринология
Версия для печати
Введение
Профилактическая направленность восстановительной медицины реализуется путем выявления и коррекции нарушений на ранних этапах их формирования. Первичная и вторичная профилактика позволяет снизить как заболеваемость, так и осложнения уже развившихся заболеваний. Методическая база, основанная на применении природных и преформированных физических факторов, дает возможность широко использовать их для лечения, реабилитации и профилактики.
Климактерический период, являющийся естественным этапом в жизни женщины, характеризуется существенной перестройкой функциональных систем организма, что часто приводит к формированию различных заболеваний [1, 2]. Именно в перименопаузе, являющейся ранним периодом климакса, регистрируются первые проявления таких заболеваний, как артериальная гипертензия (АГ) и остеопороз, которые в дальнейшем приводят к стойкой потере здоровья. Известно, что распространенность сахарного диабета (СД) и гипотиреоза возрастает в старших возрастных группах, при этом оба заболевания более распространены среди женщин, поэтому многие женщины вступают в климакс с заболеваниями, которые способствуют развитию остеопороза и болезней сердечно-сосудистой системы. Очевидно, что более раннее начало профилактики осложнений климакса позволяет приостановить формирование стойких изменений как сердечно-сосудистой, так и костной системы.
Научным обоснованием выбора лечебно-профилактических технологий для разработки программ восстановительной медицины у данной категории больных послужили исследования, показавшие эффективность бальнеотерапии (радоновые, йодобромные, контрастные ванны) как в устранении факторов риска и реабилитации больных с ишемической болезнью сердца (ИБС), АГ, нейроциркуляторной астенией, так и в коррекции климактерического синдрома [3, 4]. Физиотерапевтические составляющие разработанных программ основаны на исследованиях, показавших патогенетическую направленность трансцеребральных воздействий, ультразвука, низкоэнергетического лазерного излучения при климактерической миокардиодистрофии [4], АГ, и экспериментальных исследованиях, продемонстрировавших возможность влияния этих факторов на метаболизм кальция [5].
Цель исследования: разработать и научно обосновать дифференцированные программы коррекции проявлений климактерического синдрома и профилактики поздних осложнений климакса у женщин с сахарным диабетом и гипотиреозом.
Материалы исследования
Для решения поставленных задач в отделении реабилитации больных с заболеваниями эндокринной системы ФГУ «Российский научный центр восстановительной медицины и курортологии Росздрава» и отделении эндокринологии и гинекологии Центральной больницы № 6 ОАО «Российские железные дороги» было обследовано 363 женщины, находящихся в перименопаузальном периоде, в возрасте от 47 до 52 лет. Средний возраст больных составил 50,4 ± 2,3 года. Все больные были разделены на 3 группы. Среди обследованных больных выделяли женщин с климактерическим синдромом без сопутствующей эндокринной патологии — 117 человек (1-я группа); группу больных, климактерический синдром у которых протекал на фоне развившегося ранее CД типа 2, компенсированного приемом пероральных сахароснижающих препаратов, — 124 человека (2-я группа); группу с сопутствующим гипотиреозом, компенсированным приемом L-тироксина, составили 122 человека (3-я группа). Группы были сопоставимы по возрасту пациенток. Длительность СД в группе 2 составила от 2 до 7 лет, в среднем 4,8 ± 1,6 года. Длительность гипотиреоза на фоне хронического аутоимунного тиреодита (АИТ) от 1 года до 5 лет, в среднем 3,8 ± 0,4 года. Больные СД получали терапию сахароснижающими препаратами, 27 человек получали препараты сульфонилмочевины, 56 — сочетание препаратов сульфонилмочевины и метформина, 41 — метформин. Пациентки с гипотиреозом получали заместительную терапию L-тироксином.
Критериями включения пациенток в исследования являлись: возраст 45–55 лет; наличие признаков климактерического синдрома; период пременопаузы и 1 год менопаузы; АГ не выше 1–2-й стадии, индекс массы тела (ИМТ) не выше 32; для больных СД типа 2 —глюкоза крови натощак не выше 9 ммоль/л; для больных гипотиреозом — тиреотропный гормон (ТТГ) не выше 4,0 нмоль/л
Критерии исключения: наличие опухолевых образований (в том числе миомы матки, фиброзно-кистозной мастопатии); декомпенсация СД2 или диабет типа 1; хронический АИТ с признаками гипертиреоза.
В структуре сопутствующих заболеваний обращало на себя внимание наличие АГ у 199 больных (54,8 %). Повышение артериального давления (АД) встречалось среди 67,4 % пациенток с сопутствующим СД в группе без эндокринной патологии и с гипотиреозом АГ выявлялась в 42,0 и 52,3 % случаев соответственно. Заболевания опорно-двигательного аппарата выявлены у 44,6 % всех обследованных, в том числе у 51,6 % больных с гипотиреозом. Заболевания пищеварительной системы наблюдались чаще у пациенток с сопутствующей эндокринной патологией (43,5 % — во 2-й группе и 48,4 % — в 3-й против 35,9 % в 1-й группе).
При обследовании были выявлены следующие факторы риска развития остеопороза: сопутствующие заболевания органов пищеварения — 43,0 % больных, гиподинамия — 45,0 %, отягощенная по переломам наследственность — 24,0 % женщин. У 48,4 % пациенток отмечалось наличие 2 факторов риска, а у 51,6 % зарегистрировано наличие 3 и более факторов риска развития остеопороза. При определении минеральной плотности костной ткани (МПКТ) оказалось, что только у 21 % больных этот показатель оказался в пределах нормы, у 10 % определялся остео- пороз и у 69 % — остеопения.
Все больные имели 2 и более факторов риска развития атеросклероза и ИБС. Курение и гиподинамия являются факторами развития не только остеопороза, но и сердечно-сосудистых заболеваний (ССЗ). Гиперлипидемия отмечена у 284 больных (78,2 %). Среди женщин без сопутствующей эндокринной патологии гиперлипидемия наблюдалась у 68 (58,1 %), при сопутствующем гипотиреозе процент гиперлипидемии возрос до 85,2 % (104 больных), а в группе с сопутствующим СД число больных составило уже 90,3 % (112 женщин). У 249 (68,5 %) пациенток среди ближайших родственников были диагностированы сердечно-сосудистые заболевания.
Методы исследования
Для решения поставленных в работе задач, помимо общеклинических, были включены специальные методы исследования углеводного, липидного, минерального обменов, гормонов крови, эхокардиография (ЭхоКГ).
Исследования гормонов проводили методами радиоиммунного и иммунохимического анализа. Использовали иммуноферментные анализаторы Multiscan (Финляндия), ELECTRICS швейцарской фирмы Hoffman la Rosсhe и стандартные коммерческие тест-наборы: hPTH-с-к Cis (Франция), КT — Byk-Mallinckrodt (Германия), D3 — Bahlmann (Швейцария), FSH, LG, Estradiol EIA COBAS CORE (Hoffman La Rosсhe, Швейцария), остеокальцин — Ostk-PR Cis (Франция), ТТГ — TSH ILMA (Immunotech, Финляндия), иммунореактивный инсулин (ИРИ) — Ins-Cis (Франция). Активность общей щелочной фосфатазы (ОЩФ), выражаемую в ЕД/л, определяли на биохимическом анализаторе Co-BAS-MIRAS (Швейцария).
Эхокардиографию выполняли на аппарате SKI-500 (Xonix, Англия) путем М- и секторального сканирования. По общепринятым методикам изучали и оценивали показатели центральной и внутрисердечной гемодинамики: минутный (МО), конечный систолический (КСО) и конечный диастолический (КДО) объемы, фракцию выброса (ФВ), массу миокарда (ММ).
Минеральную плотность костной ткани исследовали методом двухэнергетической рентгеновской абсорбциометрии на денситометрах DMS Chаllenger (Франция). Основным параметром, характеризующим МПКТ по данным денситометрического исследования, является индекс Т. Для диагностики остеопороза использовали значения, основанные на данных денситометрии и анамнеза: Т-критерий от –1,0 до –2,5 — остеопения; Т-критерий от –2,5 или меньше без предшествующих переломов — остео- пороз; Т-критерий от –2,5 или меньше с предшествующими переломами — тяжелый остеопороз.
Для выявления клинических проявлений климакса, степени его тяжести и выраженности нейровегетативных, обменно-эндокринных и психоэмоциональных нарушений использовали расчет менопаузального индекса Куппермана в модификации Е.В. Уваровой — модифицированный менопаузальный индекс (ММИ).
В соответствии с поставленными задачами методом рандомизации больные были разделены на группы, получавшие различные виды лечения. В 1-ю группу вошли женщины, находящиеся в периоде перименопаузы, не имевшие сопутствующей эндокринной патологии. Вторую группу составили женщины, страдавшие СД типа 2, получавшие пероральную сахароснижающую терапию. Третья группа больных составлена из женщин перименопаузального периода, имевших в анамнезе хронический гипотиреоз и получавших терапию L-тироксином. Все пациентки получали базовую терапию, состоявшую из диеты с достаточным содержание кальция (не менее 1000 мг), курсов лечебной гимнастики и фитопрепаратов седативного действия.
Каждая из групп была разделена на подгруппы в соответствии с получаемыми комплексами лечения:
— подгруппы 1А, 2А и 3А являлись контрольными, получали базовую терапию;
— подгруппы 1Б, 2Б и 3Б получали комплекс, состоявший из контрастных ванн и интерференционных токов трансцеребрально. Методика проведения контрастных ванн: температура холодной воды — 22–24 °С, горячей — 38–39 °С, контраст температур — 14–17 °С. Соотношение пребывания больных в горячей и холодной воде в течение процедуры составляло 3 и 1 мин, 2 и 2 мин, 1 и 3 минуты соответственно. Количество процедур — 10–12. Воздействие интерференционными токами проводили от аппарата АИТ-КС-50-01 (Россия), позволяющего осуществить интерференцию трех синусоидальных токов при ритмически меняющейся частоте интерференционных токов в диапазоне от 0 до 150 Гц с ощущением легкой вибрации. Для проведения процедуры использовалось электродное устройство (маска) для применения интерференционных токов по методике электросна, представляющее собой 3 пары электродов, вмонтированных в резиновую манжетку. Силу тока дозируют по ощущениям больной, в среднем она составляет 2,5 мА. Процедуры проводили ежедневно, длительность 15 минут. На курс лечения 10–12 процедур;
— подгруппы 1В, 2В и 3В получали комплекс, состоявший из радоновых ванн и ультразвука паравертебрально. Радоновые ванны температурой 36–37 °С, 10–20 минут, назначали начиная с концентрации 1,5 кБк/л и постепенно увеличивая концентрацию радона до 3,0 кБк/л. Процедуры проводили 2 дня подряд, третий день — перерыв. На курс 10–12 ванн. Через 40–60 минут после ванны проводилась ультразвуковая терапия от аппарата УЗТ-101Ф, частота 880 кГц в импульсном режиме (10 мс) паравертебрально на грудной и шейный отделы позвоночника, интенсивность 0,2–0,4 Вт/см2 по 5 минут на поле. Процедуры проводили по лабильной методике, излучатель 4 см2, контактная среда «Ультрагель», на курс назначали 10–12 процедур ежедневно;
— подгруппы 1Г, 2Г и 3Г получали йодобромные ванны и лазеротерапию. Йодобромные ванны (I — 10 мг/л, Br — 25 мг/л): общая минерализация 20 г/л, температура 37–38 °С, по 20 минут ежедневно, на курс 10–12 процедур. Облучение проекционных зон позвоночной артерии и воротниковой области проводили низкоэнергетическим инфракрасным лазерным излучением (0,89 мкм) от аппарата «Азор-2К». Излучатель устанавливали контактно в проекционную область позвоночных артерий (на уровне 2-го шейного позвонка, на 2 см латеральнее от позвоночника). Режим импульсный. Частота следования импульса 10 Гц. Импульсная мощность 5,5 Вт. Экспозиция 30–60 с ежедневно или через день, 10–12 процедур на курс лечения. Курс лечения во всех группах повторялся через 6 месяцев. Отдаленные результаты оценивали через год после завершения курса лечения.
Статистическую обработку цифровых данных проводили на персональном компьютере IBM PC-Pentium. Применен метод вариационной статистики, с вычислением средней арифметической (М), средней ошибки средней величины (м), степени свободы и вероятности (Р). Сравнение средних величин двух выборок (сравниваемых показателей) проводили по t-критерию Стьюдента и методами непараметрической статистики с использованием критерия Манна — Уитни и Вилкоксона. Достоверным считалось различие более 95 % (Р < 0,05). Выполнялся корреляционный анализ с вычислением коэффициента корреляции (r), пошаговый дискриминантный анализ. Отклонение от гипотезы независимости оценивалось по критерию хи-квадрат Пирсона. При статистическом анализе использован пакет компьютерных программ Statistica 7.0.
Результаты исследования и их обсуждение
Все пациентки отмечали проявления климактерического синдрома различной степени тяжести. ММИ в группе пациенток без эндокринной патологии составил 41,85 ± 3,23, у больных с сопутствующим СД — 54,1 ± 2,7, а у пациенток с тиреоидной патологией — 57,5 ± 4,7, т.е. определялась средняя степень выраженности климактерического синдрома. Различия средних показателей ММИ были достоверны между группой без сопутствующей эндокринной патологии и группами с СД и патологией щитовидной железы. В группе больных без эндокринной патологии легкая степень выраженности климактерического синдрома наблюдалась у 14,6 % пациенток, умеренная — у 83,3 % больных, тяжелая — у 2,1 %. В группе больных сахарным диабетом слабая выраженность симптомов встречалась у 14 человек (11 % случаев), умеренная — у 95 больных (76,8 %), тяжелая — у 15 (11,6 %) пациентов. В третьей группе больных с сопутствующим гипотиреозом слабая выраженность симптомов климактерического синдрома не встречалась, умеренная и тяжелая составили 105 (86,4 %) и 17 (13,6 %) соответственно.
Структура симптомов в группах различалась. У больных без эндокринной патологии в большей степени были выражены нейровегетативные и психо-эмоциональные проявления климактерического синдрома, метаболические проявления были выражены в меньшей степени. У больных с сопутствующим сахарным диабетом доминировали метаболические и психоэмоциональные составляющие при меньшей значимости нейровегетативных расстройств. В группе пациенток с сопутствующей тиреоидной патологией все три составляющие климактерического синдрома были одинаково значимы.
Анализ результатов после курса лечения показал, что комплексное физиобальнеотерапевтическое лечение уменьшает проявления климактерического синдрома. В 1-й группе до лечения было 17 (14,6 %) пациенток с легкими проявлениями, после курса лечения в целом по группе их число возросло до 34 (29,1 %). Количество больных со средней степенью уменьшилось с 97 (83,3 %) до 79 (67,5 %) больных. Во 2-й группе в подгруппе 2Б увеличилось число пациенток с легким течением синдрома (с 16,7 до 30 %) и несколько уменьшилось число больных с тяжелыми проявлениями (с 10 до 6,7 %). В подгруппе 2В динамика была более выражена (увеличение числа женщин с легким течением с 6,3 до 31,3 %). Также уменьшилось количество женщин с тяжелым течением климакса (15,6 % до лечения и 3,1 % после лечения). В подгруппе 2Г до лечения доля женщин с легким течением составила 12,9 %, после лечения — 25,8 %. В то же время уменьшился процент женщин с тяжелым течением — с 12,9 до 6,5. В 3-й группе среди женщин, входящих в подгруппу 3Б, уменьшилось число больных со средней тяжестью климактерического синдрома с 89,7 до 79,3 %, у 10,4 % пациенток течение климакса после лечения было оценено как легкое, количество пациенток с тяжелым течением не изменилось. В подгруппе 3В уменьшилось число больных с тяжелыми проявлениями климакса (16,2 % до и 9,7 % после) и среднетяжелыми проявлениями (83,8 % до 74,1 % после), у 16,2 % климакс принял легкое течение. В подгруппе 3Г количество женщин с тяжелыми проявлениями климакса снизилось с 15,6 до 6,5 %, со среднетяжелыми — с 84,4 до 72,9 %, количество женщин с легким течением после лечения составило 18,8 % при отсутствии таковых до курса лечения. ММИ достоверно уменьшался в 1-й группе примерно в равной степени независимо от используемого комплекса. Во 2-й и 3-й группах достоверные изменения получены в подгруппах, получавших радоновые ванны и ультразвук (20,8 и 15,4 %), йодобромные ванны и лазеротерапию (24,4 и 16,1 %).
У больных без эндокринной патологии улучшение происходило за счет нейровегетативных и психоэмоциональных составляющих при отсутствии видимого влияния на метаболические параметры, тогда как у больных с сахарным диабетом влияние комплексов происходило в большей степени на психоэмоциональные и метаболические компоненты. В группе больных гипотиреозом комплексная терапия влияла на все составляющие климактерического синдрома, но в большей степени — на психоэмоциональный компонент.
В группе 1 определялось достоверное увеличение уровня глюкозы крови и ТТГ, значения которых тем не менее не выходили за рамки нормальных показателей; значительное повышение атерогенного индекса (АИ), а также уровня ИРИ. Это может быть связано с наличием значительного числа женщин с избыточной массой тела, формирующейся гиперинсулинемией и нарушением толерантности к глюкозе.
У больных сахарным диабетом отличия от 1-й группы прежде всего и в наибольшей степени относились к показателям углеводного обмена (уровень в крови глюкозы и НbА1с) и концентрации ИРИ в плазме крови (Р < 0,02), достоверно превышали не только нормальные показатели, но и те же показатели в группе без эндокринной патологии. Также достоверными были различия по индексу массы тела, величине атерогенного индекса, содержанию в крови иона К+ и активности в крови общей щелочной фосфатазы. В 3-й группе глюкоза крови, гликированный гемоглобин, ИРИ, атерогенный индекс не отличались существенно от таковых в группе 1. Следует отметить, что в данной группе определялся наиболее высокий уровень ТТГ, что свидетельствовало о недостаточной коррекции у ряда больных гипотиреозом.
Во всех группах определялось повышение уровня ФСГ и снижение уровня эстрадиола, типичное для перименопаузального периода.
В результате проведенного лечения у больных 1-й группы наблюдалось снижение уровня тощаковой глюкозы крови, АИ и ИРИ во всех основных группах, что, по-видимому, было связано с некоторым снижением веса. Во 2-й группе, помимо уровней глюкозы крови, ИРИ, АИ, наблюдалось и снижение уровня гликированного гемоглобина, что свидетельствовало об улучшении компенсации диабета, а также уменьшение инсулинорезистентности, что, по-видимому, связано с уменьшением веса. В 3-й группе достоверно уменьшился АИ во всех лечебных подгруппах и достоверно снизился ТТГ в контрольной группе и подгруппах 3В и 3Г.
Уровень ФСГ достоверно снизился только в группах 1Г и 2Г и 3Г, тогда как уровень эстрадиола существенно не изменился ни в одной из групп. В контрольных группах значимой динамики изученных показателей не наблюдалось, за исключением ТТГ в подгруппе 3А, где нескольким больным была увеличена доза L-тироксина. Снижение уровня ионизированного кальция по сравнению с нормой (1,24 ± 0,03 нмоль/л) было недостоверно в группе больных без эндокринной патологии (1,19 ± 0,04) и достоверно в группе 2 (1,18 ± 0,03, Р < 0,05) и группе 3 (1,16 ± 0,03, Р < 0,05). Активный метаболит витамина D — кальцитриол плазмы (норма 30,90 ± 1,15 нг/мл) был снижен во всех группах (1-я группа — 25,10 ± 2,23, Р < 0,05; 2-я группа — 23,80 ± ± 2,05, Р < 0,05; 3-я группа — 20,70 ± 3,05, Р < 0,05), наиболее низкий уровень отмечался у больных с гипотиреозом. Уровень паратиреоидного гормона (норма 38,1 ± 2,9 пмоль/л) достоверно отличался от нормального у больных 3-й группы (42,8 ± 5,6, Р < 0,05). Остеокальцин сыворотки (норма 6,2 ± 2,2 нг/мл) достоверно был повышен у всех больных (1-я группа — 8,8 ± 3,7, Р < 0,05; 2-я группа — 9,60 ± 2,85, Р < 0,05; 3-я группа — 11,80 ± 0,75, Р < 0,05), в большей степени у пациенток третьей группы. Общая щелочная фосфатаза достоверно отличалась от нормы (75,80 ± ± 5,12 Ед/л) у больных сахарным диабетом (105,3 ± 3,8, Р < 0,05) и гипотиреозом (110,5 ± 5,1, Р < 0,05). Полученные данные свидетельствовали о дисбалансе в системе костного метаболизма в сторону преобладания процессов остеолизиса над процессами остеосинтеза.
По данным денситометрии, индекс Т (норма 0,69 ± 0,02 ед.) свидетельствовал о наличии остеопении у пациенток обследованных групп, причем остеопения была более выражена у пациенток при наличии гипотиреоза (1-я группа — 1,40 ± 0,05, Р < 0,05; 2-я группа — 1,10 ± 0,07, Р < 0,05; 3-я группа — 2,45 ± 0,04, Р < 0,05).
Динамика показателей костного метаболизма в группах была следующей. У больных 1-й группы достоверное увеличение ионизированного кальция наблюдалось в подгруппах, получавших контрастные ванны и трансцеребральную электротерапию и радоновые ванны и ультразвук (на 18,1 и 11,3 % соответственно). Во 2-й и 3-й группах уровень ионизированного кальция увеличивался у больных, получавших радоновые ванны и ультразвук (на 12,9 и 19,3 %) и йодобромные ванны и лазеротерапию (на 9,6 и 32,4 %). Паратиреоидный гормон достоверно снизился у больных 3-й группы, получавших радоновые ванны и ультразвук и йодобромные ванны и лазеротерапию (на 14,9 и 13,4 % соответственно). Уровень кальцитриола достоверно повысился у больных 1-й группы при всех изучаемых лечебных программах, у больных 2-й и 3-й группы достоверное повышение этого показателя наблюдалось при назначении комплексов, состоявших из радоновых ванн и ультразвука и йодобромных ванн и лазеротерапии. Аналогичные изменения выявлены со стороны остеокальцина и щелочной фосфатазы. Различия наблюдались в 1-й группе, где ОЩФ не изменялась. Индекс Т — интегральный показатель состояния костного метаболизма — достоверно не изменялся ни в одной из лечебных групп, что свидетельствует о приостановке потери костной массы.
Наличие АГ установлено у 54,8 % больных. Систолическое артериальное давление (САД) было достоверно повышено относительно нормы (117,6 ± 9,2 мм рт.ст.) во всех группах больных и составило у больных без эндокринной патологии 149,9 ± 10,8 мм рт.ст. (Р < 0,05), у больных СД — 155,4 ± 8,7 мм рт.ст. (Р < 0,05) и у больных с гипотиреозом — 153,1 ± 10,2 мм рт.ст. (Р < 0,05). Диастолическое давление (ДАД) также было достоверно выше нормальных показателей (66,3 ± 4,18 мм рт.ст.) во всех группах, при этом у пациенток без эндокринной патологии его увеличение было выражено в меньшей степени (85,7 ± 6,2 мм рт.ст.), чем у больных с СД (98,7 ± 7,1 мм рт.ст.) и гипотиреозом (92,2 ± 8,1 мм рт.ст.). Для обследованных больных была характерна склонность к тахикардии, что проявлялось в увеличении числа сердечных сокращений относительно нормы (68,2 ± 4,2 уд/мин) и составило 79,70 ± ± 3,25 уд/мин у больных с климактерическим синдромом без эндокринной патологии, 75,1 ± 5,5 — у больных СД и 80,0 ± 6,6 уд/мин — у больных с гипотиреозом.
При эхокардиографическом исследовании зарегистрировано увеличение относительного минутного объема (норма 4,60 ± 0,31 л/мин), который был достоверно выше во всех группах: в первой группе — 5,22 ± ± 0,21 л/мин; во второй группе — 6,14 ± 0,41 л/мин; в третьей группе — 5,75 ± 0,23 л/мин. Обращает на себя внимание, что минутный объем был в большей степени увеличен у больных с сопутствующей эндокринной патологией. Фракция выброса оказалась ниже, чем в группе здоровых, и составила в первой группе 66,19 ± ± 2,22 %, во второй — 57,06 ± 4,72 %, в третьей — 62,10 ± 2,95 %, что достоверно ниже, чем в группе здоровых (70,26 ± 1,98 %). Конечный систолический и диастолический объемы также отличались. Так, КСО составил в первой группе 39,21 ± 4,13 мл, во второй — 52,72 ± 6,36 мл, в третьей — 42,68 ± 2,90 мл, в группе здоровых — 32,72 ± 2,25 мл. Аналогичные изменения касались конечного диастолического объема, значения которого составили для первой группы 123,43 ± ± 5,40 мл, для второй — 149,32 ± 7,34 мл, для третьей — 142,68 ± 2,90 мл. У больных обследованных групп наблюдалось увеличение массы миокарда левого желудочка по сравнению с группой здоровых (124,82 ± ± 4,61 г), которое в первой группе составило 141,42 ± ± 8,80 г, во второй — 157,18 ± 7,40 г, в третьей — 154,71 ± 5,91 г.
Оценка динамики параметров эхокардиографии у больных без эндокринной патологии показала, что МО снизился в данной группе под влиянием комплекса 1Г (на 10,9 %) и 1В (на 8,23 %). В подгруппе 1Б существенного влияния на этот параметр не выявлено. Во всех лечебных подгруппах наблюдалось повышение фракции выброса, которое составило 24,6 % в подгруппе 1Б, 22,8 % — в подгруппе 1Г, наименьшая динамика в подгруппе 1В — 20,2 %. КСО уменьшился в большей степени при использовании комплекса 1Г (36,8 %) и в меньшей степени — при использовании комплекса 1Б (27,9 %). Комплекс с радоновыми ваннами на этот показатель повлиял недостоверно. Уменьшение КДО наблюдалось во всех лечебных подгруппах, однако достоверно снижалось у больных, получавших комплекс 1Г (22,3 %) и 1Б (12,9 %). Аналогично снижалась ММ: в подгруппе 1Б — на 6,4 %, в подгруппе 1Г — на 12,0 %.
В группе с сахарным диабетом достоверное снижение систолического АД наблюдалось в равной степени во всех подгруппах: в подгруппе 2Б — 8,8 %, 2В — 9,1 % и 2Г — 7,9 %. Снижение диастолического давления наблюдалось в равной степени в подгруппах 2Б (25,5 %) и 2Г (24 %) и в меньшей степени — в подгруппе 2В (20,1 %). Наблюдавшееся снижение частоты сердечных сокращений (ЧСС) было статистически недостоверным.
У больных с гипотиреозом (группа 3) под влиянием комплексного лечения достоверно уменьшился МО: в подгруппе 3В — на 7,32 %, в подгруппе 3Г — на 5,7 %. Фракция выброса достоверно возрастала под влиянием этих комплексов (на 23,6 и 22,6 % соответственно). КСО уменьшался во всех подгруппах, получавших лечебные комплексы, при этом по влиянию на этот показатель наиболее эффективным оказался комплекс в подгруппе 3В (15,6 %), в меньшей степени — 3Г (13,7 %), в подгруппе 3Б динамика КСО оказалось недостоверной. Положительное действие на КДО наблюдалось только в подгруппах 3Г (17,0 %) и 3В (снижение на 8,4 %). Как и у больных диабетом, у больных с гипотиреозом не было найдено существенной динамики ММ под влиянием проводившихся курсов лечения. В группе с гипотиреозом нами отмечено достоверное процентное снижение только диастолического артериального давления у больных, получавших комплекс 3В (11,8 %) и 3Г (17,3 %). Снижение ЧСС было недостоверным. В контрольных группах положительной динамики не наблюдалось.
Оценка эффективности лечения проводилась по комплексу показателей, включающих субъективную оценку больным состояния, и результатов лабораторных и функциональных исследований после второго курса лечения. В соответствии с принятыми подходами выделялось три категории оценки: улучшение, без динамики, ухудшение. Улучшение проявлялось в уменьшении проявлений климактерического синдрома по данным ММИ, отсутствии прогрессирования в потере костной массы, в положительной динамике САД, ДАД и ЧСС, показателей углеводного и липидного обмена, гормональных показателей, положительной динамике ЭхоКГ.
В группы больных, закончивших лечение без динамики, были отнесены больные, не отмечавшие улучшения качества жизни, уменьшения проявлений климактерического синдрома по данным ММИ, при лабораторном и/или функциональном обследовании которых положительной динамики показателей выявлено не было, а также больные, не отмечавшие заметного субъективного улучшения, подтверждавшегося результатами обследования.
К отрицательным результатам относили отсутствие положительной субъективной динамики у больных, заявивших об усилении симптомов, сопровождавшемся ухудшением биохимических и инструментальных показателей.
При оценке эффективности повторных курсов лечения с использованием различных комплексов нами было проведено как сравнение по группам, имевшим различную сопутствующую эндокринную патологию, так и сравнение влияния различных комплексов внутри каждой из групп.
При оценке общей эффективности используемых комплексов оказалось, что при использовании комплекса, состоящего из контрастных ванн и интерференцтерапии, эффективность у больных без эндокринной патологии составила 78 %, у больных с сопутствующим сахарным диабетом — 63 %, а у больных с гипотиреозом — 68 %. Следует отметить, что в группах больных с сопутствующей патологией наблюдался наибольший процент больных, закончивших лечение без существенной динамики (18 % — при сахарном диабете, 21 % — при гипотиреозе) и с ухудшением (19 % — при диабете и 16 % — при гипотиреозе).
Комплекс, состоявший из радоновых ванн и ультразвука, оказался эффективным у 64 % больных без эндокринной патологии, у 81 % пациенток с сахарным диабетом и 84 % больных гипотиреозом. При этом использование данного комплекса у 15 % больных без сопутствующей патологии не приводило к объективному улучшению состояния, а у 21 % пациенток наблюдалось некоторое ухудшение состояния. В группах с сопутствующей эндокринной патологией количество больных, закончивших курс лечения без динамики, оказался существенно ниже (8 % — при сахарном диабете, 9 % — при гипотиреозе). Также ниже оказалось число больных с отрицательными результатами лечения (11 % — при сахарном диабете, 7 % — при гипотиреозе).
При назначении йодобромных ванн и лазеротерапии улучшение наблюдалось у 83 % больных без эндокринной патологии, 72 % больных сахарным диабетом и у 79 % больных гипотиреозом. Без динамики окончили лечение 9 % больных без сопутствующей патологии, 24 % больных сахарным диабетом и 15 % с гипотиреозом. Что касается ухудшения, то при назначении данного комплекса оно наблюдалось наиболее редко (у 8 % больных без патологии, у 4 и 6 % — при диабете и гипотиреозе соответственно).
Резюмируя вышеизложенное, можно заключить, что для больных с климактерическим синдромом без сопутствующей эндокринной патологии более эффективными были комплексы, состоявшие из контрастных ванн и электросна, а также из йодобромных ванн и лазеротерапии. Для больных сахарным диабетом и гипотиреозом более эффективно назначение комплекса из радоновых ванн и ультразвука и йодобромных ванн и лазеротерапии. Следует учитывать, что при примерно равной эффективности этих комплексов у данных категорий больных йодобромные ванны и лазеротерапия менее эффективны у больных сахарным диабетом по сравнению с больными гипотиреозом.
В группе больных без эндокринной патологии на проявления остеопороза в большей степени влияли все три лечебные программы, тогда как на состояние сердечно-сосудистой системы в большей степени оказывали влияние комплексы, состоящие из контрастных ванн и интерференцтерапии, а также йодобромных ванн и лазеротерапии.
Сравнение эффективности программ у больных сахарным диабетом выявило, что все лечебные программы в большей или меньшей степени влияли положительно на состояние сердечно-сосудистой системы у этих больных. Вместе с тем несколько большее положительное воздействие на МО, ФВ и КСО оказывали радоновые ванны и ультразвук и йодобромные ванны и лазеротерапия. Систолическое и диастолическое артериальное давление в большей степени изменялись под влиянием контрастных ванн и трансцеребральной терапии, хотя остальные программы также достоверно снижали уровень АД.
Изменения показателей углеводного обмена также носили однонаправленный положительный характер. Результаты были сопоставимы во всех группах больных, за исключением гликированного гемоглобина, который был достоверно ниже в группе, получавшей радоновые ванны и ультразвук. Данное наблюдение свидетельствует о том, что более адекватная долговременная коррекция углеводного обмена наблюдалась именно у больных, получавших этот комплекс. Что касается улучшения липидного обмена, то оно отмечено во всех группах, в большей степени — у больных сахарным диабетом, получавших контрастные ванны и трансцеребральную терапию. В этой же группе происходило достоверное снижение ТТГ. Достоверное повышение ионизированного кальция наблюдалось у больных подгрупп 2Б и 2Г, тогда как снижение цитозольного кальция выявлено во всех группах. Произошло значительное повышение уровня витамина D и снижение уровня остеокальцина, больше в подгруппе 2В. Обращает на себя внимание значительное снижение уровня ОЩФ во всех лечебных группах. Отсутствие существенной динамики индекса Т свидетельствовало о замедлении развития остеопенического синдрома.
Таким образом, у больных сахарным диабетом на состояние сердечно-сосудистой системы все изученные программы влияли примерно в одинаковой степени, а на проявления остеопении в большей степени влияли радоновые ванны и ультразвук и йодобромные ванны и лазеротерапия.
В группе больных с гипотиреозом результаты были наименее ярко выраженными. Следует отметить, что все исследованные программы влияли на ФВ и КСО, при этом большая динамика наблюдалась в подгруппе 3Г. В этой же подгруппе наблюдалось снижение МО и КДО, также ЧСС. ДАД значительно снижалось у больных подгрупп 3В и 3Г.
При использовании этих же программ наблюдалось значительное снижение ММИ и цитозольного кальция и повышение кальция ионизированного. На фоне повышения последнего происходило снижение уровня паратиреоидного гормона, витамина D, остеокальцина и щелочной фосфатазы. Индекс Т оставался относительно стабильным у больных, получавших эти программы, тогда как у больных подгруппы 3Б происходило некоторое дальнейшее снижение плотности костной ткани. Существенное влияние на показатели углеводного обмена все программы в этой группе не оказывали, тогда как улучшение липидного обмена наблюдалось во всех подгруппах.
Таким образом, как на состояние сердечно-сосудистой системы, так и на проявления остеопении в большей степени влияли программы, состоявшие из радоновых ванн и ультразвука и йодобромных ванн и лазеротерапии.
Отдаленные результаты оценивались через год после проведенного лечения по следующим параметрам: ИМТ, гликированный гемоглобин, АИ, САД, ДАД, ЧСС, опросник ММИ, индекс Т. Данные показатели были выбраны в связи с тем, что они в большей степени являются интегральными, отражающими как гормонально-метаболические параметры, так и состояние сердечно-сосудистой системы. Данные получены при обследовании 281 пациентки. Из них 91 человек составил группу больных без эндокринной патологии, 96 больных — с сахарным диабетом и 94 — с гипотиреозом. Оценка отдаленных результатов через год показала, что наиболее стойким эффектом обладают радоновые ванны и ультразвук, эффект от которых сохраняется у 67 % больных без эндокринной патологии, 68 % больных сахарным диабетом и у 62 % больных с гипотиреозом. При назначении остальных программ исследовавшиеся параметры возвращались к исходным у 75, 81 и 85 % соответственно.
Поскольку при различной эффективности все программы оказывали однонаправленное действие на исследовавшиеся показатели, было выдвинуто предположение о наличии общих предикторов, определяющих эффективность лечения независимо от назначавшихся программ. Второе выдвинутое предположение состояло в том, что предикторы эффективности отличаются в группах больных в зависимости от наличия или отсутствия сопутствующей эндокринной патологии. Однонаправленность действия изучавшихся программ позволила объединить больных, включенных в лечебные подгруппы в каждой из групп, в одну основную группу и сравнить ее с контрольной. Для подтверждения достоверности различий в результатах лечения в основных и контрольной группах был проведен статистический анализ с использованием четырехпольных таблиц. Сравнение проводилось в каждой из групп между больными, закончившими лечение с улучшением, и больными, не продемонстрировавшими положительного результата.
В группе 1 в графу А четырехпольной таблицы внесено 67 человек, закончивших лечение с улучшением, в графу В — 21 больная, не продемонстрировавшая положительного результата. В графу С внесены 13 больных контрольной группы, показавшие улучшение в результате лечения, в графу D — 16 человек из контрольной группы, окончивших лечение без улучшения. В группе больных с климактерическим синдромом без сопутствующей эндокринной патологии c2 составил 9,89. Уровень достоверности различий между группами P = 0,0017.
В группе 2 в графу А четырехпольной таблицы внесено 67 человек, закончивших лечение с улучшением, в графу В — 26 больных без положительного результата лечения. В графу С внесены 13 больных контрольной группы, показавшие улучшение в результате лечения, в графу D — 18 человек контрольной группы, окончивших лечение без улучшения. В группе больных с климактерическим синдромом с сопутствующим сахарным диабетом c2 составил 9,21. Уровень достоверности различий между группами P = 0,0024.
В группе 3 в графу А четырехпольной таблицы внесена 71 пациентка, закончившая лечение с улучшением, в графу В — 21 больная, не продемонстрировавшая положительного результата. В графу С внесены 11 больных контрольной группы, показавшие улучшение в результате лечения, в графу D — 19 человек из контрольной группы, окончивших лечение без улучшения. В группе больных с климактерическим синдромом с сопутствующим гипотиреозом c2 составил 16,84. Уровень достоверности различий между группами P = 0,0001.
Таким образом, использовавшиеся программы физиобальнеотерапии оказывали достоверное положительное влияние на состояние больных с климактерическим синдромом как при отсутствии эндокринной патологии, так и при наличии сопутствующего СД и гипотиреоза.
На втором этапе для выявления причинно-следственной связи, положительной или отрицательной зависимости между изучавшимися показателями использован линейный корреляционный анализ, который показал тесную связь показателей, характеризующих метаболизм углеводов (глюкоза, ИРИ), липидов (АИ), кальциевого обмена (Са ионизированный, ПТГ, 1,25 (OH)2D3, ОК, индекс Т), ТТГ с состоянием сердечно-сосудистой системы (МО, КДО, КСО, САД, ДАД) и с проявлениями климактерического синдрома (ММИ). Представляет интерес тот факт, что при наличии эндокринной патологии увеличивается число корреляционных связей между биохимическими и гормональными показателями, характеризующими углеводный обмен, с показателями состояния сердечно-сосудистой системы (при сахарном диабете), а при гипотиреозе увеличивалось количество и качество связей, характеризующих костный метаболизм, с показателями состояния сердечно-сосудистой системы.
При сахарном диабете характер связей между показателями несколько изменился. Наряду со связями, характерными для больных без эндокринной патологии, появились новые связи. Так, появилась связь ИРИ с Са ионизированным и показателями, характеризующими костный метаболизм (D3, ОК, ОЩФ), сформировалась связь ФСГ с ТТГ. Увеличилось число связей между Са цитозольным и показателями состояния сердечно-сосудистой системы. Анализ выявленных связей позволил предположить, что в данной группе, как и в первой, возможными предикторами можно считать ИРИ, ФСГ, Са цитозольный и Са ионизированный.
В группе с гипотиреозом корреляционные связи в большей степени проявлялись между показателями, влияющими на костный метаболизм, и показателями состояния сердечно-сосудистой системы. Центральное место по количеству и качеству связей стал занимать тиреотропный гормон, тогда как ИРИ потерял ведущую роль, что позволяет предположить, что в данном случае роль предиктора перешла к ТТГ. Цитозольный и ионизированный Са продемонстрировали многочисленные связи с состоянием сердечно-сосудистой системы, уровнем тиреотропного гормона, D3, ОК, индексом Т и ММИ. ФСГ через эстрадиол также оказался связан с показателями костного метаболизма и через них — с индексом Т. В данной группе характер корреляционных связей позволяет предположить, что предикторами эффективности лечения могут быть ТТГ, ФСГ, кальций цитозольный и ионизированный.
Для подтверждения или опровержения гипотезы о значимости предполагаемых предикторов применен пошаговый дискриминантный анализ. В результате анализа была определены показатели, в большей степени влияющие на результат лечения, которые совпали с гипотетическими.
Результаты дискриминантного анализа подтвердили выдвинутую гипотезу и показали, что предикторами эффективности в группе больных без эндокринной патологии и с сопутствующим сахарным диабетом являются уровень ИРИ, ФСГ, ионизированного и цитозольного кальция. В группе больных с сопутствующим гипотиреозом предикторами эффективности являются уровни ТТГ, ФСГ, цитозольного и ионизированного кальция.
С клинической точки зрения, полученные результаты имеют под собой достаточное основание и подтверждаются динамикой показателей, оцениваемых как предикторы.
Группы пациентов с отрицательными и положительными результатами при применении программ лечения с использованием методов физиобальнеотерапии достоверно различались по всем показателям, которые выступали как предикторы эффективности лечения. Так, положительные результаты во всех группах были получены у больных с более низкими уровнями ФСГ и Са цитозольного и более высоким уровнем Са ионизированного (Р < 0,05). В группах 1 и 2 положительные результаты лечения были получены у больных с более низким уровнем ИРИ, а в группе 3 — с более низким ТТГ.
Таким образом, можно заключить, что эффективность лечения выше у больных с меньшими отклонениями данных показателей от нормы, а следовательно, чем раньше начаты профилактические мероприятия с использованием программ физиобальнеотерапии, тем большую эффективность можно ожидать.
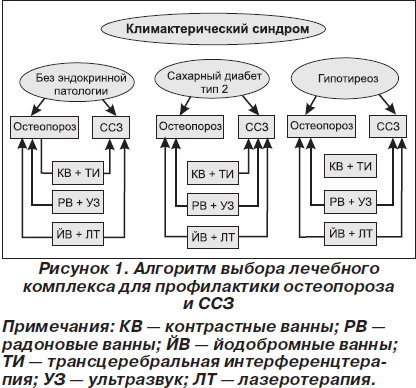
Полученные результаты позволили разработать алгоритм назначения программ лечения (рис. 1).
Выводы
1. Разработанные дифференцированные программы корригируют проявления климактерического синдрома. Об этом свидетельствует уменьшение количества больных с тяжелыми проявлениями климакса и увеличение — с легкими его проявлениями. Наибольшая эффективность отмечена в группах, не отягощенных эндокринопатиями. Улучшение происходит за счет нейровегетативных и психоэмоциональных составляющих при отсутствии достоверного влияния на метаболические. У больных с ассоциированным сахарным диабетом влияние программ происходит в большей степени на метаболические и психоэмоциональные процессы. В группе больных аутоиммунным гипотиреозом отмечено влияние на все составляющие климактерического синдрома, но в большей степени — на психоэмоциональный компонент.
2. Программа, включающая контрастные ванны и трансцеребральную интерференцтерапию, корригирует углеводный и липидный обмены, тормозит потерю костной массы, улучшает функциональное состояние миокарда, приводит к снижению артериального давления у больных без ассоциированной эндокринной патологии и у больных сахарным диабетом типа 2. У больных с аутоиммунным гипотиреозом данный комплекс улучшает липидный обмен, не оказывая положительного влияния на сохранение костной массы, и незначительно влияет на функциональное состояние миокарда и сосудов.
3. Программа, включавшая радоновые ванны и ультразвук, положительно влияет на показатели углеводного обмена у больных без эндокринной патологии и у больных сахарным диабетом, тормозит потерю костной массы во всех группах, улучшает состояние сердечно-сосудистой системы у больных всех групп, в большей степени — у больных с сопутствующей эндокринной патологией.
4. Йодобромные ванны и лазеротерапия в отличие от других программ приводят к снижению уровня ФСГ, улучшают состояние липидного обмена, тормозят потерю костной массы, улучшают состояние сердечно-сосудистой системы у больных всех групп, в большей степени — у больных без эндокринной патологии и у больных диабетом, а также оказывают положительное влияние на показатели углеводного обмена в этих группах.
5. У больных сахарным диабетом все исследуемые программы оказались эффективными в отношении влияния их на состояние сердечно-сосудистой системы. На состояние костной системы в большей степени влияют программы, состоящие из радоновых ванн и ультразвука, йодобромных ванн и лазеротерапии.
6. У больных с гипотиреозом программы, включавшие контрастные ванны и трансцеребральную интерференцтерапию, а также йодобромные ванны и лазеротерапию, в большей степени влияют на костную и на сердечно-сосудистую системы, не оказывая существенного влияния на показатели углеводного обмена.
7. Предикторами эффективности предложенных программ у больных без эндокринной патологии и у больных сахарным диабетом являются уровни ИРИ, ФСГ и цитозольного кальция, у больных гипотиреозом — уровни ТТГ, ФСГ, ионизированного и цитозольного кальция. При меньшем отклонении от нормы этих показателей эффект лечения повышается.
1. Калинин А.П., Лукьянчиков В.С., Королевская Л.И. Щитовидная железа: физиология, классификация тиреоидных болезней, методы диагностики и лечения // Materia Medica. — 2001. — № 2. — С. 3-11.
2. Лукьянчиков В.С., Калинин А.П., Королевская Л.И. Тиреотоксический синдром // Materia Medica. — 2001. — № 2. — С. 12-19.
3. Королевская Л.И. Геронтологический аспект патогенеза артериальной гипертонии при сахарном диабете и первичном альдостеронизме // Сборник научно-практических трудов сотрудников ЦБ № 6 МПС. — 2002. — С. 25-27.
4. Лукьянчиков В.С., Королевская Л.И., Кочергина И.И., Зефирова Г.С. Сахарный диабет // Проблемы эндокринной патологии. — 2003. — № 2. — С. 77-85.
5. Ильенко Л.И., Лукьянчиков В.С., Королевская Л.И. Климакс и его осложнения (учебное пособие). — М.: МГМСУ, 2003. — 21 с.
