Журнал «Медицина неотложных состояний» 3(34) 2011
Вернуться к номеру
Гемодинамічна відповідь на рідинну ресусцитацію у хворих з абдомінальним сепсисом
Авторы: КУРСОВ С.В. Харківський національний медичний університет
Рубрики: Семейная медицина/Терапия, Медицина неотложных состояний
Версия для печати
У 244 пацієнтів з ознаками абдомінального сепсису вивчено ефект рідинної ресусцитації за допомогою сучасних плазмозамінників на зміни показників центральної гемодинаміки. При оцінці тяжкості стану за шкалою Acute Physiology And Chronic Health Evaluation II (АРАСНЕ-ІІ) не більше 10 балів не знайдено переваг сумісного застосування колоїдних та кристалоїдних розчинів перед використанням виключно кристалоїдних плазмозамінників. При оцінці тяжкості стану за шкалою АРАСНЕ-ІІ у межах 11–20 балів перевагу мали схеми, що включали застосуванням колоїдних розчинів. При оцінці тяжкості стану понад 20 балів можна простежити істотні недоліки використання виключно кристалоїдних розчинів. Ефективна гемодинамічна підтримка досягається лише за умови лікування, що передбачає введення колоїдних плазмозамінників. Найкращі результати одержані при застосуванні похідних гідроксиетилкрохмалю.
Абдомінальний сепсис, центральна гемодинаміка, кристалоїдні плазмозамінники, гелофузин, рефортан, венофундин.
Вступ
Згідно з положеннями Міжнародної програми, що розроблена Кампанією за виживаність при сепсисі (Surviving Sepsis Campaign), одним із провідних заходів інтенсивної терапії хворих на сепсис є рання рідинна ресусцитація [1, 3, 7]. Швидка рідинна ресусцитація в перші 6 годин від діагностування захворювання вірогідно забезпечує зростання показника виживаності хворих із сепсисом у найближчі 28 днів [3, 7, 8]. Причому під час проведення рідинної ресусцитації при сепсисі ще й досі відсутні очевидні докази переваги будь-якого з сучасних плазмозамінників. Тобто кристалоїдні розчини за своїм ефектом не поступаються колоїдним, а серед останніх відсутні ті, що мають найкращий ефект щодо зниження смертності [3]. Зазначене положення викликає чималу кількість сумнівів у практичних лікарів, тому що певні переваги колоїдних плазмозамінників є добре відомими. Колоїдні плазмозамінники значно довше утримуються в судинному руслі, через що зменшується загальний об’єм інфузійної терапії, потрібний для забезпечення ефективної центральної гемодинаміки (ЦГД), мікроциркуляції, транспорту кисню без небезпечного зростання об’єму рідини в інтерстиціальному секторі позаклітинного водного простору, набряку мембран та погіршення процесів дифузії газів [4, 5]. Беручи до уваги той факт, що більшість досліджень, на підставі яких розроблене положення про ранню рідинну ресусцитацію, проводилися без чіткого врахування віку та тяжкості стану хворих, ми вирішили зробити власний аналіз ефекту терапії кристалоїдними та колоїдними плазмозамінниками у хворих з ознаками абдомінального сепсису із розподіленням їх за групами згідно зі ступенем тяжкості стану за шкалою Acute Physiology And Chronic Health Evaluation II (APACHE-II) [1, 2, 6].
Шкала АРАСНЕ-ІІ являє собою сучасну систему оцінки тяжкості стану та життєздатності хворих, що враховує їх вік, супутню патологію, плановість чи ургентність виконання хірургічної корекції, а також показники центральної гемодинаміки, частоти дихання, забезпечення киснем, показники гематокриту, концентрації електролітів та буферних основ у плазмі крові, ректальну температуру, величину лейкоцитозу та ін. [1, 2, 6]. Разом із підвищенням кількості балів за шкалою APACHE-II зростає і показник летальності хворих. Так, при оцінці, що становить 0–9 балів, летальність не перевищує 7,5 %, при оцінці 10–14 балів смертність досягає 11 %, а при оцінці 25–29 балів може сягати 51 % [6].
Мета дослідження — простежити у хворих з абдомінальним сепсисом, які мають різну стартову оцінку тяжкості стану за шкалою Acute Physiology And Chronic Health Evaluation-II, зміни гемодинаміки при різному складі рідинної ресусцитації.
Матеріали і методи
Дослідження проведено у 244 пацієнтів віком від 18 до 91 років з ознаками абдомінального сепсису.
Відносно низьку стартову оцінку тяжкості стану, що становила не більше 10 балів за шкалою APACHE‑II, мали 92 пацієнти. У 26 хворих (1-ша група) застосовані тільки кристалоїдні плазмозамінники (базовий — розчин Рінгера). 21 пацієнт (2-га група) разом із кристалоїдами отримували колоїдний розчин на основі модифікованої желатини — гелофузин. 27 хворим (3-тя група) разом із кристалоїдами вводили препарат гідроксиетилкрохмалю 200/0,5 (ГЕК 200/0,5) — 6% розчин рефортану. У 18 хворих (4-та група) разом із кристалоїдами застосований препарат останньої генерації ГЕК — гідроксиетилкрохмаль 130/0,4 (ГЕК 130/0,4) — венофундин.
У 88 пацієнтів з ознаками абдомінального сепсису середня стартова оцінка тяжкості стану становила 11–20 балів за шкалою APACHE-II. У 16 хворих (5-та група) застосовано тільки кристалоїдні плазмозамінники (базовий — розчин Рінгера). 22 пацієнти (6-та група) разом із кристалоїдами отримували гелофузин. 26 хворим (7-ма група) разом із кристалоїдами вводили 6% розчин рефортану. У 24 хворих (8-ма група) разом із кристалоїдами застосований венофундин.
Високу стартову оцінку тяжкості стану, що становила понад 20 балів за шкалою APACHE-II, мали 64 хворі. У 8 хворих (9-та група) застосовані тільки кристалоїдні плазмозамінники (розчин Рінгера). 17 пацієнтів (10-та група) разом із кристалоїдами отримували гелофузин. 25 хворим (11-та група) разом із кристалоїдами вводили 6% розчин рефортану. У 14 хворих (12-та група) разом із кристалоїдами застосований венофундин.
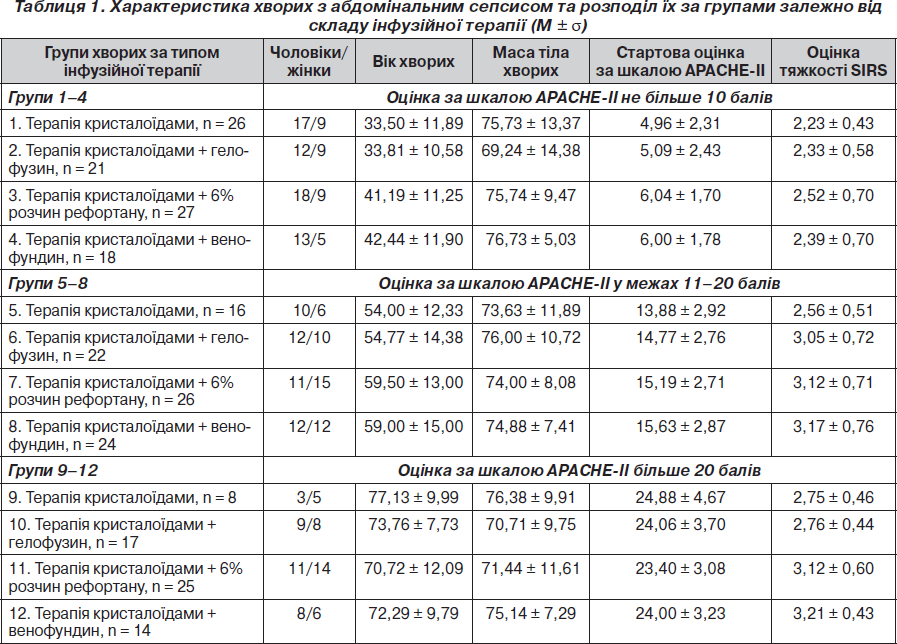
Колоїдні плазмозамінники вводилися в дозі від 1000 до 1500 мл на добу залежно від маси тіла пацієнтів. Згідно з рекомендаціями програми Surviving Sepsis Campaign за допомогою інфузій намагалися досягти у хворих через 6 годин лікування значення центрального венозного тиску (ЦВТ) 100 мм вод.ст. та підтримувати його на цьому рівні протягом 3 діб. Інші компоненти інтенсивної терапії значно не відрізнялися. Більше ніж у 90 % випадків антибактеріальна терапія проводилася за допомогою цефалоспоринів ІІІ покоління разом із фторхінолонами ІІ–IV покоління та метронідазолом. Тяжкість проявів абдомінального сепсису визначена за шкалою SIRS (синдром системної запальної відповіді) [1–3]. Згідно з класифікацією R. Bone, щоб встановити діагноз «сепсис», достатньо 2 ознак наявності системної запальної реакції (температура тіла вище 38 °С або нижче 36 °С, частота серцевих скорочень (ЧСС) понад 90 за хвилину, частота дихання — понад 20 за хвилину при напруженні вуглекислого газу в артеріальній крові 32 мм рт.ст. та менше, кількість лейкоцитів у крові понад 12 ґ 109/л або менше 4 ґ 109/л, або наявність не менше 10 % незрілих клітин) та, обов’язково, вогнища інфекції. У всіх хворих були такі ознаки. Прояви SIRS характеризувалися наявністю 2–4 ознак. Відомості про групи хворих, які включені до дослідження, наведені у табл. 1.
Показники ЦГД вивчали перед операцією та на 1-шу, 2-гу, 3-тю, 5-ту та 7-му добу після неї за допомогою тетраполярної інтегральної реографії, артеріотензометрії та флеботензометрії. ЧСС визначали за кількістю комплексів QRS на моніторі Utas, а частоту пульсу (ЧП) — за кількістю хвиль реограми або сфігмограми за хвилину. За даними реограми розраховували ударний об’єм серця (УОС) та за допомогою останнього, ЧП і значень артеріального тиску (АТ) — усі інші показники. У 1, 2, 3 та 4-й групах ЦВТ вивчали тільки протягом перших 3 діб, оскільки це визначалося швидким покращенням стану хворих та відсутністю потреби у тривалій катетеризації центральних вен. У 5–12-й групах ЦВТ вивчали протягом 7 діб через більш тяжкий стан хворих, потребу в тривалій інфузійній підтримці та контроль за випадками виникнення серцевої слабкості і коригування темпу введення рідини до організму. Результати дослідження оброблено з використанням t-критерію Стьюдента.
Результати дослідження та їх обговорення
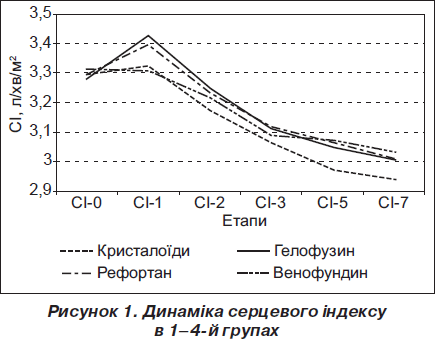
Аналіз результатів дослідження показав, що при оцінці тяжкості стану хворих за шкалою АРАСНЕ-ІІ, що не перевищувала 10 балів, не було знайдено переваг застосування колоїдних плазмозамінників. Показники ЦГД у хворих 1–4-ї груп протягом 7 діб дослідження істотно не відрізнялися. Виявлено, що на 5-ту добу дослідження в пацієнтів, яким уводили 6% розчин рефортану, був вірогідно більший ударний індекс (УІ), ніж той, що спостерігали при введенні виключно кристалоїдних розчинів (УІ5 = 37,13 ± 2,36 мл/м2 та 38,96 ± 2,19 мл/м2; р = 0,008). Середній АТ на 3-тю добу був також вищим при використанні рефортану порівняно з даними хворих 1-ї групи (САТ3 = 90,06 ± 7,89 мм рт.ст. та 94,57 ± 5,42 мм рт.ст.; р = 0,0187). Проте випадків смертності серед хворих з відносно низькою оцінкою тяжкості стану не спостерігали. Усі 92 пацієнти були переведені з відділення інтенсивної терапії (ВІТ) до хірургічних відділень і потім виписані з лікарні. Таким чином, суттєвих переваг застосування колоїдних плазмозамінників у цього контингенту хворих не було знайдено. Ситуацію ілюструє динаміка серцевого індексу (СІ) в 1–4-й групах, що відображено на рис. 1.
При стартовій оцінці за шкалою АРАСНЕ-ІІ, що становила 11–20 балів, у хворих з ознаками абдомінального сепсису виявлено перевагу використання колоїдних плазмозамінників. Так, при застосуванні похідних ГЕК 200/0,5 та 130/0,4 порівняно з ресусцитацією виключно кристалоїдними розчинами у хворих вірогідно швидше усувалася тахікардія. На 2-гу та 3-тю добу ЧСС при використанні виключно кристалоїдів становила 102,31 ± 11,57 за 1 хв та 100,75 ± 12,99 за 1 хв, тоді як при застосуванні 6% розчину рефортану — 92,04 ± 9,80 за 1 хв та 89,04 ± 9,70 за 1 хв (р = 0,0037 та р = 0,0018). На 5-ту та 7-му добу ЧСС при інфузії виключно кристалоїдів дорівнювала 93,69 ± 12,27 за 1 хв та 84,18 ± 3,31 за 1 хв, тоді як при додаванні венофундину — 83,95 ± 5,27 за 1 хв та 80,76 ± 3,42 за 1 хв (р = 0,003 та р = 0,011).
УОС, що становив на 2-гу добу в 5-й групі 59,94 ± 10,75 мл, був вірогідно нижчим, ніж при застосуванні рефортану (68,69 ± 7,23 мл; р =0,003) та венофундину (66,83 ± 8,35; р = 0,028). На 3-тю добу дослідження УОС виявився вірогідно вищим при використанні всіх колоїдних плазмозамінників. При введенні кристалоїдів він дорівнював 58,56 ± 12,07 мл, при додаванні гелофузину — 65,67 ± 8,87 мл, рефортану — 70,23 ± 8,33 мл, венофундину — 68,50 ± 10,26 мл. На 5-ту та 7-му добу дослідження виявлено вірогідно вищі показники УОС при застосуванні венофундину порівняно з ресусцитацією виключно кристалоїдними розчинами.
Хвилинний об’єм кровообігу (ХОК) після хірургічної корекції в усіх випадках виявився вищим при використанні колоїдних плазмозамінників порівняно з терапією виключно кристалоїдами, проте вірогідну відмінність виявлено лише на 3-тю добу. В цей час у 5-й групі ХОК дорівнював 5,78 ± 0,71 л/хв, а при додаванні рефортану — 6,19 ± 0,45 л/хв (р = 0,027).
Серцевий індекс при використанні на 2-гу добу був вірогідно вищим при застосуванні гелофузину порівняно з інфузією виключно кристалоїдів. У хворих 5-ї групи СІ в цей час становив 3,24 ± 0,25 л/хв/м2, тоді як у хворих 6-ї групи дорівнював 3,41 ± 0,26 л/хв/м2 (р = 0,049). На 3-тю добу СІ в усіх групах, де застосували колоїдні плазмозамінники, був вірогідно вище, ніж при використанні виключно кристалоїдів.
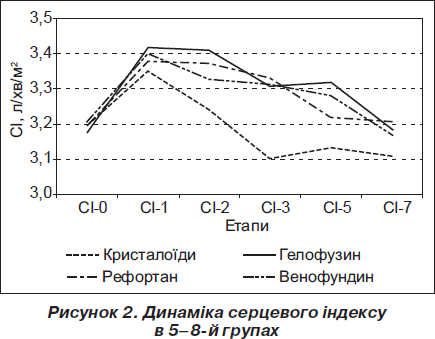
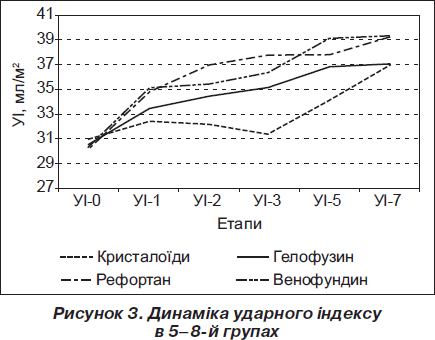
Показник УІ, як і показник ХОК, протягом усього часу спостереження після операції при терапії колоїдними плазмозамінниками був вірогідно вищим, ніж у хворих 5-ї групи. Вірогідні відмінності знайдено протягом усього часу спостереження при застосуванні венофундину. УІ дорівнював у 5-й та 8-й групах на 1-шу, 2-гу, 3-тю, 5-ту і 7-му добу дослідження відповідно 32,41 ± 4,82 мл/м2 і 35,21 ± 3,78 мл/м2; 32,16 ± 5,03 мл/м2 і 35,45 ± 3,73 мл/м2; 31,39 ± 5,63 мл/м2 і 36,33 ± 4,84 мл/м2; 34,00 ± 5,21 мл/м2 і 39,08 ± 1,46 мл/м2; 36,97 ± 1,69 мл/м2 і 39,24 ± 1,37 мл/м2 (р = 0,047; 0,023; 0,005; 0,0002; 0,0003). На 2-гу та 3-тю добу спостереження порівняно з УІ 5-ї групи виявлено вірогідну перевагу використання рефортану. На рис. 2 і 3 зображено динаміку серцевого та ударного індексів у групах хворих, в яких зареєстровано оцінку за шкалою АРАСНЕ-ІІ у межах 11–20 балів.
Смертність у групах виявилася такою: у 5-й групі (кристалоїди) — 31,25 %; 6-й групі (кристалоїди + гелофузин) — 13,64 %; 7-й групі (кристалоїди + 6% розчин рефортану) — 11,54 %; 8-й групі (кристалоїди + венофундин) — 12,50 %.
У групах хворих з оцінкою за шкалою АРАСНЕ-ІІ понад 20 балів на 1-шу добу лікування у ВІТ знайдено, що пацієнти 11-ї та 12-ї груп мали меншу ЧСС, ніж хворі 9-ї групи (р = 0,038 та р = 0,008). Меншою в них була і ЧП (р = 0,007 та р = 0,022). ЧСС була меншою у хворих 12-ї групи порівняно з хворими 10-ї групи (р = 0,049). ЧП суттєво зменшилася при використанні ГЕК 200/0,5 та вірогідно відрізнялася від ЧП хворих, яким уводили модифіковану желатину (р = 0,031). УОС був вірогідно більшим у хворих, яким уводили похідні ГЕК, порівняно з тими, хто отримував лише кристалоїдні розчини (р = 0,009 і р = 0,002). СІ та УІ виявилися вірогідно більшими при використанні всіх колоїдних плазмозамінників (для СІ: р = 0,026, р = 0,0003 і р = 0,002; для УІ: р = 0,028, р = 4,32 ґ Е–5, р = 0,0002).
На 2-гу добу пацієнти, яким уводили гелофузин, мали перевагу перед хворими, яким уводили виключно кристалоїди, за показником УІ (р = 0,039). Натомість у тих, хто отримував похідні ГЕК (обидві групи — 11‑та і 12-та), порівняно з хворими 9-ї групи були: менша ЧСС (р = 0,008 та р = 0,03), менша ЧП (р = 0,002 та р = 0,008), більший УОС (р = 0,01 та р = 0,002), більший СІ, що не притаманний гіпердинамії (р = 0,0021 та р = 0,0022) та більший УІ (р = 2,99 ґ Е–5 та р = 0,0002). ЧСС була меншою у хворих 11-ї та 12-ї груп, ніж у пацієнтів 10-ї групи (р = 0,026 і р = 0,012). СІ також виявився кращим при застосуванні похідних ГЕК порівняно з желатиною (р = 0,045 і р = 0,049).
На 3-тю добу показники ЧСС та ЧП у хворих 11-ї та 12-ї групи залишалися кращими за ті, що реєстрували при застосуванні виключно кристалоїдних розчинів (для ЧСС: р = 0,003 та р = 0,007; для ЧП: р = 0,008 та р = 0,016). В усіх групах дослідження, де використані колоїдні плазмозамінники, показники СІ та УІ були вірогідно вищими за показники пацієнтів 9-ї групи (для СІ: р = 0,016, р = 0,0001 та р = 0,003; для УІ: р = 0,048, р = 2,99 ґ Е–5 та р = 0,003). В усіх групах, де використані колоїди, констатовано наявність більшого діастолічного АТ, ніж був у тих, кому вводили виключно кристалоїди (р = 0,027, р = 0,03 та р = 0,045). При цьому у хворих, яким уводили колоїдні розчини, спостерігали менші показники ЦВТ, що в даній ситуації вказувало на меншу кількість випадків серцевої слабкості (р = 0,049, р = 0,042 та р = 0,031). Порівняно з тими, хто отримував модифіковану желатину, у хворих, яким уводили розчини ГЕК, спостерігалися менші прояви тахікардії (для ЧП: р = 0,047 і р = 0,044). Пацієнти, яким уводили 6% розчин рефортану, мали більший показник УІ порівняно з хворими, які отримували гелофузин (р = 0,018).
На 5-ту добу дослідження виявлено суттєву перевагу лікування модифікованою желатиною порівняно з терапією виключно кристалоїдами, проте на той час смертність становила: в 9-й групі — 37,5 %, 10-й групі — 29,41 %, 11-й групі — 12 %, 12-й групі — 0 %. Усі пацієнти з ознаками абдомінального сепсису, які отримували модифіковану желатину, загинули в 3–4-денний період. Тому надалі 10-та група пацієнтів мала кращі показники ЦГД. Та при порівнянні цих показників з показниками хворих, які отримували 6% розчин рефортану і венофундин, переваги терапії похідними желатини не виявлено. Серед тих, хто вижив, у 10-й групі дослідження спостерігали більший відсоток пацієнтів із гіпертонічною хворобою.
На 7-му добу пацієнти 11-ї групи мали менші прояви тахікардії, ніж хворі 9-ї групи (для ЧСС — р = 0,022; для ЧП — р = 0,011). УІ був більшим у пацієнтів 10-ї та 11-ї груп порівняно з 9-ю групою (р = 0,039 та р = 0,019). Порівняно з тими, кому у складі інфузійної терапії вводили виключно кристалоїдні розчини, при застосуванні ГЕК 200/0,5 спостерігали більше значення СІ (р = 0,003). Хворі 11-ї групи мали меншу за хворих 10-ї групи ЧП (р = 0,045).Також при застосуванні 6% розчину рефортану порівняно з випадками використання гелофузину виявлено перевагу в показнику УІ (р = 0,026). Смертність на 7-му добу дослідження становила: в 9-й групі — 50 %, 10-й групі — 29,41 %, 11-й групі — 16 %, 12-й групі — 7,14 %.
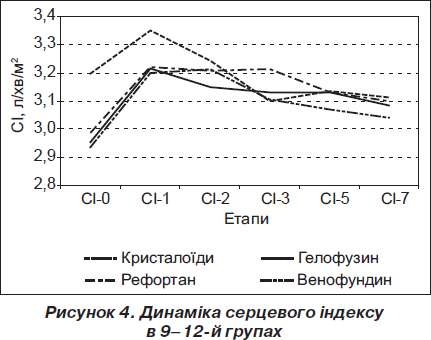
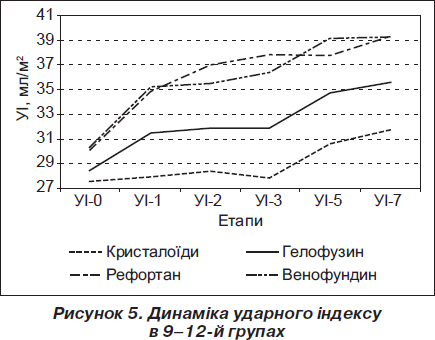
На рис. 4 і 5 подано динаміку серцевого та ударного індексу в групах хворих з абдомінальним сепсисом при стартовій оцінці за шкалою АРАСНЕ-ІІ понад 20 балів.
Висновки
Результати дослідження свідчать, що у хворих з абдомінальним сепсисом, які мають відносно низьку оцінку тяжкості стану за шкалою АРАСНЕ-ІІ, ефективна ресусцитація можлива без використання колоїдних плазмозамінників, що підтверджує доцільність рекомендацій Кампанії за виживаність при сепсисі. Проте при більш тяжкому стані хворих до складу рідинної ресусцитації потрібно обов’язково включати колоїдні плазмозамінники. Це супроводжується покращенням гемодинамічних показників та зниженням смертності хворих. Перевагу слід віддати похідним гідроксиетилкрохмалю.
1. Мальцева Л.А. Сепсис: этиология, эпидемиология, патогенез, диагностика, интенсивная терапия / Мальцева Л.А., Усенко Л.В., Мосенцев И.Ф. — Москва: МЕДпресс-информ, 2005. — 176 с.
2. Оценка тяжести состояния хирургического больного / Сипливый В.А., Дронов А.Н., Конь Е.В., Евтушенко Ф.В. — Киев: Майстерня книги, 2009. — 128 с.
3. Dellinger R.P. Surviving Sepsis Campaign: International guidelines for management of severe sepsis and septic shock: 2008 / R.P. Dellinger, M.M. Levy, J.M. Carlet et al. // Intensive Care Medicine. — 2008. — Vol. 34(1). — P. 17-60.
4. Finfer S. SAFE Study Investigators (2004). A comparison of albumin and saline for fluid resuscitation in the intensive care unit / S. Finfer, R. Bellomo, N. Boyce et al. // New England Journal of Medicine. — 2004. — Vol. 350. — P. 2247-2256.
6. Hoffman J.N. Hydroxyethyl starch, but not crystalloid support, improves microcirculation during normotensive endotoxemia / J.N. Hoffman, B. Vollmar, M.W. Laschke et al. // Anesthesiology. — 2002. — Vol. 97(2). — P. 460-470.
7. Knaus W.A. APACHE-II: a severity of disease classification system / W.A. Knaus, E.A. Draper, D.P. Wagner, J.E. Zimmerman // Critacal Care Medicine. — 1985. — Vol. 13(10). — P. 818-829.
8. Otero M.R. Early goal-directed therapy in severe sepsis and septic shock revisited concepts, controversies and contemporary findings / M.R. Otero, H.B. Nguyen, D.T. Huang et al. // Chest. — 2006. — Vol. 130(5). — P. 1579-1595.
9. Rivers E. Early Goal-Directed Therapy Collaborative Group (2001). Early goal-directed therapy in the treatment of severe sepsis and septic shock / E. Rivers, B. Nguyen, S. Havstad et al. // New England Journal of Medicine. — 2001. — Vol. 345(19). — P. 1368-1377.