Журнал «Медицина неотложных состояний» 5 (36) 2011
Вернуться к номеру
Клінічний досвід використання гідроксіетилкрохмалю другої генерації Хетасорб у пацієнтів із травматичним, геморагічним шоком та гіповолемічними станами
Авторы: Недашківський С.М., Бишовець С.М. НМАПО ім. П.Л. Шупика, кафедра анестезіології та інтенсивної терапії, м. Київ Крилов С.В. Вишгородська центральна районна лікарня Кучма А.В. Київська обласна клінічна лікарня
Рубрики: Семейная медицина/Терапия, Медицина неотложных состояний
Версия для печати
Хирург славен теми операциями, которых сумел избежать; анестезиолог — теми кровопотерями, при которых обошелся без гемотрансфузий.
А.П. Зильбер [2]
За даними ВООЗ, упродовж року від політравми гине близько 2 мільйонів людей [3, 7]. Серед осіб молодого віку смертність від неї перевищує смертність від серцево-судинних захворювань у 10, а від онкологічних — у 20 разів [1, 4]. Згідно з абсолютними показниками летальних випадків травматизм займає друге місце після серцево-судинних захворювань, а серед осіб працездатного віку — перше. Із числа померлих від дорожньо-транспортних пригод в Україні 18,6 % постраждалих помирає на госпітальному етапі, а 81,4 % — безпосередньо на місці пригоди. У 80 % постраждалих із травматичними ушкодженнями смерть настає в перші шість годин, переважно від гострої масивної крововтрати й пов’язаних із нею патологічних реакцій та внаслідок черепно-мозкової травми (Шищук В.Д., Шкатула Ю.В., 2009 р.).
Пацієнти з гострими порушеннями мозкового кровообігу, породіллі з кровотечами, хворі з септичними станами також становлять значний відсоток від госпіталізованих до відділень інтенсивної терапії і потребують своєчасної корекції волемічного стану, порушень мікроциркуляції й пов’язаних із ними метаболічних розладів.
Незважаючи на існування численних рекомендацій і протоколів щодо інтенсивної терапії шокових станів, гострої крововтрати, гіповолемії, тактика інфузійної терапії, вибір оптимальних препаратів до останнього часу є предметом дискусій.
Патофізіологічні зміни, що відбуваються в потерпілих унаслідок зменшення кількості циркулюючої рідини в судинному руслі, характеризується розвитком низки патологічних та компенсаторних реакцій, унаслідок чого зменшується серцевий викид, підвищується загальний периферичний опір судин (окрім випадків септичного шоку), порушується мікроциркуляція тканин, відбувається централізація кровообігу, що, у свою чергу, посилює органну гіпоперфузію та гіпоксемію, зумовлює тяжкі метаболічні порушення.
Однією з важливих ланок розладів мікроциркуляції є зміни в ендотелії капілярів. Унаслідок гіпоксії спостерігається набрякання ендотеліоцитів, адгезія до них поліморфноядерних лейкоцитів, що посилює зменшення кровотоку. При відсутності своєчасного й адекватного лікування погіршується доставка кисню кардіоміоцитам, посилюється ацидоз міокарда, що клінічно виявляється тахікардією, гіпотензією, задишкою. Прогресивне погіршення тканинної перфузії спричиняє розвиток тотальної ішемії з подальшим реперфузійним пошкодженням тканин. У разі виживання хворого його стан ускладнюється розвитком синдрому поліорганної дисфункції.
У випадках гострої крововтрати існує значний дефіцит факторів згортання крові та еритроцитів. Однак більшість фахівців вважає найбільш гострою проблемою гіповолемію і, відповідно, на перше місце у схемах інтенсивної терапії ставлять поповнення об’єму циркулюючої крові, що є вирішальним для підтримання й відновлення стабільної геодинаміки, мікроциркуляції та газообміну.
Разом із тим успішність та ефективність інфузійно-трансфузійної терапії залежить від цілеспрямованого обґрунтування її програми, характеристик засобів для інфузії, їх фармакокінетики та фармакологічних властивостей.
Переважне використання монокомпонентної терапії (використання кристалоїдів, альбуміну, надання переваги декстранам) у попередні десятиріччя показало її недостатність та небезпечність унаслідок значної кількості ускладнень.
Про небезпечність необґрунтованої та рутинної тактики використання гемотрансфузій свідчать дані Ferraris V.A., Ferraris S.P., Saha S.P. et al. (2007) [6]:
1. Інфекційні ускладнення:
— ВІЛ — 1 на 1,4–2,4 х 106;
— гепатит В — 1 на 58 000–148 000;
— гепатит С — 1 на 872 000–1,7 х 106;
— бактерійне інфікування — 1 на 2000.
2. Імунологічні реакції:
— фібрильні негемолітичні реакції — 1 на 100;
— анафілактичні трансфузійні реакції — 1 на 20 000–50 000;
— гемоліз — 1 на 60 000;
— летальний кінець — 1 на 60 000;
— лейкоцит-індуковане пошкодження органів — 1 на 20–50;
— легеневі ускладнення — 1 на 2000.
3. Ятрогенні помилки, пов’язані з методикою трансфузії — 1 на 14 000.
Використання лише кристалоїдів при масивній крововтраті також належним чином не забезпечує очікуваних результатів. Болюсне введення кристалоїдів із швидкістю, що перевищує 80 мл/кг/год, можливо, не збільшує ефективність ресусцитації рідиною. Ресусцитація кристалоїдним розчином упродовж більше ніж 2 год може бути шкідливою внаслідок надмірної ретенції рідини.
Сучасна концепція комплексної збалансованої інфузійної терапії, прийнятої на основі результатів низки багатоцентрових досліджень, передбачає комплексне призначення кристалоїдів, гідроксіетилкрохмалів (ГЕК) та (у разі масивної крововтрати) компонентів крові.
Гідроксіетилкрохмалі — відносно новий клас препаратів, створений на основі природних компонентів. Основою ГЕК із середньою молекулярною масою 200 000 дальтон (Да) є a-амінопектин, у якого в молекулі 5 глюкозних залишків із 10 замінені гідроксильними групами (коефіцієнт заміщення 0,5) у положенні С2-С6. Це дозволяє збільшувати об’єм циркулюючої крові на 100 % від внутрішньовенно введеного розчину упродовж 3–4 годин (6% розчин ГЕК другої генерації), а при введенні 10% ГЕК — до 6–8 годин. Метаболізуються препарати a-амілазою, не накопичуючись у клітинах ретикулоендотеліальної системи, виводяться нирками.
Ефективність використання ГЕК досліджена упродовж останнього десятиріччя проведеними метааналізами з використанням проспективних подвійних рандомізованих досліджень у провідних європейських центрах на масивах хворих із гострою крововтратою, травматичним шоком, опіками, гострим порушенням мозкового кровообігу, нейротравмами, септичними станами [5, 8, 9]. Отримані дані свідчать про високу їх ефективність, значне просування до «ідеального» плазмозамінника та низький відсоток побічних реакцій, що реєструвалися у хворих із септичним станом (порушувалася функція нирок при тривалому застосуванні ГЕК), у хворих із тяжкими опіками при призначенні гіперонкотичних розчинів ГЕК у першу добу (Vlachoua E., 2010) [10].
Ми досліджували ГЕК другої генерації Хетасорб (6%, 10%) на базі відділень анестезіології та інтенсивної терапії Київської міської клінічної лікарні швидкої медичної допомоги, Київської обласної клінічної лікарні та Вишгородської центральної районної лікарні. Ми використовували цей препарат у 34 пацієнтів із гострою крововтратою, травматичним шоком, гіповолемічними станами внаслідок інфекційних ускладнень (прооперовані хірургічні хворі). Досліджувалися центральний венозний тиск, артеріальний тиск, число серцевих скорочень, діурез, стан мікроциркуляції. Критерії заборони використання препарату: Хетасорб не слід застосовувати в разі відомої гіперчутливості до гідроксіетилкрохмалю, при гіперволемічних станах, гіпергідратації, гіперхлоремії або гіпернатріємії, застійній серцевій недостатності, набряку легень, нирковій недостатності, внутрішньочерепній кровотечі, тяжких порушеннях згортання крові, вираженій печінковій недостатності, дитячому віці (ефективність та безпека не встановлені). При використанні 10% розчину Хетасорбу до цих протипоказань додається дегідратація, гіпокаліємія, перебування пацієнтів на гемодіалізі, перший триместр вагітності.
Методика застосування
Загальна доза, тривалість та швидкість інфузії залежать від об’єму крововтрати та/або гемодинамічного статусу й загального клінічного стану пацієнта. Необхідно враховувати можливий ризик перевантаження серцево-судинної системи при великій швидкості інфузії або призначенні великих доз.
Максимальна швидкість інфузії залежить від клінічного стану пацієнта. Пацієнти з гострим геморагічним шоком: до 20 мл/кг маси тіла/годину (що відповідає 0,33 мл/кг маси тіла/хв). У ситуаціях, що загрожують життю, — 500 мл швидкої внутрішньовенної інфузії.
Максимальна добова доза гідроксіетилкрохмалю не повинна перевищувати 2 г/кг маси тіла/добу. Це відповідає 33 мл/кг маси тіла/добу 6% розчину (20 мл/кг маси тіла/добу 10% розчину). Максимальна доза 10% Хетасорбу не повинна перевищувати 2 г гідроксіетилкрохмалю/кг маси тіла. У зазначених дозах ми використовували цей препарат до двох діб.
Під час вивчення ефективності використання Хетасорбу нами не було зареєстровано побічних ефектів, хоча, за висновками інших досліджень із більшою кількістю хворих, потрібно враховувати підвищення ризику розвитку побічних ефектів у разі високих доз. До побічних реакцій слід віднести анафілактичні реакції різного ступеня тяжкості (рідко), дозозалежні порушення згортання крові. При застосуванні гідроксіетилкрохмалю може підвищуватися концентрація сироваткової a-амілази. Цей ефект виникає внаслідок формування комплексу «субстрат — фермент», який включає амілазу й гідроксіетилкрохмаль, що призводить до уповільнення елімінації нирками комплексу, тому визначення амілази не має діагностичного значення для оцінки порушення функції підшлункової залози.
Тривале застосування гідроксіетилкрохмалю у високих дозах часто спричиняє свербіж. Це ускладнення може виникнути навіть через кілька тижнів після останньої інфузії, тривати декілька місяців і спричинити дискомфорт.
Критерії ефективності застосування: зменшення та/або усунення порушень мікроциркуляції (залежно від тяжкості гіповолемії), нормалізація діурезу, стабілізація артеріального тиску та частоти серцевих скорочень, збільшення центрального венозного тиску.
Результати нашого дослідження виявили ефективність застосування Хетасорбу (6%, 10%). Перевагою цього препарату порівняно з іншими ГЕК другої генерації є також збалансована фармакоекономічна складова. Це дає підставу рекомендувати його до широкого застосування в комплексному лікуванні гіповолемії та шоку різного ступеня, звужуючи при цьому показання для використання препаратів крові або суттєво зменшуючи їх кількість для корекції глобулярного об’єму.
Як ілюстрацію успішного та ефективного комплексного використання кристалоїдів та Хетасорбу наводимо 2 клінічних випадки, що увійшли до нашого дослідження.
Клінічний випадок 1
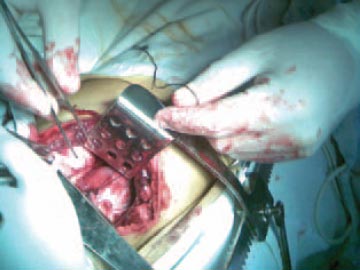
Хворий М. Діагноз: різане проникаюче поранення грудної клітки зліва. Гемопневмоторакс зліва. Геморагічний шок ІІІ ст.
Основні показники: АТ 70/40 мм рт.ст., Ps — 116 за 1 хв, SpO2 — 92 %. Вихідний Hb — 116 г/л. При торакотомії виявлене проникаюче поранення лівого шлуночка серця. Інфузійна терапія: NaCl 0,9% 400,0 + NaCl 10% 100,0, розчин Рінгера лактат 1500,0, Хетасорб 6% 1000,0. Стан хворого стабілізувався за показниками гемодинаміки інтраопераційно.
Результат: виписаний за 7 днів.
Клінічний випадок 2
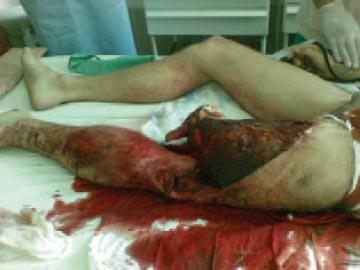
Хворий Р., 28 р. Травма внаслідок ДТП (мотоцикліст). Ds: ЗЧМТ (струс головного мозку), пневмоторакс зліва, закритий перелом плечової кістки зліва, травматична неповна ампутація лівої нижньої кінцівки на рівні нижньої третини лівого стегна. Травматичний шок ІІІ ст.
При госпіталізації — у ясній свідомості. АТ — 50/0 мм рт.ст., Ps — 136 за 1 хв. SpO2 — 90 %. ЦВТ — 30 мм вод.ст. Вихідний Hb — 104 г/л.
Інтенсивна терапія. Інфузія у 3 венозних доступи (у т.ч. у v.subclavia). Розчин Рінгера лактат 1000,0 + NaCl 10% 100,0; розчин Рінгера лактат 1500,0 + NaCl 10% 100,0; Хетасорб 6% 1000,0 + Хетасорб 10% 500,0; сорбілакт 200,0, реосорбілакт 200,0 (після перев’язки судин і зняття джгута). Гемотрансфузія одногрупної сумісної за Rh-фактором еритроцитарної маси (320,0).
Регіонарна аналгезія: nn.femoralis, ischiathicus — маркаїн 0,3% 30 + 30 мл, фентаніл 100 мкг + дексалгин 2,0 (на догоспітальному етапі вводився омнопон 2% 2,0).
Через 4 години при переведенні до іншого стаціонару (наполягання родичів). На час переводу: АТ 110/55 мм рт.ст., Ps — 106 за 1 хв, SpO2 — 98–99 %, ЦВТ — 70 мм вод.ст., діурез — 500 мл. Свідомість ясна. Препарати інотропної підтримки не застосовувались.
Висновки
1. Хетасорб 6%, 10% зарекомендував себе як ефективний препарат плазмоекспандерної дії при кровотечі та шоці, гіповолемічних станах у поєднанні з комплексною інфузійною терапією.
2. При використанні цього препарату не виявлено побічних ефектів.
1. Гур’єв С.О., Барамія Н.М., Заруцький Я.Л. та ін. Полісистемні та поліорганні пошкодження як проблемне питання // Проблеми військової охорони здоров’я: Збірник наукових праць УВМА / За ред. проф. В.Я. Білого. — К., 2002. — Вип. 11. — С. 150-164.
2. Зильбер А.П. Кровопотеря и гемотрансфузия (принципы и методы бескровной хирургии). — Петрозаводск, 1999. — 60 с.
3. Мазуренко О.В., Кузьмін В.Ю. Аналіз летальності потерпілих з ізольованою та поєднаною травмою // Клінічна хірургія. — 1998. — № 12. — С. 21-23.
4. Москаленко В.Ф., Рощін Г.Г., Волошин В.О., Вершигора А.В. Концептуальні положення щодо розвитку і реформування екстреної медичної допомоги населенню України // Український журнал екстремальної медицини ім. Г.О. Можаєва. — 2001. — Т. 2, № 2. — С. 7-11.
5. Cheng D. et al. Colloids for perioperative plasma volume expansion: systematic review with meta-analysis of controlled trials // Transfusion Alternatives in Transfusion Medicine. — 2007. — Vol. 9 (Suppl. 1). — S3.
6. Ferraris V.A., Ferraris S.P., Saha S.P., Hessel E.A. II et al. Hemotransfusion complications // Ann. Thorac. Surg. — 2007. — Vol. 83. — P. 27-86.
7. Mulner T., Kutsha-Lissberg F., Kwasny O., Vescei V. Das Polytrauma in Osterreich Kritische Analyse der njtwendigenstrukturellen Voranssetzungen und deren Finanzierbaekeit in der Zukunft // Acta Chir. Austriaca. — 1998. — J. 30, № 4. — Р. 250-253.
8. Neff T.A., Doelberg M., Jungheinrich C. et al. Repetitive large-dose infusion of the novel hydroxyethyl starch in patients with severe head injury // Anesth. Analg. — 2003. — 96. — 1453-9.
9. Ronald J. Trof, Sharwan P. Sukul, Jos W.R. Twisk, Armand R.J. Girbes, Johan A.B. Groeneveld. Greater cardiac response of colloid than saline fluid loading in septic and non-septic critically ill patients with clinical hypovolaemia // Journal Intensive care medicine. — Vol. 36. — Issue 4. — P. 697-701 (Apr 2010) ISSN: 1432-1238 [Electronic] United States.
10. Vlachoua E. Hydroxyethylstarch supplementation in burn resuscitation. Clinical Biochemistry Departments, University Hospital Birmingham NHS Foundation Trust, Birmingham, UK. Available online 16 June 2010.
