Международный неврологический журнал 5 (43) 2011
Вернуться к номеру
Электромиографическое исследование мышечной активности у пациентов с болезнью Паркинсона и их родственников
Авторы: Карабань И.Н.1, Луханина Е.П.2, Березецкая Н.М.1, Чивликлий М.А.1, 1ГУ «Институт геронтологии НАМН Украины им. Д.Ф. Чеботарева», г. Киев, 2Институт физиологии им. А.А. Богомольца НАН Украины, г. Киев
Рубрики: Неврология
Версия для печати
Проведение сравнительного анализа амплитудных параметров и статистических характеристик поверхностной электромиограммы (ЭМГ) в состоянии покоя у пациентов с болезнью Паркинсона (БП), здоровых лиц среднего и пожилого возраста и клинически здоровых родственников пациентов, страдающих БП, с целью выявления скрытых признаков нарушенной мышечной активности. Основными признаками экстрапирамидной недостаточности у пациентов с БП являются: повышенная амплитуда ЭМГ в покое, наличие залповых разрядов с частотой 4–9 Гц, значительное увеличение (р < 0,001) статистических параметров ЭМГ (размаха амплитуды, дисперсии, коэффициента эксцесса). Выявлена достоверная (p < 0,01) зависимость между коэффициентом эксцесса и баллами пункта 20 UPDRS, оценивающими интенсивность тремора той руки, на которой регистрировалась ЭМГ, что позволяет рассматривать коэффициент эксцесса в качестве объективного показателя меры синхронизации в активации моторных единиц, ответственной за возникновение залповых мышечных разрядов. Установлено, что у клинически здоровых родственников пациентов с БП в 2,3 раза чаще встречается повышенная амплитуда ЭМГ и наличие разрядов с частотой 5–10 Гц регистрируется в 5,9 раза чаще, чем в контрольной группе соответствующего возраста. Установлена достоверная корреляционная зависимость между повышенной мышечной активностью у родственников пациентов с БП и их возрастом (р < 0,05). По статистическим параметрам ЭМГ у 43 % исследованных родственников обнаружены признаки нарушенной мышечной активности. С целью предотвращения манифестации заболевания БП для группы риска разработаны рекомендации относительно распорядка жизни, пищевого рациона и лекарственных средств, длительного применения которых следует избегать.
Интерференционная электромиография, дисперсия, эксцесс, болезнь Паркинсона, родственники пациентов с болезнью Паркинсона.
Введение
В развитии болезни Паркинсона (БП), одного из наиболее распространенных нейродегенеративных заболеваний центральной нервной системы, существенное значение имеет генетический фактор. Центральным звеном в генезе этого заболевания признается мутация гена a-синуклеина — белка пресинаптических нервных терминалей, расположенного на хромосоме 4q21-23 [15, 20, 23, 28]. Еще один ген аутосомно-доминантной формы БП, кодирующий синтез убиквитин-карбокситерминальной гидролазы L1, был картирован на хромосоме 4р14 [12, 19]. При аутосомно-рецессивном ювенильном паркинсонизме (с ранним началом) были обнаружены мутации в гене белка паркина на хромосоме 6q25-27 [18, 26]. О большом значении генетической составляющей в предрасположенности к БП свидетельствуют данные эпидемиологических исследований, установившие, что риск возникновения данного заболевания у родственников больных с БП в 2–7 раз выше, чем в контрольной группе [13]. Функциональная несостоятельность экстрапирамидной системы может развиваться за несколько десятилетий до возможного проявления паркинсонизма [11]. Для предотвращения или замедления развития заболевания требуется выявление ранней, пресимптоматической стадии нейродегенеративного процесса и поиск информативных биомаркеров БП [4].
В основе двигательных расстройств (брадикинезии, мышечной ригидности, тремора покоя) при БП лежат нарушения центральной регуляции тонуса мышц, обусловленные дефицитом супраспинального тормозного контроля и избыточной тонической импульсацией из сегментарных альфа- и гамма-мотонейронов [6, 24]. Объективным диагностическим показателем БП является биоэлектрическая активность мышц III типа, регистрируемая со сгибателей и разгибателей конечностей при помощи поверхностных электродов [5, 17]. Электромиограмме (ЭМГ) III типа присущи высокий уровень биоэлектрической активности мышц в покое и залповые разряды, соответствующие ритму тремора [2, 8]. Достоинством ЭМГ-метода является его неинвазивность и информативность при выявлении скрытых субклинических проявлений экстрапирамидной недостаточности [7, 17, 25].
Цель настоящей работы заключалась в проведении сравнительного анализа амплитудных параметров и статистических характеристик поверхностной ЭМГ в состоянии покоя (гистограмм распределения амплитуды ЭМГ, дисперсии и коэффициента эксцесса) у пациентов с БП, здоровых лиц среднего и пожилого возраста и использовании указанных показателей для выявления скрытых признаков нарушенной мышечной активности у клинически здоровых родственников пациентов, страдающих БП. В задачу исследования входила разработка рекомендаций для выявленной группы риска по паркинсонизму.
Методика
Исследования проведены в четырех группах людей: 1) 33 пациента с БП (21 женщина и 12 мужчин, возраст от 47 до 85 лет, средний возраст 63,9 ± 1,5 года), страдающих акинетико-ригидно-дрожательной либо акинетико-ригидной формами данного заболевания в стадии 1,5–3,0 по международной классификации Хена и Яра [16]; 2) 24 практически здоровых лица контрольной группы пожилого возраста (16 женщин и 8 мужчин, возраст от 60 до 74 лет, средний возраст 65,0 ± 1,5 года); 3) 37 клинически здоровых родственников больных с БП (дети, братья и сестры, 22 женщины и 15 мужчин, возраст от 30 до 56 лет, средний возраст 45,6 ± 1,5 года); 4) 20 практически здоровых лиц соответствующей контрольной группы молодого и среднего возраста (19 женщин и 1 мужчина, возраст от 35 до 58 лет, средний возраст 47,7 ± 2,3 года). Возрастные группы определяли согласно классификации Всемирной организации здравоохранения [1]. Все испытуемые давали согласие на проведение исследований.
У больных с БП для оценки тяжести симптоматики использовали унифицированную международную рейтинговую шкалу — Unified Parkinson’s Disease Rating Scale (UPDRS) [14]. Баллы I (нарушения в мышлении, настроении), II (снижение дневной активности, нарушение гигиенических навыков) и III (расстройства моторной функции, в том числе брадикинезия, ригидность, тремор) разделов шкалы вычисляли на основании 4-балльной градации каждого из симптомов. У исследованных в данной работе больных суммарный балл UPDRS колебался в пределах 41–105, его среднее значение составляло 60,0 ± 3,3.
У всех испытуемых записывали интерференционную (суммарную) ЭМГ биполярно на приборе «НейроМПВ» (Москва) с помощью поверхностных электродов, которые помещали на сгибателе (m. biceps brachii) и разгибателе (m. triceps brachii) плеча. Площадь электродов составляла 0,5 ´ 1,0 см2, межэлектродное расстояние было фиксированным и равнялось 1,5 см. ЭМГ регистрировали у больных на стороне клинически доминирующего гемисиндрома, у остальных для анализа выбирали амплитудные параметры ЭМГ той стороны, где они имели большее значение. Регистрацию ЭМГ проводили в состоянии покоя лежа на спине, давая указание испытуемому расслабиться. Биоэлектрические сигналы подавали на усилитель с полосой пропускания 10 Гц–10 кГц. Время каждой записи достигало 10 с. Минимальная амплитуда турна была равна 3 мкВ.
С помощью специализированной компьютерной программы вычисляли амплитуду осцилляций от пика до пика: среднюю (АС) и максимальную (АМ) в мкВ. Определяли также сумму всех амплитудных значений (СА) ЭМГ-сигналов за промежуток времени одна секунда в мВ/с. Выявляли характерные для БП залповые мышечные разряды (ЗМР) с частотой 4–9 Гц. Высокоамплитудные ЗМР хорошо определялись на ЭМГ визуально. Но когда амплитуда ЭМГ была небольшой, компьютерная программа позволяла выявлять ЗМР путем построения амплитудных спектральных графиков в логарифмическом масштабе с использованием математического низкочастотного фильтра 2–10 Гц. Наряду с этим 10-секундные потоки ЭМГ-сигналов анализировали с помощью компьютерных программ Origin-8 и «Статистика-8». Строили гистограммы распределения амплитудных значений ЭМГ. Определяли размах (range), дисперсию (variance) и коэффициент эксцесса (kurtosis). Размах (Р) вычисляется как разность максимального и минимального значений амплитуды в потоке ЭМГ-сигналов, измеренных относительно базовой линии. Дисперсия (Д, s2) является мерой разброса исследуемого параметра. Таким образом, Р и Д хорошо отражают уровень мышечной активации. Коэффициент эксцесса (КЭ) характеризует остроту пика гистограммы распределения амплитудных значений ЭМГ. Если КЭ отрицательный, то пик более закруглен, чем при нормальном распределении, если положительный, то пик заострен. Есть точка зрения, что острота пиков ЭМГ гистограмм и, соответственно, величина КЭ могут служить мерой синхронизации в активации моторных единиц, лежащей в основе возникновения залповых мышечных разрядов [22].
Данные, полученные в разных группах испытуемых, усредняли и сравнивали посредством системы ANOVA и критерия c2. Проводили корреляционный анализ статистических характеристик ЭМГ с клиническими баллами международной рейтинговой шкалы UPDRS: их суммарной величиной, баллами I, II и III подразделов этой шкалы, а также с баллами пунктов 20 и 22 (соответственно тремора и ригидности руки, на которой регистрировалась ЭМГ). Корреляционные связи определяли непараметрическим методом Спирмена. Статистический критерий достоверности был принят на уровне p < 0,05.
Результаты
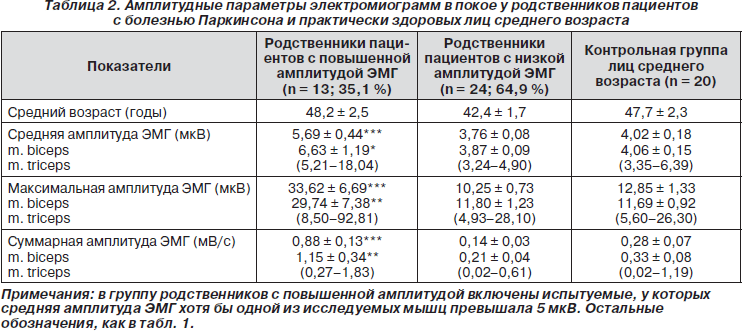
Характерной особенностью ЭМГ у больных с БП являлась повышенная биоэлектрическая активность мышц в состоянии покоя вследствие невозможности мышечного расслабления (ригидности). АМ у отдельных пациентов достигала 210–508 мкВ, АС — 35–98 мкВ и СА — 5–7 мВ/с (табл. 1). В контрольных группах эти показатели не имели существенных отличий: АМ у разных индивидуумов колебалась преимущественно в пределах 5,6–24,6 мкВ, АС — 3,4–5,0 мкВ и СА — 0,02–0,71 мВ/с. Лишь у трех (15 %) лиц контрольной группы среднего возраста и у трех (12,5 %) лиц контрольной группы пожилого возраста амплитуда ЭМГ покоя хотя бы одной из исследуемых мышц превышала указанные значения и расценивалась нами как показатель ослабления супраспинального контроля.
В группе клинически здоровых родственников пациентов с БП число лиц с повышенной амплитудой ЭМГ покоя было в 2,3 раза больше по сравнению с соответствующей контрольной группой среднего возраста, а именно: статистически достоверное увеличение биоэлектрической активности мышц обнаружено у 13 (35,1 %) лиц (табл. 2). В эту подгруппу мы включили родственников, у которых АС хотя бы одной из исследуемых мышц превышала 5 мкВ. У девяти из них повышение амплитудных характеристик ЭМГ было весьма существенным: АМ достигала 25–93 мкВ, АС — 15–18 мкВ и СА — 0,9–1,8 мВ/с. Повышение биоэлектрической активности мышц у родственников больных с БП положительно коррелировало с их возрастом, причем возраст более 45 лет в этом отношении являлся критическим. Число лиц старше 45 лет, у которых СА превышала среднее значение этого параметра в контрольных группах испытуемых, достоверно превалировало над количеством лиц старше 45 лет с низкими значениями СА (Р < 0,05, критерий c2 ). Коэффициент корреляции между возрастом испытуемых и величиной СА составлял 0,40; P < 0,05 (из m. biceps brachii и m. triceps brachii выбиралась СА той мышцы, где величина этого показателя было более значительной).
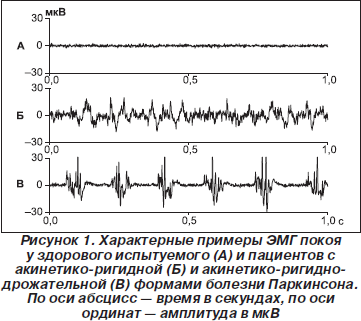
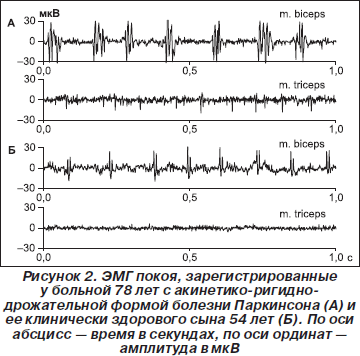
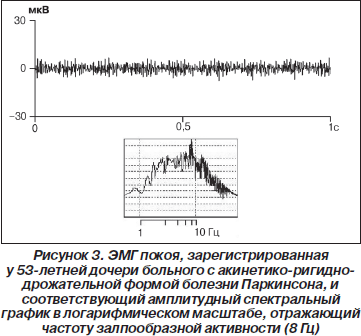
Другим диагностическим признаком БП служило периодическое возникновение в ЭМГ покоя веретено- образных ЗМР (III тип ЭМГ по Юсевич). ЗМР регистрировались у пациентов с акинетико-ригидно-дрожательной формой заболевания (рис. 1), их частота возникновения варьировала в пределах 4–9 Гц. Каждый ЗМР состоял из 4–10 и более потенциалов. Длительность ЗМР колебалась от 30 до 120 мс, амплитуда отдельных колебаний в их составе достигала 80–508 мкВ. У клинически здоровых родственников пациентов с БП типичные ЗМР подобной длительности и амплитуды не встречались. Однако у шести (16,2 %) из них в ЭМГ покоя были зарегистрированы короткие разряды из 2–3 потенциалов (реже — одного) с частотой 5–10 Гц. Амплитуда этих потенциалов не превышала 52 мкВ. Чаще они выявлялись у лиц старше 45 лет. На рис. 2 представлены ЭМГ, зарегистрированные у больной с акинетико-ригидно-дрожательной формой БП и ее клинически здорового сына. Видно, что у сына ЗМР возникают чаще, их амплитуда и продолжительность значительно меньше. Еще у пяти (13,5 %) родственников пациентов с БП наблюдалась залпообразная активность на фоне достаточно низкой амплитуды ЭМГ, при которой частоту ЗМР можно было определить с помощью амплитудных спектральных графиков (рис. 3). В контрольных группах подобные короткие разряды с частотой 5–10 Гц или залпообразная активность в ЭМГ покоя наблюдались значительно реже: у двух испытуемых контрольной группы пожилого возраста (8,4 %) и у одного — контрольной группы среднего возраста (5 %), то есть в 5,9 раза реже, чем в группе родственников пациентов с БП.
Следует отметить, что у родственников пациентов с БП признаки ослабленного супраспинальной контроля, то есть экстрапирамидной недостаточности, визуально выявлялись плохо. Повышенная амплитуда ЭМГ-потенциалов или вспышки залповых разрядов могли возникать лишь спорадически. Сами залповые разряды, имея маленькую амплитуду, плохо дифференцировались. Поэтому мы полагали, что анализ достаточно продолжительных (10-секундных) потоков ЭМГ-сигналов с использованием статистических методов окажется более эффективным способом выявления патологических признаков мышечной активности. Сравнительный анализ показал, что ЭМГ в состоянии покоя у здоровых испытуемых характеризовалась пологой симметричной гистограммой и небольшими значениями Р, Д и КЭ (табл. 3). Р не превышал 20 мкВ, Д — 7 и КЭ — 0,4. Никакой существенной разницы в контрольных группах среднего и пожилого возраста не отмечалось. У пациентов с акинетико-ригидной формой БП усредненные по группе статистические параметры ЭМГ были высоко достоверно (p < 0,001) увеличены по сравнению с контролем. У отдельных больных Р достигал 66 мкВ, Д — 56 повышался до 1,4 (табл. 3). Еще более высокие статистические параметры отмечались у пациентов с акинетико-ригидно-дрожательной формой БП при наличии в ЭМГ веретенообразных залповых разрядов. Гистограммы распределения амплитудных значений при указанной форме заболевания характеризовались острым пиком. Р в этой группе пациентов достигал 382 мкВ, Д — 951, КЭ у всех пациентов отличался большой величиной, колеблясь от 1 до 13 (табл. 3). Корреляционный анализ статистических характеристик ЭМГ у больных БП и клинических баллов международной рейтинговой шкалы UPDRS выявил достоверную зависимость между КЭ и баллами пункта 20 UPDRS, характеризующими интенсивность тремора той руки, на которой регистрировалась ЭМГ. Коэффициент корреляции по Спирмену между этими показателями составлял 0,46 (p < 0,01). Другие достоверные связи не были обнаружены.
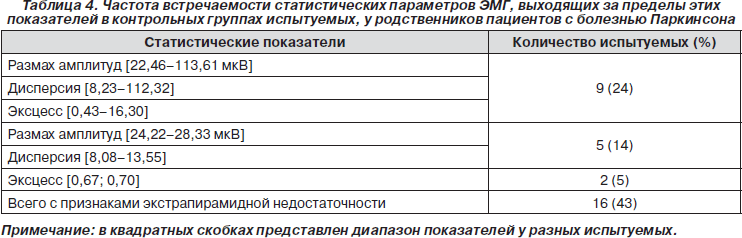
При анализе ЭМГ у родственников пациентов с БП мы считали статистические параметры мышечной активности выходящими за пределы нормы, если они превышали крайние значения этих показателей в контрольных группах испытуемых, то есть если Р превышал 20 мкВ, Д — 7 и КЭ — 0,4. Всего было выявлено 16 (43 %) родственников пациентов с БП, у которых наблюдались превышения нормальных параметров ЭМГ-сигналов. Оказалось, что у пяти родственников (14 %) за пределы нормы выходили амплитудные характеристики ЭМГ (Р и Д). У двух (5 %) отмечался увеличенный КЭ, по-видимому, отражающий повышенную синхронизацию в деятельности моторных единиц. Еще у девяти лиц (24 %) наблюдалось увеличение Р, Д и КЭ (табл. 4). Следует отметить, что отклонения от нормальных значений статистических характеристик ЭМГ чаще выявлялись у лиц старше 45 лет.
Задачей данной работы являлась разработка рекомендаций лицам обнаруженной группы риска по паркинсонизму с целью профилактики возможности развития заболевания. Такие рекомендации были нами предложены. Они включали рациональный распорядок дня, пищевой рацион, содержащий витамин В6 (пиридоксин, который является главным катализатором синтеза дофамина), а также перечень лекарственных препаратов, длительного употребления которых следует избегать. В их число входят средства, которые истощают регуляторную функцию дофаминергической системы или снижают ее активность: галоперидол, индола резерпин, флуоксетин (прозак), метоклопрамид (церукал), клозапин, кордарон, производные фенотиазина и бутирофенона, препараты лития.
Обсуждение результатов
Сравнительный анализ ЭМГ у пациентов с БП и здоровых лиц контрольных групп показал, что амплитудные параметры и статистические характеристики поверхностной ЭМГ в состоянии покоя являются информативными показателями экстрапирамидной недостаточности, обусловленной ослаблением тормозного супраспинального контроля на фоне снижения функции центральной дофаминергической системы. Они оказались также эффективными критериями для выявления скрытых признаков нарушенной мышечной активности у клинически здоровых родственников пациентов, страдающих БП. Повышенная амплитуда биоэлектрической активности мышц в спокойном расслабленном состоянии встречалась у родственников в 2,3 раза чаще и наличие в ЭМГ разрядов с частотой 5–10 Гц наблюдалось в 5,9 раза чаще у родственников пациентов, страдающих БП, чем в контрольной группе соответствующего возраста. В этом результаты нашего исследования совпадают с данными других авторов об информативности ЭМГ-метода для выявления субклинических проявлений ослабленного супраспинального контроля [7, 17, 25], а также о важном значении генетической составляющей в предрасположенности к развитию экстрапирамидной недостаточности [3, 13].
В работе установлена достоверная корреляционная зависимость между повышенной мышечной активностью у родственников пациентов с БП и их возрастом (P < 0,05). Показано, что признаки отсутствия полного мышечного расслабления в основном появляются после 45 лет. Необходимо отметить, что нарушения мышечной регуляции у клинически здоровых родственников пациентов с БП никогда не достигали выраженной степени. Так, если СА у больных с БП могла составлять 5–7 мВ/с, то в подгруппе родственников с повышенной амплитудой наибольшие значения этого показателя были 0,85–1,8 мВ/с. ЗМР у больных состояли из 4–10 и более потенциалов, вследствие чего их продолжительность достигала 100–120 мс. У родственников пациентов с БП мышечные разряды были короткие и обычно состояли из 2–3 потенциалов. Признаки ослабленного супраспинального контроля в виде повышенной амплитуды ЭМГ в покое и наличия мышечных разрядов зарегистрированы у 15 из 37 (40,5 %) исследованных родственников. Анализ статистических параметров ЭМГ-сигналов, по нашему мнению, также оказался эффективным для выявления у клинически здоровых родственников пациентов с БП признаков нарушенной мышечной активности, которые обычно непостоянны и плохо выявляются визуально. Всего нами было обнаружено 16 (43 %) родственников пациентов с БП, у которых статистические параметры ЭМГ превышали критические значения таковых в контрольных группах здоровых лиц соответствующего возраста. Подобная частота встречаемости экстрапирамидной недостаточности (45 %) у здоровых родственников больных с БП была отмечена ранее Маньковским с соавторами [7].
При корреляционном анализе нами выявлена достоверная (p < 0,01) зависимость между КЭ и баллами пункта 20 UPDRS, оценивающими интенсивность тремора той руки, на которой регистрировалась ЭМГ. Этот факт согласуется с точкой зрения [22] о том, что КЭ отражает синхронизацию в активации моторных единиц, ответственную за возникновение залповых мышечных разрядов.
В основе всех нейродегенеративных заболеваний, в том числе БП, лежит единый патогенетический фактор — конформационные изменения тех или иных клеточных белков на посттрансляционной стадии [3]. Благодаря компенсаторным и детоксикационным системам клетки она способна в течение многих лет успешно справляться с аномальными белковыми субстратами [27]. Отсроченная манифестация клинических проявлений заболевания является характерной чертой конформационных болезней мозга. Патологический процесс может протекать в латентной форме на протяжении длительного периода времени, до 30 лет [5]. При БП отчетливые двигательные расстройства развиваются лишь тогда, когда гибнет не менее 70 % дофаминергических нейронов черной субстанции [21]. Имеются литературные данные о замедленном темпе патологических изменений в нервных клетках в пресимптоматический период, в то время как на стадии манифестации болезни гибель нейронов значительно ускоряется [9]. В связи с вышеизложенным важное значение придается диагностике субклинических скрытых признаков нарушенной деятельности мышц [4, 5, 10]. С целью предупреждения манифестации заболевания БП лицам, входящим в группу риска по паркинсонизму, следует придерживаться определенных рекомендаций. Особое внимание при составлении таких рекомендаций, с нашей точки зрения, следует уделять дифференцированному употреблению лекарственных средств, истощающих регуляторную функцию дофаминергической системы или снижающих ее активность.
1. Аршавский И.А. Основы возрастной периодизации // Возрастная физиология. — Л.: Наука, 1975. — С. 5-67.
2. Зенков Л.Р., Ронкин М.А. Функциональная диагностика нервных болезней. — М.: Медицина, 1991.
3. Иллариошкин С.Н. Конформационные болезни мозга. — М.: Янус-К, 2002.
4. Иллариошкин С.Н. Молекулярные основы болезни Паркинсона // Болезнь Паркинсона и расстройства движений: Руководство для врачей по материалам I Национального конгресса. — М., 2008. — С. 8-17.
5. Крыжановский Г.Н., Карабань И.Н., Магаева С.В., Карабань Н.В. Компенсаторные и восстановительные процессы при паркинсонизме. — К.: Институт геронтологии АМН Украины, 1995.
6. Крыжановский Г.Н., Карабань И.Н., Магаева С.В., Кучеряну В.Г., Карабань Н.В. Болезнь Паркинсона. — М.: Медицина, 2002.
7. Маньковский Н.Б., Вайншток А.Б., Олейник Л.И. Сосудистый паркинсонизм. — К.: Здоров’я, 1982.
8. Юсевич Ю.С. Очерки по клинической электромиографии. — М.: Медицина, 1972.
9. Antonini А., Leenders K.L., Eidelberg D. [11C] raclopride-PET studies of the Huntington’s disease rate of progression: relevance of the trinucleotide repeat length // Ann. Neurol. — 1998. — 43, № 2. — Р. 253-255.
10. Berg D., Becker G., Zeiler B., Tucha O., Hofmann E., Preier M. et al. Volnerability of the nigrostriatal system as detected by transcranial ultrasound // Neurology. — 1999. — 53, № 5. — Р. 1026-1031.
11. Berg D., Roggendorf W., Schroder U., Klein R., Tatschner T., Benz P. et al. Echogenicity of the substantia nigra: association with increased iron content and marker for susceptibility to nigrostriatal injury // Arch. Neurol. — 2002. — 59, № 6. — Р. 999-1005.
12. Dawson T.M. Parkin and defective ubiquitination in Parkinson’s disease // J. Neural. Transm. Suppl. — 2006. — 70. — Р. 209-213.
13. Elbaz А., Grigoletto F., Baldereschi М., Breteler М.М., Manubens-Bertran J.M., Lopez-Pousa S. et al. Familial aggregation of Parkinson’s disease: a population-based case-control study in Europe. EUROPARKINSON Study Group // Neurology. — 1999. — 52, № 9. — 1876-1882.
14. Fahn S., Elton R.L. Members of the UPDRS Development Commettee, Unified Parkinson’s Disease rating scale // Recent developments in Parkinson’s disease / Eds. S. Fahn, C.D. Marsden, D.B. Calne, M. Goldstein. — Florham Park; New York: Macmillan Health Care Information, 1987. — Vol. 2. — Р. 153-164.
15. Farrer М., Kachergus J., Forno L., Lincoln S., Wang D.S., Hulihan M., Maraganore D., Gwinn-Hardy К., Wszolek Z., Dickson D., Langston J.W. Comparison of kindreds with parkinsonism and alpha-synuclein genomic multiplications // Ann. Neurol. — 2004. — 55, № 2. — 153-156.
16. Hoehn М.М., Yahr M.D. Parkinsonism: onset, progression and mortality // Neurology. — 1967. — 17. — 427-442.
17. Hoshiyama М., Kaneoke Y., Koike Y., Takahashi А., Watanabe S. Hypokinesia of associated movement in Parkinson’s disease: a symptom in early stages of the disease // J. Neurol. — 1994. — 241, № 9. — 517-521.
18. Klein С., Grunewald А., K. Hedrich К. Early-onset parkinsonism associated with PINK1 mutations: frequency, genotypes, and phenotypes // Neurology. — 2006. — 66, № 7. — 1129-1130.
19. Leroy Е., Boyer R., Auburger G., Leube В., Ulm G., Mezey Е. et al. The ubiquitin pathway in Parkinson’s disease // Nature. — 1998. — 395, № 6701. — 451-452.
20. Maraganore D.M., de Andrade М., Elbaz А., Farrer M.J., Ioannidis J.P., Kruger R. et al. Collaborative analysis of alpha-synuclein gene promoter variability and Parkinson disease // JAMA. — 2006. — 296, № 6. — 661-670.
21. Marsden C.D. Parkinson’s disease // J. Neurol. Neurosurg. Psychiatry. — 1994. — 57, № 6. — 672-681.
22. Meigal А., Rissanen S., Tarvainen M.P., Karjalainen P.A., Iudina-Vassel I.A., Airaksinen О., Kankaanpāā М. Novel parameters of surface EMG in patients with Parkinson’s disease and healthy young and old controls // Journal of Electromyography and Kinesio-logy. — 2009. — 19. — e206-e213.
23. Neystat М., Lynch Т., Przedborski S., Kholodilov N., Rzhetskaya М., Burke R.E. Alpha-synuclein expression in substantia nigra and cortex in Parkinson’s disease // Mov. Disord. — 1999. — 14, № 3. — 417-422.
24. Rascol O.J., Sabatini U., Chollet F., Montastruc J.L., Marc-Vergnes J.F., Rascol А. Impaired activity of the supplementary motor area in akinetic patients with Parkinsons disease. Improvement by the dopamine agonist apomorphine // Adv. Neurol. — 1993. — 60. — 419-421.
25. Robichaud J.A., Pfann K.D., Leurgans S., Vaillancourt D.E., Comella C.L., Corcos D.M. Variability of EMG patterns: a potential neurophysiological marker of Parkinson’s disease? // Clin. Neurophysiol. — 2009. — 120, № 2. — 390-397.
26. Satoh J., Kuroda Y. Association of codon 167 Ser/Asn he-terozygosity in the parkin gene with sporadic Parkinson’s disease // Neuroreport. — 1999. — 10, № 13. — 2735-2739.
27. Sherman M.Y., Goldberg A.L. Cellular defenses against unfolded proteins: a cell biologist thinks about neurodegenerative disease // Neuron. — 2001. — 29, № 1. — 15-32.
28. Wakabayashi К., Engelender S., Tanaka Y., Yoshimoto М., Mori F., Tsuji S., Ross C.A., Takahashi Н. Immunocytochemical localization of synphilin-1, an alpha-synuclein-associated protein, in neurodegenerative disorders // Acta Neuropathol. (Berl). — 2002. — 103, № 3. — 209-214.