Международный неврологический журнал 6 (44) 2011
Вернуться к номеру
Клинические соотношения между наличием вегетативных расстройств и шкалой UPDRS у пациентов с болезнью Паркинсона
Авторы: Труфанов Е.А., Луганский государственный медицинский университет, кафедра неврологии и нейрохирургии
Рубрики: Неврология
Версия для печати
Целью нашего исследования являлось изучение взаимосвязи между наличием вегетативных расстройств и тяжестью заболевания по шкале UPDRS у пациентов с болезнью Паркинсона. Обследовано 205 больных с идиопатической болезнью Паркинсона. Результаты исследования показали, что имеется тесная взаимосвязь между наличием или отсутствием вегетативных расстройств и тяжестью заболевания по шкале UPDRS. Средняя сумма баллов всей шкалы UPDRS, а также I, II, III и IV разделов UPDRS у пациентов с болезнью Паркинсона с наличием вегетативных расстройств достоверно превышала среднюю сумму баллов у больных без вегетативных расстройств. Самые высокие показатели наблюдались в подгруппе больных болезнью Паркинсона с наличием непроизвольного мочеиспускания.
Болезнь Паркинсона, UPDRS, вегетативные расстройства, симптоматическая ортостатическая гипотензия.
Введение
Болезнь Паркинсона (БП) — первое описанное и наиболее изучаемое заболевание экстрапирамидной системы [8], которое клинически характеризуется четырьмя главными признаками: тремором покоя, брадикинезией, ригидностью и постуральной неустойчивостью [4, 14].
Несмотря на то что имеющиеся лекарственные препараты могут драматически уменьшить ведущие проявления болезни Паркинсона, заболевание неуклонно прогрессирует и его долгосрочный прогноз является неблагоприятным [9]. Через 15 лет после начала болезни более 70 % больных БП умирают или имеют выраженную инвалидизацию [9].
Частыми инвалидизирующими осложнениями БП являются вегетативные нарушения, которые существенно влияют на качество жизни больного и его повседневную активность, а в некоторых случаях могут приводить к смерти [1, 5, 6, 10, 11, 13]. Существует мнение, что возможна зависимость между двигательными расстройствами, когнитивной дисфункцией и вегетативными нарушениями у больных БП [2, 3, 7]. Следовательно, вегетативные нарушения и когнитивные расстройства могут служить потенциальными прогностическими факторами прогрессирования двигательных расстройств у больных БП.
Кроме того, лекарственные препараты, применяющиеся для лечения двигательных расстройств при болезни Паркинсона, иногда могут также вызывать или усиливать вегетативные расстройства, делая лечение болезни Паркинсона затруднительным [1].
Целью нашего исследования являлось изучение взаимосвязи между наличием вегетативных расстройств и тяжестью заболевания по шкале UPDRS у пациентов с болезнью Паркинсона.
Методы исследования
Нами обследовано 205 больных с идиопатической болезнью Паркинсона (140 мужчин и 65 женщин) в возрасте от 35 до 88 лет (средний возраст — 68,4 года).
Оценивались сумма баллов шкалы UPDRS, I (мышление, поведение, настроение), II (повседневная жизненная активность), III (исследование двигательных функций) и IV (осложнения терапии) ее разделов, а также суммы баллов по шкалам брадикинезии и ригидности (19, 22–26, 29, 31), тремора (16, 20, 21), шкалам падения, застывания, ходьбы, вставания со стула, позы, походки и постуральной стабильности UPDRS (13–15, 27–30), шкалам дискинезии (32–35) и клинических флуктуаций (36–39).
Результаты исследования
По нашим данным, симптоматическая ортостатическая гипотензия наблюдалась у 78 обследуемых больных (38,05 % всех больных болезнью Паркинсона), учащенное мочеиспускание, связанное с болезнью Паркинсона, встречалось у 74 больных (36,1 %), непроизвольное мочеиспускание при позывах, связанное с болезнью Паркинсона, — у 22 больных (10,73 %), задержки мочеиспускания — у 12 больных (5,85 %), запоры наблюдались у 104 больных (50,73 %).
Только 55 пациентов с болезнью Паркинсона (26,83 %) не имели вегетативных расстройств (табл. 1). У 94 больных (45,85 %) наблюдались 2 вегетативных расстройства и более, у 37 больных (18,05 %) — три или четыре вегетативных расстройства.
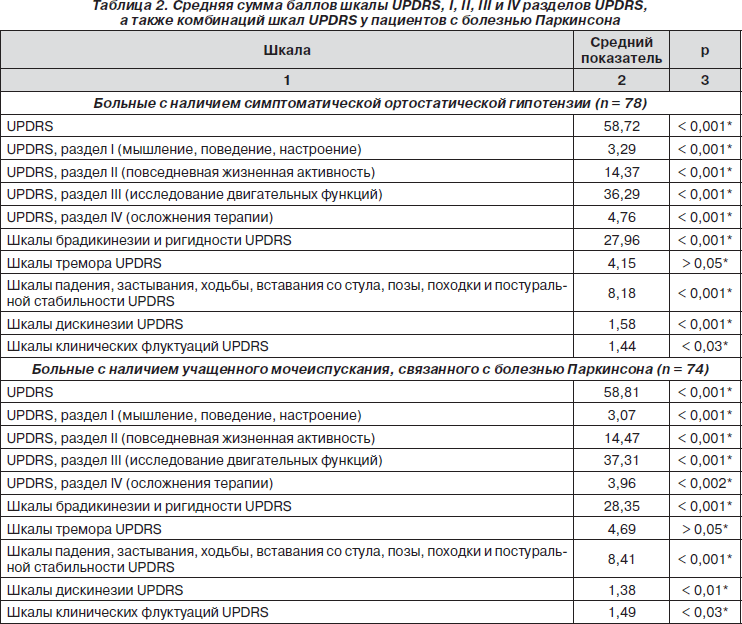
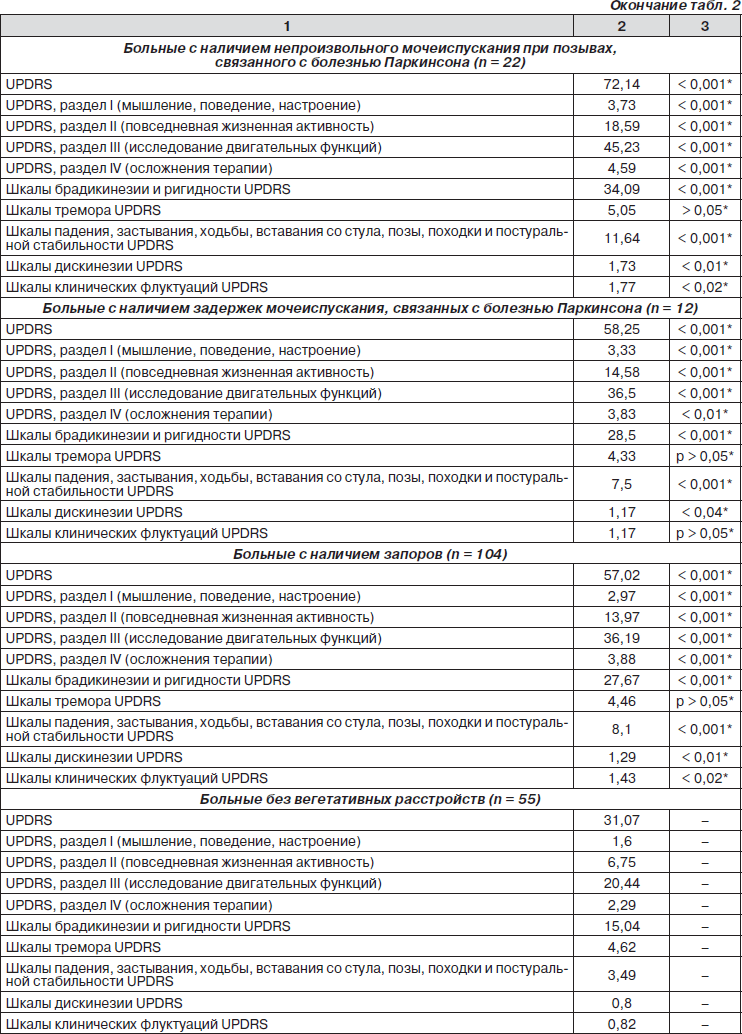
Средняя сумма баллов шкалы UPDRS у пациентов с болезнью Паркинсона с наличием вегетативных расстройств достоверно превышала таковую у больных без вегетативных расстройств (табл. 2). В группе больных с непроизвольным мочеиспусканием при позывах, связанным с болезнью Паркинсона, наблюдался самый высокий средний показатель шкалы UPDRS — 72,14. У больных с другими вегетативными расстройствами (симптоматическая ортостатическая гипотензия, учащенное мочеиспускание, связанное с болезнью Паркинсона, задержки мочеиспускания, связанные с болезнью Паркинсона, и запоры) этот показатель составлял от 57,02 до 58,81 балла, у больных без вегетативных расстройств — только 31,07 балла.
Похожая статистическая картина наблюдалась при оценке средней суммы баллов по I, II и III разделам UPDRS, а также шкалам брадикинезии и ригидности, шкалам падения, застывания, ходьбы, вставания со стула, позы, походки, постуральной стабильности и шкалам дискинезии UPDRS (табл. 2).
При оценке IV раздела UPDRS (осложнения терапии) наиболее высокие средние показатели наблюдались в группах больных с наличием симптоматической ортостатической гипотензии и непроизвольного мочеиспускания (табл. 2).
При оценке средней суммы баллов шкал клинических флуктуаций получены достоверные различия между группой больных без вегетативных расстройств и группами больных с наличием симптоматической ортостатической гипотензии, учащенного мочеиспускания, непроизвольного мочеиспускания и запоров. Не получено достоверных различий между группой больных без вегетативных расстройств и группой больных с наличием задержек мочеиспускания (табл. 2).
В то же время не было получено никаких различий между группами больных с наличием вегетативных расстройств и без них при оценке средней суммы баллов по шкалам тремора UPDRS (p > 0,05). В группах больных с различными вегетативными расстройствами средняя сумма баллов по шкалам тремора составляла от 4,15 до 5,05, в то время как в группе больных без вегетативных расстройств — составлял 4,62 (табл. 2).
Выводы
1. Вегетативные расстройства являются частым осложнением болезни Паркинсона (73,17 % больных).
2. Почти у половины больных (45,85 %) наблюдались два вегетативных расстройства или более.
3. Средняя сумма баллов всей шкалы UPDRS, а также I, II, III и IV разделов UPDRS, шкал брадикинезии и ригидности, шкал падения, застывания, ходьбы, вставания со стула, позы, походки, постуральной стабильности, шкал дискинезии и шкал клинических флуктуаций UPDRS у пациентов с болезнью Паркинсона с наличием вегетативных расстройств достоверно превышала среднюю сумму баллов у больных без вегетативных расстройств. Самые высокие показатели наблюдались в подгруппе с наличием непроизвольного мочеиспускания.
4. Не получено никаких статистических различий между группами больных с наличием вегетативных расстройств и без них при оценке выраженности тремора по шкалам тремора UPDRS.
5. Вегетативные расстройства при болезни Паркинсона существенно влияют на качество жизни больного, могут даже приводить к смерти [1, 4–6, 13] и требуют к себе такого же внимания, как и двигательные симптомы.
1. Dubow J.S. Autonomic Dysfunction in Parkinson’s Disease // Disease-a-month. — 2007. — № 53. — P. 265-274.
2. Autonomic and Cognitive dysfunction in Parkinson’s disease / J. Idiaquez, E.E. Benarroch, H. Rosales [et al.] // Clinical Autonomic Research. — 2007. — № 17. — P. 93-98.
3. Locascio J.J. Relation Between Clinical Characteristics of Parkinson’s Disease and Cognitive Decline // J.J. Locascio, S. Corkin, J.H. Growdon // Journal of Clinical and Experimental Neuropsychology. — 2003. — Vol. 25, № 1. — P. 94-109.
4. Parkinson’s Disease / W. Martin, O. Suchowersky, K.K. Burns, E. Jonsson. — Weinheim: WILEY-VCH Verlag GmbH & Co. KGaA, 2010. — 336 p.
5. Orthostatic Hypotension: Evaluation and Treatment / S. Maule, G. Papotti, D. Naso [et al.] // Cardiovascular & Haematological Disorders — Drug Targets. — 2007. — № 7. — P. 63-70.
6. Characteristics of orthostatic hypotension in Parkinson’s disease / H. Oka, M. Yoshioka, K. Onouchi [et al.] // Brain. — 2007. — № 130. — P. 2425-2432.
7. Medical Services Utilization and Prognosis in Parkinson’s Disease: A Population-Based Study / S.A. Parashos, D.M. Maraganore, P.C. O’Brien [et al.] // Mayo Clinic Proceedings. — 2002. — Vol. 77. — P. 918-925.
8. Patten J. The Extrapyramidal System and the Cerebellum // Neurological Differential Diagnosis. — Glasgow: Springer, 2004. — P. 178-212.
9. Poewe W. Clinical Measures of Progression in Parkinson’s Disease // Movement Disorders. — 2009. — Vol. 24, Suppl. 2. — P. S671-S676.
10. Poewe W. Dysautonomia and Cognitive Dysfunction in Parkinson’s Disease // Movement Disorders. — 2007. — Vol. 22, Suppl. 17. — P. S374-S378.
11. Prognostic Factors for the Progression of Parkinson’s Disease: A Systematic Review / B. Post, M.P. Merkus, R.J. de Haan [et al.] // Movement Disorders. — 2007. — Vol. 22, № 13. — P. 1839-1851.
12. Movement Disorders / N. Quinn, K. Bhatia, P. Brown et al. // Neurology: A Queen Square Textbook / Ed. by C. Clarke, R. Howard, M. Rossor, S. Shorvon. — Oxford: Blackwell Publishing Ltd, 2009. — P. 155-187.
13. The relationship between anosmia, constipation, and orthostasis and Parkinson’s Disease duration / A.L. Ramjit, L. Sedig, J. Leibner [et al.] // International Journal of Neuroscience. — 2010. — № 120. — P. 67-70.
14. Practice Parameter: Diagnosis and prognosis of new onset Parkinson’s Disease (an evidence-based review). Report of the Quality Standards Subcommittee of the American Academy of Neurology / O. Suchowersky, S. Reich, J. Perlmutter et al. // Neurology. — 2006. — № 66. — P. 968-975.