Журнал «Медицина неотложных состояний» 7-8 (38-39) 2011
Вернуться к номеру
Парентеральное питание, обеспечивающее ограниченное количество линолевой кислоты у пациентов с тяжелыми ожогами.
Авторы: Garcia-de-Lorenzo A., Denia R., Hospital Universitario La Paz, Intensive Care Unit, Paseo de la Castellana, Madrid, Spain Atlan P., Baxter SAS, R&D Nutrition, Maurepas Cedex, France Martinez-Ratero S., Hospital Universitario La Paz, Intensive Care Unit, Paseo de la Castellana, Madrid, Spain Le Brun A., Evard D., Baxter SAS, R&D Nutrition, Maurepas Cedex, France Bereziat G., Laboratory of Biochemistry, Saint-Antoine Hospital, Paris, France
Рубрики: Семейная медицина/Терапия, Медицина неотложных состояний
Версия для печати
Считается, что жировая эмульсия (ЖЭ) с ограниченным содержанием линолевой кислоты может улучшать безопасность проводимого полного парентерального питания (ППП). Переносимость ППП и его эффект на метаболизм жирных кислот были оценены в данном рандомизированном двойном слепом исследовании: проводилось сравнение 2 жировых эмульсий — деривата масел оливок и соевых бобов (ЖЭДОСБ), содержащих в своем составе длинноцепочечные триацилглицериды (ДТАГ), с жировой эмульсией, содержащей в своем составе среднецепочечные триацилглицериды (СТАГ) и ДТАГ (ЖЭСТАГ) (в соотношении 50 : 50), у 2 групп пациентов с тяжелыми ожогами тела (группы Д и С, по 11 человек в каждой). После проведения интенсивной терапии (на протяжении 48–72 ч) пациенты получали ППП, обеспечивающее 147 кДж/кг/день (35 ккал/кг/день), поступление жиров обеспечивалось за счет жиров плазмы на протяжении 6 дней в дозе 1,3 г/кг/день, после чего проводилось исследование лабораторных показателей, включающих печеночные пробы, определение уровня цитокинов плазмы до и после проведения ППП. Побочные эффекты и клинические исходы у пациентов после проведенного ППП регистрировались на протяжении 6 мес. При введении обеих ЖЭ процессы превращения линолевой кислоты в ее высшие производные (ди-гомо-γ-линолевую кислоту) значительно улучшились, а дефицит незаменимых жирных кислот (НЖК) не манифестировал. Ненормальные показатели печеночных тестов регистрировались чаще в группе С (9 пациентов), чем в группе Д (3 пациента) (Р = 0,04, тест Suissa-Shuster). 7 пациентов (4 из группы Д и 3 из группы С) умерли от последствий тяжелого сепсиса через 3–37 дней после завершения 6-дневного периода получения ППП. Если сравнивать группы выживших пациентов с теми, которые умерли, последние были старше (Р = 0,01), уровень гипергликемии на входе исследования был значительно выше (Р < 0,001) и уровень интерлейкина-6 (ИЛ-6) плазмы крови возрастал в динамике (Р < 0,04). Хотя метаболизм жиров и переносимость ППП были схожими при использовании обеих жировых эмульсий, зафиксированное в данном исследовании сохранение функции печени при использовании ЖЭДОСБ требует дополнительного подтверждения.
Ожоги, жировая эмульсия, оливковое масло, печеночные пробы.
Ожоговая болезнь — одно из тяжелейших физиологических состояний, приводящих к разрушительным ответам организма на метаболический стресс. Хотя ранние критерии выживаемости пациента в большинстве своем зависят от распространенности ожогов, не менее важными показателями являются возраст и наличие сопутствующей патологии, и стратегии проведения полного парентерального питания (ППП) могут благоприятствовать выздоровлению с возможным уменьшением показателей смертности данных пациентов. Несмотря на то что специфических рекомендаций по проведению ППП для пациентов ожогового стационара в качестве стандартов утверждено не было, природа и количество потребления питательных веществ являются критически важными для пациентов данного профиля, которые одновременно страдают от процессов гиперметаболизма, воспаления и иммуносупрессии и поэтому являются крайне чувствительными к рискам развития септических состояний.
Некоторые публикации демонстрировали, что избыточное потребление жиров может отрицательно влиять на иммунную систему и клинический исход у пациентов в критическом состоянии, особенно с ожоговой болезнью. Понимание взаимоотношений между высоким потреблением жиров и искаженным иммунным ответом возникло из работ, в которых ранее использовали жировые эмульсии (ЖЭ) — дериваты масел оливок и соевых бобов (ЖЭДОСБ), поскольку именно они и являлись основным и наиболее часто используемым источником жиров. ЖЭДОСБ богаты n-6 полиненасыщенными жирными кислотами (ПНЖК), а именно линолевой кислотой (ЛК 18 : 2n-6), которая, по многим представлениям, вызывает чрезмерную продукцию простагландинов и других эйкозаноидов, связанных с потенциальным риском ухудшения существующего иммуносупрессивного и воспалительного статуса у пациентов в критическом состоянии.
Альтернативами ЖЭДОСБ являются эмульсии, содержащие ограниченное количество ЛК. Липидные эмульсии (ЛЭ), которые в настоящее время стали доступными на рынке, основаны на смеси оливкового масла и масла соевых бобов (4 : 1) и характеризуются низким содержанием ЛК (18 % от содержания всех жирных кислот) и высоким содержанием олеиновой кислоты (ОК), n-9 среднененасыщенной жирной кислоты. Клинические исследования уже подтвердили питательную и метаболическую эффективность данной жировой эмульсии, а также ее общую безопасность как при кратковременном ППП у пациентов в критическом состоянии и недоношенных, так и при более длительных сроках ППП у взрослых и пациентов педиатрического профиля.
Для подтверждения потенциального интереса к применению данной ЖЭ с низким содержанием ЛК у пациентов в критическом состоянии мы осуществили данное двойное слепое рандомизированное исследование у пациентов с тяжелыми ожогами. Для определения роли ограниченного поступления ЛК мы провели сравнительный анализ использования данной ЖЭ с использованием эмульсии, в составе которой было также низкое содержание ЛК (26 % от общего содержания ЖК, Lipofundina, B. Braun, Melsungen, Germany), а среднецепочечные и длинноцепочечные триацилглицериды (СТАГ и ДТАГ) содержатся в соотношении 50 : 50. Использование этой внутривенной ЖЭ оправданно во многих клинических ситуациях, и она повседневно применяется в отделениях интенсивной терапии (ОИТ).
Методы
Протокол исследования был одобрен Комитетом по правам человека в Университетском госпитале «La Paz» и соответствовал регуляторной политике European Good Clinical Practice.
Пациенты и дизайн исследования
Взрослые пациенты с тяжелыми ожогами (индекс тяжести ожогов і 7), которые пребывали на лечении в ОИТ, были включены в исследование, ППП было показано на срок от 5 до 7 дней согласно стандартам ведения таких пациентов в вышеуказанном лечебном учреждении. Показаниями к проведению ППП были требования к высокому энергопотреблению и формальные противопоказания к энтеральному питанию. Перед проведением ППП пациентам проводились мероприятия интенсивной терапии, направленные на восстановление объема циркулирующей крови, на протяжении менее 3 дней раствором Рингера или 0,9% раствором хлорида натрия в сочетании со свежезамороженной плазмой.
Пациенты исключались из исследования, если у них были ранее существующие патологические состояния, например ВИЧ, хронические заболевания почек (креатинемия > 2 мг/дл), нарушения функции печени (уровень билирубина вдвое больше верхней границы нормы (> 2 ВГН), АЛТ или АСТ > 4 ВГН или протромбиновое время < 50 %), нарушения обмена жиров (триацилглицериды (ТАГ) > 250 мг/дл) или наличие противопоказаний к введению компонентов ППП. Пациенты, которым проводилась седация пропофолом, исключались из исследования в связи с тем, что данный препарат является ЖЭ. Все пациенты получали сходное лечение раневой поверхности, включая иссечение некротизированных тканей и трансплантацию кожи при ожогах 2-й и 3-й степени, ИВЛ, аналгезию и антибиотикотерапию.
Пациенты включались в данное контролируемое двойное слепое рандомизированное моноцентровое исследование при наличии свободных коек в данном центре. Пациенты были информированы о ранее проведенных клинических исследованиях по сравнению эффективности ЖЭ деривата соевых белков (ЖЭДСБ) и ЖЭ деривата оливкового масла (ЖЭДОМ) и изучению влияния ЖЭ на профиль жирных кислот плазмы крови в качестве первичного критерия оценки их эффективности.
Парентеральное питание (ПП)
Пациенты рандомизированно включались в состав одной или другой группы для получения определенного (эксклюзивного) для данной группы ПП с использованием либо 20% ClinOleic (Baxter, Maurepas, France, группа Д), либо Lipofundina СТАГ/ДТАГ (B. Braun, группа С) на протяжении 6 дней. Состав ЖЭ представлен в табл. 1.
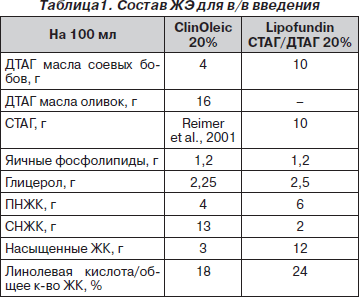
Питательная смесь готовилась ежедневно по разработанной методике, используемой регулярно в данном клиническом учреждении, упаковывалась в пластиковые контейнеры без этикеток, вводилась постоянно на протяжении 24 часов через катетер в центральном венозном сосуде. Для подтверждения идентичности энергетического и азотного состава употребляемого парентерального питания в 2 группах ППП (на 1 кг нормального веса тела в день) содержало 147 кДж энергии и 0,25 г азота в азотных соединениях в качестве Synthamin (Baxter). Жиры вводились из расчета 1,3 г/кг нормального веса тела в день, глюкоза — 4,3 г/кг нормального веса тела в день, что составляло 40 и 60 % энергообеспечения пациента небелкового происхождения соответственно. Витамины (Cernevit, Baxter, Maurepas, France), микроэлементы (Addamel, Fresenius Kabi, Bad Homburg, Germany) и электролиты (Na, K) назначались согласно индивидуальной необходимости.
Профиль жирных кислот фосфолипидов плазмы крови
Образцы для исследования забирались до первой жировой инфузии (день 1) и через 4–8 часов после последней инфузии (день 6). Образцы хранились при температуре –20 °С в пробирках, которые содержали 2мл плазмы в 0,4 мл раствора бутилированного гидрокситолуэна (1 г/л абсолютного этанола) в качестве антиоксиданта. Жирные кислоты фосфолипидов измерялись по методике Driss et al. с использованием газожидкостной хроматографии на хроматографе Carlo Erba (Erba & Sciences, Paris, France), оснащенном полярной колонкой (Omegawax Supelco Inc., Bellafonte, PA, USA) и пламенно-ионизационным детектором. Определялись уровни (%) каждой фракции насыщенных ЖК, СНЖК и ПНЖК. Уровень арахидоновой кислоты (АК), АК : ЛК, сумма высших производных ЛК (еn-6, C > 18 + 18 : n-6) к ЛК и соотношение 20 : 3n-6 : АК рассчитывались как отражение активности d6- и d5-десатуратов. Соотношение триены/тетраены (20 : 3n-9 к 20 : 4n-6) и отношение n-3 к n-6 были установлены как показатели уровня недостаточности незаменимых ЖК, текучести мембраны и иммунной функции.
Показатели клинической и биологической безопасности
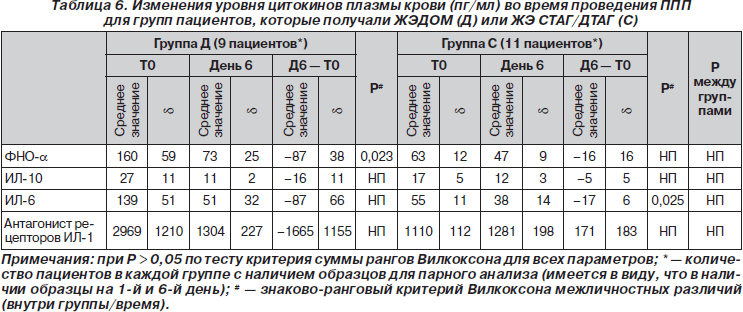
Все пациенты мониторировались по следующим показателям: потребление ППП, побочные эффекты, биохимические показатели (альбумин плазмы, С-реактивный белок, фибриноген, глюкоза, мочевина, креатинин, Na, K, Cl), гематологические показатели (гемоглобин, эритроциты, тромбоциты), липиды (общий холестерин, ТАГ), начиная с периода введения пациента в исследование и заканчивая 6-м днем. Уровень концентрации в плазме крови провоспалительных (ИЛ-6, ФНО-a) и противовоспалительных (антагонист рецепторов ИЛ-1, ИЛ-10) цитокинов количественно определялся на 1-й день перед первым введением ЖЭ и на 6-й день, 4–8 часов спустя после введения последней дозы ЖЭ, реактивами ELISA (Quantikine, R&D Systems Europe, Abingdon, Oxfordshire, UK).
Поскольку печеночные пробы являются критическими параметрами безопасности во время парентеральной инфузии ЖЭ, мы провели детальный анализ этих параметров. Все аномальные показатели интерпретировались следующим образом:
1) холестаз — когда уровень показателя оказался выше ВГН во время периода лечения и повышенный уровень регистрировался хотя бы для 2 из следующих параметров: конъюгированный билирубин, щелочная фосфатаза, ГГТ-транспептидаза;
2) цитолиз — когда уровень АСТ и/или АЛТ во время периода лечения > 2 ВГН.
Побочные эффекты и клинические исходы
Септические состояния, шкала синдрома полиорганной недостаточности (ПОН), длительность ИВЛ, заболеваемость, смертность, длительность пребывания в ОИТ и госпитале учитывались во время периода двойного слепого исследования и в последующем периоде наблюдения по истечении 6 мес.
Статистический анализ
Результаты выражены как средние величины со стандартными отклонениями (d). Программа SAS (SAS Institute Inc, Cary, NC, USA) для Windows была использована для анализа статистических данных. Было проведено сравнение исходных (день 1) клинических и лабораторных параметров пациентов. Для количественных критериев был использован метод непараметрического анализа. Сравнение групп проводилось с использованием критерия суммы рангов Вилкоксона, для определения межличностных различий на 6-й день и 1-й день использовался знаково-ранговый критерий Вилкоксона.
Для тестирования аномалий печеночных проб проводили тест Suissa-Shuster. Этому тесту отдали предпочтение в сравнении с тестом c2 или тестом Fischer, поскольку тест Fischer не совсем точен, когда речь идет о небольших выборках, а условия применения теста c2 не были выполнены до конца (менее 5 для некоторых параметров/событий).
Анализ был проведен на группах по назначенному лечению (intention-to-treat), а уровень достоверности установлен как Р Ј 0,05.
Результаты
Характеристика исходных групп пациентов
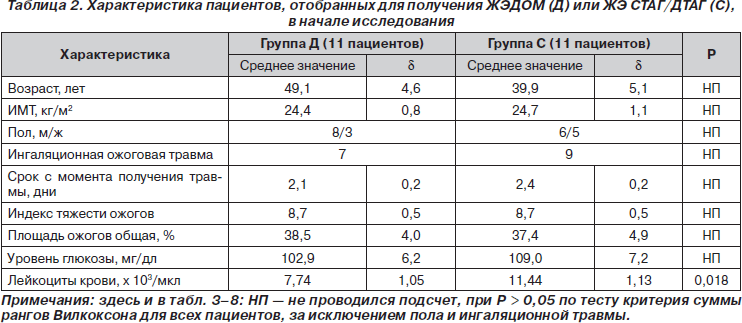
После получения информированного добровольного согласия 22 пациента были включены (11 в каждой группе) в исследование. Все они были здоровыми до получения ожогов. Обе группы не имели существенных возрастных, биометрических различий, различий по гендерному составу, площади ожоговой поверхности или необходимости в ИВЛ на этапе начала исследования (табл. 2). Некоторые аномалии гепатобилиарной системы определялись в обеих группах пациентов (холестаз — один случай в группе Д, цитолиз — 2 случая в группе Д против 1 случая в группе С). Исходные лабораторные показатели существенно не отличались в 2 группах, кроме усредненного показателя количества лейкоцитов в группе С.
Парентеральное питание
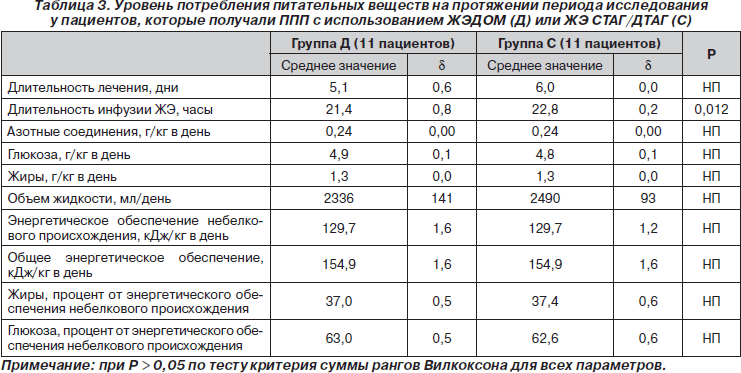
Во время двойного слепого исследования средние показатели (на 1 кг/день) количества парентерально вводимых жиров, азотсодержащих соединений и глюкозы были сходными в обеих группах (табл. 3). Использование других медикаментозных препаратов, включая витамины, микроэлементы, заменители плазмы, фракции белков плазмы, кровь и ее препараты, несущественно отличалось в 2 группах (данные не представлены).
Жирные кислоты фосфолипидов плазмы
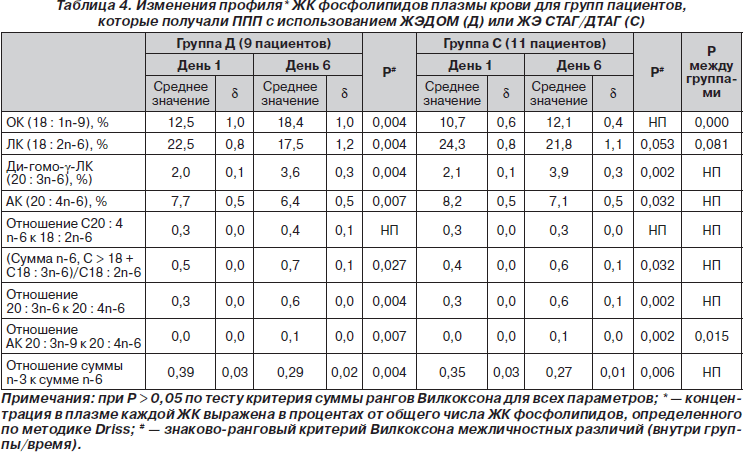
Изменения в составе жирных кислот фосфолипидов плазмы с 1-го по 6-й день несущественно отличались в 2 группах, за исключением ОК, показатели которой значительно выросли в группе Д в сравнении с группой С (Р < 0,001, табл. 4).
Уровни ЛК в плазме уменьшились в обеих группах (–5,06 (d = 0,65), Р = 0,004, и 2,52 (d = 0,91), Р = 0,05, в группах Д и С соответственно). Эти изменения были связаны со статистически достоверным уменьшением уровня АК (–1,32 (d = 0,43), Р = 0,01, и –2,52 (d = 0,91), Р = 0,03 в группах Д и С соответственно). Несмотря на это, превращение ЛК в ее производные С20-С22 сохранялось, что показано на примере соотношения АК и ЛК, которое не изменилось, а соотношение между суммой высших производных ЛК и ЛК существенно изменилось (Р = 0,03 в обеих группах). Возрастание уровня ди-гомо-g-линолевой кислоты (С20 : 3n-6) в обеих группах (Р = 0,004 и Р = 0,002 в группах Д и С соответственно) также сильно контрастировало в сравнении со снижением уровня АК. Соотношение триены/тетраены (хотя уровни обеих субстанций возрастали) сохранялось ниже уровня порогового значения 0,2 у всех пациентов, указывая на то, что у них не развивалось дефицита незаменимых жирных кислот (НЖК). И наоборот, показатели соотношения n-3 и n-6 снижались в обеих группах (Р = 0,004 и Р = 0,007 в группах Д и С соответственно).
Нутритивный и воспалительный статус
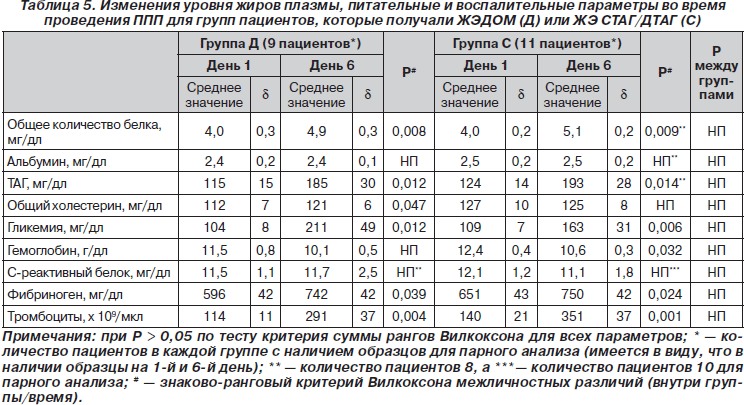
Изменения в нутритивном статусе и параметров — индикаторов воспаления, включая показатели цитокинов плазмы крови, статистически не отличались в обеих группах (табл. 5 и 6).
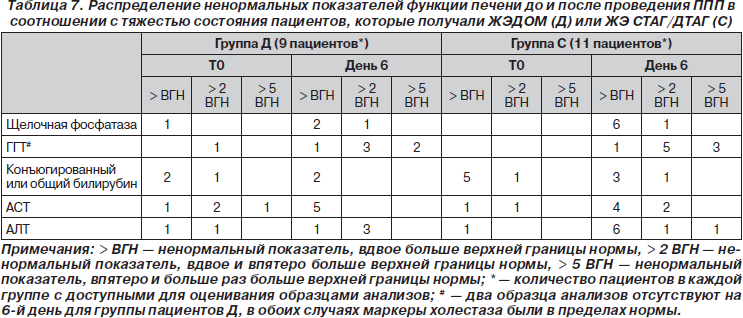
Печеночные пробы
После 6-дневного периода инфузионной терапии, аномальные показатели печеночных проб встречались чаще в группе С (табл. 7). Маркеры холестаза выявлялись при проведении ППП у 3 из 9 пациентов в группе Д в сравнении с 9 из 11 пациентов группы С. Эти различия были статистически достоверными между 2 группами (Р = 0,04, тест Suissa-Shuster). Маркеры цитолиза также были ассоциированы с маркерами холестаза у 2 пациентов группы Д и 3 пациентов группы С.
Сравнительный анализ клинических и лабораторных параметров в группах пациентов с наличием и отсутствием признаков аномальной функции печени (11 против 10 соответственно) показал отсутствие зависимости в изменении этих параметров от возраста пациентов, гендерной принадлежности, индекса массы тела (ИМТ), индекса тяжести ожогов, характера парентерального питания или частоты возникновения септических состояний. Исходные показатели уровня глюкозы, профиль жирных кислот фосфолипидов и индикаторов воспаления, включая цитокины, и их изменения существенно не отличались у тех пациентов, которые имели отклонения функции печени, в сравнении с пациентами без них.
Другие лабораторные параметры
Изменения уровня жиров плазмы крови статистически не отличались между 2 группами (табл. 5). Показатели ТАГ плазмы крови возрастали в пределах 1 и 2 ВГН у 3 пациентов в каждой группе и выше 2 ВГН у 1 пациента из группы С. Уровень общего холестерина был в пределах нормы в начале исследования, но ниже нормы у 2 пациентов из каждой группы. Эти показатели оставались неизменными или нормализовались с течением времени у всех пациентов, за исключением 2 из группы С, у которых данные показатели имели тенденцию к снижению (информация утеряна для 2 пациентов группы Д).
Были зафиксированы эпизоды гипергликемии или повышения уровня гликемии в обеих группах в пределах 1 и 2 ВГН у 5 пациентов группы Д в сравнении с 3 пациентами группы С и выше 2 ВГН у 3 пациентов группы Д в сравнении с 2 пациентами группы С. Статистически достоверной разницы по другим общеклиническим показателям между 2 группами пациентов зафиксировано не было (данные не представлены в табличном виде).
Побочные эффекты и клинические исходы
На протяжении 6-дневного периода ППП у 6 пациентов из каждой группы были зафиксированы септицемия, подтвержденная легочная инфекция и инфекция раневой ожоговой поверхности.
После прекращения ППП 7 пациентов умерло из-за критического нарушения функции одной из систем органов в ОИТ (от 4 до 37 дней после введения последней инфузии ЖЭ, 4 пациента из группы Д, включая смерть на 2-й день, 3 пациента из группы С). Других смертей на протяжении 6-месячного периода зафиксировано не было. Для каждого летального исхода прямой причиной смерти являлось септическое состояние пациентов (Bone, 1992).
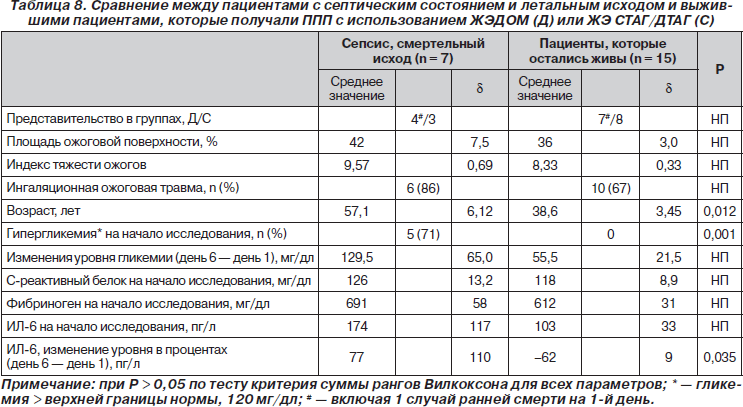
При сравнительном анализе информации об умерших пациентах (7 чел.) и информации о тех пациентах, которые выжили, следующие исходные показатели не отличались друг от друга: ИМТ, индекс тяжести ожогов, индикаторы воспаления, уровень ТАГ, общего холестерина и уровни альбумина сыворотки крови (табл. 8). Уровень потребления питательных веществ тоже существенно не отличался. У 7 пациентов с летальным исходом ожоги тела сочетались с ожогами органов дыхания, хотя эти показатели в соответствии со шкалой тяжести ожогов не делали этих пациентов статистически отличными от выживших. У 7 пациентов с летальным исходом были значительные статистические отличия от выживших пациентов по 3 параметрам: возраст, исходная гипергликемия, изменения уровня цитокинов плазмы крови. Действительно, пациенты, которые умерли, были значительно старше и исходный уровень гипергликемии у них был значительно выше (> 110 мг/дл). Относительный риск (ОР) смертности на протяжении 6 месяцев с момента получения ожоговой травмы был в 8,5 раза выше у пациентов с исходной гипергликемией (ОР = 8,5, 95%). Проведя анализ изменения уровня цитокинов плазмы, мы пришли к выводу, что уровень ИЛ-6 изменялся у пациентов по-разному: так, уровень ИЛ-6 продолжал возрастать у пациентов с фатальным септическим состоянием и понижаться у других пациентов.
Изменения в шкале ПОН, длительность ИВЛ (11,0 (d = 3,6) в сравнении с 13,0 (d = 4,9) дня), длительность пребывания в ОИТ (32,9 (d = 3,2) в сравнении с 41,8 (d = 4,9) дня) и госпитале (57,0 (d = 4,6) в сравнении с 64,9 (d = 8,2) дня) не были статистически достоверными при сравнении в группах Д и С соответственно.
Обсуждение
Глубокие изменения в метаболизме жирных кислот как следствие ожоговой травмы описаны в литературе и являются основополагающим процессом в развитии иммуносупрессивного и гипервоспалительного статуса в посттравматическом периоде. В частности, уровень ЛК и высших производных ЛК фосфолипидов плазмы и клеточных мембран, включая АК, существенно снижается в раннем посттравматическом периоде и характеризуется длительным и прогрессирующим нарастанием дефицита в динамике на протяжении не менее 2 недель после получения ожоговой травмы. Изменения профиля жирных кислот фосфолипидов достигают своего максимума на 7–10-й день после травмы и сопровождаются одновременным поражением иммунной системы и накоплением воспалительных медиаторов.
Это первая публикация в мировой литературе, которая освещает проблему влияния парентерального питания на метаболизм ЖК у пациентов с термальной травмой. Это исследование по своей сути было экспериментальным, поскольку никто ранее не сравнивал эффекты ЖЭ деривата масла оливок и ЖЭ СТАГ/ДТАГ у пациентов в критическом состоянии. Выбор в пользу ЖЭ СТАГ/ДТАГ в качестве ЖЭ для сравнения был сделан на основании предварительного использования данной ЖЭ в данном клиническом центре. Мы подтвердили, что ЖЭ с высоким содержанием ЛК потенциально оказывает влияние на иммунные и воспалительные процессы. В нашем исследовании сравнительное использование 2 ЖЭ с ограниченным содержанием ЛК подтверждает следующие предположения: улучшение показателей метаболизма ЖК во времени (процессы превращения ЛК в ди-гомо-g-линолевую кислоту) и общую безопасность ЖЭ у пациентов с тяжелыми ожогами тела.
Наши данные коррелируют с ранее опубликованной информацией. Так, на 6-й день (что соответствует 7–9-му дню после получения ожоговой травмы) наблюдается снижение уровня ЛК и АК, что частично объясняется как последствие синтеза простагландинов-2 по пути окислительного метаболизма из АК. Мы наблюдали в 2 группах статистически достоверное увеличение суммы уровней n-6 высших производных, соотношения АК : ЛК и уровня ди-гомо-g-линолевой кислоты (С20 : 3n-6), непосредственного прекурсора простагландинов-1, антиагреганта, противовоспалительного эйкозаноида. Эти данные могут отражать положительный эффект на метаболизм ЛК ЖЭ со сниженным содержанием ЛК, несмотря на сохраняющийся воспалительный ответ у пациентов с тяжелыми ожогами тела.
Хотя существенной разницы в общей безопасности ЖЭ не было найдено, статистически большее количество пациентов испытывали негативные изменения функции печени при получении СТАГ/ДТАГ ЖЭ, что поднимает вопросы относительно переносимости данной ЖЭ и предполагает наличие охранного эффекта на функцию печени ЖЭДОМ/ЖЭДСБ.
Ранее опубликованные данные свидетельствуют о том, что функция печени может существенно ухудшаться у пациентов с тяжелыми ожогами. Ранние изменения структуры печени могут быть результатом шока и гиповолемии, но более существенные изменения развиваются значительно позже, как результат септического состояния и других отягчающих факторов. Отрицательные изменения функции печени часто развиваются у пациентов, которые получают парентеральное питание, особенно на протяжении длительного периода. В нашем исследовании, в котором тяжелые причинные факторы могут иметь место (статус пациента, тяжесть полученных ожогов, сепсис), ни один из них не являлся основополагающим в объяснении причин патологических изменений функции печени.
Анализируя предыдущие клинические исследования, мы пришли к заключению, что переносимость для функционального статуса печени ЖЭ ClinOleic описывалась как сходная с таковой у ЖЭДОМ/ЖЭДСБ. Более того, некоторые экспериментальные работы, проведенные на крысах, показали преимущества ClinOleic. Во-первых, продемонстрировано, что ClinOleic существенно не влияет на билиарную секрецию в отличие от ЖЭДСБ. Во-вторых, на модели грамотрицательной бактериемии проводилось сравнение ClinOleic с ЖЭ СТАГ/ДТАГ и ЖЭДОМ/ЖЭДСБ. Функция мононуклеарной фагоцитарной системы гораздо лучше сохранялась при использовании ЖЭДОМ. Бактериальный клиренс печени животных, функция селезенки и легких значительно ухудшались при использовании парентерального питания одной из вышеуказанных ЖЭ по сравнению с контрольной группой, которая получала пероральное питание.
Что касается ЖЭ СТАГ/ДТАГ, экспериментальные работы также доказали преимущества данной ЖЭ. Предполагается, что СТАГ оказывают положительное влияние на возможность возникновения и течение процессов патологических изменений в печени, вызванных липополисахаридами. С другой стороны, это не первые работы, которые указывают на ухудшение функции печени при использовании этой ЖЭ, хотя ни одного убедительного объяснения причин возникновения данного состояния дано не было. Кроме того, кратковременные инфузии ЖЭ СТАГ/ДТАГ у людей приводят к увеличению уровня общих жиров и холестерина в желчи и увеличению риска камнеобразования у пациентов с камнями или без них в желчном пузыре. Недавние исследования, проведенные на пациентах в септическом состоянии, которым требовалось полное парентеральное питание, подтвердили, что инфузия ЖЭ СТАГ/ДТАГ в сравнении с инфузией ЖЭДСБ приводит к росту уровня ТАГ и общего несвязанного холестерина в плазме крови. Наконец, необходимо помнить, что ЖЭ, произведенные в различных условия на разных производствах, могут вызывать разные побочные эффекты, несмотря на то что основные ингредиенты состава остаются неизменными.
Сепсис остается одной из основных причин смертности в остром периоде ожоговой болезни. В данном исследовании количество септических осложнений, с высоким уровнем смертности пациентов, совпадает с такими показателями в предыдущих исследованиях, что может частично объясняться высокими баллами по шкале оценки тяжести ожогов и частотой наличия больных с ожоговыми травмами дыхательной системы (ожоговая ингаляционная травма).
Другие факторы риска смертности в послеожоговом периоде оценивались по определенным критериям (возраст, изменения уровня цитокинов, а также гипергликемия до и после периода интенсивной терапии до момента начала ППП). В соответствии с недавним исследованием Van den Berghe, которое подтвердило, что даже умеренная гипергликемия может увеличить риск смертности у пациентов ОИТ, наши данные показали возрастание относительного риска смертности в 8,5 раза на протяжении 6 месяцев после получения ожоговой травмы при наличии гипергликемии до начала ППП. У этих пациентов гипергликемия скорее объясняется действием ожоговой травмы и связанным с ней стрессовым статусом всех систем, чем введением раствора глюкозы некоторым из них. Принимая во внимание количество (объем) ЖЭ, обогащенной СНЖК, введенной пациентам для нормализации обмена глюкозы, мы считаем, что 6-дневный период является слишком коротким для подтверждения положительного влияния инфузии и демонстрации этих эффектов.
Наконец, в некоторых исследованиях изучали эффект в/в ведения ЖЭ на уровень продукции цитокинов. Эти исследования были в основном направлены на подтверждение иммуносупрессивного влияния ЖЭДСБ и возможности потенциального использования альтернативных форм ЖЭ, например СТАГ/ДТАГ, ЖЭ со структурированными жирами или ЖЭДОМ. Ниже поданы результаты нашего исследования:
1) уровень про- и противовоспалительных цитокинов имеет тенденцию к снижению, хотя их показатели остаются на достаточно высоком уровне через 10 дней после ожоговой травмы;
2) изменения уровня ИЛ-6, с постоянной тенденцией к возрастанию у умерших пациентов, могут быть относительным предвестником летального исхода.
В заключение можно отметить, что использование ПП, которое содержит в своем составе ЖЭ с ограниченным количеством ЛК, является эффективным для предотвращения и нормализации нарушений метаболизма НЖК у пациентов с тяжелой ожоговой травмой. Различия, найденные в изменениях параметров функции печени, могут говорить в пользу ЖЭДОМ/ЖЭДСБ при ее использовании в качестве альтернативы другим ЖЭ при проведении ППП у пациентов с тяжелой ожоговой травмой.
Перевод Константина Кремца
Оригинал статьи опубликован в British Journal of Nutrition (2005), 94, 221-230.
1. Alexander J.W. Mechanism of immunologic suppression in burn injury // J Trauma (1990) 30, 70S-75S.
2. Alpers D.H. Liver complications and failure in patients on home parenteral nutrition // Curr Opin Gastroenterol (2001) 17, 147-149.
3. Barlow Y. T-lymphocytes and immunosuppression in the burned patient: a review // Burns (1994) 20, 487-490.
4. Battistella F.D., Widergren J.T., Anderson J.T., Siepler J.K., Weber J.C. & MacColl K. A prospective, randomized trial of intravenous fat emulsion administration in trauma victims requiring total parenteral nutrition // J Trauma (1997) 43, 52-60.
5. Beau P., Barrioz T. & Ingrand P. Is parenteral nutrition-related cholestatic liver disease an infectious disease? // Gastroenterol Clin Biol (1994) 18, 63-67.
6. Beau P., de Lйdinghen V. & Ingrand P. Total parenteral nutritionrelated liver disease and medium chain triglycerides lipid emulsions // Nutr Clin Metabol (1995) 9, 117-122.
7. Bellinati-Pires R., Waitzberg D.L., Salgado M.M. & Carneiro-Sampaio M.M. Functional alterations of human neutrophils by medium-chain triglyceride emulsion: evaluation of phagocytosis, bacterial killing, and oxidative activity // J Leukoc Biol (1993) 53, 404-410.
8. Bone R.C. Definitions for sepsis and organ failure and guidelines for the use of innovative therapies in sepsis. The ACCP/SCCM Consensus Conference Committee. American College of Chest Physicians/Society of Critical Care Medicine // Chest (1992) 101, 1644-1655.
9. Bouletreau P., Berrada K. & Chambrier C. Tolйrance hйpatique de l’йmulsion lipidique ClinOleic® // Nutr Clin Mйtabol (1996) 10, 335-365.
10. Calder P.C. & Newsholme E.A. PUFAs suppress human peripheral blood lymphocytes proliferation and interleukin-2 production // Clin Sci (1992) 75, 695-700.
11. Capron J.P., Gineston J.L., Hervй M.A. & Braillon A. Metronidazole in prevention of cholestasis associated with total parenteral nutrition // Lancet (1983) 1, 446-447.
12. Carsin H., Assicot M., Feger F., Roy O., Pennacino I., Le Bever H., Ainaud P. & Bohuon C. Evolution and significance of circulating procalcitonin levels compared with IL-6, TNF alpha and endotoxin levels early after thermal injury // Burns (1997) 23, 218-224.
13. Cavicchi M., Bean P., Crenn P., Degott C. & Messing B. Prevalence of liver disease and contributing factors in patients receiving home parenteral nutrition for permanent intestinal failure // Ann Intern Med (2000) 132, 525-532.
14. Cetinkale O. & Yazici Z. Early postburn fatty acid profile in burn patients // Burns (1997) 23, 392-399.
15. Chambrier C., Guiraud M., Gibault J.P., Labrosse H. & Bouletreau P. Medium- and long-chain triacylglycerols in postoperative patients: structured lipids versus a physical mixture // Nutrition (1999) 15, 274-277.
16. Charcon Castro M.P., Jimenez Sesй B., Salvado Salvat J., Sabin Urquia P., Pascual Mostaza C. & Planas Vila M. Influence of two fatty emulsions with a different triglyceride composition on the lipid metabolism of the septicemic patient // Nutr Hosp (2000) 15, 13-17.
17. De Francesco A., Balzola F.A., Come A., Le Brun A., Evard D., Atlan P., Dutot G. & Balzola F. Long-term safety of home parenteral nutrition (HPN) with a new olive oil-based lipid emulsion (LE): a randomised, double-blind, comparative trial // Clinical Nutrition (1999) 18, Suppl. 1, 46.
18. Deitch E.A. Nutrition support of the burn patient // Nutrition in the Critically Ill Patient, pp. 735-750 [C.H. Lang, editor]. — Philadelphia: W.B. Saunders, 1995.
19. Driss F., Darcet P., Delhaye N. & Mendy F. Effect of eicosapentanoic acid on RBC filterability and fatty acid composition // Clin Hemorrheol (1988) 8, 679-685.
20. Drost A.C., Burleson D.G., Cioffi W.G. Jr, Jordan B.S., Mason A.D. Jr & Pruitt B.A. Jr. Plasma cytokines following thermal injury and their relationship with patient mortality, burn size, and time postburn // J Trauma (1993) 35, 335-339.
21. Endo S., Inada K., Yamada Y. et al. Plasma levels of interleukin-1 receptor antagonist (IL-1ra) and severity of illness in patients with burns // J Med (1996) 27, 57-71.
22. Eritsland J. Safety considerations of polyunsaturated fatty acids // Am J Clin Nutr (2000) 71, 197S-201S.
23. Freeman J., Goldmann D.A., Smith N.E., Sidebottom D.G., Epstein M.E. & Platt R. Association of intravenous lipid emulsion and coagulase-negative staphylococcal bacteremia in neonatal intensive care units // N Engl J Med (1990) 323, 301-308.
24. Friedman B. & Deppe S.A. Nutritional considerations in the severely burned patient // Nutritional Considerations in the Intensive Care Unit, pp. 245-258 [S.A. Shirota, R.G. Martindale and S.D. Scwaitzberg, editors]. — Silver Spring, CO: Kendall/Hunt Publishing Company & ASPEN, 2002.
25. Garcia-de-Lorenzo A. Metronidazole, cholestasis and total parenteral nutrition // Lancet (1983) 21, 1161.
26. Garcia-de-Lorenzo A. & Culebras J.M. Linoleic acid and the immune system. Controversies about lipid emulsions // Nutr Hosp. (1992) 7, 377-387.
27. Garnacho-Montero J., Ortiz-Leyba C., Garnacho-Montero M.C., Garcia-Garmendia J.L., Perez-Paredes C., Moyano-Del Estad M.R., Barrero-Almodovar A. & Jimenez-Jimenez F.J. Effects of three intravenous lipid emulsions on the survival and mononuclear phagocyte function of septic rats // Nutrition (2002) 18, 751-754.
28. Garrel D.R., Razi M., Lariviere F., Jobin N., Naman N., Emptoz-Bonneton A. & Pugeat M.M. Improved clinical status and length of care with low-fat nutrition support in burn patients // J Parenter Enter Nutr (1995) 19, 482-491.
29. German G., Barthold U., Lefering R., Raff T. & Hartmann B. The impact of risk factors and pre-existing conditions on the mortality of burn patients and the precision of predictive admission-scoring systems // Burns (1997) 23, 195-203.
30. Gobel Y., Koletzko B., Bohles H.J., Engelsberger I., Forget D., Le Brun A., Peters J. & Zimmermann A. Parenteral fat emulsions based on olive and soybean oils: a randomized clinical trial in preterm infants // J Pediatr Gastroenterol Nutr (2003) 37, 161-167.
31. Goulet O., De Potter S., Antebi H. et al. Long-term efficacy and safety of a new olive oil-based intravenous fat emulsion in paediatric patients: a double blind randomized study // Am J Clin Nutr (1999) 70, 338-345.
32. Granato D., Blum S., Rцssle C., Le Boucher J., Malnoe A. & Dutot G. Effects of parenteral lipid emulsions with different fatty acid composition on immune cell functions in vitro // J Parenter Enter Nutr (2000) 24, 113-118.
33. Guo Y., Dickerson C., Chrest F.J., Adler W.H., Munster A.M. & Winchurch R.A. Increased levels of circulating interleukin 6 in burn patients // Clin Immunol Immunopathol (1990) 54, 361-371.
34. Hageman J.R., McCulloch K., Gora P., Olsen E.K., Pachman L. & Hunt C.E. Intralipid alterations in pulmonary prostaglandin metabolism and gas exchange // Crit Care Med (1983) 11, 794-798.
35. Herndon D.N., Stein M.D., Rutan T.C., Abston S. & Linares H. Failure of TPN supplementation to improve liver function, immunity, and mortality in thermally injured patients // J Trauma (1987) 27, 195-204.
36. Herruzo-Cabrera R., Fernandez-Arjona M., Garcia-Torres V., Martinez-Ratero S., Lenguas-Portero F. & Rey-Calero J. Mortality evolution study of burn patients in a critical care burn unit between 1971 and 1991 // Burns (1995) 21, 106- 109.
37. Holman R.T. The ratio of trienoic:tetraenoic acids in the tissue lipids as a measure of essential fatty acid requirement // J Nutr (1960) 70, 405-410.
38. Karlstad M.D., DeMichele S.J., Leathem W.D. & Peterson M.B. Effect of intravenous lipid emulsions enriched with gamma-linolenic acid on plasma n-6 fatty acids and prostaglandin biosynthesis after burn and endotoxin injury in rats // Crit Care Med (1993) 21, 1740-1749.
39. Kinsella J.E., Lokesh B., Broughton S. & Whelan J. Dietary polyunsaturated fatty acids and eicosanoids: potential effects on the modulation of inflammatory and immune cells: an overview // Nutrition (1990) 6, 24-44.
40. Kono H., Fujii H., Asakawa M., Matsuda M., Maki A. & Matsumoto Y. Protective effects of medium-chain triglycerides on the liver and gut in rats administered endotoxin // Ann Surg (2003) 237, 246-255.
41. Kowal-Vern A., Walenga J.M., Hoppensteadt D., Sharp-Pucci M. & Gamelli R.L. Interleukin-2 and interleukin-6 in relation to burn wound size in the acute phase of thermal injury // J Am Coll Surg (1994) 178, 357-362.
42. McManus A.T., Mason A.D. Jr, McManus W.F. & Pruitt B.A. Jr Twenty-five year review of Pseudomonas aeruginosa bacteremia in a burn center // Eur J Clin Microbiol (1985) 4, 219-223.
43. Masini J.P., Fichelle A., Pescio M., Bйrйziat G., Desmonts J.M. & Lienhart A. Tolйrance clinique et biologique et effets sur les paramйtres lipidiques de ClinOleicw comparй а l’Intralipide® chez des patients de rйanimation chirurgicale // Nutr Clin Mйtabol (1996) 10, 21S-24S.
44. Montegut W.J. & Lowry S.F. Nutrition in burn patients // Semin Nephrol (1993) 13, 400-408.
45. Morlion B.J., Torwesten E., Lessire H., Sturm G., Peskar B.M., Furst P. & Puchstein C. The effect of parenteral fish oil on leukocyte membrane fatty acid composition and leukotriene-synthesizing capacity in patients with postoperative trauma // Metabolism (1996) 45, 1208-1213.
46. Moussa M., Le Boucher J., Garcia J., Tkaczuk J., Ragab J., Dutot G., Ohayon E., Ghisolfi J. & Thouvenot J.P. In vivo effects of olive oil-based lipid emulsion on lymphocyte activation in rats // Clin Nutr (2000) 19, 49-54.
47. Nordenstrom J., Jarstrand C. & Wirniek A. Decreased chemotactic and random migration of leukocytes during intralipid infusion // Am J Clin Nutr (1979) 32, 2416-2420.
48. Pakula R., Konikoff F.M., Moser A.M., Greif F., Tietz A., Gilat T. & Rubin M. The short term lipid infusion on plasma and hepatic bile lipids in humans // Gut (1999) 45, 453- 458.
49. Papini R.P., Wilson A.P., Steer J.A., Hill G., McGrouther D.A. & Parkhouse N. Plasma concentrations of tumour necrosis factor-alpha and interleukin-6 during burn wound surgery or dressing // Br J Plast Surg (1997) 50, 354-361.
50. Peck M.D. Interaction of lipids with immune function. I. Biochemical effects of dietary lipids on plasma membranes // J Nutr Biochem (1994) 5, 466-478.
51. Pelaez J., Garcia-de-Lorenzo A., Denia R., Martinez-Ratero S., Lopez J. & Caparros T. Nutritional support for the large burn patient // Nutr Hosp (1997) 12, 121-133.
52. Pratt V.C., Tredget E.E., Clandinin M.T. & Field C.J. Fatty acid content of plasma lipids and erythrocyte phospholipids are altered following burn injury // Lipids (2001) 36, 675-682.
53. Pratt V.C., Tredget E.E., Clandinin M.T. & Field C.J. Alterations in lymphocyte function and relation to phospholipid composition after burn injury in humans // Crit Care Med (2002) 30, 1753-1761.
54. Reimer T., Morlion B., Fьrst P, Le Brun A., Atlan P., Dutot G. & Puchstein C. Effects of an olive oil based intravenous lipid emulsion (ILE) on plasma and leukocyte membrane fatty acid (FA) composition and on clinical outcomes in postoperative patients // Clin Nutr (2001) 20, suppl. 40.
55. Rocca A.S., LaGreca J., Kalitsky J. & Brubaker P.L. Monounsaturated fatty acid diets improve glycemic tolerance through increased secretion of glucagon-like peptide-1 // Endocrinology (2001) 142, 1148-1155.
56. Rossle C., Breton I., Bereziat G. et al. Evolution of plasma phospholipid FA pattern in patients receiving postoperative TPN including soybean oil or olive oil-based lipid emulsions: a comparative multicenter study // Clin Nutr (1992) 11, suppl. 19.
57. Rubin M., Halpern Z., Charach G., Dvir A., Antebi E., Gilat T. & Lichtenberg D. Effect of lipid infusion on bile composition and lithogenicity in patients without cholesterol gallstones // Gut (1992) 33, 1400-1403.
58. Rubin M., Pakula R., Moser A., Halpern Z., Shimonov M. & Lichtenberg D. Does lipid infusion affect bile composition in humans? // Isr J Med Sci (1996) 32, 1308-1313.
59. Sadeghi S., Wallace F.A. & Calder P.C. Dietary lipids modify the cytokine response to bacterial lipopolysaccharide in mice // Immunology (1999) 96, 404-410.
60. Schwacha M.G. & Chaudry I.H. The cellular basis of post-burn immunosuppression: macrophages and mediators // Int J Mol Med (2002) 10, 239-243.
61. Seidner D.L., Mascioli E.A., Istfan N.W., Porter K.A., Selleck K., Blackburn G.L. & Bistrian B.R. (1989) Effects of long-chain triglyceride emulsions on reticuloendothelial system function in humans // J Parenter Enter Nutr 13, 614-619.
62. Sparkes B.G. Immunological responses to thermal injury // Burns (1997) 23, 106-113.
63. Spielmann D., Bracco U., Traitler H., Crozier G., Holman R., Ward M. & Cotter R. Alternative lipids to usual n-6 PUFAS: g-linolenic acid, a-linolenic acid, stearidonic acid, EPA, etc. // J Parenter Enter Nutr (1988) 12, 111S-123S.
64. Suissa S. & Shuster J.J. Exact unconditional sample sizes for the 2 by 2 binomial trial // J Roy Statist Soc (1985) A148, 317-327.
65. Thomas-Gibson S., Jawhari A.U., Atlan P., Le Brun A., Farthing A. & Forbes A. Safe and efficacious prologed use of an olive oil-based lipid emulsion (ClinOleic) in chronic intestinal failure // Clin Nutr (2004) 23, 697-703.
66. Tobiasen J., Hiebert J.M. & Edlich R.F. The abbreviated burn severity index // Ann Emerg Med (1982) 11, 260-262.
67. Ueyama M., Maruyama I., Osame M. & Sawada Y. Marked increase in plasma interleukin-6 in burn patients // J Lab Clin Med (1992) 120, 693-698.
68. Vahedi K., Bereziat G., Le Brun A., Perennec V., Evard D., Atlan P., Dutot G. & Messing B. A randomised, double-blind 3-month study in home parenteral nutrition (HPN) patients with olive or soy oil-based lipid emulsions (ILE): safety, nutritional status, plasma and cell-membrane fatty acid profiles // Clin Nutr (1999) 18, Suppl. 48.
69. Van den Berghe G., Wouters P., Weekers F., Verwaest C., Bruyninckx F., Schetz M., Vlasselaers D., Ferdinande P., Lauwers P. & Bouillon R. Intensive insulin therapy in critically ill patients // N Engl J Med (2001) 345, 1359-1367.
70. Waitzberg D.L., Bellinati Pires R., Salgado M.M., Hypolito I.P., Colleto G.M., Yagi O., Yamamuro E.M., Gama-Rodrigues J. & Pinotti H.W. Effect of total parenteral nutrition with different lipid emulsions on human monocyte and neutrophils functions // Nutrition (1997) 13, 128-132.
71. Wanten G.J.A., Roos D. & Naber A.H.J. Effects of structurally different lipid emulsions on human neutrophil migration // Clin Nutr (2000) 19, 327-331.
72. Warden G.D., Wilmore D.W., Rogers P.W., Mason A.D. & Pruitt B.A. Jr. Hypernatremic state in hypermetabolic burn patients // Arch Surg (1973) 106, 420-427.
73. Weissman C. Nutrition in the intensive care unit // Crit Care (1999) 3, 67R-75R.
74. Yamada Y., Endo S. & Inada K. Plasma cytokine levels in patients with severe burn injury with reference to the relationship between infection and prognosis // Burns (1996) 22, 587- 593.
75. Ythier-Moury P., Dutot G. & Melin C. Modifications of biliary secretion associated with parenteral nutrition in the rat: influence of fat emulsion composition // Clin Nutr (1990) 9, suppl. 26.
76. Zawacki B.E., Azen S.P., Imbus S.H. & Chang Y.T. Multifactorial probit analysis of mortality in burned patients // Ann Surg (1979) 189, 1-5.