Журнал «Медицина неотложных состояний» 7-8 (38-39) 2011
Вернуться к номеру
Опыт применения селеназы в комплексе интенсивной терапии при критических состояниях
Авторы: Усенко Л.В., Кобеляцкий Ю.Ю., Мосенцев Н.Ф., Йовенко И.А. Днепропетровская государственная медицинская академия Днепропетровская областная клиническая больница им. И.И. Мечникова
Рубрики: Семейная медицина/Терапия, Медицина неотложных состояний
Версия для печати
Проведено изучение эффективности и переносимости использования в/в введения 1000–2000 мкг селеназы в течение 7–10 дней в комплексе интенсивной терапии у 40 больных с тяжелым сепсисом и 30 больных с политравмой и тяжелой ЧМТ. Эффективность лечения оценивали по общепринятым шкалам (APACHE II, SOFA, CTCOFR, RLAS — при сепсисе и TS, ISS, GCS, RLAS, APACHE II — при травме), уровню летальности, потребности в ИВЛ и ее продолжительности, частоте инфекционных осложнений. Показано, что применение селеназы способствует более быстрому регрессу проявлений системной воспалительной реакции, разрешению органных дисфункций, уменьшению частоты инфекционных осложнений и снижению летальности при хорошей переносимости и безопасности ее применения.
Тяжелый сепсис, политравма, ЧМТ, интенсивная терапия, селеназа.
К настоящему времени показано, что ключевым звеном в патогенезе критических состояний инфекционного и неинфекционного генеза является синдром системного воспалительного ответа (ССВО) с риском развития полиорганной недостаточности (ПОН), что связано с оксидативным стрессом вследствие увеличения активных форм кислорода и снижения эндогенной антиоксидантной защиты [1, 2].
Как отмечает А.А. Богданов (2008), оксидативный стресс является конечным этапом повреждения клеток и нарушения функций органов, которые наблюдаются при разного рода критических состояниях, таких как сепсис, тяжелая травма, ишемия/реперфузия и другие.
Критические состояния с развитием ССВО и ПОН сопровождаются высокой летальностью. Это обусловило усиление в последние годы интереса к изучению роли нарушений баланса между системой пероксидации липидов и системой антиоксидантной защиты организма в генезе критических состояний и к поискам антиоксидантных средств для контроля и ограничения свободнорадикального окисления липидов, играющего универсальную роль в регуляции гомеостаза и причинно-следственных механизмах развития различных функциональных органно-системных расстройств.
Включение в комплекс интенсивной терапии критических состояний антиоксидантов рассматривается как одно из новых перспективных направлений в повышении качества лечения и снижении летальности у этой категории больных [3].
Из множества антиоксидантов доказанными положительными свойствами обладают препараты селена — селенит, селенат натрия, селенцистеин, селенметионин, что служит основанием для их дополнительного введения значительному числу больных в отделениях интенсивной терапии.
Селен — это незаменимый микроэлемент, являющийся кофактором в нескольких ферментах человеческого организма, а также катализатором синтеза гормонов [4, 5].
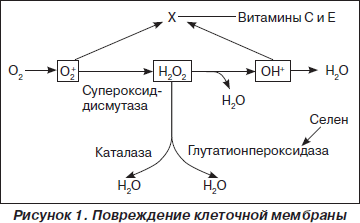
В механизмах антиоксидантной защиты ключевую роль играет система глутатиона, продуцирующая эндогенные антиоксидантные ферменты, мощным кофактором которых является селен: глутатионпероксидаза, фосфолипид-глутатионпероксидаза, глицинредуктаза, другие оксиредуктазы, а также основные антиоксидантные соединения некоторых трансфераз [6].
Среди вышеназванных ферментов важнейшим звеном антиоксидантной системы является глутатионпероксидаза [7]. Последняя предохраняет клетки от токсического воздействия перекисных радикалов и разрушает как перекись водорода, так и перекиси липидов. Она контролирует окислительно-восстановительные процессы на уровне клетки.
Уровень селена в крови 89–113 мкг/л, пороговый уровень — 60 мкг/л, суточная потребность — 50–200 мкг/л.
Его уровень снижен при депрессии, эмоциональном истощении, ассоциируется с ускоренным снижением когнитивных функций у пожилых, при его дефиците замедляется скорость восстановления некоторых нейромедиаторов [4].
Фармакодинамическим обоснованием для его использования в комплексе интенсивной терапии при критических состояниях служат его следующие механизмы действия:
— подавление эндотелиальной адгезии и защита эндотелия от повреждения кислородными радикалами;
— снижение продукции провоспалительных цитокинов;
— подавление гиперактивности ядерного фактора NF-kB;
— уменьшение активности системы комплемента;
— поддержание утилизации пероксидов;
— стабилизация глюкокортикоидных рецепторов;
— стимуляция инсулинового сигнального каскада, за счет инсулиноподобного эффекта улучшающая контроль глюкозы.
Вышеперечисленное способствует предупреждению микроциркуляторно-митохондриальной дисфункции как универсального звена полиорганной недостаточности.
При критических состояниях отмечается возрастающее потребление селена и недостаточное его поступление в организм извне, что приводит к дефициту селена в организме и делает его беззащитным при воздействии свободных радикалов кислорода и каскада реакций, вызываемых их активацией [8].
Установлена зависимость между низкой концентрацией селена в сыворотке крови и тяжестью состояния больных, уровнем летальности, что послужило основанием для раннего включения препаратов селена в схему интенсивной терапии при критических состояниях [7, 8].
Ряд авторов считает, что включение в комплекс интенсивной терапии препаратов селена открывает новые горизонты в лечении критических состояний.
С 2009 г. селен включен в рекомендации ESPEN как фармакологический модуль (Grade C), с 2010 г. — в национальное руководство по лечению сепсиса в Германии (Grade C) [9].
Среди больных, находящихся в критическом состоянии, особого внимания заслуживают больные с сепсисом и политравмой.
Нами обследовано 70 пациентов — 40 больных с сепсисом и септическим шоком и 30 больных с политравмой и ЧМТ — с целью определения эффективности и безопасности применения у них препарата селеназа в комплексе интенсивной терапии.
Сепсис среди критических состояний остается актуальной проблемой медицины вследствие неуклонного роста числа случаев этого заболевания, высокой летальности и значительных экономических затрат на его лечение.
Ежегодно с 1979 г. по 2000 г. количество случаев сепсиса повышалось на 8,7 % [10].
Сепсис-ассоциированная летальность с 1999 г. по 2005 г. ежегодно возрастала на 0,67 %, в то время как связанная с возрастом снижалась на 0,18 % [11].
Затраты на лечение больных с сепсисом только в США ежегодно составляют 16,7 млрд долларов [12].
Проведенные мультицентровые исследования показали, что снижение уровня селена в сыворотке крови ниже 0,6 мкмоль/л у больных с сепсисом ассоциируется с риском развития госпитальной пневмонии, органной недостаточности и летального исхода [13, 14].
В то же время отмечено, что включение в комплекс интенсивной терапии больным с сепсисом препаратов селена сопровождается снижением летальности на 14,3 % к 28-му дню заболевания [15, 16].
В отделении интенсивной терапии сепсиса нами проведено открытое сравнительное исследование, в которое было включено 40 больных с сепсисом из категории высокого риска летальности по шкале MEDS с прогнозируемым уровнем летальности 25,3 %.
В зависимости от назначенной терапии больные были разделены на 2 подгруппы по 20 человек, 1-я из которых получала стандартную терапию согласно международным рекомендациям, больным 2-й подгруппы дополнительно назначалась селеназа в дозе 1000 мкг в сутки внутривенно в течение 10 дней.
Эффективность лечения оценивалась по динамике первичных точек:
— по шкалам APACHE II и SOFA;
— признакам явного или скрытого шока по шкале P.E. Spronk;
— композитному времени до разрешения органных дисфункций (CTCOFR);
— частоте гипергликемии выше 8,3 ммоль/л;
— достижению VIII уровня качества жизни по шкале Rancho Los Amigos (RLAS) на 14-й день.
А также по конечным точкам:
— летальности;
— наличии персистирующих органных дисфункций до 28-го дня заболевания.
Проведена статистическая обработка полученных данных.
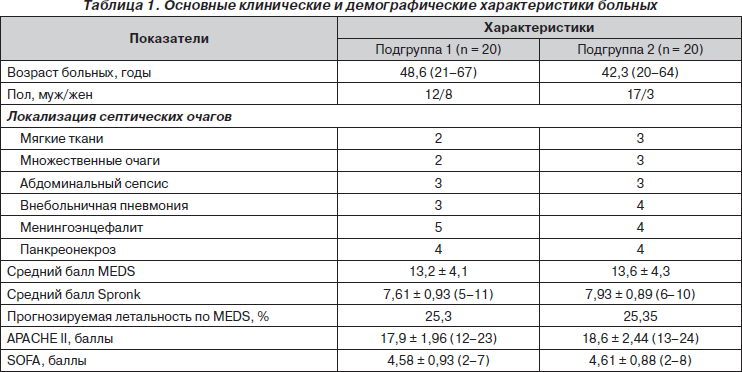
Основные клинические и демографические характеристики больных представлены в табл. 1.
По основным демографическим и клиническим характеристикам, как видно, на начальном этапе исследования различия между группами сравнения не наблюдалось. Исходная тяжесть состояния больных по шкалам APACHE II и SOFA ассоциировалась с прогнозом летального исхода от 24 до 30 %, у всех больных наблюдались проявления явного или скрытого септического шока.
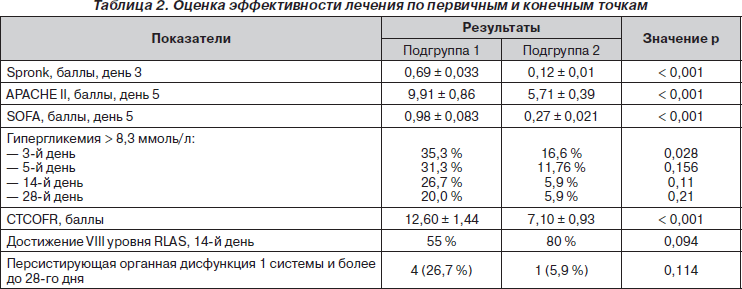
Оценка эффективности лечения по первичным и конечным точкам представлена в табл. 2.
К 3-му дню исследования число баллов шкалы P.E. Spronk в контрольной группе составило 0,69 ± 0,33, в то время как в основной группе отмечалось его достоверное снижение до 0,12 ± 0,01 (р < 0,001).
До 5-го дня лечения по протоколу достоверные различия наблюдались при интегральной оценке состояния больных по шкале APACHE II. В контрольной группе средний балл шкалы составлял 9,91 ± 0,86, тогда как в группе с дополнительным введением селеназы — 5,71 ± 0,39 (р < 0,001).
Достоверные различия выявлены при оценке проявлений полиорганной дисфункции. До 5-го дня исследования в контрольной группе число баллов шкалы SOFA составляло 0,980 ± 0,083 при снижении его в группе селеназы до 0,270 ± 0,021 (на 72,4 %, р < 0,001), а композитное время до разрешения органных дисфункций CTCOFR в контрольной группе на 5,5 балла превышало аналогичный показатель в группе селеназы (р < 0,001).
Отчетливое влияние селеназы на гомеостаз глюкозы проявлялось снижением случаев гипергликемии выше 8,3 ммоль/л на 18,7 % на 3-й день исследования (р = 0,028), на 19,5 % — на 5-й день (р = 0,156), на 20,8 % — на 14-й день (р = 0,11) и на 14,1 % — на 28-й день (р = 0,21).
Влияние селеназы на восстановление качества жизни проявлялось увеличением числа случаев достижения VIII уровня шкалы RLAS до 14-го дня на 25 % (р = 0,094).
Снижение летальности в исследуемой группе по сравнению с контрольной на 10 % и на 10,35 % по сравнению с прогнозируемой по шкале MEDS (р > 0,1) сочеталось со снижением количества случаев персистирующей органной дисфункции одной или более систем до 28-го дня болезни на 20,8 % (р = 0,114).
Таким образом, применение селеназы у больных с тяжелым сепсисом и септическим шоком (APACHE II > 15 баллов и SOFA > 4 баллов) способствует более быстрому разрешению органных дисфункций с сокращением композитного времени по сравнению с контрольной группой, снижением частоты персистирующей органной дисфункции до 28-го дня болезни и снижением летальности по сравнению как с прогнозируемой, так и с контрольной группой при хорошей переносимости и безопасности.
Для модификации независимых факторов летальности при сепсисе, наблюдаемых у 95 % пациентов (запоздалая хирургическая санация очагов, неудачная антибиотикотерапия, запоздалая ранняя целенаправленная терапия, респираторная, нутритивная поддержка), приоритетными должны быть соответствующие мероприятия, эффективность которых может возрастать после назначения селеназы.
Назначение последней в комплексе интенсивной терапии особенно целесообразно у больных, поступающих после 6 часов от начала заболевания (запоздалое обращение), имеющих высокий риск развития органной дисфункции после госпитализации.
Не менее актуальной для Украины является проблема лечения больных с политравмой и ЧМТ.
В Украине ежегодно травмы разной степени тяжести получают 4,5 млн человек. В последнее десятилетие смертность от травматизма в нашей стране остается высокой и составляет 135,5–148,5 на 100 тысяч населения.
Летальность при тяжелой политравме в Украине составляет от 10 до 80 % [17], при этом 39 % пострадавших умирают в стационарах, что значительно выше уровня в развитых странах [18].
Критические состояния у больных с травмой, так же как и при сепсисе, сопровождаются повышенной продукцией свободных радикалов пропорционально тяжести травмы. У больных развиваются сильный оксидативный стресс, интенсивная воспалительная реакция, длительный гиперметаболизм.
Вместе с тем лишь в единичных работах последних лет появились сообщения об использовании в комплексе интенсивной терапии у этих больных препаратов селена [2, 19, 20].
Нами в отделении интенсивной терапии политравмы обследовано 30 больных с политравмой и ЧМТ. В зависимости от назначенной терапии больные были разделены на 2 подгруппы по 15 человек, 1-я из которых получала терапию согласно стандартному протоколу лечения. Больным 2-й подгруппы в дополнение к ней назначалась селеназа в дозе 1000 мкг внутривенно 2 раза в сутки в течение 7–10 дней.
Эффективность лечения оценивалась на основании:
— определения тяжести состояния по шкалам TS, ISS, GCS, RLAS, APACHE II;
— учета потребности в ИВЛ и ее продолжительности;
— частоты инфекционных осложнений;
— уровня летальности до 28-го дня.
Сравнительная характеристика исследованных групп представлена в табл. 3.
По демографическим данным, клиническим характеристикам, степени тяжести исходного состояния при оценке по общепринятым шкалам травмы и неврологического дефицита, а также по потребности в проведении ИВЛ группы больных исходно были идентичны.
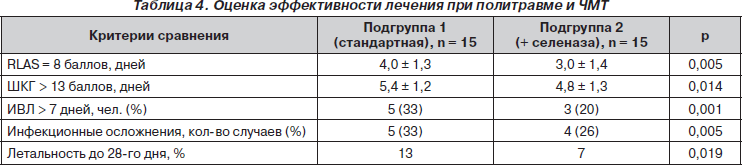
Данные об оценке эффективности лечения в исследуемых группах больных представлены в табл. 4.
Выявлено положительное влияние селеназы на восстановление качества жизни больных, что проявлялось укорочением времени достижения VIII уровня шкалы RLAS на 25 % (р = 0,005), уровня сознания по шкале ком Глазго > 13 баллов на 11 % (р = 0,014).
Количество больных, нуждающихся в ИВЛ длительностью более 7 дней, в подгруппе с назначением селеназы было меньше на 13 % (р = 0,001), что могло быть связано как с более быстрым улучшением неврологического статуса, так и с меньшей на 7 % частотой возникновения инфекционных осложнений (р = 0,005).
В исследуемой группе отмечено снижение летальности до 28-го дня наблюдения на 6 % по сравнению с контрольной группой (р = 0,019).
Осложнений и побочных явлений после применения селеназы у больных обеих групп не наблюдалось.
Выводы
1. Включение селеназы в комплекс интенсивной терапии больных с сепсисом и септическим шоком, сочетанной травмой и ЧМТ способствует ускорению регресса системной воспалительной реакции, более быстрому разрешению органных дисфункций, уменьшению частоты инфекционных осложнений и снижению летальности.
2. Включение селеназы в протокол лечения тяжелого сепсиса, политравмы и ЧМТ в высоких дозах (1000–2000 мкг/сутки) на протяжении 7–10 дней характеризуется хорошей переносимостью и безопасностью и может быть рекомендовано для широкого использования в комплексе интенсивной терапии исследованных нами групп больных отделений интенсивной терапии.
1. Гусев Е.Ю., Юрченко Л.Н., Зотова Н.В., Копалова Ю.А. Критические состояния: качественный уровень системы воспалительной реакции // Интенсивная терапия. — 2006.
2. Berger M.M. Antioxydant micronutrients in major trauma and burns: evidence and practice // Nutr. Clin. Pract. — 2006. — Vol. 21, № 5. — P. 438-449.
3. Громова О.А., Гоголева Н.В. Селен — впечатляющие итоги и перспективы применения // Мед. неотл. состояний. — 2010. — № 6 (31). — С. 124-128.
4. Rayman M.P. The importance of selenium to human health // Lancet. — 2000. — Vol. 356. — Р. 233-241.
5. Попов Т.В., Глушко А.Р., Яковлева И.И., Гельфанд Б.Р. Опыт использования Селеназы в комплексе интенсивной терапии больных деструктивным панкреатитом // Инфекции в хирургии. — 2008. — Т. 6, № 1. — С. 54-56.
6. Зайчик А.Ш., Чурилов Л.П. Общая патофизиология. — СПб.: Элби, 2001.
7. Geoghegan M., McAnley D., Eaton S., Powell-Tuck J. Selenium in critical illness: сurrent opinion // Critical Care. — 2006. — Vol. 12, № 2. — Р. 136-141.
8. Bulger E.M., Meier R.V. Antioxydant in criticall illness // Arch. Surg. — 2001. — № 136. — P. 1201-1207.
9. Bozzetti F., Forbes A. The ESPEN clinical practice guidelines on parenteral nutrition: present status and perspectives for future research // Clin. Nutr. — 2009. — № 28. — Р. 359-364.
10. Chanem-Zoubi N.O., Vardi M., Laor A. et al. Assessment of disease-severity scoring systems for patients with sepsis in general internal medicine departaments // Critical. Care. — 2011. — № 15. — Р. 95.
11. Melamet A., Sorvillo F.J. The burden of sepsis-associated mortality in the United States from 1999 to 2005: an analysis of multicause — of death data // Critical. Care. — 2009. — № 13. — Р. 28.
12. Dellinger R.P., Levy M.M., Collet J.M. et al. Surviving sepsis campaigning International Guidelines for management of severe sepsis and septic shock // Intensive Care Medicine. — 2008. — № 34. — Р. 17-60.
13. Мухачева С.Ю., Руднов В.А., Галян С.Л., Кадочникова Т.Ю. Эффективность селена и альфа-токоферола в терапии больных с абдоминальным сепсисом // Инфекции в хирургии. — 2007. — Т. 5, № 1.
14. Manzanares W., Biestro A., Galusso F. et al. Serum selenium and glutationeperoxidase-3 activity biomarkers of systemic inflammation in the critically ill // Intensive Care Medicine. — 2009. — № 35. — Р. 882-889.
15. Angstwurm M.W., Engelmann L., Zimmermann T. et al. Selenium in Intensive Care (SIC): results of a prospective randomized, placebo-controlled, multiple-center study in patients with severe systemic inflammatory response syndrome, sepsis, and septic shock // Critical. Care Medicine. — 2007. — Vol. 35, № 1. — Р. 118-126.
16. Manzanares W., Hardy G. Selenium supplementation in critically ill patients: pharmacological issues and current evidence // Nutr. Hosp. — 2009. — Vol. 24, № 4.
17. Гур’єв С.О., Шишук В.Д. Особливості полісистемних пошкоджень, що виникають внаслідок дорожно-транспортних пригод // Зб. наук. праць Укр. військ. мед. академії. — Вип. 17. — К., 2006. — С. 21-27.
18. Шлапак І.П., Пилипенко М.М., Бурчинський В.Г. Структура смертності від ЧМТ в Україні: епідеміологічне дослідження // Зб. наук. праць Укр. військ. мед. академії. — Вип. 17. — К., 2006. — С. 251-254.
19. Сollier B.R., Giladi A., Dosset L.A. Effects of trace element supplementation on the inflammatory response in a rabbit model of major trauma // J. of Trace Elements in Medicine and Biology. — 2010. — Vol. 24, № 1. — P. 36-41.
20. Giladi A.M., Dosset L.A., Fleming S.B. et al. High-dose antioxydant administration is associated with a reduction in post-injury complications in critically ill trauma patients // Injury int. J. Care Injured. — 2011. — № 42. — Р. 78-82.