Международный неврологический журнал 4(4) 2005
Вернуться к номеру
Течение и рациональная терапия эпилепсии /Natural history and rational treatment of epilepsy/
Авторы: М.Дж. БРОДИ, Великобритания
Рубрики: Неврология
Разделы: Справочник специалиста
Версия для печати
Хотя в современных исследованиях было показано, что у большинства больных с впервые диагностированной эпилепсией достигается длительная ремиссия, приступы остаются резистентными к лечению у существенной части популяции — вплоть до 40%. Было постулировано, что фармакорезистентность можно заподозрить в ситуации, когда 2 адекватных, хорошо переносимых противоэпилептических препарата (ПЭП) или один в качестве монотерапии и одна комбинация препаратов не дали результата из-за недостаточной эффективности. К плохим прогностическим факторам в плане развития фармакорезистентности относятся: низкий ответ на первый ПЭП, специфические синдромы, симптоматическая этиология, семейный анамнез, сопутствующие психические заболевания, высокая частота приступов. Эти наблюдения предполагают, что прогноз часто может быть определен на ранних этапах заболевания. Мы предлагаем способ ведения пациентов с эпилепсией с целью максимального увеличения шансов успешной лекарственной терапии, включая раннее использование «рациональной политерапии» у больных, не отвечающих на монотерапию, и выявления пациентов, подходящих для оперативного вмешательства, особенно с мезиальной височной эпилепсией. Правильный подход к каждому эпилептическому синдрому увеличивает вероятность полного контроля над приступами и поможет большему числу людей вести полноценную жизнь.
Вступление
Популяционные исследования, проведенные в развитых странах, предполагают, что у от 40 до 70 человек на 100 000 населения ежегодно выявляется эпилепсия [1]. Rochester Epidemiology Project, одна из самых больших и самых значительных из подобных баз данных, выявил ежегодную заболеваемость 52,3 человека на 100 000 населения [2]. Большинство пациентов с впервые выявленной эпилепсией в развитом мире начинают лечение с противоэпилептических препаратов (ПЭП). Хотя у многих больных припадки будут отсутствовать на фоне первой или второй подобранной терапии, часто комбинация ПЭП назначается тем пациентам, у которых монотерапия неэффективна. Когда эпилепсия остается неконтролируемой, она называется рефрактерной, или фармакорезистентной. Некоторым из этих пациентов будет предложено хирургическое лечение или стимуляция блуждающего нерва. У детей можно воспользоваться кетогенной диетой.
Большая проблема состоит в недостаточном понимании и определении фармакорезистентности или медикаментозной рефрактерности. До недавнего времени врачи имели относительно ограниченные терапевтические возможности для лечения эпилепсии. После лицензирования новых 9 ПЭП за последние 10 лет выбор существенно расширился и число возможных комбинаций сейчас почти безгранично. Остается много вопросов, требующих ответов. Сколько попыток применения одного ПЭП должно быть предпринято, прежде чем пациента перевести на два препарата? Сколько ПЭП, один или в комбинации (и в скольких комбинациях), должны быть неэффективны, прежде чем заболевание можно будет расценивать как медикаментозно-рефрактерное и будет необходима операция? На каком этапе эпилепсия становится фармакорезистентной к лечению ПЭП? Существуют ли клинические характеристики, которые позволяют предсказывать последующую рефрактерность? Ответы на эти вопросы зависят от понимания различных аспектов течения эпилепсии.
Прогноз лечения эпилепсии
До недавнего времени прогноз при эпилепсии традиционно рассматривался с пессимизмом. W.R. Cowers [3] допустил, что «спонтанное прекращение приступов — событие слишком редкое, чтобы его предсказывать в каждом конкретном случае». Несмотря на пользу эффективной фармакотерапии, появившейся после синтеза фенобарбитала в 1911 г., мрачный взгляд Говерса продолжает отражаться в поколениях. Кстати, в исследовании 1968 г. Родин пришел к выводу, что только 30% пациентов с эпилепсией когда-либо выходили в 2-годичную ремиссию [4]. Эти ранние исследования, однако, были внутрибольничными и ретроспективными. Наоборот, результаты недавних проспективных длительных популяционных исследований указывают на более благоприятную картину и улучшают наше понимание прогноза лечения эпилепсии.
Первые крупные серии исследований, которые обеспечивают более точную и положительную оценку естественной истории лечения эпилепсии были проведены в Рочестере, штат Миннесота. Результаты в отношении заболеваемости, распространенности и случаев приступов и эпилепсии первично были опубликованы в сериях статей за 1935-1967 [6], 1940-1980 [7], 1935-1984 [8], 1980-1984 [2] и в резюмирующих статьях за 50-летний период [5, 9]. Результаты ремиссии и ранние прогностические факторы были рассмотрены в двух работах [10, 11]. В первичном анализе вероятность пребывания в ремиссии в течение 5 лет при 20-летнем анамнезе после диагностики (т.е. терминальная ремиссия) эпилепсии составила 70% [10]. Затем эти данные были исправлены на 75% [11]. Предикторами лучшего исхода являлись: отсутствие на ранних этапах жизни мозговых травм, генерализованной эпилептиформной активности на ЭЭГ, генерализованных тонико-клонических судорог. Прогностическая значимость этих факторов, однако, была слабая [11].
Исследование NGPSE (The National General Practice Study of Epilepsy), проведенное в Англии, — самое большое проспективное популяционное исследование прогноза эпилепсии [12]. Пациенты с подтвержденной или подозреваемой впервые выявленной эпилепсией были отобраны из 275 общих клиник в Англии за период с 1984 по 1987 гг. При среднем сроке наблюдения в течение 7,1 года, среди 564 пациентов с «определенной» эпилепсией, шанс достижения 5-летней ремиссии после 9 лет после установки диагноза равнялся 68%, и около 54% пациентов оставались в терминальной ремиссии [13]. Анализ потенциальных прогностических факторов показал, что только количество припадков в первые 6 месяцев после начала заболевания предсказывает вероятность ремиссии [14]. Другие современные крупные исследования иллюстрируют также, что у пациентов с впервые выявленным заболеванием, наблюдаемых в течение длительного периода, уровень ремиссии составляет около 60-80% и показывает, что большинство пациентов с эпилепсией имеют относительно благоприятный прогноз [11, 13, 15-17].
Исход по отношению к лечению
Хотя эти исследования и обеспечивали более точную оценку вероятности продолжительной ремиссии по отношению к периоду после установки диагноза, в анализе прогностических факторов часто не учитывалась тактика лечения. Не исследовалось никаких специфических взаимоотношений между исходом заболевания и курсом ПЭП-терапии. Огромное количество пациентов, по крайней мере в развитых странах, сразу после установления диагноза получают лекарственную терапию. С практической точки зрения, было бы полезно оценить вероятность успеха на фоне первого любого ПЭП, так же как на фоне других режимов терапии. В случаях, когда первый ПЭП не способен купировать приступы, как это часто случается, имеется недостаточно данных о пациентах, имеющих ответ на последующую монотерапию или комбинацию препаратов, а также есть ли какая-то разница эффективности между этими двумя стратегиями лечения. Отсутствие серьезных доказательств прогресса в ответ на лечение определяет отсутствие единства мнений в определении понятия рефрактерной эпилепсии [18-19] и препятствует развитию стратегического подхода к возможностям лечения.
Исследования в Глазго
Изменение течения эпилепсии в ответ на лечение специфически изучалось в серии продолжительных исследований, проведенных в Глазго с 1982 г. В одном исследовании 525 подросткам и взрослым пациентам был поставлен диагноз эпилепсии, начинающейся с ПЭП-терапии, и данных больных впоследствии наблюдали до 16 лет (в среднем 5 лет) [20]. Среди 470 пациентов, которые никогда раньше не получали лечение ПЭП, 64% вошли в ремиссию, по крайней мере, на 1 год. У 47% пациентов прекратились приступы на первом препарате, у 13% — на втором, но только у 4% на третьем или на комбинации двух препаратов. У 35% пациентов (7% всей популяции), которые имели ответ на первую или вторую монотерапию, после отмены лечения приступы не возобновились. Из тех больных, у кого приступы контролировались первым препаратом, более 90% достигли этого на малых или умеренных дозах (суточные дозы — 800 мг карбамазепина или меньше, 1500 мг вальпроата натрия или меньше, 300 мг ламотриджина или менее) [21].
Ответ на первый ПЭП был наиболее сильным предиктором прогноза [20]. Среди 248 пациентов, у которых лечение первым препаратом было безуспешным, только 79 (32%) в последующем освободились от приступов. Действительно, только у 11% из 113 пациентов, у которых первый препарат не работал из-за недостаточности эффективности, позже отмечался полный контроль над приступами. Предсказуемость «неудачи первого использования ПЭП» для будущей рефрактерности также была показана в ретроспективном исследовании детей с височной эпилепсией [22].
В недавнем усовершенствованном анализе базы данных в Глазго, включающей 780 пациентов, показано, что с впервые выявленной эпилепсией 59% больных достигли длительной ремиссии, у 6% больных 1 год прошел без припадков перед рецидивом и у 35% так и не удалось добиться адекватного контроля над припадками [23]. Уровень рецидива зависел от времени: у 9% пациентов, принимавших ПЭП до 1995 г., в последующем развилась рефрактерная эпилепсия после начального хорошего ответа. Интересно, что 31% пациентов никогда больше не имели ни одного приступа после первого же приема их первого ПЭП [24]. Тяжелая ЧМТ, фебрильные судороги, семейный анамнез эпилепсии, психические заболевания, более молодой возраст начала заболевания и большое количество приступов до начала лечения были связаны с худшим исходом. У пациентов с идиопатической эпилепсией (66% ремиссии) исходы были лучше, чем при криптогенной (57% ремиссии) или симптоматической (56% ремиссии) эпилепсии. Меньшие когорты пациентов с корковой дисплазией (60% ремиссии), атрофией гиппокампа (50% ремиссии) и первичной опухолью мозга (57% ремиссии) не имели существенной разницы по сравнению с другими случаями симптоматической или криптогенной эпилепсии. Большое количество (92%) пациентов вошло в ремиссию в течение 3 лет после начала лечения. Большинство больных имели положительный ответ на первый или второй ПЭП. Только 7% пациентов, которым было недостаточно двух хорошо сочетающихся препаратов, в последующем достигли ремиссии, а для тех, кому было недостаточно трех, этот показатель достигал только 3%.
Медикаментозная рефрактерность — рабочее определение
Наблюдения из этих исследований подтверждают гипотезу, что большинство пациентов с впервые выявленной эпилепсией включают 2 отдельные популяции, которые могут быть достаточно рано выявлены в курсе лечения [25]. У 60% пациентов будет хороший прогноз. У них не будет приступов на низких или умеренных дозах ПЭП первого или второго выбора в монотерапии без развития резистентных побочных эффектов. У некоторых из этих пациентов лечение может быть отменено без рецидива приступов. Около 5% будут иметь ответ на лечение, и затем припадки никогда не возобновятся и будет достигнут оптимальный контроль за ними. Остальные 35% больных имеют плохо контролируемые приступы с самого дебюта эпилепсии. Предикторы плохого прогноза включали специфические синдромы, симптоматическую этиологию, высокое первичное число и частоту приступов, наличие психических заболеваний и семейный анамнез эпилепсии [14, 18, 20, 23, 26-27].
Данные из исследований в Глазго поддерживают рабочее определение рефрактерной эпилепсии как безуспешное использование 2 подходящих ПЭП или одной монотерапии и одной комбинации препаратов из-за недостаточной эффективности и неплохой переносимости, которое должно провоцировать дальнейшие попытки использования препаратов. Данных пациентов можно отнести к потенциально хирургически курабельным, если они имеют хирургически излечимый синдром, прототипом которого является мезиальная височная эпилепсия [28]. Подобные рабочие определения имеют значение также для отбора пациентов для вагусной стимуляции и попыток использования экспериментальных препаратов. Определение медикаментозной рефрактерности как функции «числа безуспешных ПЭП» — более существенный критерий, чем «длительность заболевания», которая более необоснованна и вариабельна. Данный подход обеспечивает рациональность для ранних хирургических вмешательств у соответствующих пациентов [29].
Фармакорезистентная эпилепсия — de novo versus progressive
Одна из возможностей ранней идентификации пациентов с резистентной эпилепсией состоит в том, что 2 лекарственные схемы были безуспешны из-за недостаточной эффективности за короткий период времени после назначения лечения. Это определяет то, переходит ли пациент из одной прогностической группы в другую. Подобные исходы были проспективно изучены Бергом у 613 детей с впервые выявленными различными эпилептическими синдромами [30]. При двухгодичном наблюдении 595 пациентов у 53% отмечалась ремиссия, по крайней мере, в течение 1 года (хороший исход), 8% были определены как «резистентные / плохой исход» (неудачное применение двух или более ПЭП, 1 или более приступ ежемесячно в течение 18 месяцев и более), тогда как остальные исходы считались неопределенными. Когда 390 пациентов были осмотрены на 4-м году, хороший и плохой исходы имели место более чем в 80% случаев. 8% пациентов из неопределенной группы стали резистентными. При отдельном анализе было обнаружено, что среди 442 детей, вошедших в двугодичную ремиссию, 107 (74%) рецидивировали и только у 31 (7%) рецидив произошел спонтанно на фоне стабильного приема ПЭП [31].
Это наблюдение демонстрирует, что прогноз эпилепсии может быть определен у большинства пациентов на ранних этапах заболевания. До резистентности «дорастает» только небольшая часть пациентов. Однако течение индивидуальных эпилептических типов / синдромов значительно вариабельно. Ярким примером является мезиальная височная эпилепсия, связанная со склерозом гиппокампа, по отношению к которой накапливаются доказательства, предполагающие прогрессивное течение у некоторых пациентов [32-34], хотя и не у всех [24, 35].
Недавно было обследовано 242 пациента (старше 12 лет), которые прошли резективную операцию по поводу медикаментозно-резистентной эпилепсии (у 88% проведена передняя височная лобэктомия), у 26% из них имел место период, по крайней мере, 1 года ремиссии [36]. Исследователи определили медикаментозную рефрактерность как неудачное использование двух ПЭП первого ряда, средний период времени лечения при этом составил 9,1 года. В наших собственных исследованиях только 5% из 780 пациентов с впервые выявленной эпилепсией рецидивировали после начального хорошего ответа [23]. Среднее время до рецидива составило 25 месяцев. Существует возможность, что приступы сами по себе могут вызывать некоторые нейропластические изменения, включая потерю клеток [27-38]. Это может приводить к когнитивным нарушениям и психосоциальной дисфункции [39].
Стратегия лечения
Гипотеза, что фармакорезистентность может быть, по крайней мере, у некоторых пациентов, de novo, не должна подразумевать нигилистическое отношение к лечению ПЭП. Также стратегический подход должен быть адаптирован для максимальной вероятности ремиссии на фоне лекарственного лечения у пациентов с «мягким» течением. Должна быть уверенность, что ПЭП адекватны и эффективны, прежде чем расценить их как «неуспешные» у пациентов с «тяжело контролируемой эпилепсией», так чтобы более радикальные методы лечения могли бы быть предложены без ненужной задержки [29].
Монотерапия
Так как публикации серий открытых исследований 70-х гг. показали, что многие пациенты испытывают меньше побочных эффектов и даже улучшается контроль над приступами после перевода на монотерапию ПЭП [40-41], монотерапия стала «золотым стандартом» лечения эпилепсии. Ситуация усложнилась после появления 9 новых ПЭП. Так как шанс ремиссии при впервые выявленной эпилепсии для таких пациентов наиболее высок на первом ПЭП, существенное внимание нужно обратить на оптимальный выбор первого препарата. Эффективность — это функция действенности и переносимости [42]. Определение наиболее подходящего лечения требует знаний характеристик эпилепсии, пациента и доступных ПЭП [43].
Профиль активности против различных типов приступов различен среди ПЭП (табл. 1). Было обнаружено, что ряд эпилептических синдромов особенно чувствителен к определенным ПЭП. Ювенильная миоклоническая эпилепсия, например, хорошо отвечает на вальпроат натрия (ВПА), тогда как вигабатрин (ВГБ) рассматривается многими педиатрами как препарат выбора при детских спазмах [44]. Поэтому очень важно точно классифицировать тип приступа и эпилептический синдром, основываясь на клиническом анамнезе, физикальном осмотре, лабораторных данных, включая ЭЭГ и адекватный метод нейровизуализации [43].
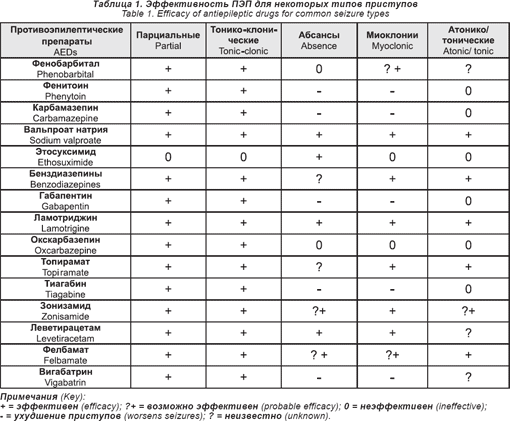
Существующие ПЭП — фенобарбитал (ФБ), примидон (ПРМ), фенитоин (ФТ), карбамазепин (КБЗ) и вальпроат натрия (ВПА) были сравнены в нескольких рандомизированных контролируемых исследованиях (РКИ) у пациентов с парциальными и генерализованными тонико-клоническими приступами (ГТКП), как наиболее частыми типами приступов. Обнаружение общей разницы в эффективности оставалось иллюзорным [45-48], с возможным исключением меньшей пользы КБЗ над ВПА для парциальных приступов только во время первых приступов [46]. Хотя ФБ показал более высокий уровень отмены его по сравнению с ФТ, его нейротоксичность может быть меньшей, как это было показано в некоторых открытых исследованиях [45].
Ни один из новых ПЭП не показал наивысшую эффективность при сравнении с известными агентами лечения парциальных приступов и ГТКП [49]. Действительно, было выявлено, что ВГБ реже приводит к ремиссии, чем КБЗ у пациентов с впервые выявленной ЛОЭ [50]. Также были продемонстрированы доказательства лучшей переносимости, особенно меньшей выраженности побочных эффектов, обусловленных нейротоксичностью [51]. Таким образом, ламотриджин (ЛТД) и окскарбазепин (ОКЗ) показали лучшую эффективность, чем КБЗ [52-53] и ФТ [54] соответственно.
Относительно небольшой охват и короткая продолжительность РКИ не позволяют адекватно оценить негативные аспекты ПЭП, особенно идиосинкратические реакции, нежелательные взаимодействия препаратов, хронические побочные эффекты и тератогенность. Эти исследования должны быть дополнены длительными популяционными данными, которые лучше отражают ежедневную клиническую практику [42]. Так как приступы у большинства пациентов с впервые выявленной эпилепсией будут отвечать на монотерапию при средней дозировке [21], часто необходимо пожизненное лечение, длительная безопасность особенно необходима, а потенциально угрожающие жизни идиосинкратические реакции [55] или серьезные хронические побочные эффекты должны избегаться.
Политерапия
Результаты исследований исходов в Глазго предполагают, что приблизительно 50% впервые выявленных пациентов не входят в ремиссию на первом ПЭП. Когда монотерапия безуспешна, часто пробуют полифармацию, но когда и как должны подбираться комбинации ПЭП до сих пор не было изучено. Альтернативный препарат неизбежен, когда у пациента развиваются непереносимые побочные эффекты, но приступы сохраняются, несмотря на высокие дозы ПЭП первого ряда, при этом не ясно, необходимо заменять препараты или их комбинировать [56]. В пользу замены указывают и токсичность полифармации. Однако это предположение было сделано на основании исследований, в которых показано, что пациенты, получающие более одного ПЭП, не испытывали большей токсичности, чем те, кто принимал монотерапию, когда концентрация препарата была сопоставима [57]. Среди пациентов в исследовании в Глазго, у которых первый ПЭП в начале лечения не имел успеха из-за недостаточной эффективности, те, кто получал дополнительную терапию, имели более высокий уровень ремиссии (26% против 17%) и более низкую распространенность побочных эффектов (12% против 26%), чем те, кого лечили альтернативной монотерапией [58]. Результаты из этих наблюдательных исследований, полученные С.L.P. Deckers и соавт. помогли определить дальнейший исход переносимости политерапии на основании РКИ, в которых 130 нелеченных взрослых пациентов были рандомизированы в равной степени на группу, получавшую монотерпию КБЗ или на группу, получавшую КБЗ / ВПА в комбинации [59]. В двух группах не было разницы по токсичности (первичный исход) или числу приступов. Похожие данные были получены Е. Beghi и соавт.
Вопрос, возможно ли комбинировать ПЭПы рационально, горячо обсуждается. С не менее 15 ПЭП, доступными в настоящее время для лечения парциальных приступов, возможно 105 комбинаций дуотерапии. Такое огромное число возможностей делает «рациональную терапию» не просто академическим интересом, но и практической необходимостью. Одна из стратегий, которая защищается и активно изучается — это механистический подход, основанный на типах действия ПЭП. Хотя все механизмы не совсем понятны, их можно разделить на крупные категории (табл. 2) [6]. Препараты типа ФТ, КБЗ и ЛТД действуют посредством блокады натриевых каналов. Эта способность свойственна некоторым из новых ПЭП, таких как ОКЗ и зонизамид (ЗНЗ). Это суксимид (ЭСМ) уникально снижает низкий порог Т-кальциевых потоков. Некоторые ПЭП, такие как барбитураты и бензодиазепины, ВГБ и тиагабин увеличивают ингибиторное действие ГАМК. Другие препараты, такие как топирамат (ТПМ), ЗНЗ и ацетазоламид, ингибируют карбоангидразную активность. Действие на кальциевые и калиевые канала и уменьшение глутаматопосредованного возбуждения также способствуют антиэпилептическим свойствам некоторых препаратов. Многие из новых препаратов, особенно габапентин, ТПМ, фелбамат, ЗНЗ и, вероятно, также ЛТД и леветирацетам, обладают множественным фармакологическим действием [63].
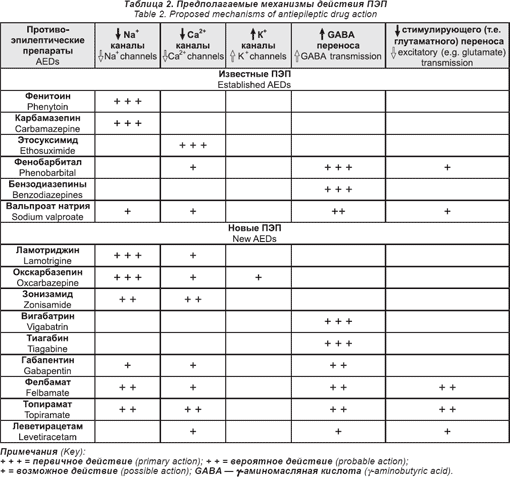
Теоретически, комбинация разных механизмов действия систематически изменяется для того, чтобы установить, дополняют они друг друга или же являются синергистами. Наиболее научно значимым подходом к исследованиям взаимодействий ПЭП является изоболограмный метод, при котором они даются в различных дозах, чтобы выявить наиболее эффективный режим для контроля над приступами. Этот подход был успешно применен в исследованиях на животных [64-65], но представляет логистические сложности в клинических испытаниях. С.L.P. Deckers и соавт. [61] всесторонне осветили ограниченные данные по животным и человеку и сообщили, что комбинации, вовлекающие блокаторы натриевых каналов и препараты с ГАМК-ергическими свойствами, оказываются особенно эффективными. Наши собственные данные свидетельствуют в пользу добавления ПЭП с множественными механизмами действия [58]. Лучшее доказательство успеха синергизма существует при применении ВПА и ЛТД для парциально-дебютирующих и генерализованных приступов [66-67]. Другие рекомендуемые комбинации включают ВПА и ЭСМ для абсансных приступов [68], КБЗ и ВГБ или ВПА для парциальных приступов [69] и ЛТД с ТПМ для разных типов приступов [70]. Необходимо, чтобы РКИ выявляли клинически полезные комбинации и, что, возможно, более важно, определяли, какие факторы способствуют синергизму ПЭП и когда должна применяться рациональная политерапия.
Методика ведения
Данные теоретические заключения имеют практическое применение для лечения эпилепсии с момента постановки диагноза. Так как у большинства впервые выявленных пациентов припадки будут отсутствовать на фоне приема одного ПЭП, часто на низких или умеренных дозах, акцент для этой популяции пациентов должен делаться на переносимости и безопасности. Необходимо выбрать препарат со спектром профилей активности, побочных эффектов и взаимодействия, который может привести данного пациента к ремиссии без выраженной токсичности при длительной эффективности [71]. Выбор должен идеально соответствовать типу приступов пациента и/или эпилептическому синдрому, возрасту, полу, весу, психиатрическому анамнезу, другим показателям заболевания, сопутствующему лечению и образу жизни.
Если первый препарат приводит к идиосинкратическим реакциям, побочным эффектам на низких или умеренных дозах или не контролирует приступы, он должен быть заменен другим. Если первый препарат хорошо переносится, доза должна быть увеличена до предела переносимости для полного освобождения от приступов. Если контроль над приступами стал существенно лучше, но не достигнута полная ремиссия, должен быть добавлен ПЭП с другим механизмом действия. Комбинация препаратов также может быть рекомендована после двух неудачных попыток монотерапии, так как шанс успеха третьего препарата минимален [20]. Очень мало данных, подтверждающих, что комбинация блокаторов натриевых каналов с ПЭП, обладающими ГАМК-ергическими свойствами или множественными механизмами действия,может иметь рациональную основу. Часто необходимо уменьшать дозу оригинального препарата, особенно если у пациента имеются или развились побочные эффекты. С практической целью резистентная эпилепсия может быть заподозрена, когда контроль над приступами не наблюдается на фоне двух адекватных и хорошо переносимых ПЭП, принимаемых в качестве монотерапии или на фоне первого выбора и первого режима комбинации. В этом случае может быть рекомендовано оперативное вмешательство, особенно если было выявлено потенциально операбельное структурное изменение, как, например, височный склероз. В настоящее время также необходимо искать факторы, которые могли бы привести к «псевдорезистентности», с помощью точной классификации приступов и/или синдромов, результатов нейровизуализации, комплаентности пациента и наличия негативных факторов образа жизни, таких как употребление алкоголя или лекарственная зависимость [18].
Если первая комбинация неэффективна и операция нежелательна, должен быть опробован ряд комбинаций ПЭП с подходящими типами действия. К сожалению, подобных данных недостаточно. Небольшое число пациентов избавится от приступов на третьем ПЭП, но лечение четвертым и далее препаратом вряд ли будет успешным [72]. Отчасти это связано с тем, что чем больше «тяжесть» препарата, тем менее вероятно, что политерапия будет переносима и, следовательно, эффективна. «Тяжесть» препарата является функцией дозы препарата, также как и его количества, и поэтому уменьшение дозы одного или более ПЭП может помочь способствовать дальнейшему применению лекарственных средств.
Заключение
Хотя современные популяционные эпидемиологические исследования показали, что 30-40% пациентов с эпилепсией не выходят в ремиссию, остается неясным, какие факторы способствуют развитию фармако-резистентности. Исследования фокусировались на двух аспектах процесса, т.е. на диагнозе и ремиссии или резистентной эпилепсии, без учета того, как пациенты переходят из одного состояния в другое. Понимание сущности проблемы может пролить свет на биологические механизмы, обусловливающие лекарственную резистентность. У пациентов, которые не достигают ремиссии, отмечается широкий спектр степени выраженности заболевания, начиная от редких и легких приступов, которые не влияют на качество жизни, до частых, инвалидизирующих приступов, которые более свойственны для резистентной эпилепсии [39].
Был достигнут консенсус в том, что с практическими целями медикаментозную резистентность можно заподозрить, если 2 адекватных, хорошо переносимых препарата первого ряда или один в монотерапии и одна комбинация не дали результата из-за недостатка эффективности. Однако временные рамки могут значительно варьировать. Вызов, брошенный клиницистами, состоит в том, чтобы разработать индивидуализированные протоколы, которые дадут максимальный шанс успешной лекарственной терапии, включая ранее использование «рациональной политерапии» для пациентов, не отвечающих на монотерапию, и которые выявят больных, подходящих для хирургического лечения, особенно среди пациентов с височной эпилепсией. Адекватный подход к лечению каждого отдельного эпилептического синдрома оптимизирует шанс полного контроля над приступами и поможет большему числу людей вести полноценный образ жизни.
1. Sander J.W.A.S., Shorvon S.D. Epidemiology of the epilepsies // J. Neurol Neurosurg Psychiatry 1996; 61 : 433-43.
2. Zarrelli M.M., Beghi E., Rocca W.A., Hauser W.A. Incidence of epileptic syndromes in Rochester, Minnesota: 1980-1984 // Epilepsia 1999; 40 : 1708-1714.
3. Gowers W.R. Epilepsy and other chronic convulsive diseases. London: Churchill, 1881.
4. Rodin E. The prognosis of patients with epilepsy. Springfield, IL: Charles С Thomas, 1968.
5. Annegers J.F., Rocca W.A., Hauser W.A. Causes of epilepsy: contributions from the Rochester Epidemiology Project // Mayo Clin Proc 1996; 71 : 570-5.
6. Hauser W.A., Kurland L.T. The epidemiology of epilepsy in Rochester, Minnesota, 1935 through 1967 // Epilepsia 1975; 16 : 1-66.
7. Hauser W.A., Annegers J.F., Kurland L.T. Prevalence of epilepsy in Rochester, Minnesota: 1940-1980 // Epilepsia 1991; 429-45.
8. Hauser W.A. Annegers J.F., Kurland L.T. Incidence of epilepsy and unprovoked seizures in Rochester, Minnesota: 1935-1984 // Epilepsia 1993; 34 : 453-68.
9. Hauser W.A., Annegers J.F., Rocca W.A. Descriptive epidemiology of epilepsy: contributions of population-based studies from Rochester, Minnesota // Mayo Clin Proc 1996; 71 : 576-86.
10. Annegers J.F., Hauser W.A., Elverback L.R. Remission of seizures and relapse in patients with epilepsy // Epilepsia 1979; 20 : 729-737.
11. Shafer S.Q., Hauser W.A., Annegers J.F., Klaus D.W. EEC and other early predictors of epilepsy remission: a community study // Epilepsia 1988; 29 : 590-600.
12. Hart Y.M., Sander J.W., Shorvon S.D. National General Practice Study of Epilepsy and Epileptic Seizures: objectives and study methodology of the largest reported prospective cohort study of epilepsy // Neuroepide-miology 1989; 8 : 221-7.
13. Cockerell О.С., Johnson A.L., Sander J.W.A.S., et al. Remission of epilepsy: results from the national general practice study of epilepsy // Lancet 1995; 346 : 140-4.
14. MacDonald B.K., Johnson A.L., Goodridge D.M. et al. Factors predicting prognosis of epilepsy after presentation with seizures // Ann Neurol 2000; 48 : 833-41.
15. Elwes R.D.C., Johnson A.L., Shorvon S.D., Reynolds E.H. The prognosis for seizure control in newly diagnosed epilepsy // N Engl J. Med 1984; 311 : 944-7.
16. Collaborative Group for the Study of Epilepsy. Prognosis of epilepsy in newly referred patients: a multicenter prospective study of the effects of monotherapy on the long-term course of epilepsy // Epilepsia 1992; 33 : 45-51.
17. Sillanpaa M., Jalava M., Kaleva O., Shinnar S. Longterm prognosis of seizures with onset in childhood // N Engl J. Med 1998; 338:1715-22.
18. Perucca E. Pharmacoresistance in epilepsy: how should it be defined? // CNS Drugs 1998; 10 : 171-9.
19. Regesta G., Tanganelli P. Clinical aspects and biological bases of drug-resistant epilepsies // Epilepsy Res 1999; 34 : 109-22.
20. Kwan P., Brodie M.J. Early identification of refractory epilepsy // N Engl J. Med 2000; 341 : 314-9.
21. Kwan P., Brodie M.J. Effectiveness of first antiepileptic drag // Epilepsia 2001; 42 : 1255-60.
22. Dlugos D.J., Sammel M.D., Strom B.L., Farrar J.T. Response to first drag trial predicts outcome in childhood temporal lobe epilepsy // Neurology 2001; 57 : 2259-64.
23. Mohanraj R., Brodie M.J. Predicting outcomes in newly diagnosed epilepsy // Epilepsia 2003; 44 (suppl 9) : 15-16.
24. Brodie M.J., Mohanraj R. Response to treatment in newly diagnosed epilepsy // Epilepsia 2003; 44 (suppl 9) : 14.
25. Brodie M.J., Kwan P. Staged approach to epilepsy management // Neurology 2002; 58 (Suppl 5) : S2-8.
26. Arts W.F.M., Geerts A.T., Brouwer O.F., et al. The early prognosis of epilepsy in childhood: the prediction of a poor outcome // Epilepsia 1999; 40 : 726-34.
27. Berg A.T., Shinnar S., Levy S.R. et al. Early development of intractable epilepsy in children. A prospective study // Neurology 2001; 56 : 1445-2.
28. Engel J., Wiebe S., French J., et al. Practice parameter: temporal lobe and localised neocortical resections for epilepsy: Report of the Quality Standards Subcommittees of the American Academy of Neurology in association with the American Association of Neurological Surgeons // Neurology 2003; 60 : 538-547.
29. Trevathan E., Gilliam F. Lost years. Delayed referral for surgically treatable epilepsy // Neurology 2003; 61 : 432-433.
30. Berg A.T., Shinnar S., Levy S.R. et al. Defining seizure outcomes in pediat-ric epilepsy: the good, the bad and the in-between // Epilepsy Res 2001; 43 : 75-84.
31. Berg A.T., Shinnar S., Levy S.R. et al. Two-year remission and subsequent relapse in children with newly diagnosed epilepsy // Epilepsia 2001; 42 : 1553-62.
32. Semah F., Picot M-C, Adam С. et al. Is the underlying cause of epilepsy a major prognostic factor for recurrence? // Neurology 1998; 51 : 1256-1262.
33. Stephen L.J., Kwan P., Brodie M.J. Does the cause of localization-related epilepsy influence the response to antiepileptic drug treatment? // Epilepsia 2001; 42 : 357-362.
34. Fuerst D., Shah J., Shah A. Watson C. Hippocampal sclerosis is a progressive disorder: a longitudinal volumetric MRI study // Ann. Neurol. 2003; 53 : 413-6.
35. Kobayashi E., Lopes-Cendes I., Guerreiro C.A.M. et al. Hippocampal atrophy in familial mesial temporal lobe epilepsy and its relationship with seizure outcome // Neurology 2001; 56 : 168-172.
36. Berg A.T., Langfitt J., Shinnar S. et al. How long does it take for partial epilepsy to become intractable? // Neurology 2003; 60 : 186-90.
37. Meldrum B.S. Why and when are seizures bad for the brain? // TIPS 2001; 22 : 445-446.
38. Sutula T.P., Hagen J., Pitkanen A. Do epileptic seizures damage the brain? // Curr Opin Neurol 2003; 16 : 189-95.
39. Kwan P., Brodie M.J. Refractory epilepsy: a progressive, intractable but preventable condition? Seizure 2002; 11: 77-84.
40. Shorvon S.D., Reynolds E.H. Reduction in polypharmacy for epilepsy // Br. Med. J. 1979; 2 : 1023-5.
41. Schmidt D. Reduction of two-drug therapy in intractable epilepsy // Epilepsia 1983; 24 : 368-76.
42. Mohanraj R., Brodie M.J. Measuring the efficacy of antiepileptic drugs // Seizure 2003; 12 : 413-443.
43. Brodie M.J., French J.A. Management of epilepsy in adolescents and adults // Lancet 2000; 356 : 323-9.
44. Appleton R.E., Peters A.C., Mumford J.P., et al. Randomised, placebo-controlled study of vigabatrin as first-line treatment of infantile spasms // Epilepsia 1999; 40 : 1627-33.
45. Taylor S., Tudur Smith C., Williamson P.R., Marson A.G. Phenobarbitone versus phenytoin monotherapy for partial onset seizures and generalized onset tonic-clonic seizures // The Cochrane Database Syst Rev 2001; 4 : CD002217.
46. Marson A.G., Williamson P.R., Hutton J.L. et al. Carbamazepine versus valproate monotherapy for epilepsy: a metaanalysis // Epilepsia 2002; 43 : 505-513.
47. Tudur Smith C., Marson A.G., Williamson P.R. Phenytoin versus valproate monotherapy for partial onset seizures and generalized onset tonic-clonic seizures // Cochrane Database Syst Rev 2001; 4 : CD0017690.
48. Tudur Smith C., Marson A.G., Clough H.E., Williamson P.R. Carbamazepine versus phenytoin monotherapy for epilepsy // Cochrane Database Syst Rev 2002; 2 : CD001911.
49. Kwan P. Brodie M.J. Clinical trials of antiepileptic medications in newly diagnosed patients with epilepsy. Neurology 2003; 60 (Suppl 4) : S2-12.
50. Chadwick D. Safety and efficacy of vigabatrin and carbamazepine in newly diagnosed epilepsy: a multicenter randomised double-blind study // Lancet 1999; 354 : 13-9.
51. Kwan P., Brodie M.J. Neuropsychological effects of epilepsy and antiepileptic drags // Lancet 2001; 357:216-22.
52. Brodie M.J., Richens A. Yuen AWC. Double-blind comparison of lamotri-gine and carbamazepine in newly diagnosed epilepsy // Lancet 1995; 345 : 476-9.
53. Brodie M.J., Overstall P.W., Giorgi L. and the UK Lamotrigine Elderly Study Group. Multicentre, double-blind, randomized comparison between lamotrigine and carbamazepine in elderly patients with newly diagnosed epilepsy // Epilepsy Res 1999; 37 : 81-87.
54. Guerreiro M.M., Vigonius U., Pohlmann H. et al. A double-blind controlled clinical trial of oxcarbazepine versus phenytoin in children and adolescents with epilepsy // Epilepsy Res 1997; 27:205-13.
55. Arroya S., De la Morena A. Life-threatening adverse events of antiepileptic drugs // Epilepsy Res 2001; 47 : 155-174.
56. Schmidt D., Gram L. Monotherapy versus polytherapy in epilepsy. A reappraisal // CNS Drugs 1995; 3 : 194-208.
57. Lammers M.W., Hekster Y.A. Keyser A et al. Monotherapy or polytherapy for epilepsy revisited: a quantitative assessment // Epilepsia 1995; 36 : 440-6.
58. Kwan P., Brodie M.J. Epilepsy after the first drug fails: substitution or add-on? // Seizure 2000; 9 : 464-8.
59. Deckers C.L.P., Hekster Y.A., Keyser A. et al. Monotherapy versus polytherapy for epilepsy: a multicenter double-blind randomized study // Epilepsia 2001; 42 : 1387-94.
60. Beghi E., Gatti G., Tonini C. et al. Adjunctive therapy versus alternative monotherapy in patients with partial epilepsy failing on a single drug: a multicentre, randomised pragmatic trial // Epilepsy Res 2003; 57 : 1-13.
61. Deckers C.L.P., Czuczwar S.J., Hekster Y.A. et al. Selection of antiepileptic drug polytherapy based on mechanisms of action: the evidence reviewed // Epilepsia 2000; 41 : 1364-74.
62. Kwan P., Sills G.J., Brodie M.J. The mechanisms of action of commonly used antiepileptic drugs // Pharmac Ther 2001; 90 : 21-34.
63. Sills G.J., Brodie M.J. Update on the mechanisms of action of antiepileptic drugs // Epil Dis 2001; 3 : 165-172.
64. Sun M., van Rijn C.M., Liu Y., Wang M. Combination of carbamazepine and valproate in different dose proportions in maximal electroshock seizure model in mice // Epilepsy Res 2002; 51 : 5-11.
65. Luszczki J.J., Borowicz K.K., Swiader M., Czuczwar S.J. Interactions between oxcarbazepine and conventional antiepileptic drugs in the maximal electroshock test in mice: an isobolographic analysis // Epilepsia 2003; 44 : 489-99.
66. Brodie M.J., Yuen A.W.C. and the 105 Study Group. Lamotrigine substitution study: synergism with sodium valproate? // Epilepsy Res 1997; 26 : 423-32.
67. Pisani F., Otero G., Russo M.E., et al. The efficacy of valproate-lamotrigi-ne comedicatoin in refractory complex partial seizures: evidence for a pharmacodynamic interaction // Epilepsia 1999; 40 : 1141-6.
68. Rowan A.J., Meijer J.W.A., de Beer-Pawlikowski N. et al. Valproate ethos-uximide combination therapy for refractory absence seizures // Arch Neurol 1983; 40 : 797-802.
69. Brodie M.J., Mumford J.P. and the 012 Study Group. Double-blind substitution of vigabatrin and valproate in carbamazepine-resistant partial epilepsy // Epilepsy Res 1999; 34 : 199-205.
70. Stephen L.J., Sills G.J., Brodie M.J. Lamotrigine and topiramate may be a useful combination // Lancet 1998; 351 : 958-9.
71. Brodie M.J., Kwan P. The star systems: overview and use in determining antiepileptic drug choice // CNS Drugs 2001; 15 : 1-12.
72. Stephen L.J., Brodie M.J. Seizure freedom with more than one antiepileptic drug // Seizure 2002; 11 : 349-51.
73. Brodie M.J., Leach J.P. Success or failure with antiepileptic drug therapy: beyond empiricism? // Neurology 2003; 60 : 162-163.
