Международный неврологический журнал 3(3) 2005
Вернуться к номеру
Лорноксикам (ксефокам) — новый нестероидный противовоспалительный препарат с интенсивным и пролонгированным анальгетическим эффектом
Авторы: А.В. Авксентюк, Институт терапии СО РАМН, Новосибирск (директор — академик РАМН, проф. Ю.П. Никитин)
Рубрики: Неврология
Разделы: Справочник специалиста
Версия для печати
Нестероидные противовоспалительные препараты (НПВП) широко применяются в терапии состояний, сопровождающихся воспалением и болевым синдромом. Хотя в настоящее время известно уже около ста НПВП различных классов, поиск новых препаратов этой группы продолжается. Это связано с потребностью в препаратах, имеющих как оптимальное соотношение обезболивающего и противовоспалительного действия, так и высокую степень безопасности. Такие широко используемые в настоящее время анальгетики, как метамизол (анальгин), входящий в состав некоторых комбинированных препаратов (баралгин, максиган и т.д.), а также более современный кеторолак, имеют неблагоприятный профиль побочных эффектов и низкие противовоспалительные свойства, в то время как у большинства других НПВП анальгетические свойства недостаточны [14, 15]. В этом плане большой интерес врачей всех специальностей вызвало появление на фармацевтическом рынке препарата лорноксикам, выпускаемого компанией «Никомед-Амершам» под торговой маркой Ксефокам.
Фармакокинетика лорноксикама
В проведенных исследованиях выявлено быстрое, линейно зависимое от дозы и почти полное всасывание лорноксикама после его перорального и внутримышечного введения [24, 27]. Его пероральный прием в дозах от 4 до 16 мг биологически эквивалентен внутривенному введению этих же доз. Свечи, содержащие 4-8 мг лорноксикама, обеспечивают лишь 65-74-процентную биодоступность препарата по сравнению с внутривенным введением.
Пероральный прием лорноксикама после стандартного завтрака сопровождался некоторым замедлением всасывания и уменьшением количества всасываемого препарата на 20-30% по сравнению с приемом утром натощак. Однако такое влияние пищи на всасывание не считается клинически значимым, что позволяет принимать лорноксикам без связи с приемом пищи [5].
После приема 8 мг лорноксикама его концентрация в плазме достигает пиковой в течение 1,5 часов, а затем снижается и через 12 часов составляет одну десятую от исходной [5, 16]. Период полувыведения лорноксикама из плазмы составляет примерно 4 часа, что значительно меньше аналогичного периода у других НПВП группы оксикамов [24]. Лорноксикам более чем на 99% связывается с белками плазмы, однако это не препятствует активному проникновению его в суставы. Проведенные исследования проникновения лорноксикама в синовиальную жидкость, в том числе и у больных с экссудацией в коленные суставы, связанной с ревматоидным артритом или остеоартритом, показали, что в суставах длительное время сохраняется активность препарата — даже в то время, когда в плазме его концентрация снижается до уровня, предшествовавшего введению дозы [16, 43].
Благодаря короткому периоду полувыведения из плазмы, лорноксикам обладает меньшей выраженностью побочных эффектов, так как в период между введениями доз возможно восстановление защитных физиологических уровней простагландинов, необходимых для защиты слизистой желудка и поддержания нормального кровотока в почках [23]. При этом сохранение активности препарата внутри суставов и в других воспаленных тканях в течение более длительного времени (10-12 часов) позволяет принимать лорноксикам 2 раза в день [5, 16].
Лорноксикам полностью метаболизируется в печени под действием цитохрома Р450 с образованием фармакологически неактивных метаболитов, примерно одна треть которых выводится почками с мочой, а две трети — печенью и кишечником, при этом энтеропеченочная циркуляция отсутствует [16, 24, 27]. Такой двойной путь экскреции снижает нагрузку на данные органы и улучшает переносимость лорноксикама. Исследования фармакокинетики у пациентов с различными степенями почечной и печеночной недостаточности показали, что за исключением случаев тяжелого поражения печени или почек, какого-либо уменьшения принимаемой дозы не требуется [41, 42].
После многократного введения лорноксикама его кумуляция в плазме не отмечается, что снижает риск побочных эффектов по сравнению с препаратами, имеющими длительный период полувыведения [48].
Фармакокинетика лорноксикама примерно одинакова у пожилых людей и людей молодого или зрелого возраста, поэтому какой-либо коррекции дозы лорноксикама у пожилых не требуется [48].
Выявленные взаимодействия лорноксикама с другими лекарственными препаратами типичны для НПВП в целом. Лорноксикам усиливает противосвертывающее действие варфарина и противодиабетическое действие пероральных производных сульфонилмочевины. Лорноксикам увеличивает уровень лития в плазме. Он может препятствовать антигипертензивному эффекту эналаприла, ослабляет действие фуросемида. Необходимо проявлять осторожность при введении лорноксикама одновременно с высокими дозами аспирина и даже низкими дозами метотрексата, дигоксином (особенно при почечной недостаточности). Циметидин, но не ранитидин, могут замедлять метаболизм лорноксикама, а хелат висмута — уменьшать его биодоступность [5].
Клинические исследования
Клинические исследования лорноксикама были проведены при разнообразных заболеваниях, сопровождающихся болями и воспалением.
Послеоперационные боли
Значительное число работ посвящено различным видам послеоперационной боли (ламинэктомия, дискэктомия, операции на передней крестообразной связке, гистерэктомия, эпизиотомия, экстракция ретинированного зуба мудрости).
Во время и после операции из поврежденных тканей высвобождаются медиаторы боли и простагландины, а НПВП специфически уменьшают локальную, спинальную и центральную сенсибилизацию по отношению к возникающим болевым импульсам. Применение НПВП позволяет значительно снизить дозу опиоидов, а иногда даже полностью отказаться от них. Важен и противовоспалительный эффект НПВП, они значительно улучшают течение репаративных процессов, уменьшают отек, снижают риск расхождения швов [4].
В большинстве исследований эффективности лорноксикама при послеоперационных болях использован двойной слепой метод. Лорноксикам сравнивали с опиоидами и другими НПВП. При использовании после ламинэктомии или дискэктомии метода «контролируемого пациентом обезболивания», когда пациент сам регулирует введение препаратов с помощью специального устройства, лорноксикам в дозе около 20 мг внутривенно в сутки по обезболивающему эффекту был эквивалентен 22 мг морфина [20]. При этом в начале введения пациенты использовали несколько большую дозу лорноксикама по сравнению с морфином, однако затем доза вводимого лорноксикама оставалась примерно на одном уровне, в то время как введение морфина постоянно возрастало.
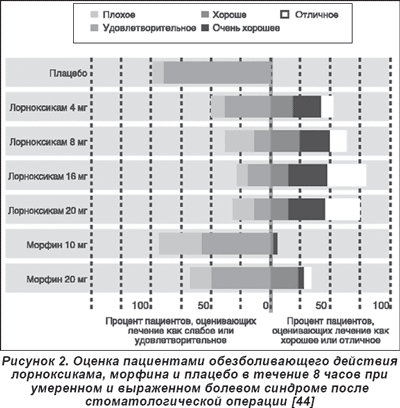
В исследовании, включавшем 252 пациента, сравнивали однократные внутримышечные дозы лорноксикама (4, 8, 16 и 20 мг) с морфином в дозах 10 и 20 мг при выраженном и умеренном болевом синдроме после стоматологической операции. Если в течение первого часа лорноксикам в дозе не менее 8 мг (8, 16 или 20 мг) и морфин в дозе 20 мг имели одинаковое обезболивающее действие, превосходящее 4 мг лорноксикама и 10 мг морфина, то через 3 часа после введения, по оценке пациентов, все дозы лорноксикама превосходили любую дозу морфина (рис. 2) [29].
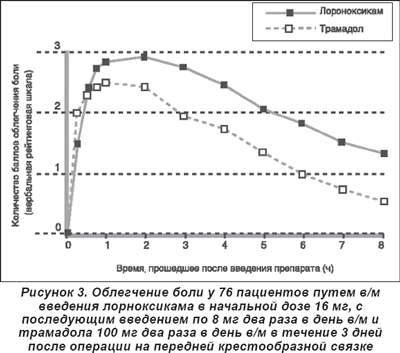
После операции на передней крестообразной связке лорноксикам в дозе 8 мг два раза в день (первоначальная доза 16 мг) давал достоверно (р = 0,014) более полный анальгетический эффект по сравнению с трамадолом в дозе 100 мг два раза в день внутримышечно (рис. 3) [18]. После гинекологических операций (гистерэктомии) обезболивающий эффект от 8 мг лорноксикама внутривенно был выше, чем от 50 мг трамадола. Эффективность 4 мг лорноксикама была несколько ниже этой дозы трамадола, но превышала эффект плацебо [28].
Частота побочных эффектов при применении лорноксикама была значительно ниже по сравнению с опиоидами. Так, при применении морфина частота побочных эффектов составила 38% против 21,7% у лорноксикама [20], частота побочных эффектов при использовании трамадола также значительно превышала таковую у лорноксикама. Следует также иметь в виду риск возникновения лекарственной зависимости при применении опиоидов.
Таким образом, при послеоперационных болях анальгетический эффект лорноксикама, вводимого парентерально в дозе не менее 8 мг, не уступает средним дозам опиоидов при значительно лучшем профиле безопасности. Однако при сопоставлении лорноксикама с опиоидами необходимо иметь в виду два момента. Несмотря на наличие определенного центрального механизма действия, лорноксикам не обладает каким-либо заметным седативным действием, что во многих ситуациях является преимуществом. Однако при выраженным болях, особенно в ночное время, когда седативный эффект желателен, в дополнение к лорноксикаму необходимо вводить соответствующие препараты. Если дозу лорноксикама в 16 мг можно рассматривать как «потолковую» (верхний предел действия), то препараты морфия практически не имеют потолка обезболивающего действия. Поэтому в тех ситуациях, когда применение лорноксикама в качестве монотерапии не дает достаточного эффекта, целесообразна его комбинация с опиоидами. При этом лорноксикам дает «опиоидсберегающий эффект» за счет уменьшения им дозы опиоидов, что позволяет снизить риск таких побочных эффектов последних, как тошнота, рвота, подавление дыхания, уменьшение моторики кишечника, гемодинамические нарушения.
Эффект перорального применения лорноксикама был изучен при стоматологических операциях и эпизиотомии. Показано, что дозы 2 или 4 мг были более эффективны, чем плацебо. Дозы 8 и 16 мг были более эффективны, чем 650 мг аспирина или 400-800 мг ибупрофена [5]. При сравнении лорноксикама с достаточно часто применяемым в России кеторолаком показано, что в первые часы после приема обезболивающий эффект 10 мг кеторолака занимал промежуточное положение между 8 и 16 мг лорноксикама. Однако длительность действия лорноксикама была значительно большей, и через 5 часов после приема обезболивающий эффект кеторолака был ниже, чем у 8 мг лорноксикама [49]. Наиболее существенным недостатком кеторолака является высокая частота побочных эффектов. Максимально допустимая продолжительность лечения кеторолаком — 5 дней [14], в то время как у лорноксикама, благодаря его высокой безопасности, подобные ограничения отсутствуют.
Онкологические боли
Применение лорноксикама для лечения онкологических болей особенно обосновано в рамках «Трехступенчатой схемы обезболивания ВОЗ», которая относит НПВП к ненаркотическим адъювантным анальгетикам и рекомендует их использование как для монотерапии, так и для усиления действия опиоидов [1]. У онкологических больных лорноксикам может быть использован самостоятельно, если боль вызвана метастазами в кости скелета, когда наряду с болевыми импульсами имеются элементы перифокального воспаления, сопутствующего метастатическому очагу. В рандомизированном двойном слепом исследовании, включавшем 29 пациентов, испытывавших боли из-за костных метастазов, обезболивающий эффект, по оценкам как врачей, так и самих больных, был выше при приеме 8 мг лорноксикама три раза в день, чем при приеме 500 мг напроксена 2 раза в день [50].
Достаточно высокая эффективность лорноксикама в дозе 8 мг два раза в день (15% — полный эффект, 54% — частичный эффект) при лечении больных с хронической онкологической болью в терминальной стадии заболевания показана в исследованиях Российского Онкологического Научного Центра РАМН [8]. При этом у 31% пациентов лорноксикам применяли в качестве монотерапии, у 69% — в сочетании с опиоидами.
Боли в спине
По данным статистики, поясничными болями страдает более половины населения всей планеты. В терапии данного состояния ведущее место занимают НПВП, причем важно наличие как противовоспалительного, так и выраженного анальгетического эффекта. В этом плане лорноксикам вызывает особый интерес.
Пероральное, внутривенное и внутримышечное введение 2-16 мг лорноксикама в виде одиночной дозы или два раза в день значительно уменьшало острую боль в пояснице по сравнению с плацебо. Действие лорноксикама 4 и 8 мг при введении два раза в день было эквивалентно действию напроксена в дозе 500 мг [44]. Эффект лорноксикама, применяемого при острых поясничных болях перорально по следующей схеме: 1-й день — 16 и 8 мг, 2-4-й день — 8 мг два раза в день, 5-й день — 8 мг, не уступал приему 50 мг диклофенака три раза в день и значительно превосходил плацебо (р = 0,015) [25]. При исследовании пациентов с хроническими болями в спине было показано, что прием 4 мг лорноксикама два раза в день в течение 14 дней приводил к облегчению болей у 80% пациентов, что не уступало по эффективности 50 мг диклофенака 2 раза в день [30]. В другом исследовании пациенты, получавшие по 8 мг лорноксикама два раза в день, показали значительное уменьшение боли по сравнению с исходным уровнем и нуждались в достоверно меньшем количестве дополнительных анальгетиков по сравнению с пациентами, получавшими 500 мг напроксена 2 раза в день или 4 мг лорноксикама два раза в день [31].
По данным исследований межрегионального противоболевого центра (г. Новосибирск), применение лорноксикама у больных с вертеброгенным болевым синдромом в дозе 8 мг два раза в день в течение 3 недель значительно превосходило как по эффективности, так и по безопасности индометацин в дозе 75 мг три раза в день [12]. Высокая эффективность лорноксикама в дозе 8 мг три раза в день в течение трех дней у пожилых больных с вертеброгенными болями показана в исследованиях в Санкт-Петербурге; значительное улучшение отмечено у 58% больных, улучшение — у 25% [6].
Таким образом, лорноксикам можно рассматривать как препарат выбора при терапии болей в спине, особенно учитывая сочетание анальгетических и противовоспалительных свойств.
Мигрень
НПВП являются традиционным компонентом профилактики и купирования приступов мигрени. Прием 4 мг лорноксикама три раза в день значительно уменьшал частоту мигрени (р < 0,05) и потребление анальгетиков по сравнению с плацебо [33].
Исследования, проведенные в Санкт-Петербурге, подтвердили возможность использования лорноксикама в терапии мигрени [6].
Ксефокам при других болевых синдромах
Лорноксикам, вводимый в дозе 4 мг два раза в день в течение 7 дней пациентам с костно-суставными болями, связанными с переломами, тендосиновитом или другими поражениями, устранял боли в покое, при движении и ночью [32].
Показана возможность применения лорноксикама в терапии болевого синдрома у больных с опийной наркоманией. В острый период абстиненции лорноксикам применялся совместно с трамадолом, при купировании «повторных волн» абстиненции и «псевдоабстинентного» синдрома — в качестве монотерапии в дозе от 16 до 32 мг в сутки. Анальгетический эффект лорноксикама превышал таковой у кеторолака и диклофенака [10].
Ревматоидный артрит и остеоартрит
Значение лорноксикама в лечении ревматических заболеваний определяется тем, что у него имеется не только сильное анальгетического действие, но и достаточно выраженный противовоспалительный эффект (в отличие от таких анальгетиков, как кеторолак, метамизол, анальгин, парацетамол). Появление нового НПВП особенно важно ввиду того, что многих больных ввиду их индивидуальных особенностей не удовлетворяет терапия имеющимися препаратами. Известный датский ревматолог — доктор Хоскинсон — говорил, что среди пациентов гораздо больше различий, чем среди имеющихся на сегодня препаратов [3]. Поэтому появление лорноксикама позволяет расширить спектр применяемых НПВП и оптимизировать лечение больных с учетом их индивидуальных потребностей. Особое внимание привлекают также сообщения о том, что лорноксикам может стимулировать синтез протеогликанов и ослаблять деструктивные эффекты, возникающие при ревматоидном артрите [2, 5, 23].
Сравнение лорноксикама с плацебо и традиционно используемыми в клинике НПВП при ревматоидном артрите было осуществлено более чем в 10 двойных слепых рандомизированных исследованиях, выполненных как в России, так и за рубежом и включавших в общей сложности более 2000 больных [5, 7, 9, 16]. Оценивали индекс суставов Ричи, количество суставов, вовлеченных в основное заболевание, продолжительность утренней скованности, облегчение боли и функциональной способности, а также общие оценки пациента и врача. Было показано, что прием даже 2 мг лорноксикама два раза в день был эффективнее, чем плацебо [45]. При этом была отмечена связь между дозой и эффектом: прием 4 мг лорноксикама три раза в день или 8 мг два раза в день был более эффективным, чем прием 2-4 мг два раза в день [5]. В то же время дополнительного усиления эффективности по сравнению с приемом 8 мг два раза в день не обнаружено.
Сравнение с пироксикамом на протяжении курса терапии в 12 недель показало, что применение лорноксикама в дозе 4 мг два раза в день практически эквивалентно приему 20 мг пироксикама [34]. При сравнении лорноксикама и диклофенака в течение 12 недель наибольшее улучшение индекса суставов Ричи отмечено у больных, принимавших лорноксикам 4 мг три раза в день (улучшение на 25%) или 8 мг два раза в день (на 24%); у больных, принимавших 50 мг диклофенака три раза в день, индекс Ричи улучшался только на 20% (рис. 4) [35]. При продолжении данного исследования в течение 9 месяцев действие лорноксикама сохранялось или усиливалось.

Была показана эффективность лорноксикама в дозе 4 мг три раза в день в течение 4 недель при анкилозирующем спондилите [36]. Есть наблюдения о применении лорноксикама в терапии больных псориатическим артритом [11].
Многочисленные исследования эффективности лорноксикама у больных с остеоартритом (коленного и тазобедренного суставов) подтвердили, что доза лорноксикама 8 мг два раза в день значительно превосходит плацебо [5]. При приеме лорноксикама в течение 4 недель значительно снижалась боль в покое, боль, связанная с нагрузкой весом при активном движении, улучшалась функция суставов, снижалось дополнительное потребление анальгетиков [46]. В открытом многоцентровом исследовании была показана отдаленная эффективность лорноксикама при приеме 8 мг два раза в день в течение 12 месяцев пациентами пожилого возраста (средний возраст 71 год). Через 1 месяц и 12 месяцев индекс Lesquesna улучшился по сравнению с исходным на 20% и 45% соответственно, баллы болезненности на 25% и 55% соответственно. Врачи оценили улучшение минимум как «хорошее» у 58% пациентов с остеоартритом спустя 1 месяц и у 69% пациентов спустя 12 месяцев [37].
В России исследования эффективности лорноксикама при ревматоидном артрите и остеоартрите проводились в Институте ревматологии РАМН. 40 пациентов получали лорноксикам в суточной дозе 16 мг в течение 4 недель. Клиническая эффективность по совокупности показателей была расценена исследователями как значительное улучшение и улучшение у 82% больных [7]. Высокая эффективность применения лорноксикама при ревматоидном артрите и деформирующем остеоартрозе подтверждена исследованиями Санкт-Петербургской государственной медицинской академии и Новосибирского городского диспансера клинической иммунологии [6, 9].
Другие возможные области применения лорноксикама (ксефокама)
Лорноксикам может применяться и в других ситуациях, в которых показано применение НПВП. Есть сообщения о возможности применения лорноксикама в комплексной терапии больных хроническим вирусным гепатитом для повышения эффективности и безопасности интерферонотерапии [13].
Переносимость
Прием препаратов группы оксикамов «первого поколения» (пироксикам, теноксикам) сопровождается достаточно высокой частотой осложнений со стороны ЖКТ, что может быть связано с большой длительностью периода полувыведения (20-70 часов), не позволяющей защищающим желудок простагландинам возвращаться до нормального уровня в интервале между введениями препарата, низким сродством к сывороточному альбумину и большим объемом распределения [5, 15, 16]. Однако лорноксикам по данным свойствам принципиально отличается от традиционных оксикамов — у него короткий период полувыведения, позволяющий восстанавливать протекторный уровень простагландинов ЖКТ, высокая степень средства к альбумину сыворотки, низкий объем распределения. Таким образом, можно предположить, что лорноксикам обладает значительно более благоприятным профилем токсичности по сравнению с другими НПВП группы оксикамов.
Это предположение было подтверждено результатами клинических исследований. В исследованиях первой фазы этот препарат не оказывал влияния на жизненно важные параметры или данные лабораторных тестов. Побочные эффекты со стороны ЖКТ, характерные для большинства НПВП, встречались менее часто и в меньшей степени, чем при использовании индометацина или напроксена [38, 39]. Каких-либо воздействий на функцию почек не обнаружено. Отмечены небольшие изменения показателей свертываемости крови (незначительное увеличение времени гемостаза и времени коагуляции, а также небольшое уменьшение тромболитической активности), однако эти изменения были в пределах нормальных показателей [5].
У 4349 пациентов, участвовавших в исследованиях лорноксикама (примерно 300 пациентов принимали его 4-6 месяцев, 600 — более одного года), общая частота побочных эффектов составила 24,9%. Жалобы со стороны ЖКТ были наиболее частыми (отмечались у 16,4% пациентов) и сводились в основном к диспепсии, болям в животе, тошноте, рвоте, диарее. Жалобы общего порядка встречались с такой же частотой, как и при использовании плацебо.
Побочные воздействия на мочевую систему были отмечены лишь у 0,5% пациентов, на печень — у 0,3% пациентов [47]. Побочные воздействия на ЖКТ прямо связаны с дозой препарата. При длительном лечении пожилых пациентов риск развития побочных эффектов в отношении ЖКТ не увеличивался по сравнению с пациентами зрелого и молодого возраста. Не выявлено различий по этому показателю в зависимости от пола пациентов. Также не выявлено достоверных отличий в частоте побочных эффектов у пациентов с заболеваниями ЖКТ в анамнезе и без таковых.
Большинство побочных эффектов возникают в течение первого месяца лечения лорноксикамом. Каких-либо характерных изменений лабораторных параметров при приеме лорноксикама отмечено не было [5].
Сообщения о случаях смерти, связанных с применением лорноксикама, отсутствуют [5].
При проведении сравнительных исследований показано, что частота побочных эффектов такого безопасного препарата, как диклофенак, занимает промежуточное место между аналогичными показателями при приеме 4 мг лорноксикама три раза в день и 8 мг лорноксикама два раза в день [47]. Частота побочных эффектов при приеме лорноксикама была ниже, чем при приеме напроксена, пироксикама, индометацина [7, 12, 47]. При анализе частоты тяжелых побочных реакций со стороны ЖКТ при пероральном приеме различных НПВП данный показатель был наиболее низким у лорноксикама (0,9%), затем следовал мелоксикам (1,7%), диклофенак и лироксикам (по 4,9%), напроксен (7,8%) [19].
При исследованиях на животных не выявлено тератогенности, канцерогенности лорноксикама [5]. Токсическая доза (LD50), выявленная экспериментально на животных, была очень высока и составляла при пероральном введении не менее 10 мг/кг [40].
Заключение
Таким образом, лорноксикам является мощным обезболивающим и противовоспалительным препаратом с документально подтвержденной эффективностью при лечении разнообразных состояний, сопровождающихся болями и воспалением.
Биодоступность пероральных форм практически аналогична парентеральным и составляет 90-100%. Лорноксикам хорошо накапливается в очагах воспаления и в синовиальной жидкости. Есть данные о возможном предотвращении лорноксикамом деструкции хрящевой ткани.
Доказана высокая клиническая эффективность лорноксикама при ревматоидном артрите, остеоартрите, болях в пояснице, онкологических болях, послеоперационных болях. Возможно использование лорноксикама при мигрени, болевом синдроме у больных опийной наркоманией, при костно-суставных болях, связанных с переломами. Лорноксикам оказался, по крайней мере, эквивалентен, а по данным многих исследований, и более эффективен, чем такие НПВП, как диклофенак, индометацин, пироксикам, напроксен, кеторолак. При применении лорноксикама парентерально при послеоперационных болях его анальгетический эффект не уступал средним дозам опиоидов (морфин, трамадол). Лорноксикам может использоваться в качестве монотерапии, а в таких ситуациях, как послеоперационные, онкологические боли, — совместно с опиоидами, что позволяет снизить дозу последних благодаря синергизму.
Оптимальная доза лорноксикама при болевом синдроме составляет 8 мг два раза в день. При выраженном болевом синдроме вначале необходим прием ударной дозы 16 мг, далее, по мере надобности, дозу увеличивают с шагом 8 мг, доводя ее в первые 24 часа до 32 мг, в дальнейшем принимают по 8 мг два раза в сутки. При лечении ревматоидных заболеваний доза подбирается индивидуально, но не менее 4 мг два раза в день. Более высокие дозы — 8 мг три раза в день — использовались у пациентов с костными метастазами.
Лорноксикам хорошо переносится, степень его безопасности аналогична диклофенаку и превышает таковую у индометацина, пироксикама, напроксена. В отличие от такого анальгетика, как кеторолак, возможно длительное применение лорноксикама.
Таким образом, лорноксикам (ксефокам) как новый представитель группы НПВП представляет собой существенное дополнение к имеющимся фармакологическим средствам для лечения состояний, сопровождающихся болями и воспалением, и может широко использоваться в практике врачей различных специальностей (включая неврологов, нейрохирургов, психиатров).
1. Брюзгин В. Грамотная терапия уменьшает болевой синдром практически у всех больных раком / V Российский национальный конгресс «Человек и лекарство». Симпозиум «Обезболивание: современные клинические подходы и препараты» // Медицинский курьер. — 1998. — С. 52-53.
2. Фисенко В. Нестероидные препараты могут стать основными в лечении боли // Медицинский курьер. — 1998. — С. 53-54.
3. Браньенберг П.Э. Ксефокам не менее эффективен, чем морфий, но более безопасен // Медицинский курьер. — 1998. — С. 54-55.
4. Осипова И. Превентивное лечение снимает остроту болевого синдрома // Медицинский курьер. — 1998. — С. 58.
5. Лорноксикам. Новый обезболивающий и противовоспалительный препарат. Монография по продукту. — Никомед Фарма. JPbureau. — Июнь, 1998.
6. Арьев А.Л. Боль и ее лечение. — №10. — С. 26.
7. Балабанова P.M. Боль и ее лечение. — №10. — С. 15.
8. Брюзгин В.В. Боль и ее лечение. — №10. — С. 26.
9. Долгалева А.А. Боль и ее лечение. — №10. — С. 18.
10. Кузнецов А.К. Боль и ее лечение. — №10. — С. 22.
11. Куликова Р.Л. Боль и ее лечение. — №10. — С. 26.
12. Павленко С.С. Боль и ее лечение. — №10. — С. 4.
13. Радченко В.Г. Боль и ее лечение. — №10. — С. 25.
14. Справочник Видаль . — 1999. — Е -129.
15. Martindale. The Extra Pharmacopoeia, 31st Edition. — London, 1996.
16. Proceedings of round table on lornoxicam. — Vienna, May, 1998.
17. COX-2 inhibitors will have major impact. — Scnp. №2407. — 1999. — Р. 24.
18. Staunstrup H. et al. Abstract, 8th World Congress on Pain, IASP. — Vancouver, August. — 1996.
19. Distel et al. Inflammopharmacology. — 1996. — 4. — 71-81 and Summary part IV, June 96, F. Kursten
20. Rosenov D.E., Albrechtsen M. and Stoike D. A comparison of patient-controlled analgesia with lornoxicam versus morphine in parents undergoing lumbar disk surgery // Anesthesia and. Analgesia. — 1998. — 86. — 1045-50.
21. McCormack K. The spinal actions of nonsteroidal anti-inflammatory drugs and the dissociation between their anti-inflammatory and analgesic effects // Drugs. — 1994. — 47, Suppl. 6. — 28-45.
22. McCormack K. Non-steroidal antiinflammatory drugs and spinal nociceptive processing // Pain. — 1994. — 59. — 6-43.
23. Pruss T.P., Stroissnig H., Radnofer-Welte S. et al. Overview of the pharmacological properties, pharma-cokinetics and animal safety assessment of lornoxicam // Postgrad Med J. 1990. — 66, Suppl. 4. — S. 18-21.
