Международный неврологический журнал 1(1) 2005
Вернуться к номеру
Взаимосвязь между лечением вальпроевой кислотой, ламотриджином и топираматом и прогнозом идиопатических генерализованных эпилепсий
Авторы: А. Николсон, Hope Hospital, Stott Lane, Salford, UK; Р.Е. Эплетон, Roald Dahl EEG Unit, Alder Hey Children’s Hospital, Liverpool, UK; Д.В. Чадвик, Д.Ф. Смит, The Walton Centre for Neurology and Neurosurgery, Fazakerley, Liverpool, UK
Рубрики: Неврология
Разделы: Клинические исследования
Версия для печати
Цель: исследовать большую группу пациентов с идиопатической генерализованной эпилепсией (ИГЭ) и оценить в целом процент ремиссии для ИГЭ и малых эпилептических приступов среди основных клинических групп. Изучены случаи ремиссии при приеме вальпроевой кислоты, ламотриджина, топирамида и комбинации данных противоэпилептических препаратов; исследованы факторы, определяющие прогноз.
Методы: Все пациенты с ИГЭ определены на основании компьютерной базы данных и данных ЭЭГ в крупных эпилептических клиниках для взрослых и детей. Данные исследования зарегистрированы ретроспективно в виде демографической и клинической информации, описания видов приступов и синдромов заболевания, подробностей противоэпилептического лечения и случаев ремиссии.
Результаты: из 962-х пациентов 54,3% достигли периода ремиссии сроком 1 год благодаря монотерапии (52,1%) вальпроевой кислотой с уменьшением частоты приступов при приеме ламотриджина и топирамата (16,7% и 34,6%, ретроспективно). Комбинация вальпроевой кислоты и ламотриджина вызывала ремиссию в 15,3% случаев. Порядок последовательности применения противоэпилептических препаратов был наиболее предрешающим фактором, определяющим положительный прогноз лечения. В стадии ремиссии после отмены противоэпилептических средств случаи рецидивов высокие (79,9%), особенно при ювенильной миоклонической эпилепсии (93,6%).
Заключение: Вальпроевая кислота — возможно наиболее эффективный противоэпилептический препарат для лечения ИГЭ. Комбинированная терапия может быть применена в случае неэффективности монотерапии вальпроевой кислотой, что предпочтительнее, чем переход на альтернативную монотерапию [1, 2]. У многих взрослых пациентов с ИГЭ противоэпилептическая медикаментозная терапия должна быть пожизненной [2].
Несмотря на то что идиопатическая генерализованная эпилепсия (ИГЭ) большей частью проявляется в детстве и юности, она встречается приблизительно у 30% пациентов эпилептических клиник для взрослых. Выделяют несколько степеней различий в диагностических группах, но в целом, при лечении вальпроевой кислотой, можно увидеть хорошую реакцию на соответствующее противоэпилептическое медикаментозное лечение. Тем не менее, 20-30% больных остаются рефрактерными к лечению.
Рандомизированные контролируемые клинические исследования — золотой стандарт в определении эффективной и толерантной противоэпилептической терапии. Как правило, рандомизированные контролируемые исследования медикаментозного лечения эпилепсии сравнивались с результатами противоэпилептических препаратов и плацебо, а не с другими противоэпилептическими препаратами. При ИГЭ сравнительные исследования особенно редки [3-5]. Проводилось только небольшое количество рандомизированных контролируемых исследований у пациентов с ИГЭ, частично потому, что ответная реакция на прием вальпроевой кислоты положительная, а также из-за трудности вовлечения детей и подростков в клинические исследования. Во вновь диагностируемых группах есть пациенты, вовлеченные в исследования с ИГЭ, но в ходе этих исследований трудно идентифицировать подгруппы. Метаанализы могут обрабатывать данные для большего количества пациентов. Но метаанализ исследования с карбамазепином, в сравнении с монотерапией вальпроевой кислотой, выдвигает на первый план проблему неправильной классификации эпилептических синдромов в пределах клинических исследований, что приводит к выводу о сомнительном преимуществе вальпроевой кислоты [6].
Тем не менее, несколько данных, отличных от результатов, полученных в ходе клинических опытов, обосновывают лечение наших пациентов с ИГЭ. Несмотря на это, общепринято, что вальпроевая кислота является препаратом выбора для лечения ИГЭ, так как ее эффективность доказана в группах пациентов с генерализованными приступами [7]. Cуществуют некоторые сомнения, связанные с возможными побочными эффектами вальпроевой кислоты, особенно у женщин детородного возраста [8-12]. Имеются данные исследований на животных и клинические данные об эффективности более новых противоэпилептических препаратов ламотриджина и топирамата при ИГЭ [13-16]. Основываясь на последних данных, мы не можем определить, имеют ли новые препараты преимущество по сравнению с вальпроевой кислотой в пределах толерантности и эффективности у пациентов, рефрактерных к вальпроевой кислоте, или это особая подгруппа пациентов, у которых мы должны запланировать применение новейших противоэпилептических препаратов как первоначальную терапию.
Наша цель в этом исследовании была изучить группу пациентов с ИГЭ, оценить все случаи ремиссии ИГЭ и специфических эпилептических синдромов, определить случаи ремиссии при приеме вальпроевой кислоты, ламотриждина, топирамата и комбинации этих препаратов. Мы также хотели определить факторы, прогнозирующие исход, и выяснить, является ли ремиссия эпилепсии со временем подобной ИГЭ и фокальным эпилепсиям [17].
Методы
Данные о пациентах эпилептической клиники Mersey компьютеризированы, начиная с 1989 года, внесены демографические сведения, подробности диагностики и лечения. Пациенты ИГЭ определялись на основании этой базы данных в Walton Centre. В клинике, курируемой DS, пациенты взяты из данных картотеки. Дети отобраны на основании изучения диагностических кодов из истории болезни и электроэнцефалографических данных (ЭЭГ). Синдромальная диагностика эпилепсии проведена у каждого пациента на основании, по возможности, клинических и ЭЭГ-данных, в соответствии с классификацией Международной Противоэпилептической Лиги [18]. Но, учитывая более широкую представленность клинических описаний, были включены субсиндромы, включающие детскую абсанс-эпилепсию ДАЭ, выделяющуюся в ювенильную миоклоническую эпилепсию (ЮМЭ), трансформацию ювенильной абсанс-эпилепсии (ЮАЭ) в ЮМЭ, идиопатическую абсансную или миоклоническую ИГЭ, не укладывающуюся в картину распознанных субсиндромов, и миоклонию век с абсансами. Были исследованы отличительные признаки у всех идентифицированных пациентов. Для включения в исследования необходимо:
— клинические критерии диагноза ИГЭ, полностью описанные в историях болезни, даже если нет по данным ЭЭГ распространенной спайк-волны;
— включены также пациенты без возрастного предела, при котором начинается ИГЭ (до 2-х или после 26-ти лет), если было подозрение, что диагноз скрытый.
Пациенты были исключены при недостатке критериев или если база данных или истории болезни оказались недоступны. Из истории болезни были взяты следующие данные: основные демографические данные, семейный анамнез эпилепсии в первом колене, анамнез фебрильных судорог, типы приступов и давность их начала, данные ЭЭГ, анамнез противоэпилептического лечения и наиболее длинный межприступный период при каждом медикаментозном противоэпилептическом режиме.
Результаты
В общем, в исследования включены 962 пациента с ИГЭ в трех центрах. Среди них 408 пациентов мужского пола и 554 — женского. Из них 117 были взяты из педиатрической клиники. Таблица 1 суммирует частоту субсиндромов ИГЭ в пределах популяции. Семейный анамнез эпилепсии отмечался в первом колене родственников у 216-ти пациентов (22,5%), предшествующие фебрильные судороги — у 105-ти пациентов (10,9%). Данные ЭЭГ были доступны у 902-х пациентов, при этом генерализованная спайк-волна отмечена у 613 (68%). У всех 257-ми пациентов (28,5%) — фотопароксизмальная ответная реакция (наиболее общий признак при ювенильной миоклонической эпилепсии (ЮМЭ)) и изолированные клонико-тонические приступы (32,6%), наименее общие при детской абсанс-эпилепсии (ДАЭ), и генерализованные клонико-тонические судороги при пробуждении (19,2% и 20% соответственно).
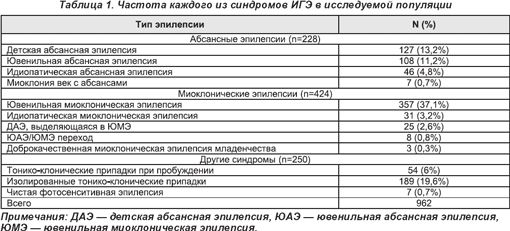
Полная информация по применению противоэпилептических препаратов была доступна у 787-ми пациентов, включая информацию о периодах ремиссии по каждому. Из 899-ти, которые диагностировались более 1-го года, 488 (54,3%) достигли периода ремиссии 1 год в разное время. Чаще всего это достигнуто при монотерапии вальпроевой кислотой (52,1%); реже наблюдалось при монотерапии ламотриджином и топираматом (16,7% и 34,6% соответственно). Наиболее часто использована комбинация вальпроевой кислоты и ламотриджина, что вызвало ремиссию у 15,3% пациентов (табл. 2). Отмечено 334 пациента (37,2%), пребывавших в ремиссии предыдущие 12 месяцев и продолжающих находиться в ней и в дальнейшем.
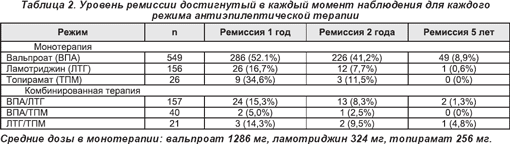
Если лечение вальпроевой кислотой было неэффективным, она была заменена ламотриджином (у пациентов, не получавших ранее ламотриджин), 6 из 44-х пациентов достигли ремиссии (13,6%). Это отмечалось только у тех пациентов, которые прекратили лечение вальпроевой кислотой из-за побочных эффектов, тогда как у тех, у кого она была неэффективна для контроля приступов, ремиссия не наблюдалась.
После того как к вальпроевой кислоте был добавлен ламотриджин, 10 из 83 (12%) пациентов достигли ремиссии, независимо от причины неудачи в приеме вальпроевой кислоты. В обратной ситуации (добавить или назначить вальпроевую кислоту после неэффективности ламотриджина) количество исследуемых было очень малым, но 3 из 6-ти достигли ремиссии, переключившись на вальпроевую кислоту.
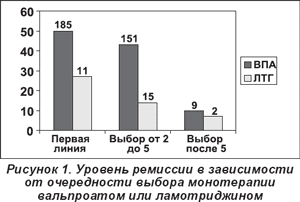
Успех каждого противоэпилептического препарата зависит также от последовательности, в которой давались препараты. Каждый препарат имел больше шансов вызвать ремиссию, когда был дан как первый препарат для лечения по сравнению с режимами от 2-х до 5-ти или более 5-ти режимов (рис. 1). Результат не зависел от того, где лечение было начато, в стадии ремиссии в любое время встречается 51,4% пациентов, диагностированных в научных центрах (114 из 222) по сравнению с 55,4% (375 из 677), диагностированными в других местах. Однако отличие заключалось в начальной противоэпилептической терапии и зависело от того, где это лечение было начато. Почти 90% пациентов, которым впервые проводилось лечение в одном из научных центров, начали с вальпроевой кислоты или ламотриджина. Только 60% пациентов, диагностированных вне научных центров, начали лечение с вальпроевой кислоты или ламотриджина, 30% этих пациентов начали лечение с карбамазепина.
Факторы, обусловливающие прогноз, отражены в таблице (табл. 3).
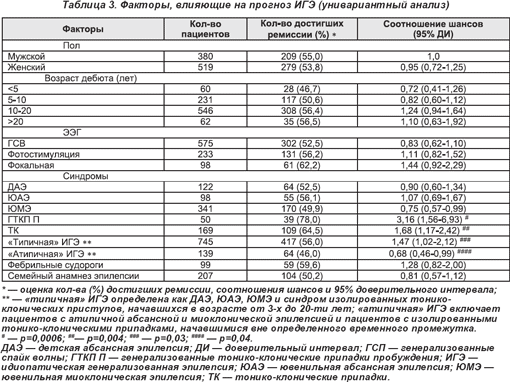
Пациенты с генерализованными клонико-тоническими приступами при пробуждении и с изолированными клонико-тоническими приступами (коэффициент преимущества (КП) 3,16 и 1,62 соответственно) имели лучшие результаты. Факторы, определяющие плохой прогноз: возраст пациентов до 5-ти лет (КП, 0,72) или «атипичные» проявления. В «типичных» случаях ремиссии при монотерапии составляли 48,3% (262 из 543-х) при приеме вальпроевой кислоты и 14,4% (24 из 167-ми) — ламотриджина. В «атипичных» случаях эти данные уменьшились до 37,5% (39 из 104-х) и 11,6% (5 из 43-х) соответственно.
164 пациента пытались отменять противоэпилептические препараты во время ремиссии и возвращались к приему в 79,9% случаев (131). У пациентов, отменивших противоэпилептическую терапию, период последействия длился не менее 6-ти месяцев. 84 из них (51,2%) находились в ремиссии на текущий момент (42 (25,6%) были без противоэпилептических препаратов). Рецидивы отмечались преимущественно у пациентов с ЮМЭ (44 из 47 (93,6%)), и были менее распространенными при ДАЭ (19 из 29-ти (65,5%) и ЮАЭ (13 из 19 (68,4%)).
Обсуждение
В этом исследовании есть и недостатки. Возможно, необъективно отобрано количество пациентов. Первоначально учитывалось, что в пределах специализированных центров, возможно, не были представлены подгруппы с очень хорошими результатами, но в каждом случае сделана попытка обеспечить наиболее полные данные путем использования компьютерной базы данных и историй болезни центра так же, как и данными других клинических учреждений. Пациенты без типичных изменений ЭЭГ генерализованного паттерна спайк-волны включались в исследование, если клинический диагноз, установленный на демографических и семиотических данных, был безоговорочным. При наличии каких-либо сомнений в обосновании диагноза пациент исключался, в связи с этим уменьшилось количество пациентов без ИГЭ. Этот подход приближает исследования к клинической практике.
Случаи ремиссии встречались в исследовании реже, чем это обычно описывается для ИГЭ [2]. Это характерно для большинства пациентов клиник для взрослых и для них также характерна ИГЭ, продолжающаяся в течение всей жизни. Добавим, что у детей, проходивших лечение в специализированных детских неврологических клиниках, может ожидаться относительно рефрактерная эпилепсия. Возможно, что учтены не все случаи ремиссии, и для того, чтобы уравновесить эти потери, случаи эпилепсии должны были бы находиться под тщательным контролем. Также следует напомнить, что эта отобранная популяция, вероятно, представляет собой наиболее тяжелые случаи. Поэтому данное исследование не дает симптомов прогноза в популяциях больных с ИГЭ в общем, но показывает, что значительное количество пациентов с ИГЭ остаются рефрактерными к противоэпилептической медикаментозной терапии.
Наличие многих противоэпилептических средств предполагает также использование и других препаратов в данной популяции, а не только вальпроевой кислоты и ламотриджина. Множество препаратов предназначено для купирования соответствующих приступов (например этосуксимид и бензодиазепины), более старые препараты (например фенобарбитон) и неспецифические препараты применяются, в тех случаях, если начальный синдром не распознается как ИГЭ. Эта ошибка диагностики не очень характерна для специализированных центров, но все случаи ремиссии были похожи, когда назначалась соответствующая противоэпилептическая терапия, предполагающая сходные клинические проявления между двумя группами.
Один из наиболее существенных факторов в оценке эффективности противоэпилептических препаратов при ИГЭ состоит в последовательности, с которой дается препарат (рис. 1). Вывод согласуется с предыдущей работой обо всех прогнозах эпилепсии в исследованиях, состоящих в большей степени из пациентов с парциальной (очаговой) эпилепсией [17]. Впервые показано в исследованиях, проведенных исключительно у пациентов с ИГЭ.
Фактором, прогнозирующим плохой исход, был возраст начала приступов у детей до 5-ти лет. Диагноз преимущественно классифицирован либо как «идиопатический абсанс», либо как миоклоническая эпилепсия, так как он не соответствует общепринятой классификации. Это могут быть пациенты с меньшим стажем приступов абсанс или миоклонической эпилепсии и без каких-либо отклонений, а, с другой стороны, те, кто соответствует клиническому диагнозу ИГЭ, представляющему генотипические варианты с плохим прогнозом. Эта группа включает также несколько пациентов с менее распространенными синдромами, известными своими плохими прогнозами; такими как миоклония век с абсансами [19]. Если пациент с типичной ИГЭ только один раз включен в этот разбор (возраст начала приступов старше 3-х лет), в таком случае процент ремиссии был выше, около 62,5% (15 из 24); коэффициент преимущества 1,42 (95% уверенный интервал, 0,57-3,7). Худший прогноз, общий для пациентов, не имеющих типичных синдромных диагнозов, был также обоснован.
Общие результаты при абсансных эпилепсиях были хуже, чем предполагалось в популяции с данным диагнозом. Это может быть отчасти пропорциональным отражением у взрослых, у которых эпилепсия длится с детства. Синдром тонико-клонических приступов при пробуждении имел высокую степень прогноза, который подтверждается предыдущими исследованиями [1].
Традиционным противоэпилептическим препаратом выбора при лечении ИГЭ является вальпроевая кислота. Тем не менее, с введением новых препаратов, таких как ламотриджин и топирамат, возрастает возможность избежать побочных воздействий и тератогенности вальпроевой кислоты. В результате ламотриджин — сейчас наиболее пропагандируемый препарат для лечения ИГЭ у женщин.
Нет сравнительных исследований, демонстрирующих, так ли эффективны новые препараты при ИГЭ, как и вальпроевая кислота, или предлагаются преимущества удовлетворительной переносимости при длительном приеме. Наше исследование предоставляет доказательства, что ламотриджин не столь эффективен, как вальпроевая кислота в этих условиях. Несмотря на то что нет прямого сопоставления между длительностью эпилепсии и возможной необъективностью в выборе, частота ремиссии для ламотриджина ниже (16,7%), чем для вальпроевой кислоты (52,1%). Хорошо известно, что реакция на первый противоэпилептический препарат — важный предиктор исхода [20], но даже если препарат дан как первый, считалось, что результаты отличались значительно между ламотриджином и вальпроевой кислотой (рис. 1), несмотря на то что количество пациентов в группе ламотриджина было сравнительно малым. Различия между двумя группами могут также влиять на реакцию на специфические медикаменты.
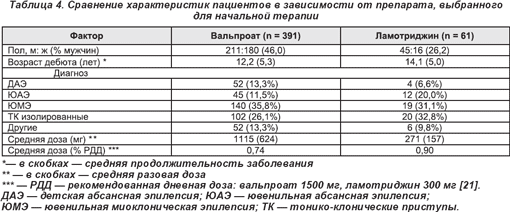
Пациенты с ДАЭ хуже отвечали на терапию ламотриджином, чем вальпроевой кислотой, в первой линии выбора терапии, однако использование 2-х препаратов при абсансной эпилепсии было сходным в обеих группах (табл. 4). Пациентам женского пола ламотриджин был более подходящим как первый препарат лечения, несмотря на это маловероятно влияние на исход (табл. 3, 4). Анализ результатов добавления или замены вальпроевой кислоты на ламотриджин согласуется с тем, что ламотриджин является менее эффективным. Мы делаем выводы, что в случае недостаточной эффективности вальпроевой кислоты, замена на ламотриджин неуместна, чтобы получить эффект в этой ситуации, нужно добавить второй противоэпилептический препарат. Если, тем не менее, от приема вальпроевой кислоты приходится отказываться из-за побочных эффектов, тогда замена на альтернативный препарат обоснована.
Топирамат представляется полезной альтернативой с обнадеживающими результатами, но количество пациентов очень мало для определения четких выводов. Общепринятые для назначения противоэпилептические препараты, комбинируемые при ИГЭ, — вальпроевая кислота и ламотриджин, так как очевиден их синергизм [22, 23]. Частота ремиссий в этом исследовании выше (15,3%), чем обычно ожидается при комбинации противоэпилептических препаратов [24], и обеспечивает дальнейшее основание для эффективности этой конкретной комбинации.
Дилемма в том, что оба — и пациент, и врач — сомневаются, стоит ли пытаться отменять противоэпилептические препараты в период ремиссии. Сложно распространить данные на ИГЭ из предыдущих исследований, проведенных большей частью у пациентов с парциальными эпи-приступами. В нашем исследовании степень рецидивов, следующих после отмены противоэпилептических препаратов, была 79,9%, что подтверждает положение о том, что многие пациенты с ИГЭ нуждаются в пожизненной терапии. Это может быть даже недооценено при истинных рецидивах, так как некоторые пациенты могли иметь рецидивы, но не возвращались в клиники.
Синдромный диагноз имел значимое влияние на степень рецидивов, и данные, полученные нами, подтверждают, что ремиссия после отмены противоэпилептических препаратов — редкий случай при ЮМЭ [25]. Степень рецидивов при всех ИГЭ синдромов в этой популяции высока, и это нужно учитывать, когда даются рекомендации взрослым пациентам с ИГЭ, находящимся в ремиссии и намеревающимся отменить лечение.
Заключение
Это первое опубликованное исследование такого большого количества пациентов с ИГЭ, содержащее предусмотренные данные по аспектам прогноза и лечения недостаточно изученных форм эпилепсии. Наиболее важным фактором, влияющим на исход, является порядок назначения противоэпилептических препаратов. Вальпроевая кислота все еще может быть наиболее эффективным препаратом для лечения ИГЭ. По данным некоторых пациентов, более полезными являлись другие имеющиеся в наличии средства. Комбинированная терапия должна быть начата в том случае, если адекватная монотерапия вальпроевой кислотой неэффективна, и это предпочтительней, чем переход на альтернативную монотерапию.
Вальпроевая кислота с ламотриджином является исключительно успешной комбинацией, когда один противоэпилептический препарат неэффективен. Рецидивы при попытке отмены противоэпилептических препаратов характерны для этой популяции, особенно для пациентов с ЮМЭ, у которых противоэпилептическая медикаментозная терапия должна быть пожизненной.
1. Christe W, Janz D.Sodium valproate in idiopathic generalized epilepsies // Boll. Lega Ital. Epil., 1988. — 61. — P. 11-15.
2. Janz D., Christe W. Generalized epilepsies. In Resor S.R., Kutt H. edc. The medical treatment of epilepsy. — New York: Marcel Dekker. — 1992. — P. 145-62.
3. Sato S., White B.G., Perny J.K. et al. Valproic acid versus ethosuximide in the treatment of absence seizures // Neurology. — 1982. — 32. — P. 157-63.
4. Callaghan N. O'Hare J., O'Driscoll D. et al. Comparative study of ethosuximide and sodium valproate in the treatment of typical absence seizures (petit mal) // Dev. med. Child. Neural. — 1982. — 24. — P. 830-6.
5. Wilder B.J., Ramsay R.E., Murphy J.V. et al. Compasion of valproic acid and phenytoin in newly diagnosed tonic-clonic seizures // Neurology. — 1983. — 33. — P. 1474-6.
6. Marson A.G., Williamson P.R., Hutton J.L. et al. Carbamazepine versus valproate monotherapy for epilepsy // Epilepsia. — 2002. — 43. — P. 505-13.
7. Rowan A.J. Valproate. In: Engel J., Pedley T.A., eds. Epilepsy. Comprehensive textbook. — Philadelphia: Lippincott-Raven, 1997. — P. 1599-607.
8. Omtzigt J.D.C., Los F.J., Grobbee D.E. et al. The risk of spina bifida aperta after first-trimester exposure to valproate in a prenatal cohort // Neurology. — 1992. — 42 (suppl 5). — P. 119-25.
9. Moore S.J., Turnberry P.D., Quinn A. et al. A clinical study of 57 children with fetal anticonvulsant syndrome // J. Med. Genet. — 2000. — 37. — P. 489-97.
10. Adab N., Jacoby A., Smith D.F. et al. Additional educational needs in children born to mothers with epilepsy // J. Neurol. Neurosurg Psychiatry. — 2001. — 70. — P. 15-21.
11. Duncan S. Polycystic ovarian syndrome in women with epilepsy: a review // Epilepsia. — 2001. — 42 (suppl 3). — P. 60-5.
12. Biton V., Mirza W., Montouris G. et al. Weight change associated with valproate and lamotrigine monotherapy in patients with epilepsy // Neurology. — 2001. — 56. — P. 172-7.
13. Hosford D.A., Wang Y. Utility of the lethargic (Ih/Ih) mouse model of absence seizures in predicting the effects of lamotrigine, vigabatrin, tiagabine, gabapentin, and topiramate against human absence seizures // Epilepsia. — 1997. — 38 (4). — P. 408-14.
14. Biton V., Montouris G.D., Ritter F. et al. A randomized, placebo-controlled study of topiramate in primary generalized tonic-clonic seizures // Neurology, 1999. — 52. — P. 1330-7.
15. Leach J.P., Brodie M.J. Lamotrigine: clinical use. In: Levy R.H., Mattson R.H., Meldrum B.S., eds. Antiepileptic drugs. — New York: Raven Press, 1995. — P. 889-95.
16. Kramer L.D., Reife R.A. Topiramate. In: Engel J, Pedley TA, eds. Epilepsy. A comprehensive textbook. — Philadelphia: Lippincott- Raven, 1997. — P. 1593-8.
17. Annegers J.F., Hauser W.A., Elveback L.R. Remission of seizures and relapse in patient with epilepsy // Epilepsia. — 1979. — 20. — P. 729-37.
18. Engel J. ILAE Commission report. A proposed diagnostic scheme for people with epileptic seizures and with epilepsy: report of the ILAE task force on classification and terminology //
Epilepsia. — 2001. — 42. — P. 796-803.
19. Appleton R.E., Panayiotopoulos C.P., Acomb A.B. et al. Eyelid myoclonia with absences; an epilepsy syndrome // J. Neurol. Neurosurg Psychiatry. — 1993. — 56. — P. 1312-16.
20. Kwan P., Brodie M.J. Early identification of refractory epilepsy // N. Engl. J. Med. —2000. — 432. — P. 314-19.
21. World Health Organisation. Guidelines for ATC classification and DDD assignment. — Geneva: WHO, 1996.
22. Besag F.M.C., Panayiotopoulos C., Chivers F. et al. Therapeutic interaction of lamotrigine with valproate and suximides // Epilepsia. &‐ 1995. — 36 (suppl.3). — P. 116.
23. Brodie M.J., Yuen A.W.C., 105 Study Group. Lamotrigine substitution study: evidence for synergism with sodium valproate? // Epilepsy Res. — 1997. — 26. — P. 423-32.
24. Mattson R.H. Drug treatment of uncontrolled seizures // Epilepsy Res. Suppl., 1992. — 5. — P. 29-35.
25. Schmidt D. Response to antiepileptic drugs and the rate of relapse after discontinuation in juvenile myoclonic epilepsy. In: Schmitz B, Sander T, eds. Juvenile myoclonic epilepsy. The Janz syndrome. — Petersfield: Wrightson Biomedical. — 2000. — P. 111-20.
‐
