Газета «Новости медицины и фармации» Гастроэнтерология (407) 2012 (тематический номер)
Вернуться к номеру
Хирургическое лечение неспецифического язвенного колита и болезни Крона
Авторы: Г.Е. Полунин, Ф.И. Гюльмамедов, И.Е. Седаков, Донецкий национальный медицинский университет им. М. Горького
Версия для печати
Вопросы хирургического лечения больных с тяжелыми формами неспецифического язвенного колита (НЯК) и болезни Крона (БК) толстой кишки (ТК) и в настоящее время привлекают к себе внимание хирургов разных стран. Это объясняется не только увеличением количества случаев заболеваний, но и отсутствием единого мнения в вопросах хирургической тактики. Если 28,4 % страдающих хроническими формами воспалительных заболеваний кишечника (ВЗК) нуждаются в хирургическом лечении, то при тяжелом течении патологического процесса, особенно при острых формах и тотальном поражении, оно показано почти 60 % пациентов [12].
Обычно больные ВЗК обращают на себя внимание хирурга, когда их состояние начинает прогрессивно ухудшаться. Появляется слабость, высокая температура, боли в животе, понос, обилие крови в кале, в том числе частые ректальные кровотечения. При ректороманоскопии выявляется отечная гиперемированная слизистая с выраженной контактной кровоточивостью, наличием на стенках слизи, фибрина, язв, эрозий. К сожалению, ограничение диагностических возможностей или поздняя диагностика ВЗК могут приводить к серьезным осложнениям. Известны случаи, когда больные неоднократно подвергались лапаротомии в течение одного-двух лет по поводу так называемого «острого живота». Но при ревизии органов брюшной полости обнаруживали небольшое количество экссудата и инъецированность сосудов серозной оболочки ТК. Операции заканчивались дренированием и ушиванием брюшной полости и противовоспалительной, корригирующей инфузионной терапией в послеоперационном периоде. Поэтому важную роль играет ранняя диагностика ВЗК. По мнению ученых НИИ проктологии России, НЯК следует заподозрить во всех случаях, когда при ректороманоскопии имеется гиперемия слизистой оболочки прямой кишки (ПК) и отсутствие сосудистого рисунка. Пролонгация диагностики ВЗК встречается в 20–25 % случаев.
Существует и экономическая сторона проблемы: пик заболеваемости ВЗК приходится на 20–40 лет, это наиболее работоспособные и общественно активные члены общества [6, 20].
Показания к операции при ВЗК могут быть как абсолютными, так и относительными. Такие осложнения заболевания, как перфорация, профузное кишечное кровотечение, острая токсическая дилатация ТК, кишечная непроходимость считаются абсолютными показаниями.
Несмотря на отсутствие единого мнения об объеме операции при перфорации [4], плохие результаты при простом ушивании дефекта пораженного отдела кишки свидетельствуют о необходимости ее резекции, так как существует реальная опасность возникновения повторных перфораций [1].
Нет единого мнения и по поводу лечения острой токсической дилатации ТК. Существуют работы, свидетельствующие о возможности применения у этой категории больных консервативного лечения [9], однако большинство авторов настаивают только на оперативном. Объем операции при таком осложнении различный: субтотальная резекция толстой кишки с илеостомией или одномоментная колэктомия. Кроме этого, могут быть выполнены двухэтапные оперативные вмешательства: вначале двухствольная илеостомия, а затем колпроктэктомия или илеостомия/колостомия, а затем колэктомия.
Объем операции при кишечной непроходимости выбирается индивидуально. Причиной возникновения кишечной непроходимости при НЯК и БК может быть стриктура тонкой или толстой кишки или развитие опухоли. Риск развития рака ТК (РТК) при НЯК и БК в 7–8 раз выше, чем в общей популяции [3, 8]. К сожалению, сведения о результатах лечения рака ТК, ассоциированного с НЯК и БК, в русскоязычной литературе достаточно скудны [16]. Наличие малигнизации у больных ВЗК является абсолютным показанием к операции, а ее объем зависит от ряда причин: общего состояния больного, распространенности процесса, наличия осложнений и др.
Частота колоректального рака при 5-летнем анамнезе заболевания ВЗК составляет 2–3 %, при 10-летнем — 12 %, при 20-летнем — 23 %, а при продолжительности болезни более 25 лет — 42 % [8].
Клиника рака ТК на фоне ВЗК существенно отличается от обычного течения заболевания. Это связано с тем, что нередко ВЗК маскируют клинику рака ТК или, что случается реже, рак ТК смазывает клинику ВЗК. Под нашим наблюдением находилось 28 пациентов, оперированных по поводу рака ТК, ассоциированного с ВЗК. Необходимо подчеркнуть тот факт, что 6 (21,4 %) пациентов ранее перенесли в клинике обширные резекции ТК по поводу ВЗК, а затем все они были оперированы по поводу РТК, возникшего в сроки от 2 до 16 лет после первой операции. Радикальные операции выполнены у 20 (71,4 %) паллиативные резекции — у 2 (7,1 %), симптоматические вмешательства — у 6 (21,4 %) пациентов. Резектабельность составила 78,5 % [16].
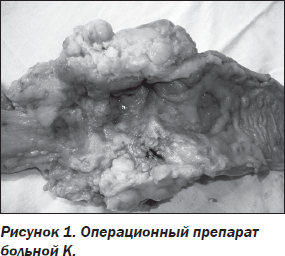 Пример. Больная К., 1979 г.р., поступила в клинику в марте 2009 года с жалобами на сильные схваткообразные боли в правой половине живота, периодическое затруднение отхождения кала и газов, вздутие живота, метеоризм, общую резкую слабость, отсутствие аппетита, позывы на рвоту, прогрессирующее похудание. Страдает болезнью Крона в течение 13 лет, отмечает периодические обострения. Неоднократно лечилась в стационаре, в гастроэнтерологическом отделении по месту жительства. В феврале 2009 года диагностирован синхронный Са правой Т4вN2М1 (Лимф) и левой Т2N2М1 (Лимф) молочной железы IV ст. (слева и справа ЦЗ-железистый Са, mts подмышечные и надключичные л/у). 05.03.2009 года выполнена двусторонняя лапароскопическая тубоовариоэктомия. Во время операции обнаружена опухоль восходящего отдела ободочной кишки, взята биопсия (ПГИ № 10118-10122: аденокарцинома). Проведен курс эндолимфатической ПХТ по схеме ЦМФ: метотрексат СОД 100 мг, циклофосфан СОД 2,4 г, фторурацил СОД 2,0 г. При поступлении: общее состояние больной тяжелое. Живот симметричный, умеренно вздут. В правых отделах при пальпации определяется болезненный плотный инфильтрат (опухоль) 15 ґ 10 см. 27.03.2009 года больная оперирована. При лапаромии в брюшной полости до 300 мл серозно-геморрагического мутного экссудата без запаха. При ревизии органов брюшной полости выявлено, что имеет место опухоль слепой кишки больших размеров, прорастающая во все слои кишечной стенки (рис. 1). Признаки кишечной непроходимости умеренно выражены. Мобилизована ободочная и подвздошная кишка. Кишка пересечена на границах мобилизации, резецирована. Сформирован дубликатурный илеосигмоанастомоз конец в конец. Гистологический ответ № 17403-420: низкодифференцированная темноклеточная аденокарцинома с глубоким инвазивным ростом до жировой клетчатки с очагами некроза. В краях резекции опухоли нет. В л/у mts низкодифференцированной аденокарциномы. В стенке толстой кишки вне опухоли признаки болезни Крона. Послеоперационный период протекал без особенностей. Выписана в удовлетворительном состоянии.
Пример. Больная К., 1979 г.р., поступила в клинику в марте 2009 года с жалобами на сильные схваткообразные боли в правой половине живота, периодическое затруднение отхождения кала и газов, вздутие живота, метеоризм, общую резкую слабость, отсутствие аппетита, позывы на рвоту, прогрессирующее похудание. Страдает болезнью Крона в течение 13 лет, отмечает периодические обострения. Неоднократно лечилась в стационаре, в гастроэнтерологическом отделении по месту жительства. В феврале 2009 года диагностирован синхронный Са правой Т4вN2М1 (Лимф) и левой Т2N2М1 (Лимф) молочной железы IV ст. (слева и справа ЦЗ-железистый Са, mts подмышечные и надключичные л/у). 05.03.2009 года выполнена двусторонняя лапароскопическая тубоовариоэктомия. Во время операции обнаружена опухоль восходящего отдела ободочной кишки, взята биопсия (ПГИ № 10118-10122: аденокарцинома). Проведен курс эндолимфатической ПХТ по схеме ЦМФ: метотрексат СОД 100 мг, циклофосфан СОД 2,4 г, фторурацил СОД 2,0 г. При поступлении: общее состояние больной тяжелое. Живот симметричный, умеренно вздут. В правых отделах при пальпации определяется болезненный плотный инфильтрат (опухоль) 15 ґ 10 см. 27.03.2009 года больная оперирована. При лапаромии в брюшной полости до 300 мл серозно-геморрагического мутного экссудата без запаха. При ревизии органов брюшной полости выявлено, что имеет место опухоль слепой кишки больших размеров, прорастающая во все слои кишечной стенки (рис. 1). Признаки кишечной непроходимости умеренно выражены. Мобилизована ободочная и подвздошная кишка. Кишка пересечена на границах мобилизации, резецирована. Сформирован дубликатурный илеосигмоанастомоз конец в конец. Гистологический ответ № 17403-420: низкодифференцированная темноклеточная аденокарцинома с глубоким инвазивным ростом до жировой клетчатки с очагами некроза. В краях резекции опухоли нет. В л/у mts низкодифференцированной аденокарциномы. В стенке толстой кишки вне опухоли признаки болезни Крона. Послеоперационный период протекал без особенностей. Выписана в удовлетворительном состоянии.
Относительные показания к оперативному лечению ВЗК отличаются большим разнообразием. Многие считают целесообразным оперативное лечение при острой или быстропрогрессирующей форме НЯК, когда консервативные мероприятия оказываются малоэффективными. Достаточно полно относительные показания сформулированы в работе М.П. Захараша и соавторов [7], которые к ним относят:
— хронические рецидивирующие формы НЯК при тотальном поражении ТК, со стойкой рефрактерностью к консервативному лечению;
— хронические непрерывные формы ВЗК в течение более 10 лет, с тотальным поражением ТК без выраженной тенденции к нормализации морфологического состояния ее слизистой оболочки;
— стероидозависимые, стероидорезистентные формы заболевания;
— выраженную активность воспалительного процесса при наличии язвенного поля и воспалительных псевдополипов (III степень активности);
— наличие высокой степени дисплазии слизистой оболочки ТК;
— задержку роста и развития детей и подростков.
Некоторые авторы к относительным показаниям относят и развитие внекишечных проявлений и осложнений.
Существует мнение о необходимости оперативного вмешательства в более ранние сроки от начала заболевания. При этом чем раньше оперируют больного, тем лучше результаты хирургического лечения [11]. Хирургическое лечение в ранние сроки заболевания, до развития выраженных осложнений приводит к уменьшению числа экстренных операций с 24 до 8 % и снижает летальность больных ВЗК. Добиться хороших результатов операции можно только при своевременном ее выполнении.
В сложной проблеме хирургического лечения ВЗК есть несколько весьма трудных для решения вопросов, имеющих важное практическое значение. В частности, в литературе встречаются разнообразные мнения по поводу объема операции, особенно при тяжелых формах заболевания.
Паллиативные вмешательства (2-ствольная илеостомия, колостомия) как самостоятельный метод лечения не оправдали себя [4]. Наряду с простотой их выполнения был отмечен ряд осложнений. Патологический процесс в толстой кишке почти всегда прогрессирует и может привести к возникновению угрожающих жизни осложнений [21].
Наиболее радикальным методом хирургического лечения, позволяющим добиться полного излечения больных, является колпроктэктомия [19]. Но те задачи, которые стремится решить хирург, нередко оказываются недостижимыми. Это связано с тем, что при тяжелом состоянии больных в первую очередь приходится думать о спасении жизни пациента. Колпроктэктомию больные с тяжелым течением заболевания не всегда могут перенести.
Убедительна в этом отношении точка зрения, согласно которой при решении вопроса о хирургической тактике у больных тяжелыми формами ВЗК необходимо принимать во внимание не только тяжесть общего состояния, но и возможность последующей социальной и медицинской реабилитации.
В 1950 году H.E. Васоn и Н.D. Trimpi была предложена субтотальная проксимальная колэктомия с формированием илеостомы и дистальной сигмостомы. Благодаря работам отечественных и зарубежных ученых, она стала наиболее распространенным хирургическим вмешательством. Операция переносится значительно легче, чем колпроктэктомия, а сохранение хотя бы части ПК оставляет надежды на выполнение в последующем восстановительной операции.
Некоторые авторы, однако, не исключают возможности внутрибрюшной перфорации оставшейся части ПК, возникновения в этом участке обострений, кровотечения, стриктуры, образования злокачественных опухолей, появления внекишечных осложнений [10].
За последние 20 лет в клинике общей хирургии № 1 Донецкого национального медицинского университета им. М. Горького под наблюдением находилось 607 больных ВЗК. Мужчин было 302 (49,8 %), женщин 305 (50,2 %). Больных НЯК было 410 (67,5 %), БК — 197 (32,5 %). Тяжелое течение заболевания выявлено у 219 (36,1 %) пациентов, средней степени тяжести ВЗК было диагностировано у 193 (31,8 %), легкое течение выявлено у 195 (32,1 %) больных. Тотальное поражение ТК установлено у 209 (34,4 %) больных, правостороннее — у 87 (14,3 %) пациентов, левостороннее поражение ТК выявлено у 116 (19,1 %) больных, а воспалительные изменения дистальных отделов ТК были у 139 (22,9 %) пациентов. Сегментарное поражение толстого кишечника было выявлено у 56 (9,2 %) больных. Внекишечные проявления наблюдали у 435 (71,7 %) пациентов.
После углубленного обследования и установления окончательного диагноза было прооперировано 205 больных (33,8 %). По абсолютным показаниям (кровотечение, перитонит, токсическая дилатация ТК, острая кишечная непроходимость, прогрессирование синдрома полиорганной недостаточности) операции проведены 167 (81,5 %) больным. По относительным — 38 (18,5 %). Следует отметить факт сокращения за последние годы количества оперативных вмешательств по относительным показаниям (в среднем на 15,2 %). Больные госпитализировались в клинику в тяжелом состоянии и оперированы в основном в ургентном порядке на 1–2-е сутки.
В зависимости от тяжести состояния больного, наличия осложнений и показаний к операции больным выполняли различные оперативные вмешательства:
— субтотальная колэктомия, илео-, сигмостомия была выполнена у 146 (71,2 %) больных;
— правосторонняя гемиколонэктомия проведена 32 (15,6 %) пациентам;
— сегментарная резекция ТК выполнялась 12 (5,9 %) больным;
— колонпроктэктомия — 10 (4,9 %) больным;
— илеостомия выполнена 5 (2,4 %) пациентам.
Можно сформулировать следующие требования к выполнению операций при ВЗК:
1. Минимальное сокращение времени проведения.
2. Простота и надежность методики выполнения.
3. Максимальное устранение риска возникновения послеоперационных осложнений.
4. Функциональная надежность отдаленных результатов.
Послеоперационная летальность за последние годы снизилась, хотя остается высокой. По нашим данным, в 60–70-е годы она составляла 50–80 %. Летальные исходы наступали у больных с тяжелым течением заболеваний, с измененной иммунной реактивностью и сниженной резистентностью, с наличием осложнений.
Наиболее часто встречались гнойно-септические осложнения: нагноение ран, абсцессы малого таза, послеоперационный перитонит, которые наблюдались у 45 (22,0 %) больных.
У больных ВЗК, особенно у страдающих НЯК, отмечалось необычное течение перитонита. Отсутствовала классическая картина с развитием напряжения передней брюшной стенки, симптомов раздражения брюшины, оживления перистальтики на ранних этапах и др. У больных ВЗК симптомы перитонита развивались на фоне пареза кишечника, который переходил в динамическую кишечную непроходимость. Живот может быть умеренно вздут, при пальпации достаточно мягкий, выраженность симптомов раздражения брюшины минимальная или отсутствует, хотя и могут встречаться признаки перитонизма. У половины этих больных допущена пролонгация с релапаротомией в силу характера течения перитонита и, с другой стороны (на первых этапах), боязнью релапаротомии, которая в таких случаях резко ухудшает прогноз заболевания.
Вторую группу осложнений при ВЗК составили тромбогеморрагические осложнения. Они были выявлены у половины больных. Тромбофлебиты, тромбоэмболии, кровотечения наблюдали у 20 (9,8 %) пациентов. В основном отмечались кровотечения из раны — у 4, культи прямой кишки — у 3 и из желудка — у 2 больных (острые язвы).
Из общехирургических осложнений после операции наиболее характерны парез желудка и кишечника, атония мочевого пузыря. Постоянно стремясь к снижению послеоперационной летальности и улучшению показателей лечения больных НЯК и БК, сотрудники клиники общей хирургии № 1 Донецкого национального медицинского университета им. М. Горького совершенствуют методики операций в сочетании с консервативными методами лечения больных. Коллектив кафедры внедрил в практику работы около десятка собственных изобретений, подтвержденных авторскими свидетельствами и патентами на изобретения.
В последние 4–5 лет удается существенно ограничить число операций у больных НЯК, в том числе при тотальных колитах с тяжелыми проявлениями заболевания. Основным препаратом для лечения больных НЯК и БК остается месалазин (салофальк) в различных официнальных формах. Важно правильно определить его дозировку в зависимости от тяжести состояния больных. Тем не менее значение корригирующей инфузионной терапии, направленной на коррекцию водно-солевого гомеостаза, белкового, жирового и углеводного обменов, дезинтоксикацию организма, трудно переоценить. С этой целью применяются растворы альбумина, реосорбилакт, смеси аминокислот, растворы глюкозы, электролитов.
В послеоперационном периоде мы рекомендуем следующее:
— все больные ВЗК должны состоять на диспансерном учете;
— проведение контрольной эндоскопии ТК с биопсией СОТК не реже одного раза в 6 месяцев;
— проведение адекватной противорецидивной терапии.
Необходимость создания илеостомы является одной из наиболее сложных проблем в хирургическом лечении ВЗК. Не менее важным этапом является выполнение восстановительной операции. Решение этого вопроса остается открытым и на сегодняшний день.
Илеоректальный анастомоз — наиболее частая восстановительная операция при субтотальной колэктомии. Дискутируются преимущества выполнения операции одновременно с колэктомией или отсроченно вторым этапом. Некоторые авторы высказывают мнение о целесообразности оперировать больных одномоментно, однако большинство хирургов предпочитают осуществлять эту операцию на втором этапе после колэктомии [18].
Сроки выполнения второго этапа операции колеблются от 1–2 до 6–18 месяцев и чаще подбираются индивидуально. Операции в два этапа позволяют уменьшить активность воспалительного процесса в оставшихся отделах толстой кишки под влиянием целенаправленного лечения, а формирование илеоректального анастомоза в таких условиях гораздо реже требует его отключения [14].
Однако в литературе, несмотря на значительное количество работ, положительно оценивающих метод восстановления кишечной непрерывности путем формирования илеоректального анастомоза, встречаются сообщения о развитии тяжелого обострения воспалительного процесса в оставшейся части ПК, что требовало разобщения анастомоза или отключения пассажа путем повторной илео- или энтеростомии. И эти осложнения не всегда напрямую зависят от сроков проведения реконструктивно-восстановительного этапа. К сожалению, и мы имеем негативный опыт развития послеоперационных осложнений после восстановительного этапа операции.
 Пример. Больной П., 1960 г.р., впервые поступил в колопроктологический центр 10.11.2004 г. При поступлении предъявлял жалобы на постоянные ноющие боли в животе, больше в нижних отделах, жидкий стул до 6–7 раз в сутки с обильной примесью крови, общую резкую слабость, повышение температуры тела до 38 °С, отсутствие аппетита. Периодические боли в животе отмечает около 2 месяцев, однако состояние резко ухудшилось 23.10.2004 года, когда во время стула выделилось большое количество крови (алой и со сгустками). Накануне поступления, после стула, сопровождавшегося обильным выделением крови, потерял сознание. Консервативная терапия без эффекта. Состояние больного прогрессивно ухудшалось. 12.01.2005 года больной оперирован, выявлено тотальное поражение ТК, произведена субтотальная колэктомия, раздельная илеосигмостомия. Гистологический ответ — болезнь Крона (рис. 2). В последующем неоднократно получал стационарно и амбулаторно курсы противовоспалительного и противорецидивного лечения. Прибавил в весе более 40 кг. При ректороманоскопии воспалительных изменений слизистой прямой кишки не выявлено. 18.10.2006 года произведено восстановление кишечной непрерывности путем формирования илеосигмоанастомоза «бок в бок». Был выписан в удовлетворительном состоянии. На 14-е сутки после операции повысилась температура тела, появились боли в нижних отделах живота. При КТ — признаки наличия абсцесса брюшной полости. 02.11.2006 года произведена лапаратомия, дренирование абсцесса брюшной полости. Ближайший послеоперационный период протекал без особенностей, однако на 4-е сутки после операции отмечено поступление кишечного содержимого в рану. 06.11.2006 года больной оперирован. Установлено, что имеет место перфорация приводящего к анастомозу участка тонкой кишки, произведена энтеростомия, дренирование брюшной полости. Послеоперационный период протекал тяжело, на фоне выраженной интоксикации, однако к 3-м суткам состояние больного стабилизировалось. Местно, в области стомированной кишки сохранялось воспаление, выраженная мацерация, стомированная кишка имела тенденцию к ретракции и рубцеванию, в связи с чем 24.11.2007 года произведено переформирование энтеростомы. В дальнейшем срединная послеоперационная рана заживала вторичным натяжением. Несмотря на проводимые неоднократно курсы противорецидивного лечения, добиться стойкой ремиссии не удалось. От предложенной проктэктомии больной отказался.
Пример. Больной П., 1960 г.р., впервые поступил в колопроктологический центр 10.11.2004 г. При поступлении предъявлял жалобы на постоянные ноющие боли в животе, больше в нижних отделах, жидкий стул до 6–7 раз в сутки с обильной примесью крови, общую резкую слабость, повышение температуры тела до 38 °С, отсутствие аппетита. Периодические боли в животе отмечает около 2 месяцев, однако состояние резко ухудшилось 23.10.2004 года, когда во время стула выделилось большое количество крови (алой и со сгустками). Накануне поступления, после стула, сопровождавшегося обильным выделением крови, потерял сознание. Консервативная терапия без эффекта. Состояние больного прогрессивно ухудшалось. 12.01.2005 года больной оперирован, выявлено тотальное поражение ТК, произведена субтотальная колэктомия, раздельная илеосигмостомия. Гистологический ответ — болезнь Крона (рис. 2). В последующем неоднократно получал стационарно и амбулаторно курсы противовоспалительного и противорецидивного лечения. Прибавил в весе более 40 кг. При ректороманоскопии воспалительных изменений слизистой прямой кишки не выявлено. 18.10.2006 года произведено восстановление кишечной непрерывности путем формирования илеосигмоанастомоза «бок в бок». Был выписан в удовлетворительном состоянии. На 14-е сутки после операции повысилась температура тела, появились боли в нижних отделах живота. При КТ — признаки наличия абсцесса брюшной полости. 02.11.2006 года произведена лапаратомия, дренирование абсцесса брюшной полости. Ближайший послеоперационный период протекал без особенностей, однако на 4-е сутки после операции отмечено поступление кишечного содержимого в рану. 06.11.2006 года больной оперирован. Установлено, что имеет место перфорация приводящего к анастомозу участка тонкой кишки, произведена энтеростомия, дренирование брюшной полости. Послеоперационный период протекал тяжело, на фоне выраженной интоксикации, однако к 3-м суткам состояние больного стабилизировалось. Местно, в области стомированной кишки сохранялось воспаление, выраженная мацерация, стомированная кишка имела тенденцию к ретракции и рубцеванию, в связи с чем 24.11.2007 года произведено переформирование энтеростомы. В дальнейшем срединная послеоперационная рана заживала вторичным натяжением. Несмотря на проводимые неоднократно курсы противорецидивного лечения, добиться стойкой ремиссии не удалось. От предложенной проктэктомии больной отказался.
Кроме того, существуют разногласия по поводу применения илеоанального соустья, однако большинство ученых считает, что илеоанальное соустье дает худшие функциональные результаты, чем илеоректоанастомоз. В первую очередь это связано с нарушением удерживающей функции сфинктера заднего прохода, отсутствием резервуарной функции прямой кишки, а возможно, и восходящим илеитом. Такой анастомоз нередко становится промежностной илеостомой, а результаты оказываются хуже, чем при колонпроктэктомии с постоянной илеостомой.
Помимо этого, в последние годы появились сообщения о возможности развития рака в культе ПК, где продолжается воспалительный процесс. Эти данные послужили причиной того, что некоторые хирурги больше стали склоняться в выборе к выполнению эндоректальных илеоанальных анастомозов. Эндоректальные илеоанальные анастомозы с 1947 года начали экспериментально разрабатывать M. Ravitch и D. Sabiston. Авторы модифицировали метод удаления слизистой оболочки ПК, описанный ранее V. Dimitrin. Колэктомия с удалением слизистой ПК является достаточно радикальной операцией, при этом одновременно сохраняющей континентную функцию тазовых органов. Несмотря на то что непосредственные результаты, приведенные авторами, расценены удовлетворительно, следует признать, что ценность данного метода может быть установлена лишь после тщательного изучения отдаленных результатов.
Одним из важных вопросов является необходимость разграничения и разработки конкретных показаний к реконструктивно-восстановительным операциям (РВО) ТК. Наиболее распространенным и главным показанием к оперативному лечению — устранению колостомы — является настойчивое желание больного. Довольно значительный контингент больных, несмотря на риск, обусловленный реконструктивно-восстановительной операцией, предупреждения хирургов о возможных послеоперационных осложнениях, настаивает на проведении восстановительного вмешательства.
При решении вопроса о закрытии колостомы мы руководствуемся, прежде всего, характером основного заболевания, объемом и возникшими осложнениями при первой операции.
Другим критерием мы считаем определение степени сложности РВО, которая зависит от вида колостомы, состояния оставшихся участков ТК, их размеров, особенностей кровоснабжения, функционального состояния сфинктера.
Следующий критерий — это общее состояние больных, возможность перенести оперативное лечение, а также технические возможности хирургической бригады и анестезиологического обеспечения.
Вопрос о целесообразности выполнения РВО должен решаться с учетом перечисленных выше факторов. Восстановление кишечной непрерывности наиболее целесообразно, по нашему мнению, в возрасте до 70 лет при отсутствии тяжелой сопутствующей соматической патологии (сердечно-сосудистые заболевания, нарушения мочевыделительной системы, хронические обструктивные заболевания легких, дыхательная и сердечная недостаточность и т.д.). Для успешного проведения РВО у больных ВЗК необходимо правильно выбрать сроки для их выполнения. Единого мнения среди авторов по этому вопросу нет.
Из 146 больных, которым на первом этапе выполнена субтотальная колонэктомия, РВО выполнена у 88 (60,3 %) человек. Остальным пациентам восстановительные операции не выполнены ввиду обострения основного заболевания, наличия тяжелой сопутствующей патологии, отказа от операции или смерти. Сроки проведения РВО определялись общим состоянием больных, степенью восстановления массы тела, коррекцией обменных нарушений, выраженностью регенеративных процессов в слизистой оболочке прямой кишки и ее функциональным состоянием. Эти сроки варьировали от 4 месяцев до 2 лет.
С нашей точки зрения, удовлетворительное общее состояние больных, а также нормальные лабораторные показатели у этой категории больных являются необходимыми условиями при решении вопроса о возможности восстановления непрерывности кишечника.
Ежегодно в мире увеличивается число пациентов молодого и трудоспособного возраста с илеоректальными анастомозами. Часть этих больных не просто не удовлетворенны результатами лечения, а впадают в депрессию из-за тяжести последствий удаления ободочной кишки [2]. И если метаболические нарушения можно временно стабилизировать, то восстановить состояние калообразующей функции является чрезвычайно сложной задачей [22]. Идея о замедлении кишечного пассажа после колэктомии послужила поводом к широкому клиническому внедрению илеоректальных конструкций, принцип которых основан на формировании тонкокишечных резервуаров в виде основных J-, С-, Y-, L-, S- и W-типов межкишечных анастомозов над уровнем культи прямой кишки (рис. 3–7).
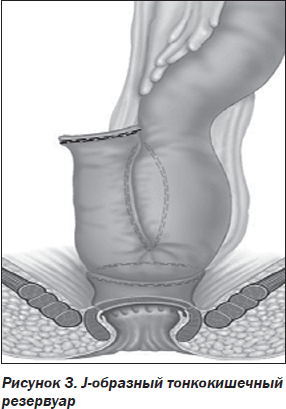
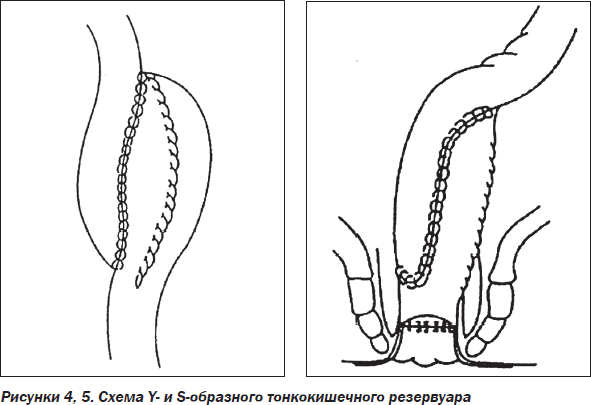
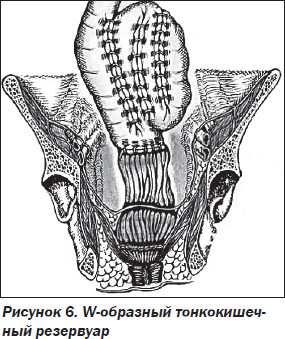
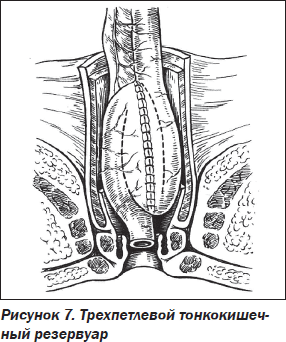
Проблема создания функционально эффективных тазовых тонкокишечных резервуаров не решена до настоящего времени. Не разработана клиническая классификация осложнений, нет единых тактических подходов [13, 23]. Существует несколько модификаций формирования тазовых тонкокишечных резервуаров. Изучена взаимозависимость между видами резервуаров, их локализацией в тазу и функцией. Общепринято мнение, что расположение резервуара вблизи анального канала улучшает его функцию. Установлено, что выраженность воспаления и дисбактериоза в отключенных отделах ТК прямо пропорциональна длине отключенного отдела и времени отключения [5]. Операция по формированию тазового тонкокишечного резервуара стала стандартной для больных с НЯК. Но некоторые авторы считают эту операцию противопоказанной при БК. В настоящее время существует множество модификаций различных видов создания тонкокишечных резервуаров [2, 15, 17].
В нашей клинике тазовые тонкокишечные резервуары сформированы 56 больным с ВЗК. Оптимальным методом в качестве 1-го этапа радикального лечения ВЗК при тотальном поражении ТК считаем субтотальную колэктомию с илео- и колостомией. Эта операция выполняется у большинства этих больных; она достаточно радикальна (при условии постоянного санирования и лечения отключенной толстой кишки, проведении консервативной базовой терапии) и в то же время оставляет больным надежду на восстановление естественной кишечной проходимости.
Произведено исследование функции тазовых тонкокишечных резервуаров, зависимости характера восстановительных операций и сроков их выполнения от результатов первых этапов хирургического лечения, послеоперационных осложнений, частоты обострений основного заболевания в послеоперационном периоде, велся бактериальный мониторинг в отключенной кишке и нарушений микробного ценоза в функционирующих отделах. Результаты рентгенологического обследования сопоставлены с данными патоморфологических исследований после операции.
Выявлено, что во всех наблюдениях после субтотальной колэктомии явления мальабсорбции требуют коррекции в течение 1–2 месяцев, при отсутствии послеоперационных осложнений. При наличии осложнений этот срок пролонгируется. Наиболее информативными показателями нарушений гомеостаза являются потеря веса, нарушения на ЭКГ в виде ранней реполяризации желудочков, снижение уровня альбумина, анемия. В раннем послеоперационном периоде проводилась индивидуальная коррекция путем инфузионной терапии. В дальнейшем достаточно эффективно применение сбалансированного питания на фоне анаболических стероидов.
Основной причиной дисфункции резервуаров было рубцовое сужение илеоанальных анастомозов. Ни трансанальное бужирование, ни хирургическая коррекция анастомозов не давали удовлетворительных результатов. Вышеизложенное позволяет сделать вывод о необходимости применения широких анастомозов «бок в бок» для предупреждения стенозирования вследствие основного заболевания.
Нами предложен способ формирования тонко-прямокишечных резервуаров (декларационный патент Украины № 39747, 2001 г.), который заключается в следующем: после субтотальной колонэктомии на переднюю брюшную стенку раздельно выводятся илеостома и сигмостома. После ликвидации воспалительных явлений в ПК и улучшения состояния больного формируется анастомоз «бок в бок» между подвздошной и сигмовидной кишкой, сигмостома ушивается. Затем, при отсутствии противопоказаний, ушивается илеостома. Сформированный таким образом резервуар способствует уплотнению каловых масс, позволяет сократить частоту стула.
Этим способом прооперировано 39 больных. Ни в одном случае не было осложнений, связанных с операцией по созданию резервуара. Однако обострения основного заболевания, в основном в сроки 2–3 месяца, наблюдались у всех больных после оперативных вмешательств, что подтверждено клиническими проявлениями и данными лабораторных исследований. Наиболее информативными лабораторными показателями обострения основного процесса являются: уровни фибриногена крови (9,37 ± 2,07 мг/л, p < 0,05, при норме 2,8 ± 0,09 мг/л), альбумина-альфа (5,49 ± 0,3 г/л, р < 0,05, при норме 13,45 ± 0,26 г/л), лейкоцитарный индекс интоксикации Даштаянца (4,47 ± ± 0,58, р < 0,05, при норме 0,83 ± 0,6).
Восстановительные операции не производились у больных с хроническим непрерывно рецидивирующим течением, вследствие нарушения функции сфинктера, а также при отказе больных. Во всех случаях при изучении операционного материала после восстановительных операций, несмотря на отсутствие макроскопических проявлений обострения, гистологически отмечено воспаление в неотерминальном отделе тонкой кишки.
Обострения в позднем послеоперационном периоде осложнились образованием наружных кишечных свищей из терминального отдела подвздошной кишки у 3 больных. После достижения ремиссии образовавшиеся свищи иссекались с ушиванием концевого отдела подвздошной кишки. Ни в одном наблюдении функция резервуара не нарушалась. У всех больных с функционирующим резервуаром нормализация функции завершалась к 6 месяцам послеоперационного периода. При заполнении резервуара во время дистальной энтерографии перед ушиванием илеостомы объем последнего составлял 500 мл, содержимое произвольно удерживалось сфинктером. Через 6 месяцев после ушивания илеостомы при исследования пассажа по желудочно-кишечному тракту было отмечено: эвакуация из желудка и двенадцатиперстной кишки — в обычные сроки, пассаж по тонкой кишке замедлялся, четко прослеживались симптомы «колонизации» подвздошной кишки, резервуар начинал заполняться спустя 2 часа. Контраст полностью заполнял резервуар спустя 24 часа. Частота стула вне периодов обострений составляла 2–3 раза в сутки, без патологических примесей. Наблюдалась нормализация веса. Несмотря на то что у всех прооперированных больных имелись обострения после завершения реконструктивно-восстановительного этапа, ни в одном наблюдении не потребовалось отключение или переформирование резервуара.
Считаем необходимым отключение пассажа на период адаптации с целью создания условий для заживления илеоанального анастомоза и предохранения кожи перианальной области от изъязвлений. Обязательным мероприятием является также лечебная физкультура для сфинктера с целью сохранения его функции.
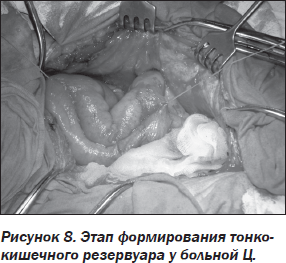 Пример. Больная Ц., 1984 г.р., впервые обратилась в клинику 12.08.2008. При поступлении предъявляла жалобы на постоянные тупые боли в животе, больше в правых отделах с иррадиацией в поясничную область, частый жидкий стул, метеоризм, общую слабость, боли в области заднего прохода и промежности, усиливающиеся при дефекации, повышение температуры тела до 38–39 °С, выделение кала и газов через влагалище. Прогрессирующее похудание. Заболела остро около 1,5 года назад, когда появились боли в животе и частый жидкий стул. Лечилась амбулаторно у гастроэнтеролога по поводу хронического эрозивного гастродуоденита, СРК, хронического холецистита, хронического панкреатита. Получала противовоспалительную, спазмолитическую терапию, однако проведенное лечение было малоэффективно, сохранялся выраженный болевой синдром, частый жидкий стул. Похудела на 15 кг (вес при поступлении 30 кг). 19.08.2008 года больная оперирована в клинике. Произведена колонпроктэктомия, резекция подвздошной кишки, энтеростомия. Гистологический ответ № 44472: болезнь Крона в стадии выраженной активности. 08.04.2009 года произведена эндоскопическая полипэктомия по поводу воспалительного полипа культи прямой кишки. 09.04.2009 года произведено иссечение ректовагинального свища, сфинктеролеваторопластика. Получала курсы противорецидивного лечения. Контрольный осмотр: при ректороманоскопии культя прямой кишки до 10 см — слизистая бледная, складчатость сохранена, сосудистый рисунок прослеживается. 18.11.2009 года произведено восстановление кишечной непрерывности, формирование тонкокишечного резервуара (рис. 8), энтеростомия. На момент подготовки публикации противопоказаний к восстановлению кишечной непрерывности нет, больная готовится к плановому оперативному вмешательству.
Пример. Больная Ц., 1984 г.р., впервые обратилась в клинику 12.08.2008. При поступлении предъявляла жалобы на постоянные тупые боли в животе, больше в правых отделах с иррадиацией в поясничную область, частый жидкий стул, метеоризм, общую слабость, боли в области заднего прохода и промежности, усиливающиеся при дефекации, повышение температуры тела до 38–39 °С, выделение кала и газов через влагалище. Прогрессирующее похудание. Заболела остро около 1,5 года назад, когда появились боли в животе и частый жидкий стул. Лечилась амбулаторно у гастроэнтеролога по поводу хронического эрозивного гастродуоденита, СРК, хронического холецистита, хронического панкреатита. Получала противовоспалительную, спазмолитическую терапию, однако проведенное лечение было малоэффективно, сохранялся выраженный болевой синдром, частый жидкий стул. Похудела на 15 кг (вес при поступлении 30 кг). 19.08.2008 года больная оперирована в клинике. Произведена колонпроктэктомия, резекция подвздошной кишки, энтеростомия. Гистологический ответ № 44472: болезнь Крона в стадии выраженной активности. 08.04.2009 года произведена эндоскопическая полипэктомия по поводу воспалительного полипа культи прямой кишки. 09.04.2009 года произведено иссечение ректовагинального свища, сфинктеролеваторопластика. Получала курсы противорецидивного лечения. Контрольный осмотр: при ректороманоскопии культя прямой кишки до 10 см — слизистая бледная, складчатость сохранена, сосудистый рисунок прослеживается. 18.11.2009 года произведено восстановление кишечной непрерывности, формирование тонкокишечного резервуара (рис. 8), энтеростомия. На момент подготовки публикации противопоказаний к восстановлению кишечной непрерывности нет, больная готовится к плановому оперативному вмешательству.
При ВЗК выполнено 146 субтотальных колэктомий. Восстановительные операции определялись состоянием культи ПК. Даже при многолетней ремиссии в культе прямой кишки оперативное вмешательство сопровождалось обострением ВЗК, что могло вызывать недостаточность швов анастомозов и тяжелые гнойно-септические осложнения. Успех восстановительного лечения определялся эффективностью консервативной терапии. К сожалению, в этой группе наблюдались 8 (5,5 %) летальных исходов после восстановительных операций. Резервуары были сформированы у 36 (24,7 %) пациентов. В 22 (66,7 %) наблюдениях функция резервуаров удовлетворительная, у 12 (33,3 %) больных отмечались нарушения, связанные с обострениями ВЗК.
Функциональные результаты у больных, перенесших реконструктивно-восстановительные операции, были оценены по трехбалльной системе.
Хорошие — после восстановительной операции полностью нормализовалась функция анального сфинктера (больные самостоятельно удерживали газы и кал). Восстановилась резервуарная функция ТК. Частота стула 1–2 раза в день. Стул оформленный или полужидкий. У таких пациентов жалобы отсутствуют или проходят в течение первых 2–3 недель после операции. У больных полностью сохранена трудоспособность.
Удовлетворительные — сохранены моторная и эвакуаторная функции ТК, однако вследствие сужения колоректального анастомоза или стриктуры имеются задержки стула, недостаточное опорожнение. Пациенты этой группы в связи с периодическими нарушениями пассажа по ТК имели ограничения трудоспособности.
Неудовлетворительными результатами мы считаем такие, когда вследствие развивающихся послеоперационных осложнений или рецидива основного заболевания возникала необходимость в повторном формировании коло- или илеостомы.
Мы стараемся убедить широкий круг врачей, которые на различных этапах сталкиваются с больными НЯК и БК, что ранняя диагностика и своевременное направление таких пациентов в специализированные центры позволит успешно оградить их от тяжелых последствий оперативных вмешательств. Необходимо развивать диспансеризацию больных ВЗК, что позволит поддерживать длительную ремиссию заболеваний путем профилактической терапии, снизить число онкозаболеваний или обеспечить их операбельность на ранних стадиях развития опухоли. Возможность восстановительных операций также зависит от диспансерного наблюдения за оперированными больными НЯК и БК.
1. Балтайтис Ю.В., Кушнир В.Е., Корсуновский А.И. Неспецифический язвенный колит. — К.: Здоров’я, 1986. — 192 с.
2. Баширов С.Р. Последствия тотального удаления ободочной кишки: патогенетические нарушения и перспективы коррекции // Бюллетень сибирской медицины. — 2003. — № 4. — С. 35-41.
3. Григорьева Г.А., Мешалкина Н.Ю. Болезнь Крона. — М.: Медицина, 2007. — 184 с.
4. Гусак В.К. Обоснование и оценка хирургического лечения неспецифического язвенного колита: Автореф. дис... д.м.н. — К., 1981. — 30 с.
5. Гюльмамедов Ф.И., Шлопов В.Г., Гюльмамедов П.Ф., Мамедов Н.З. Реконструктивно-восстановительные операции у больных с илеоколостомой. — М., 2001. — С. 147-159.
6. Захараш М.П. Состояние колопроктологической помощи в Украине, ее проблемы и перспективы // Матеріали II з’їзду колопроктологів України за міжнародною участю. — К.: Медицина, 2006. — С. 21-34.
7. Захараш М.П., Пойда А.И., Мельник В.М. Современная хирургическая тактика при неспецифическом язвенным колите // Харківська хірургічна школа. — 2009. — № 2. — С. 31-34.
8. Комаров Ф.И., Осадчук А.М., Осадчук М.А., Кветной И.М. Неспецифический язвенный колит. — М.: Медицинское информационное агентство, 2008. — 256 с.
9. Левитан М.Х., Александров В.Б., Юрков М.Ю. Новые возможности дифференциальной диагностики и оценки методов терапии неспецифического язвенного колита и болезни Крона // 3-й Всесоюз. съезд гастроэнтерологов (Материалы съезда). — М.; Л., 1984. — С. 468-469.
10. Мак-Нейш А.С. Болезнь Крона толстой кишки // Гастроэнтерология / Под ред. Александера-Вильямса Дж., Биндера Х. Дж.: Пер. с англ. — М.: Медицина, 1985. — Т. 3. — С. 91-113.
11. Матяшин И.М. Хирургическая тактика при неспецифическом язвенном колите с учетом постколэктомических расстройств // Клин. хирургия. — 1981. — № 2. — С. 13-16.
12. Мустяц А.П. Оптимизация хирургического лечения тяжелых воспалительных заболеваний толстой кишки: Дис... д.м.н.: 14.01.03 / Донецкий гос. медицинский ун-т им. М. Горького. — Донецк, 1995. — 366 c.
13. Никитин А.М., Михайлянц Г.С. Реконструктивно-восстановительные операции с созданием тазовых тонкокишечных резервуаров у больных после колэктомии // Клин. хирургия. — 1989. — № 2. — C. 142-148.
14. Олейников П.Н. Хирургическое лечение болезни Крона: Автореф. дис... д.м.н. — М., 1989. — 41 с.
15. Пойда А.И., Мельник В.М. Новые методы хирургической реабилитации после колэктомии, колэктомии и резекции прямой кишки, колэктомии и экстирпации прямой кишки // Харківська хірургічна школа. — 2009. — № 2. — С. 73-76.
16. Полунин Г.Е., Гюльмамедов Ф.И., Коктышев И.В. Оценка результатов лечения рака толстой кишки, ассоциированного с язвенным колитом и болезнью Крона // Новоутворення. — 2009. — № 3, 4. — С. 183-185.
17. Ривкин В.Л., Луцевич О.Э., Файн С.Н., Лукин В.В. Атлас практической колоректальной хирургии. — М.: ИД Медпрактика-М, 2006. — 144 с.
18. Сергевнин В.В. К обоснованию илеоректального анастомоза при неспецифическом язвенном колите: Дис... д.м.н. — М., 1974. — 274 с.
19. Федоров В.Д., Олейников П.Н., Алипьев В.Ю. Реконструктивные операции у больных неспецифическим язвенным колитом и болезнью Крона // Хирургия. — 1989. — № 10. — С. 74-77.
20. Халиф И.Л., Лоранская И.Д. Воспалительные заболевания кишечника (неспецифический язвенный колит и болезнь Крона): клиника, диагностика, лечение. — М.: Миклош, 2004. — 88 с.
21. Юдин И.Ю. Хирургическое лечение неспецифического язвенного колита. — М.: Медицина, 1976. — 200 с.
22. Юхтин В.И., Хуторянский И.Н. Оценка различных типов илеоректального анастомоза после колэктомии // Хирургия. — 1986. — № 3. — С. 103-108.
23. Яицкий Н.А., Васильев С.А. Реконструктивно-восстановительные операции при «короткой культе» прямой кишки // Сборник тезисов «Хирургия 2000». — М., 2000. — С. 400-401.
