Газета «Новости медицины и фармации» 10 (416) 2012
Вернуться к номеру
Основні принципи призначення імунотропної терапії. Імунопрофілактика. Імунореабілітація
Авторы: О.В. Ломакіна, Н.Г. Риндіна, О.І. Шушляпін, Д.В. Ольховський - Харківський національний медичний університет
Версия для печати
Продовження.
Початок в № 9 (415), 2012
Внутрішньовенні імуноглобуліни (ВІГ)безпечні в плані перенесення вірусних інфекцій, містять достатню кількість IgG3, відповідального за нейтралізацію вірусів, мають активність Fc-фрагмента. Показання до застосування:
1. Захворювання, при яких ефект ВІГ переконливо доведений:
— первинні імунодефіцити (Х-зв’язана агаммаглобулінемія; загальний варіабельний імунодефіцит; транзиторна гіпогаммаглобулінемія дітей; імунодефіцит з гіперглобулінемією М; дефіцит підкласів імуноглобуліну G; дефіцит антитіл з нормальним рівнем імуноглобулінів; тяжкі комбіновані імунодефіцити всіх типів; синдром Віскотта — Олдрича; атаксія-телеангіектазія; карликовість з вибірково короткими кінцівками; X-зв’язаний лімфопроліферативний синдром.
— вторинні імунодефіцити: гіпогаммаглобулінемія; профілактика інфекцій при хронічному лімфолейкозі; профілактика цитомегаловірусної інфекції при алогенній пересадці кісткового мозку й інших органів; синдром відторгнення при алогенній пересадці кісткового мозку; хвороба Кавасакі; СНІД у педіатричній практиці; хвороба Гійєна — Барре; хронічні демієлінізуючі запальні полінейропатії; гостра і хронічна тромбоцитопенічна пурпура, зокрема у дітей, і пов’язана з ВІЛ-інфекцією; автоімунна нейропенія.
2. Захворювання, при яких ВІГ імовірно ефективний: злоякісні новоутворення з дефіцитом антитіл; профілактика інфекцій при мієломній хворобі.
3. Захворювання, при яких застосування ВІГ, можливо, буде ефективним: судоми, що не купіруються; системний червоний вовчак (СЧВ); дерматоміозит, екзема; ревматоїдний артрит, опікова хвороба; м’язова атрофія Дюшена; цукровий діабет; тромбоцитопенічна пурпура, пов’язана з уведенням гепарину; некротичний ентероколіт; ретинопатія; хвороба Крона; множинна травма, рецидивуючий середній отит; псоріаз; перитоніт; менінгіт; менінгоенцефаліт.
Особливості клінічного застосування ВІГ
Існує декілька варіантів лікувально-профілактичного застосування імуноглобулінів: замісна терапія при імунодефіцитах, ускладнених інфекцією; імунотерапія хворих із тяжкою інфекцією (сепсис); переважна ІТ при автоалергічних і алергічних захворюваннях.
Гіпогаммаглобулінемії зазвичай зустрічаються у дітей з активними бактерійними інфекціями. У таких випадках імунотерапію слід проводити в режимі насичення, одночасно з активною протимікробною хіміотерапією. Проводять переливання нативної (свіжої або кріоконсервованої) плазми в разовій дозі 15–20 мл/кг маси тіла.
ВІГ уводять у добовій дозі 400 мг/кг внутрішньовенно краплинно або інфузійно по 1 мл/кг/год недоношеним і 4–5 мл/кг/год доношеним дітям. Недоношеним дітям з масою тіла менше 1500 г і рівнем IGG 3 г/л і нижче ВІГ уводять для профілактики інфекцій. При імунодефицитах з низьким рівнем IGG у крові ВІГ уводять до досягнення концентрації IGG у крові не нижче за 4–6 г/л. При тяжких гнійно-запальних захворюваннях уводять 3–5 ін’єкцій щодня або через день до 1–2,5 г/кг. У початковий період інтервали між вливаннями можуть бути 1–2 дні, наприкінці — до 7 днів. Достатніми виявляються 4–5 уведень, так що за 2–3 тижні хворий у середньому отримує 60–80 мл плазми, або 0,8–1,0 г ВІГ на 1 кг маси тіла. За місяць переливається не більше 100 мл плазми, або 1,2 г ВІГ на 1 кг маси тіла хворого.
Інтраглобін — ВІГ, містить в 1 мл 50 мг IGG і близько 2,5 мг IGA. Застосовують при імунодефіцитах, інфекціях, автоімунних захворюваннях.
Пентаглобін — ВІГ, збагачений IGM, містить: IGM — 6 мг, IGG — 38 мг, IGA — 6 мг в 1 мл. Застосовують при сепсисі, інших інфекціях, імунодефіциті: новонародженим — 1 мл/кг/год, по 5 мл/кг щодня — впродовж 3 днів; дорослим — 0,4 мл/кг/год, потім 0,4 мл/кг/год, далі безперервно 0,2 мл/кг до 15 мл/кг/год протягом 72 годин — 5 мл/кг упродовж 3 днів, за необхідністю — повторний курс.
Октагам — ВІГ, що містить в 1 мл 50 мг білків плазми, з них — 95% IGG; менше 100 мкг IGA і менше 100 мкг IGM. Близький до нативного IGG плазми крові, присутні всі субкласи IGG. Показання: природжена агаммаглобулінемія, варіабельні та комбіновані імунодефіцити, тромбоцитопенічна пурпура, хвороба Кавасакі, пересадка кісткового мозку.
При імунодефіциті препарати вводять до рівня IGG у плазмі крові 4–6 г/л. Початкова доза — 400–800 мг/кг, з подальшим уведенням 200 мг/кг кожні 3 тижні. Для досягнення рівня IGG 6 г/л необхідно ввести 200–800 мгр/кг на місяць. Для контролю визначають рівень IGG у крові.
Для лікування і профілактики інфекцій дози ВІГ залежать від виду інфекційного процесу. Як правило, його вводять якомога раніше. При цитомегаловірусній інфекції доза повинна становити 500 мг/кг щотижня протягом 12 тижнів, тому що період напіввиведення підкласу IgG3, відповідального за нейтралізацію вірусу, — 7 днів, а клінічно інфекція виявляється між 4–12-м тижнем після інфікування. Одночасно призначають противірусні препарати, що діють синергічно.
Для профілактики неонатального сепсису у недоношених дітей масою тіла від 500 до 1750 г рекомендується вводити від 500 до 900 мг/кг/добу IGG для підтримки його концентрації не менше 800 мг/кг під контролем рівня IGG у крові. Підвищення рівня IGG зберігається в середньому 8–11 днів після введення. Введення IGG вагітним після 32-го тижня знижувало ризик інфекції у новонароджених.
Препарати ВІГ застосовують і для лікування сепсису, особливо поєднано з антибіотиками. Рекомендований рівень у крові — понад 800 мг/кг.
Після алогенної трансплантації кісткового мозку для профілактики ЦМВ й інших інфекцій ВІГ уводять щотижня протягом 3 місяців, а потім 500 мл/кг кожні 3 тижні протягом 9 місяців.
При лікуванні автоімунних захворювань дози становлять 250–1000 мл/кг протягом 2–5 днів кожні 3 тижні. Дітям з автоімунною тромбоцитопенічною пурпурою вводять по 400 мл/кг упродовж 2 днів, дорослим — 1 г/кг протягом 2 або 5 днів.
Механізм дії імуноглобулінів залежить від стану Fc-рецепторів лейкоцитів: зв’язуючись з ними, імуноглобуліни підсилюють функції при інфекції і, навпаки, пригнічують при алергії.
Антирезусний імуноглобулін пригнічує у резус-негативної жінки синтез антитіл проти резус-позитивного плода за типом зворотного зв’язку.
Механізм дії IGG полягає в специфічному і неспецифічному ефекті. Специфічний ефект пов’язаний з дією невеликої кількості завжди присутніх антитіл. Неспецифічний — з імуномодулюючим ефектом. Обидва ефекти зазвичай опосередкують через Fc-рецептори лейкоцитів. Зв’язуючись з Fc-рецепторами лейкоцитів, імуноглобуліни активують їх, зокрема фагоцитоз. Якщо серед молекул імуноглобуліну є антитіла, то вони можуть опсонувати бактерії або нейтралізувати віруси.
Моноклональні антитіла мишей проти лімфоцитів і цитокінів людини застосовують для пригнічення автоімунних реакцій, трансплантаційного імунітету. Нижче наведені деякі варіанти використання моноклональних антитіл:
- антитіла проти CD20 В-лімфоцитів для імуносупресії (мабтера);
- антитіла проти рецепторів до інтерлейкіну-2 — при загрозі відторгнення алотрансплантата нирки;
- антитіла проти IGE — при тяжких алергічних реакціях (ксолар).
Препарати кісткового мозку, лейкоцитів і селезінки
Мієлопідотримують з культури кістковомозкових клітин свиней. Мієлопід стимулює протипухлинний імунітет, фагоцитоз, клітини-антитілопродуценти, проліферацію гранулоцитів і макрофагів у кістковому мозку. Мієлопід використовується при лікуванні септичних, затяжних і хронічних інфекційних захворювань бактерійної природи, вторинних імунодефіцитів, оскільки має здатність підсилювати синтез антитіл у присутності антигенів. Мієлопід (флакон 5 мг) уводять в/м щодня або через день. Разова доза — 0,04–0,06 мг/кг. Курс терапії складається з 3–10 ін’єкцій через день.
Лейкоцитарний чинник перенесення (трансфер-фактор) — група біологічно активних речовин, що екстрагуються з лейкоцитів здорових або імунізованих донорів за допомогою багатократних послідовних заморожувань і розморожувань. Трансфер-фактори підсилюють гіперчутливість сповільненого типу до конкретних антигенів. Препарат перешкоджає розвитку імунологічної толерантності, підсилює диференціювання Т-клітин, хемотаксис нейтрофілів, утворення інтерферонів, синтез імуноглобулінів (в основному класу М). Разова доза становить для дорослих 1–3 одиниці сухої речовини. Використовується в лікуванні первинних імунодефіцитів, особливо макрофагального типу і терапії вторинних імунодефіцитів лімфоїдного типу (при дефектах диференціювання і проліферації Т-клітин, порушенні хемотаксису і презентації антигенів).
Цитокіни — група біологічно активних глікопептидів-медіаторів, що виділяються імунокомпетентними клітинами, а також фібробластами, клітинами ендотелію, епітелію.
Беталейкін — рекомбінантний IL-lb, випускається в ампулах по 0,001; 0,005 або 0,0005 мг (5 ампул). Стимулює лейкопоез при лейкопеніях, викликаних цитостатиками і опромінюванням, диференціювання імунокомпетентних клітин. Застосовують в онкології, при післяопераційних ускладненнях, затяжних, гнійно-септичних інфекціях. Уводять в/в краплинно в дозі 5 нг/кг для імуностимуляції; 15–20 нг/кг для стимуляції лейкопоезу щодня на 500 мл 0,9% розчину натрію хлориду протягом 1–2 год. Курс — 5 інфузій.
Ронколейкін — рекомбінантний IL-2. Показання: ознаки імунодефіциту, гнійно-запальні захворювання, сепсис, перитоніт, абсцеси і флегмони, піодермії, туберкульоз, гепатит, СНІД, онкологічні захворювання. При сепсисі вводять по 0,25–1 мг (25 000–1 000 000 MО) в 400 мл 0,9% розчину натрію хлориду в/в краплинно зі швидкістю 1–2 мл/хв протягом 4–6 год., при онкологічних захворюваннях — 1–2 млн ОД 2–5 разів з інтервалами 1–3 дні, по 25 000 MО в 5 мл фізіологічного розчину вводять при синуситах у верхньощелепну або лобову пазухи; інсталяції в уретру при хламідіозі щодня по 50 000 MО (14–20 діб); перорально при ієрсиніозах і діареях — по 500 000–2 500 000 МО в 15–30 мл дистильованої води натще щоденно протягом 2–3 днів. Ампули по 0,5 мг (500 000 MО), 1 мг (1 000 000 MО).
Нейпоген (філграстим) — рекомбінантний гранулоцитарний колонієстимулюючий фактор (Г-КСФ) стимулює формування функціонально активних нейтрофілів і частково моноцитів у перші 24 години після введення, активує гемопоез. Застосовують при нейтропеніях, хіміотерапії, для профілактики інфекцій у дозі 5 мкг/кг/добу в/в або п/ш через 24 години після циклу лікування протягом 10–14 днів. При природженій нейтропенії — 12 мкг/кг/добу п/ш щодня.
Лейкомакс (молграмостим) — рекомбінантний гранулоцитарний макрофагальний колонієстимулюючий фактор (ГМ-КСФ). Застосовують при лейкопеніях у дозі 1–10 мкг/кг/добу, підшкірно за показаннями.
Граноцит (ленограстим) — гранулоцитарний колонієстимулюючий фактор, стимулює проліферацію попередників гранулоцитів, нейтрофілів. Застосовують при нейтропеніях по 2–10 мкг/кг/добу протягом 6 днів.
Лейкінферон — є комплекс цитокінів першої фази імунної відповіді, що включає IFN-a, IL-1, IL-6, IL-12, TNF-a, MIF. При бактеріальних інфекціях курс лікування повинен бути інтенсивним (через день по 1 амп., в/м) і лише при відновленні підтримуючого імунітету (2 рази на тиждень по 1 амп., в/м).
Класифікація інтерферонів за їх походженням наведена в табл. 1.
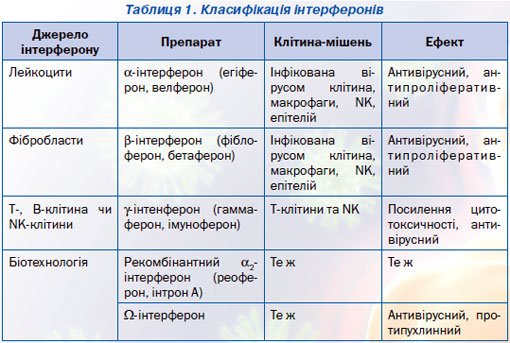
Інтерферони в дозах до 2 млн MО викликають імуностимулюючий ефект, а їх високі дози (10 млн MО) — імуносупресію.
Необхідно пам’ятати, що всі препарати інтерферонів можуть спричинювати гарячку, грипоподібний синдром, нейтропенії і тромбоцитопенії, алопецію, дерматити, порушення функції печінки і нирок та інші ускладнення.
Лейкоцитарний a-інтерферон (егіферон, велферон) використовується як профілактичний препарат у формі місцевих аплікацій на слизову оболонку в епідемічні періоди і при лікуванні ранніх стадій гострих респіраторних та інших вірусних захворювань. При вірусних ринітах необхідне введення інтраназально достатньо великої дози (3 ґ 106 MО) 3 рази на день у ранній період захворювання. Препарат швидко виводиться зі слизом й інактивується його ферментами. Застосування його понад тиждень може викликати посилення запалення. Очні інтерферонові краплі використовують при вірусних ураженнях ока.
Людський імунний g-інтерферон (гаммаферон) викликає цитотоксичний ефект, модулює активність Т-лімфоцитів і активує В-клітини. При цьому препарат може пригнічувати антитілоутворення, фагоцитоз і модифікувати відповідь лімфоцитів. Ефект гаммаінтерферону на Т-клітини зберігається 4 тижні. Застосовують при псоріазі, ВІЛ-інфекції, атопічному дерматиті, пухлинах.
Дози препаратів інтерферону для парентерального введення добирають індивідуально: від декількох тисяч одиниць на 1 кг маси тіла до декількох мільйонів одиниць на 1 ін’єкцію. Курс — 3–10 ін’єкцій. Побічні реакції: грипоподібний синдром.
Роферон-А — рекомбінантний інтерферон альфа-2а вводять в/м (до 36 млн MО) або п/ш (до 18 млн MО). При волосато-клітинному лейкозі — 3 млн МО/добу в/м упродовж 16–24 тижнів; мієломна хвороба — 3 млн MО 3 рази на тиждень в/м; саркомі Калоші та ниркоклітинній карциномі — 18–36 млн MО на добу; вірусному гепатиті В — 4,5 млн MО в/м 3 рази на тиждень протягом 6 місяців.
Віферон — рекомбінантний інтерферон a-2b застосовують у вигляді свічок (по 150 тис. MО, 500 тис. MО, 1 млн MО), мазь (40 тис. MО в 1 г). Призначають при інфекційно-запальних захворюваннях (ГРВІ, пневмонія, менінгіт, сепсис та ін.), гепатитах, герпесі шкіри і слизових оболонок — 1 раз на день або через день у свічках; при герпесі — додатково змащують уражені ділянки шкіри маззю 2–3 рази на добу. Дітям — свічки по 150 тис. MО 1 ґ 3 рази через 8 годин упродовж 5 днів; при гепатитах — по 500 тис. MО.
Реаферон (інтераль) — рекомбінантний інтерферон a2 призначають при гепатиті В, вірусному менінгоенцефаліті внутрішньом’язово по 1–2 ґ 106 MО 2 рази на день упродовж 5–10 днів, потім дозу знижують. При грипі, кору може застосовуватися інтраназально; при генітальному герпесі — мазь (0,5 ґ 106 МО/г), оперізувальному лишаї — внутрішньом’язово по 1 ґ 106 MО на день протягом 3–10 днів. Використовують також для лікування пухлин.
Вітаміни
Під впливом вітамінів змінюється активність біохімічних процесів у клітинах, у тому числі імунологічних. Деякі форми імунологічної недостатності асоціюються з дефіцитом тих або інших вітамінів. Прикладом може бути первинна форма дефекту фагоцитозу — синдром Чедіака — Хігасі. Аскорбінова кислота нормалізує активність Т-лімфоцитів і нейтрофілів у хворих із початково пониженими показниками. Проте високі дози (10 г) викликають імунодепресію.
Вітамін Е (токоферолу ацетат, a-токоферол) — міститься в соняшниковій, кукурудзяній, соєвій, обліпиховій олії, яйцях, молоці, м’ясі. Має антиоксидантні й імуностимулюючі властивості. Застосовують при м’язовій дистрофії, порушенні статевої функції, при хіміотерапії. Призначають усередину і внутрішньом’язово по 0,05–0,1 г на добу впродовж 1–2 міс. Призначення вітаміну Е в добовій дозі 300 MО протягом 6–7 днів перорально збільшує кількість лейкоцитів, Т- і В-лімфоцитів.
Фітоімуномодулятори. Настої, відвари трав мають імуномодулюючу (імуностимулюючу) активність.
Елеутерококпри нормальному імунному статусі не змінює показники імунітету. Має інтерфероногенну активність. При дефіциті числа Т-клітин нормалізує показники, підсилює функціональну активність Т-клітин, активує фагоцитоз, неспецифічні реакції імунітету. Застосовують по 2 мл спиртного екстракту за 30 хвилин до їди 3 рази на день упродовж 3–4 тижнів. У дітей для профілактики рецидивів ГРЗ — по 1 краплі/1 рік життя 1–3 рази на добу протягом 3–4 тижнів.
Женьшень.Підвищує працездатність і загальну опірність організму до захворювань і несприятливих дій, не викликає шкідливих побічних явищ і може застосовуватися тривалий час. Корінь женьшеня — сильний збудник ЦНС, не дає негативних ефектів, не порушує сон. Препарати женьшеня стимулюють тканинне дихання, збільшують газообмін, покращують склад крові, нормалізують ритм серця, підвищують світлочутливість очей, прискорюють процеси загоєння, пригнічують життєдіяльність деяких бактерій, підвищують стійкість до радіації. Препарати з нього рекомендується застосовувати в осінньо-зимовий період. Найбільш стимулюючий ефект спостерігається при використанні порошку женьшеня і настоянки на спирті 40°. Разове дозування становить 15–25 крапель спиртової настоянки (1 : 10), або 0,15–0,3 г порошку женьшеня. Приймати 2–3 рази на день до їди курсами по 30–40 днів, після чого зробити перерву.
Ехінацея (Echinacea purpurea)чинить імуностимулюючу, протизапальну дію, активує макрофаги, секрецію цитокінів, інтерферонів, стимулює Т-клітини. Препарати ехінацеї застосовують для профілактики респіраторних захворювань в осінньо-весняний період, а також для лікування вірусних і бактерійних інфекцій верхніх дихальних шляхів, сечостатевого тракту та ін. Рекомендується 40 крапель 3 рази на день, розбавлені водою. Підтримуючі дози — 20 крапель 3 рази на день перорально протягом 8 тижнів.
Імунал — настій 80% соку ехінацеї пурпурної, 20% етанолу. Призначають по 20 крапель всередину кожні 2–3 години при ГРЗ, грипі, потім 3 рази на день. Курс — 1–8 тижнів.
Біостимулятори — адаптогени: настоянка лимоннику, відвари і настої череди, чистотілу, календули, фіалки триколірної, солодкового кореня і кульбаби мають імунокоригуючий ефект.
Бактеріоімунотерапія
Дисбіози слизових оболонок відіграють важливу роль у патології. Антибіотикотерапія, цитостатична і променева терапія викликають порушення біоценозу слизових оболонок, у першу чергу кишечника, і тоді виникають дисбактеріози. Пробіотичні лактобактерії і біфідобактерії, колібактерії, виділяючи коліцини, інгібують зростання патогенних бактерій.
Лактобактерії — антагоністи патогенних мікробів, виділяють ферменти і вітаміни. Рекомендується призначати поєднано зі специфічними бактеріофагами, що пригнічують патогенну флору. Недоцільно застосовувати при кандидозах, оскільки їх кислоти підсилюють зростання грибів.
Біфідумбактерин сухий — висушені живі біфідобактерії. Дорослим — по 5 пігулок 2–3 рази на день за 20 хв до їди. Курс — до 1 міс. Дітям — у флаконах, розводять теплою кип’яченою водою (1 пігулка на 1 чайну ложку) по 1–2 дози 2 рази на день.
Застосовують при дисбактеріозах, ентеропатіях, штучному вигодовуванні дітей, лікуванні недоношених, гострих кишкових інфекціях (дизентерія, сальмонельоз та ін.), хронічних захворюваннях кишечника (гастрит, дуоденіт, коліт), променевій і хіміотерапії пухлин, кандидозних вагінітах, непереносимості їжі, харчовій алергії, дерматитах, екземі, для нормалізації мікрофлори слизової оболонки ротової порожнини при стоматитах, пародонтитах, цукровому діабеті, хронічних захворюваннях печінки і підшлункової залози, роботі в шкідливих і екстремальних умовах.
Біфікол сухий — живі висушені біфідобактерії і кишкова паличка vrt7. Дорослим і дітям старше за 3 роки — за 20–30 хв до їди по 3–5 табл. 2 рази на день, запивати водою. Курс — 2–6 тижнів.
Біфіформмістить не менше 107 Bifidobacterium lobgum, а також 107 Епterococcus faecium в капсулах. При дисбактеріозі I–II ступеня — по 1 капсулі 3 рази на день, курс — 10 днів; при дисбактеріозі II–III ступеня — збільшення курсу до 2–2,5 тижня.
Лінекс — комбінований препарат, містить три компоненти природної мікрофлори з різних відділів кишечника: в одній капсулі — 1,2 ґ 107 живих ліофілізованих бактерій Bifidobacterium infantis, Lactobacillus, Cl. dophilus і Str. faecium, стійких до антибіотиків і хіміопрепаратів. Підтримують мікробіоценоз у всіх відділах кишечника — від тонкої до прямої кишки. Призначають: дорослим — по 2 капсули 3 рази на день, запиваючи кип’яченою водою, молоком; дітям до 2 років — по 1 капсулі 3 рази на день, запиваючи рідиною або змішуючи з нею вміст капсули.
Колібактерин сухий — висушена жива кишкова паличка, штам M-l7, що є антагоністом для патогенних мікробів, стимулює імунітет, а також ферменти і вітаміни. Дорослим — 3–5 табл. 2 рази на день за 30–40 хв. до їди, запивають лужною мінеральною водою. Курс — 3 тижні — 1,5 місяця.
Хілак фортемістить продукти метаболічної активності пробіотичних штамів лактобацил і нормальних мікроорганізмів кишечника — кишкової палички і фекального стрептокока: молочна кислота, амінокислоти, жирні кислоти, лактоза. Сумісно з прийомом антибіотиків. Не рекомендується одночасне застосування антацидних препаратів унаслідок можливої нейтралізації молочної кислоти, що входить до складу хілаку форте. Призначають у дозі 20–40 крапель 3 рази на день протягом 2–3 тижнів (дітям грудного віку — 15–30 крапель 3 рази на добу), приймають у невеликій кількості рідини до або під час їди, виключаючи молоко і молочні продукти.
Гастрофарм — живі ліофілізовані клітини Lactobacillus bulgaricus-51 і метаболіти їх життєдіяльності (молочна і яблучна кислоти, нуклеїнові кислоти, ряд амінокислот, поліпептиди, полісахариди). Всередину, 3 рази на добу, розжовуючи з невеликою кількістю води. Разова доза для дітей становить 0,5 пігулки, для дорослих — 1–2 пігулки.
Імуномодулюючі ефектиантибіотиків
Умовно-патогенні мікроби не викликають хвороби у більшості людей і є нормальними мешканцями шкіри і слизових оболонок. Причина їх активації — недостатня резистентність організму — імунодефіцит. Тому основою інфекційно-запальних хвороб є природжені або придбані, гострі та хронічні імунодефіцити, що створюють сприятливі умови для розмноження мікробів, які в нормі постійно елімінуються факторами імунітету. Прикладом поширеного гострого імунодефіциту є синдром застуди, коли на тлі гіпотермії організму пригнічується природна резистентність до умовно-патогенних мікробів.
Виходить, що без відновлення реактивності організму пригнічення тільки мікрофлори часто є недостатнім для повного одужання. Більше того, чимало антибактеріальних засобів пригнічують імунітет, створюють умови для контамінації організму резистентними до антибіотиків штамами. Ще більше посилює проблему поширене профілактичне застосування антибактеріальних засобів при вірусних інфекціях. Основні шляхи вирішення проблеми: одночасне застосування антибіотиків і засобів, що нормалізують пригнічені ланки системи імунітету; додаткове застосування засобів імунореабілітації; максимальне збереження та відновлення ендоекології організму. Можливі два види впливу антибіотиків на імунну відповідь: пов’язані з лізисом або пошкодженням бактерій і обумовлені прямим впливом на клітини імунної системи.
1. Ефекти, опосередковані пошкодженими бактеріями:
- інгібіція синтезу клітинної стінки (пеніциліни, кліндаміцин, цефалоспорини, карбапенеми та ін.) — знижує стійкість бактерійних клітин до дії бактерицидних чинників лейкоцитів і макрофагів;
- інгібіція синтезу білка (макроліди, рифампіцин, тетрациклін, фторхінолони та ін.) викликає зміни клітинної мембрани мікроорганізмів і може підсилювати фагоцитоз внаслідок зниження експресії на поверхні бактерійних клітин білків з антифагоцитарними функціями, в той же час ці антибіотики пригнічують імунну відповідь у зв’язку з порушенням синтезу білка в клітинах системи імунітету;
- дезінтеграція мембрани грамнегативних бактерій і підвищення її проникності (аміноглікозиди, поліміксин В) збільшує чутливість мікроорганізмів до дії бактерицидних чинників.
2. Ефекти антибіотиків обумовлені звільненням з мікроорганізмів при їх руйнуванні біологічно активних речовин:ендотоксинів, екзотоксинів, глікопептидів та ін. Невеликі дози ендотоксинів необхідні для нормального розвитку імунітету, роблять сприятливий вплив, стимулюють неспецифічну резистентність до бактерійних і вірусних інфекцій, а також до раку. Це видно на прикладі кишкової палички, яка є нормальним мешканцем кишечника. При її руйнуванні виділяється невелика кількість ендотоксину, що стимулює місцевий і загальний імунітет. Тому при таких затяжних інфекціях часто ефективні препарати бактерійних ліпополісахаридів — продигіозан, пірогенал і лікопід. Проте при тяжкій інфекції і виділенні великої кількості ендотоксину в потік крові індуковані ним цитокіни (IL-1, TNF-a) можуть викликати пригнічення фагоцитозу, виражений токсикоз аж до токсикосептичного шоку зі зниженням серцево-судинної діяльності. З іншого боку, інтенсивний лізис великої кількості бактерій і виділення ендотоксинів можуть призвести до побічних реакцій типу Джаріша — Герксгеймера.
Ефекти, обумовлені прямим впливом антибіотиків на систему імунітету:
- бета-лактамні антибіотики підсилюють фагоцитоз і хемотаксис лейкоцитів, але у великих дозах можуть пригнічувати антитілоутворення і бактерицидність крові;
- цефалоспорини, зв’язуючись з нейтрофілами, підвищують їх бактерицидність, хемотаксис і окислюваль-ний метаболізм у хворих з імунодефіцитами;
- гентаміцин знижує фагоцитоз і хемотаксис гранулоцитів і РБТЛ.
- макроліди (еритроміцин, рокситроміцин і азитроміцин) стимулюють функції фагоцитів, бактерицидність, хемотаксис, синтез цитокінів (IL-1 та ін.).
- фторхінолони підсилюють проліферацію клітин імунної системи, підвищують синтез IL-2, фагоцитоз і бактерицидність;
- тетрациклін, доксициклін пригнічують фагоцити і синтез антитіл.
Імуномодулюючі ефекти антибіотиків на систему імунітету призводять до розвитку алергічних реакцій. Основою є взаємодія антибіотиків як гаптену з клітинами системи імунітету і активація специфічної імунної відповіді.
Основні критерії призначення імуномодулюючих препаратів
Лікарські засоби, дозволені як ІТЛЗ до медичного застосування за кордоном, і основні захворювання, при яких вони призначаються, наведені в табл. 2.
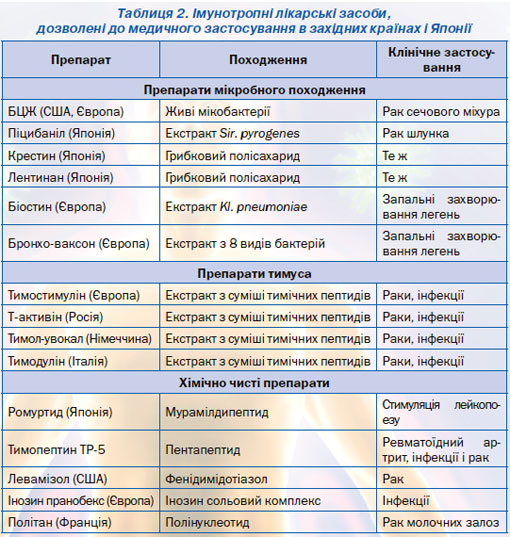
Основні лікарські препарати, дозволені до медичного застосування як ІТЛЗ в Україні та Росії, наведені в табл. 3.
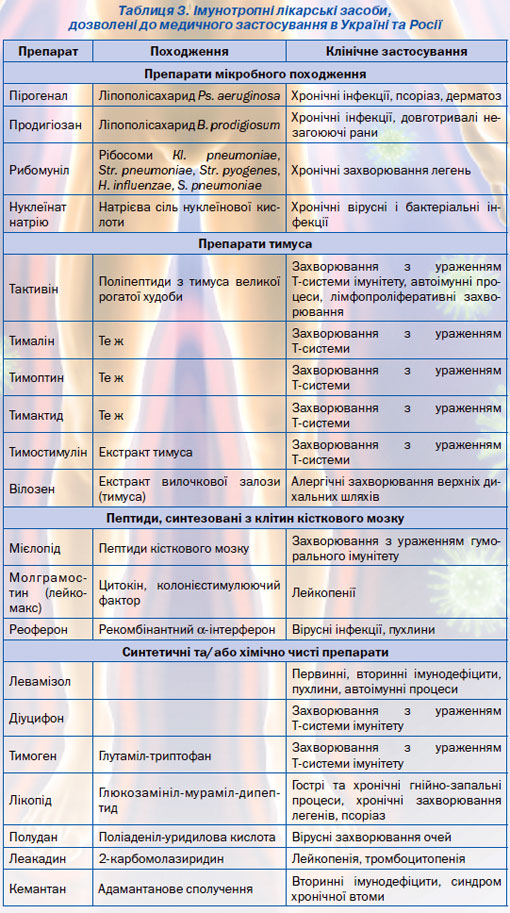
Підставою для проведення імунотерапії є результати клініко-імунологічного дослідження. На підставі даних цього обстеження можна виділити три групи людей:
1. Особи, які мають клінічні ознаки порушення імунітету і зміни імунологічних показників.
2. Особи, які мають клінічні ознаки порушення імунної системи за відсутністю змін імунологічних показників, що виявляються за допомогою звичайних лабораторних тестів.
3. Особи, які мають зміни імунологічних показників, клінічних ознак недостатності імунної системи.
Головною мішенню дії препаратів мікроб-ного походженняє клітини моноцитарно-макрофагальної системи, природним завданням яких є елімінація мікроба з організму. Вони підсилюють функціональну активність цих клітин, стимулюючи фагоцитоз. Паралельно з цим відбувається й активація цитотоксичної функції макрофагів, що виявляється в їх здатності руйнувати in vivo пухлинні клітини. Активовані моноцити і макрофаги починають синтезувати цитокіни: IL-1, IL-3, TNF, колонієстимулюючий фактор та ін. Наслідком цього є активація як гуморальної, так і клітинної ланки імунітету.
Мішенню для дії препаратів тимічного походження єТ-лімфоцити, що виявляється індукцією синтезу Т-клітинами цитокінів і посиленням проліферації, диференціювання і цитотоксичних властивостей.
Мішенню для дії препаратів кістковомозкового походження єВ-лімфоцити, що виявляється посиленням синтезу антитіл.
Вибір імуномодулюючого препаратуі схеми його застосування визначається лікарем-імунологом залежно від тяжкості основного захворювання, супутньої патології, типу виявленого імунологічного дефекту.
Правила призначення імунотропних препаратів
При ураженні клітин моноцитарно-макрофагальної системи застосовуються: поліоксидоній — в дозі від 6 до 12 мг; лікопід — в дозі 1, 10 мг. При найбільш тяжких формах ураження використовуються препарати гранулоцитарно-макрофагальних колонієстимулюючих факторів: молграмостим (лейкомакс) 150, 300, 400 мкг; філграстим (нейпоген) 300, 480 мкг. Для замісної терапії використовується лейкомаса.
При дефектах клітинної ланки імунітету застосовується один із таких препаратів: поліоксидоній — у дозі від 6 до 12 мг; тактивін 0,01% розчин — у дозі 1 мл п/ш; тимоптин — у дозі 100 мкг; тимоген 0,01% розчин — 1 мл в/м; тималін — 10 мг в/м 1 раз на день або через день.
При порушенні синтезу антитіл В-лімфоцитами показані: мієлопід 0,003 г; поліоксидоній — в дозі від 6 до 12 мг.
При порушенні гуморального імунітету (альфа- або гіпогаммаглобулінемії) проводиться замісна терапія препаратами імуноглобулінів: сандоглобулін — 1,0; 3,0; 6,0 і 12 г у флаконі; октагам — 50, 100, 200 мл у флаконі; інтраглобін — 2,5; 5,0 г; імуноглобулін нормальний людський для в/в введення — 25 мл; біавен — 1,0; 2,5 г/кг, а також препаратами, що мають у складі IgM, — пентаглобін 5% — 10,0; 20,0; 50,0 мл. Замісна підтримуюча терапія проводиться в режимі насичення (рівень імуноглобуліну G не менше 400 мкг/мл) під контролем лікаря-імунолога.
Основи імунотерапії вірусних інфекцій:
1. Активація внутрішньоклітинного противірусного захисту (інтерферон).
2. Активація фагоцитозу і кілерів (поліоксидоній).
3. Скріплення вірусів після руйнування уражених клітин і виходу вірусних частинок у периферичну кров (специфічні гамма-глобуліни, плазма крові поєднано з антибіотиками і противірусними препаратами — таміфлю).
4. Збільшення синтезу противірусних антитіл (гропринозин).
Тривалість лікування в стаціонарі — від 20 до 30 днів.
Додаткова терапія — екстракорпоральні методи імунокорекції — плазмаферез, імуносорбція, екстракорпоральна імунофармакотерапія.
Вимоги до результатів лікування: купірування клінічних проявів імунної недостатності, зменшення частоти рецидивів захворювання, нормалізація або тенденція до нормалізації початково змінених показників імунітету.
Тривалість усунення імунологічних порушень становить від 30 днів до 6–9 місяців і залежить від властивостей препарату, маркерного показника і характеру захворювання.
Продовження у наступному номері
