Журнал «Медицина неотложных состояний» 4 (43) 2012
Вернуться к номеру
Нейропротекция в интенсивной терапии у пациентов с полиэтиологическим поражением ЦНС
Авторы: Татьяна Брандис
Рубрики: Семейная медицина/Терапия, Медицина неотложных состояний
Разделы: Медицинские форумы
Версия для печати
24–26 мая 2012 года в г. Одессе прошел конгресс анестезиологов Украины и России. На конгрессе в числе многих обсуждаемых проблем рассматривались вопросы проведения интенсивной терапии больным с центральной неврологической патологией. К.м.н., заведующим отделением ОАИТ, городским анестезиологом г. Макеевки А.Н. Колесниковым был представлен доклад «Интенсивная терапия у пациентов с полиэтиологическим поражением ЦНС».
В докладе были рассмотрены следующие вопросы:
- факторы риска церебральных нарушений при политравме;
- цель-ориентированная интенсивная терапия у пациентов с острой церебральной недостаточностью (первичная нейропротекция) и время назначения нейропротекторов;
- применение холинергических препаратов в анестезиологии;
- новые возможности фармакологического применения нейропротекторов (экстракорпоральная фармакотерапия).
Среди факторов риска особое значение имеет сам факт травмы.
Было отмечено, что психоэмоциональный и болевой стресс усиливает нарушение свертываемости крови, более чем в 10 раз повышая риск тромбоэмболических осложнений.
Необходимым условием поддержания адекватного церебрального перфузионного давления является снижение внутричерепного давления в остром периоде черепно-мозговой травмы. При этом суммарный мозговой кровоток снижается, что увеличивает риск гипоперфузии мозговых капилляров вследствие развития сладж-синдрома.
Применение гепарина не препятствует образованию сладжей и развитию диссеминированного внутрисосудистого свертывания (ДВС). Подчеркнуто, что гиперкоагуляционные нарушения гемостаза являются одним из основных патогенетических звеньев, обусловливающих развитие тяжелых ишемических осложнений.
Последнее время особое внимание уделяется риску развития мозгового инсульта как следствия политравмы, операционной травмы и анестезии. Несмотря на высокий технический уровень оперативных вмешательств и анестезиологических пособий, часто крайне сложно уменьшить глобальное стрессорное воздействие на организм пациента агрессивных факторов. Данные исследований свидетельствуют о том, что до и во время операции психоэмоциональный стресс, боль, гипоксия вызывают нарушения гемостаза, системной и церебральной гемодинамики и активируют перекисное окисление липидов.
Ранний послеоперационный период является критическим в развитии различных осложнений, в том числе острых сосудистых поражений головного мозга.
Однако вопросы диагностики, профилактики и лечения церебральных инсультов при политравме остаются недостаточно изученными. Следует учитывать, что, как только присоединяется поражение ЦНС, увеличивается процент осложнений и ишемические нарушения развиваются даже у больных без перенесенной ЧМТ.
Чаще всего послеоперационное острое сосудистое поражение головного мозга протекает по типу ишемического инсульта, что наблюдается у 47,6 % больных. У 30 % больных ишемический инсульт развивается на фоне нарушения системной гемодинамики; у 15 % — в результате гипоксии. У 5 % больных ишемический инсульт развивается после пароксизмальных нарушений сердечного ритма, что дает основание предположить эмболию церебральных сосудов. Преходящие нарушения мозгового кровообращения развиваются у 34,3 % больных, у 5,6 % пациентов после операции развивается смешанный инсульт. Геморрагический инсульт возникает после операции при резком значительном повышении артериального давления на фоне гипокоагуляции в 5,6 % случаев.
В докладе были рассмотрены вопросы проведения терапии и профилактики ишемических нарушений у пациентов с политравмой. Прежде всего необходимо обеспечение адекватного поликомпонентного обезболивания: наркотические анальгетики (морфин) или агонисты-антагонисты (налбуфин), дексалгин, парацетамол (инфулган). Необходимы поддержание адекватной перфузии головного мозга и постоянный контроль показателей центральной и микрогемодинамики (МГД).
Для этого применяются средства, улучшающие кровоток в пораженных участках и реологические свойства крови.Для улучшения реологических свойств крови применяют реосорбилакт, латрен, НМГ, ГЭК. В состав интенсивной терапии должны быть также включены средства, улучшающие мозговой кровоток. По полученным данным, применение холина альфосцерата (GliceroрhosphoCholine) доказанно улучшает мозговой кровоток, что отмечено в протоколах первичной нейропротекции. Препарат влияет на увеличение синтеза и высвобождение из терминалей ацетилхолина, за счет восстановления мембран и противоотечного эффекта обеспечивает восстановление нейротрансмиссии в области повреждения, улучшает когнитивные функции.
В докладе было обращено внимание на то, что необходимо разделять введение препаратов в периоде, когда пациент находится в коме (оценка по ШКГ 4–8 баллов), — это первичная нейропротекция, или неотложная терапия, и период, когда пациент выходит из комы (ШКГ выше 8 баллов), — это вторичная нейропротекция, или восстановительная терапия.
Одним из актуальных моментов интенсивной терапии острой церебральной недостаточности является своевременное восстановление адекватной перфузии в пораженных участках головного мозга. Цель-ориентированная инфузионная терапия направлена на улучшение каких-либо показателей. В нашем случае мы должны учитывать состояние мозгового кровотока, так как при его нарушении действие многих препаратов остается неэффективным.
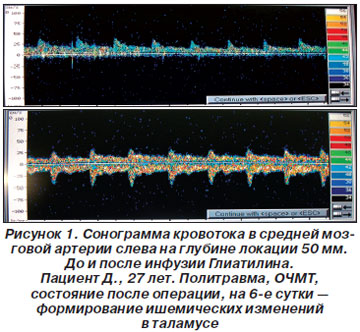
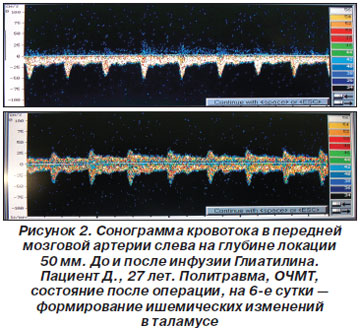
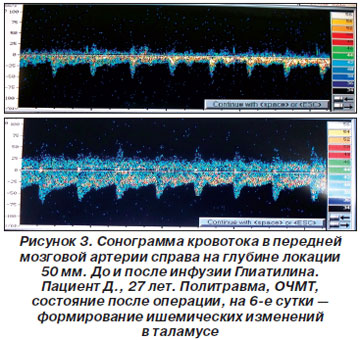
В докладе был приведен клинический случай: пациент Д., 27 лет, с политравмой и ОЧМТ доставлен бригадой скорой помощи; ему была проведена инфузия маннита и фуросемида, что вызвало резкое снижение скорости венозного оттока в венозном синусе. Выявлены признаки выраженной декомпенсации регуляции внутримозгового кровотока со значительным ростом внутричерепного давления. На 5-е сутки после операции развились ишемические нарушения в таламусе. Приведены сонограммы кровотока в средней мозговой артерии, передней левой и правой мозговой артериях, правой позвоночной артерии до и после введения Глиатилина, на которых продемонстрировано улучшение показателей (рис. 1–4).
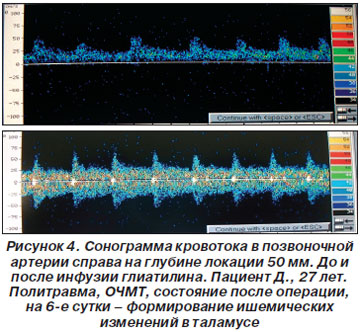
С учетом нарушения ауторегуляции сосудов головного мозга при тяжелой церебральной недостаточности сосудистого или травматического генеза возрастает влияние центральной гемодинамики на уровень мозгового кровообращения. Таким образом, полезна параллельная оценка центральной гемодинамики по данным реографии и мозгового кровотока по данным транскраниальной допплерографии (ТКДГ) на фоне мониторинга уровня сознания по клиническим шкалам и биспектральному анализу ЭЭГ.
Отсутствие влияния центральной гемодинамики на мозговой кровоток является благоприятным признаком и свидетельствует о восстановлении ауторегуляции мозгового кровотока.
Докладчик акцентировал внимание на том, что при проведении цель-ориентированнной терапии тактику инфузионной терапии определяет не патология, а тип гемодинамики.
В основе базисного лечения тяжелой церебральной недостаточности лежит интенсивная терапия, направленная на коррекцию и поддержание оптимальных показателей функционирования всех органов и систем для создания всех условий по мобилизации естественных компенсаторных механизмов. Основные методы лечения — активная реперфузия и нейропротекция — возможны при условии восстановления и поддержания показателей системной гемодинамики, обеспечивающих оптимальную доставку кислорода и фармакологических агентов к головному мозгу.
В исследовании определение глубины коматозного состояния осуществлялось BIS-монитором (BIS VISTA (A-3000)), состояние МГД и качество инфузионной нейропротекторной терапии изучали с помощью портативного аппарата EZ-Dop, показатели ЦГД-реографа Р4-02 с аналого-цифровым преобразователем и программным обеспечением. Были приведены схемы первичной нейропротекции в зависимости от типа гемодинамики с включением препарата Глиатилин. Внутривенное капельное введение 2 г Глиатилина в течение 60 минут обеспечило повышение показателей BIS и ТКДГ в среднем на 12–18 % (рис. 5).
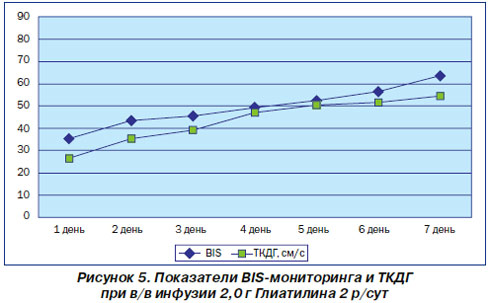
Новые возможности фармакологического применения нейропротекторов представляет экстракорпоральная фармакотерапия (ЭКФТ), которую академик Чазов назвал «точечным бомбовым ударом».
Экстракорпоральная фармакотерапия — это использование клеток аутокрови с целью изменения их свойств для направленного транспорта лекарств. Клетки, используемые для направленного транспорта, называют фармакоцитами. Клетками-контейнерами являются эритроциты, лейкоциты и тромбоциты.
В докладе была представлена модифицированная методика проведения ЭКФТ.
Пациенту производится эксфузия 50–70 мл крови. Затем эта кровь смешивается с 50 мл физиологического раствора и 5000 ЕД гепарина. Туда же добавляется высшая разовая доза фармакологического средства — Глиатилина, цитиколина. Далее выполняется инкубация в теплом месте (на магистральных сосудах) в течение 30 минут.
По истечении этого времени больному вводится кровь с нейропротектором. Повторение сеансов — каждые 24–48 часов (3–7 раз).
Уровень меченого Глиатилина в мозге составил 45 % концентрации препарата в крови. Исследование липидной фракции клеточной мембраны показало ассимиляцию радиоактивности в фосфолипидной фракции, соответствующей фосфатидилхолину. Глиатилин преодолевает гематоэнцефалический барьер при приеме внутрь в дозе 100 мг/кг.
Методика экстракорпорального введения Глиатилина и цитиколина применялась у 25 пациентов с острым ишемическим инсультом (в течение 7 суток). На данном этапе проводится подбор оптимальной дозы и кратности введения. В ходе терапии Глиатилином наиболее значимая положительная динамика неврологического дефицита прослеживалась в остром периоде церебральной ишемии. Было отмечено, что применение Глиатилина перспективно в комплексе анестезиологической защиты для обеспечения интраоперационной нейропротекции и раннего пробуждения. Также перспективным и экономически обоснованным является применение Глиатилина в виде ЭКФТ.
В завершение своего доклада А.Н. Колесников сделал следующие выводы:
- интенсивная терапия и первичная нейропротекция должны проводиться под контролем центральной и мозговой гемодинамики;
- достижение целевых значений ЦГД и МГД является точкой для назначения вторичной нейропротекции;
- доказана эффективность холинергической терапии (Глиатилин, цитиколин) в протоколе первичной нейропротекции;
- перспективно использование BIS-мониторинга для пациентов нейрореанимации.
Таким образом, применение Глиатилина в схемах первичной и вторичной нейропротекции позволяет снизить риск острого послеоперационного поражения ЦНС (ишемический инсульт, геморрагический инсульт, ТИА) у пациентов как следствия ТЧМТ, политравмы, операционной травмы и анестезии.
Подготовила Татьяна Брандис