Газета «Новости медицины и фармации» 12 (422) 2012
Вернуться к номеру
Болезни суставов и экология
Авторы: О.В. Синяченко - д.м.н., профессор, член-корр. НАМНУ, заведующий кафедрой пропедевтики внутренней медицины Донецкого национального медицинского университета им. М. Горького
Версия для печати
Отношение к экологии стало серьезно рассматриваться в качестве критерия цивилизованности стран, поскольку пренебрежение неблагоприятной средой обитания человека подрывает их поступательное социально-экономическое развитие. Загрязненность окружающей среды определяет исключительную значимость как показатель общего уровня здоровья населения и является важнейшим фактором его мониторинга. В течение последних лет широко обсуждается связь с негативными факторами окружающей среды развития ряда воспалительно-дегенеративных заболеваний суставов. Наряду с плохим качеством питьевой воды и питания экология определяет рост численности больных и с системным остеопорозом. Высокий уровень в пище людей и во вдыхаемом воздухе некоторых химических веществ способствует развитию и увеличению темпов прогрессирования ревматоидного артрита и анкилозирующего спондилоартрита.
 Гигиеническая оценка антропогенного загрязнения окружающей среды проводилась нами на основании определения ксенобиотиков в четырех ее объектах — атмосферном воздухе, почве, воде поверхностных водоемов и подземных водоисточников. Данные были получены в результате лабораторных исследований санитарно-гигиенических станций, региональных отделений Государственных комитетов по гидрометеорологии, контролю природной среды и экологической безопасности. Проанализированы сведения по 33 крупным городам и районам. Усредненная техногенная нагрузка на воздушный бассейн в этих регионах за год составляет 4987,0 ± 1432,4 т/км2, или 804,0 ± ± 209,1 кг/чел, а накопление неутилизированных токсичных промышленных отходов — 520,0 ±± 127,3 т3/км2, или 428,0 ± 89,2 т/чел. При этом на долю выбросов в атмосферу угольной промышленности приходятся 25,0 ± 6,5 %, производства стройматериалов — 21,0 ± ± 5,8 %, энергетической отрасли — 21,0 ± 6,2 %, металлургической промышленности — 8,0 ± 3,5 %, сельского хозяйства — 7,0 ± 3,5 %, машиностроения — 6,0 ± 2,9 %, транспорта — 5,0 ± ± 2,7 %, химического производства — 3,0 ± 1,5 %. Металлургическая промышленность в изученных регионах оказывает достоверное влияние на уровень диоксида азота, оксида углерода и сероводорода в воздушном пространстве, машиностроительная — на концентрацию диоксида серы и оксида углерода, химическая — на содержание диоксида азота.
Гигиеническая оценка антропогенного загрязнения окружающей среды проводилась нами на основании определения ксенобиотиков в четырех ее объектах — атмосферном воздухе, почве, воде поверхностных водоемов и подземных водоисточников. Данные были получены в результате лабораторных исследований санитарно-гигиенических станций, региональных отделений Государственных комитетов по гидрометеорологии, контролю природной среды и экологической безопасности. Проанализированы сведения по 33 крупным городам и районам. Усредненная техногенная нагрузка на воздушный бассейн в этих регионах за год составляет 4987,0 ± 1432,4 т/км2, или 804,0 ± ± 209,1 кг/чел, а накопление неутилизированных токсичных промышленных отходов — 520,0 ±± 127,3 т3/км2, или 428,0 ± 89,2 т/чел. При этом на долю выбросов в атмосферу угольной промышленности приходятся 25,0 ± 6,5 %, производства стройматериалов — 21,0 ± ± 5,8 %, энергетической отрасли — 21,0 ± 6,2 %, металлургической промышленности — 8,0 ± 3,5 %, сельского хозяйства — 7,0 ± 3,5 %, машиностроения — 6,0 ± 2,9 %, транспорта — 5,0 ± ± 2,7 %, химического производства — 3,0 ± 1,5 %. Металлургическая промышленность в изученных регионах оказывает достоверное влияние на уровень диоксида азота, оксида углерода и сероводорода в воздушном пространстве, машиностроительная — на концентрацию диоксида серы и оксида углерода, химическая — на содержание диоксида азота.
Объектом исследования стали больные, распределение которых в отношении остеоартроза, РА, подагрического артрита и АС составило 110 : 6 : 4 : 1. По сводным данным, распространенность ОА в этих регионах была равна 221,0 ± 21,0 на 10 000 населения, ПА — 20,0 ± 6,4, РА — 18,0 ± 1,2, АС — 2,0 ± ± 0,2. В почвах исследованы уровни Ba, Be, Bi, Co, Cr, Cu, Hg, Li, Mg, Mn, Mo, Ni, Pb, Sn, Ti, V и Zn, а в подземных водах — Ba, Cu, Li, Mn, Ni, Pb, Ti и Zn. Уровни техногенной нагрузки на воздушный бассейн и загрязнения почв в результате накопления токсичных промышленных отходов мало влияют на интегральный состав микроэлементов в воде и почве. В связи с этим необходимо подчеркнуть, что превышение фоновой концентрации в почвах Cr, Cu, Hg и Pb зарегистрировано во всех регионах, Zn — в 97 %, Mg — в 91 %, Мо — в 88 %, Sn — в 85 %, Ni — в 82 %, Ва — в 70 %, Mn — в 67 %, Со — в 64 %, Bi — в 52 %, V — в 49 %, Ti — в 42 %, Ве — в 36 %, а Ti, Ba, Mn, Pb, Li, Ni, Cu и Zn в подземных водах — соответственно в 88, 82, 64, 49, 24,2, 21, 15 и 6 %. Содержание в разных объектах исследования Li и Pb прямо коррелирует между собой.
Показатели техногенной нагрузки на воздушный бассейн и загрязнения почв в результате накопления токсичных промышленных отходов не влияют на интегральную распространенность заболеваний опорно-двигательного аппарата. Вместе с тем, по данным дисперсионного анализа, развитие АС связано с накоплением неутилизированных токсичных промотходов, а на распространенность ОА влияет уровень выброса в атмосферу химических веществ. Регрессионный анализ показывает прямую связь с этими гигиеническими параметрами распространенности РА.
Распространенность РА зависит от степени развитости в регионе химической промышленности, ПА — металлургической, химической, машиностроительной отраслей и транспорта, ОА — только машиностроения. АС с этими факторами не связан. Если результаты дисперсионного анализа свидетельствуют о высоком влиянии на распространенность ОА уровней в атмосфере диоксида серы, оксида углерода и сероводорода, то РА показывает прямые регрессионные связи только с диоксидом серы и оксидом углерода. Содержание в воздухе диоксида азота на распространенность болезней суставов воздействия не оказывает.
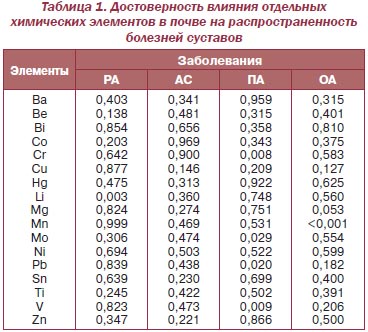
В обследованных регионах средние показатели в почве Ва составили 9386,0 ± 38,0 мг/кг, Be — 0,20 ± 0,01 мг/кг, Bi — 0,20 ± 0,01 мг/кг, Co — 1,90 ± 0,03 мг/кг, Cr — 244,0 ± 19,3 мг/кг, Cu — 63,0 ± 1,9 мг/кг, Hg — 1,30 ± 0,16 мг/кг, Li — 52,0 ± 3,3 мг/кг, Mn — 2704,0 ± 300,8 мг/кг, Mo — 3,0 ± 0,1 мг/кг, Ni — 66,0 ± 1,9 мг/кг, Pb — 113,0 ± 11,1 мг/кг, Sn — 9,0 ± 0,4 мг/кг, Ti — 465,0 ± 3,6 мг/кг, V — 101,0 ± 1,0 мг/кг, Zn — 284,0 ± 17,5 мг/кг. Нами установлены достоверные корреляционные связи уровней Ва в почве с Be, Bi, Co, Cu, Hg, Li, Mo, Sn, Ti и Zn, Be — c Bi, Co, Cu, Hg, Li, Mn, Mo, Ni, Pb, Sn, Ti, V и Zn, Bi — c Cu, Hg, Ti и Zn, Co — c Cr, Cu, Hg, Li, Mn, Mo, Ni, Pb, Sn и V, Cr — c Cu, Hg, Mn, Ni, Pb, Sn, V и Zn, Cu — c Mo, Pb, Sn, V и Zn, Hg — c Li, Mn, Mo, Ni, Pb, Sn, V и Zn, Li — c Mo, Ni, Sn, V и Zn, Mn — c Ni, Pb и Sn, Mo — c Ni, Pb, Sn, Ti, V и Zn, Ni — c Pb, Sn и V, Pb — c Sn и Ti, Sn — c Zn, Ti — c V и Zn. Направленность корреляционных связей не зависит от сопоставления эссенциальных (жизненно необходимых) МЭ с таковыми и токсичными.
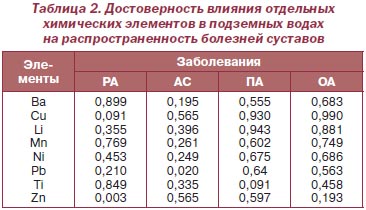
Как видно из табл. 1, параметры содержания в почве Li влияют на распространенность РА, Cr, Mo, Pb и V — ПА, Mn — ОА, концентрация Zn в подземных водах — на РА, Pb — на АС (табл. 2). Существует прямая регрессионная связь распространенности РА с уровнями в почве Ва и Ti, а в воде — Mn, Ti и Ni, АС — с Cu в почве, ПА — с Мо, ОА — с Mn, Sn и V.
Возрастание частоты ОА у работников металлургической промышленности обусловлено не только статико-динамической перегрузкой суставов, но и влиянием вредных факторов окружающей среды. Производство строительных материалов вследствие постоянного контакта людей с повышенным уровнем в атмосфере кремнезема увеличивает риск развития РА. Pабота в сельском хозяйстве мало влияет на распространенность ОА, но известно, что пребывание людей в неблагоприятных микроклиматических условиях способствует учащению дегенеративно-воспалительных заболеваний периартикулярных тканей. Серьезные эпидемиологические проблемы в рамках воспалительно-дегенеративных заболеваний опорно-двигательного аппарата у населения регионов с загрязнением атмосферы промышленными отходами угольной и коксохимической отраслей промышленности обусловлены перманентным дисбалансом иммунной системы. Учащает случаи возникновения заболеваний артрологического профиля присутствие в атмосфере бензольных продуктов нефтеперерабатывающей промышленности.
Связь распространенности РА с содержанием Li в почве, на наш взгляд, требует дополнительных фармакологических исследований, поскольку НПВП из группы ингибиторов ЦОГ-2, широко используемые при таком заболевании, повышают в крови параметры Li. Важен факт, что у пациентов, страдающих РА и АС, гиперлитиемия способна вызывать различные нарушения возбудимости миокарда и электрической проводимости сердца, ухудшать функцию почек и щитовидной железы.
Полученные нами данные еще раз подтверждают связь ПА с интоксикацией Mo и Pb. Мо является кофактором для связывания Fe трансферазами и компонентом фермента пуринового обмена ксантиноксидазы, переводящей гипоксантин в ксантин, а последнего в мочевую кислоту с дальнейшим развитием гиперурикемии (а значит, и возможной подагры). Кроме того, Мо способен влиять на активность альдегид- и сульфитоксидаз, а накопление его в организме происходит при дефиците Cu в рационе людей. По нашим данным, однако, отсутствует корреляционная связь между уровнями Мо и Cu в окружающей среде больных ПА.
По результатам однофакторного дисперсионного анализа, на содержание в крови больных подагрой Li, Pb и Zn влияет уровень одноименных МЭ в почве. Если концентрация Li, Sr и Zn тесно связана со всеми изученными в почве МЭ, то параметры S от них не зависят. Обращает на себя внимание тот факт, что показатели в крови Pb, помимо того же Pb в почве, определяет лишь содержание Hg. В целом концентрация в крови Fe связана с 12 из 16 МЭ в почве, Mn — c 11, B и Co — c 10, Ba — c 8, Cu — c 5. В большей степени на микроэлементный состав в крови больных ПА оказывают влияние Hg и Pb. Регрессионный анализ свидетельствует об отсутствии зависимости концентраций в крови больных подагрой B, Ba, Mn, Pb и S от содержания МЭ в почве, тогда как уровень Li и Sr тесно связан со всеми из них. Обращает на себя внимание всегда отрицательная связь с микроэлементным составом почвы параметров кобальтемии, от показателей Мо МЭ в крови имеют прямую зависимость, а от Ni — обратную.
Статистическая обработка полученных результатов исследования позволила сделать следующее заключение:
- с содержанием МЭ в почве тесно связан уровень в крови Li и Sr;
- от микроэлементного состава почвы не зависят показатели B, Ba, Mn, Pb и S; 3) концентрацию в крови Со определяют Cr, Cu, Hg, Mn, Pb, Sn, Ti, V и Zn, Cu — Be, Ni и Ti, Fe — Bi, Co, Li, Ni, Ti и V, Zn — Ba, Co, Li, Mo, Ni и V.
Содержание в крови Ba, Cu, Li, Mn и Zn связано с уровнем одноименных МЭ в грунтовых водах. Если все изученные МЭ оказывают воздействие на концентрации в крови Sr и Zn, то параметры Pb и S ни с одним из них не связаны. Отсутствует влияние на уровень ферремии только Zn. Регрессионный анализ выявляет также зависимость показателей в крови Cu, Li и Zn от содержания одноименных МЭ в грунтовых водах, но в первых двух случаях обратную связь, а в третьем — прямую. Отсутствуют связи концентраций в крови B, Ba, Mn, Pb и S с микроэлементным составом грунтовых вод, тогда как содержание Cu и Li зависит от всех изученных МЭ. Необходимо отметить, что показатели в крови Cu, Li и Sr с МЭ в воде имеют обратные связи, а Zn — прямые.
В обобщенном варианте мы установили, что от содержания МЭ в почве и грунтовых водах (фактически, от экологической ситуации в регионе) в наибольшей степени зависит концентрация в крови больных ПА Li (связь c Ba, Li, Mn, Ni, Pb, Ti), в меньшей — Sr (c Mn, Ni, Pb, Ti). Необходимо отметить, что у больных подагрой показатели в крови Li и Sr достоверно выше, чем у здоровых людей.
Со всеми изученными МЭ в почве связаны концентрации в волосах B и Zn. На содержание Al, Co, Cu, Fe, Li, Pb и Sn не влияет только V, на Ва и Bi — лишь Cu, тогда как уровень Ве в волосах вообще не зависит от микроэлементного состава почвы, а Cr и Se определяет исключительно Pb, Sb — Hg. Зависимость параметров МЭ в волосах отсутствует в отношении уровней в почве Be, Bi, Cu, Hg, Mo и Sn. Не выявлено связей с микроэлементным составов в почве показателей Al, As, Ba, Be, Cd, Cu, Mn, Mo и Pb. Содержание Bi и Cr зависит только от Cr, Li, Sb и Zn от Ti.
Все МЭ в грунтовых водах достоверно влияют на концентрации в волосах больных подагрой Al, As, B, Co, Cu, Fe, Li, Ni, Pb, S, Sn, Sr и V, тогда как содержание Be, Cr, Sb и Se с этими экологическими факторами не связано. Регрессионный анализ демонстрирует отсутствие зависимости в волосах лишь показателей Li. В большей степени МЭ в волосах связаны с Ва (B, Be, Cd, Co, Fe, Li, Ni, Pb, Sb, Se, Sn, Zn), а уровень В чаще зависит от микроэлементного состава грунтовых вод (от Ba, Cu, Mn, Ni, Pb, Ti, Zn).
Концентрации в волосах B, Li, Ni, Sb, Sn и Zn прямо зависят от уровня МЭ в воде, а Be, Cd, Co, Fe, Pb и Se — обратно. С учетом проведенной статистической обработки полученных данных исследования можно говорить о связях с показателями Ва в грунтовых водах B, Co, Fe, Li, Ni, Pb, Sn и Zn, c Cu — B, Sn и Zn, c Mn — B и Co, c Zn — B и Co, a B, кроме того, — c Ni, Pb и Ti.
Принимая во внимание микроэлементный состав почвы и грунтовых вод, Ba, Ni и Ti оказывают воздействие на содержание в волосах больных подагрой В и Li. С этими МЭ в окружающей среде отчасти связаны показатели в волосах Sr. В обобщенном виде отсутствует влияние только параметров Cu в почве и Li в грунтовых водах на показатели МЭ в волосах больных ПА. С окружающей средой преимущественно связаны концентрации в организме B, Co, Fe, Li, Sr и Zn, тогда как содержание Mn в крови и Pb в волосах определяет только уровень в почве Ва.
На локализацию суставного синдрома при псориазе не оказывают воздействия показатели в почве Cr, Hg, Mn, Mo, Sn и Ti. В свою очередь, не зависит от содержания МЭ в почве зон проживания больных вовлечение в патологический процесс грудинно-ключичных, верхнечелюстных, пястнофаланговых, локтевых, плечевых, дистальных межфаланговых кистей, коленных, тазобедренных, крестцово-подвздошных суставов, грудного и поясничного отделов позвоночника. На частоту поражения дистальных межфаланговых сочленений пальцев рук оказывают воздействие уровни в почве Ва и Zn, проксимальных — Ba, Li и Zn, лучезапястных — Bi, проксимальных стоп — V, плюснефаланговых — Co и Cu, голеностопных — Ni и Pb, шейного отдела позвоночника — Ва и Ве. Регрессионный анализ показывает прямую зависимость тяжести ПсА от Bi, Co и V, а с Ba, Be, Cu, Li, Ni, Pb и Zn существуют обратные связи. По данным дисперсионного анализа, на распространенность артрита оказывает воздействие только концентрация в почве Sn.
Узурация поверхностей костей и анкилозирование суставов не связаны с уровнем МЭ в почве зон проживания больных ПсА. На характер структурных изменений опорно-двигательного аппарата не влияют концентрации Co, Cr, Cu, Li, Mn, Ni, Pb и V. В свою очередь, на степень сужения артикулярных щелей оказывают воздействие Ba, Be, Hg, Mo, Sn и Zn. Кроме того, от Ва зависят процессы формирования остеокистоза и эпифизарного ОП, от Мо — только ОП, от Bi — лигаментоза, от Ti — субхондрального склероза, остеофитоза и остеокистоза.
Отсутствует влияние отдельных МЭ в грунтовых водах на форму псориаза, тогда как содержание Li оказывает воздействие на степень активности ПсА. Вместе с тем не обнаруживается достоверных корреляционных связей с уровнем Li в воде таких показателей, как скорость оседания эритроцитов, концентрации в крови С-реактивного протеина, фибриногена и b2-микроглобулина. Распространенность суставного синдрома при ПсА обратно коррелирует с содержанием в грунтовых водах зон проживания больных Zn. Не связано с микроэлементным составов в воде вовлечение в патологический процесс верхнечелюстных, пястнофаланговых, плюснефаланговых, коленных, тазобедренных, дистальных межфаланговых суставов кистей и стоп, крестцово-подвздошных сочленений, а также грудного и поясничного отделов позвоночника. В противоположность сказанному, параметры в воде Cu оказывают воздействие на поражение локтевых суставов и шейного отдела позвоночника, Mn — только позвоночника, Pb — проксимальных межфаланговых суставов кистей и стоп, Li — грудино-ключичных сочленений, Ni — лучезапястных суставов, Zn — плечевых, Ti — голеностопных. Zn определяет степень сужения суставных щелей, остеокистоза и ОП, Ва — субхондрального склероза и остеофитоза, Ni — узураций артрикулярных поверхностей костей.
Содержание в почве Ba, Be, Bi, Cu, Ti и V не влияет на концентрацию в крови изученных МЭ, а уровни в крови Ba, Cu, Li, Pb, Sr и Zn не связаны с микроэлементным составом почвы зон проживания больных. Как показывает дисперсионный анализ, на показатели боремии оказывают достоверное воздействие параметры в почве Co, Hg, Li, Ni, Pb, Sn и Zn, кобальтемии — Cr, Mn, Sn и Zn, ферремии — Li, магниемии — Mo. Регрессионный анализ свидетельствует о зависимости от уровня Bi в почве показателей в крови Sr, соответственно от Co — Co, от Cr — Zn, от Li — Sr, от Sn — Co и Zn, от V — Co, от Zn — Co. С учетом представленных данных можно сделать следующие заключения: 1) существует зависимость от микроэлементного состава почвы только концентраций в крови больных ПсА Co, Sr и Zn; 2) лишь параметры кобальтемии прямо связаны с одноименным МЭ в почве; 3) содержание в крови Со и Zn с уровнями МЭ в почве имеет обратные связи, а Sr — прямые; 4) принимая во внимание дисперсионный анализ, только показатели в крови Со определяют МЭ в почве (Sn и Zn).
При сопоставлении МЭ в крови больных ПсА и в окружающей почве установлены соответственно корреляционные связи В с Ва, Hg, Li, Sn и Zn, Со — с Mn, Sn, Ti и Zn, Mn — c Mo, Pb — c Cu, Sr — c Mn и Ti. Отсутствуют корреляции концентраций МЭ в крови при ПсА с содержанием в почве Be, Bi, Co, Cr, Ni и Pb, а также МЭ в почве с уровнями в крови Ba, Cu, Fe, Li и Zn. Обращают на себя внимание прямые корреляционные связи с микроэлементным составом в почве параметров в крови В и обратные — Со. Дисперсионный, регрессионный и корреляционный анализы установили четкую зависимость показателей кобальтемии с содержанием в почве Sn и Zn.
Только уровень в грунтовых водах Ni и Pb оказывает влияние на концентрации в крови больных ПсА МЭ, причем лишь соответственно Cо и Li. Существуют корреляционные связи между параметрами в воде Ni и в крови Co, между Pb и Li. Необходимо отметить, что уровень литемии прямо коррелирует с содержанием в грунтовых водах Ва, а стронцемии обратно соотносится с показателями Ti.
На микроэлементный состав в волосах больных ПА не влияет уровень в почве Ba, Co, Cu и Mo. В свою очередь, с содержанием МЭ в почве не связаны концентрации в волосах Al, As, B, Be, Bi, Sb, Se и Sn. В наибольшей степени с МЭ в почве связаны показатели Cr, а наибольшее влияние оказывают параметры Li и Pb. Мы обнаружили, что лишь уровни в крови Cr и Li определяют содержание в почве одноименных МЭ. Параметры в почве Ве влияют на концентрацию в крови Cu, Bi — Ba, Ni и Sr, Cr — Pb, Hg — Cr и Zn, Li — Cd, Co, Cr, Fe, Mn и Zn, Mn — Cr и Mo, Ni — Cr, Pb — Cr, Cu, Li, Mo, Sr и V, Sn — Co и Pb, Ti — Pb, V — Mo, Zn — Cd и Pb.
Регрессионный анализ показывает зависимость только трех одноименных МЭ в волосах больных ПсА от их содержания в почве (Ba, Be, Bi). Не обнаружено связей микроэлементного статуса в волосах от параметров в почве Cr, Cu, Li, Mn, Pb, Sn и Zn. От Ва зависят концентрации Al, B, Be, Cd, Co, Cr, Fe, Li, Mn, Ni, Pb, Se и Sr, от Be — Al, Cr, Fe, Mn, Ni и Sr, от Bi — B, Ba, Co, Pb и V, от Co — Cu и Se, от Hg — B, Cd, Fe, Pb и Se, от Mo — Al, Cd, Cr, Cu, Fe, Mn, Ni и Sr, от Ni — Cu и Se, от Ti — Al, As, B, Ba, Be, Mo и Pb, от V — Bi. С учетом дисперсионного анализа наибольшая связь содержания МЭ в волосах при ПсА касается Ва и Pb, соответственно с Bi и Ti.
Уровни Sn и Zn волосах прямо коррелируют с одноименными МЭ в почве. Кроме того, существуют корреляционные связи показателей Ва в почве с B и Co, Be — только c Co, Bi — c Ni, Li — c Mn, Mn — c B, Pb — c As и Cu, Sn — c B, Co, Cr и Se, Ti — c Ba и Pb, V — c Cu, Zn — c Co и Sn. Содержание Mn и Zn в грунтовых водах не влияет на уровень МЭ в волосах больных ПсА. Микроэлементный состав грунтовых вод не отражается на концентрации в волосах Al, As, Bi, Cd, Co, Fe, Mn, Mo, Sb, Se, Sn, V и Zn, тогда как на уровень в волосах B оказывают воздействие показатели Li, Ba — Ni, Be — Ti, Cr — Pb, Pb — Ва и Ti, Sr — Pb. Следует подчеркнуть, что имеют место и связи одноименных МЭ. Так, сказанное касается Cu, Li и Ni. От параметров в грунтовых водах Cu зависят концентрации в волосах больных ПсА Be, Bi, Cr, Mn, Sb и Zn, Li — Cr, Fe, Mn, Ni и Sr, от Mn — Be, Mn, Mo, Ni и Sb, от Ni — Al, B, Be, Bi, Cd, Co, Cr, Cu, Fe, Mn, Ni, Sb, Se и V, от Pb — B, Co и Mo. Таким образом, существуют достоверные связи содержания Mn и Ni в волосах от уровня одноименных МЭ в грунтовых водах. С содержанием Mn и Zn в воде ни один из показателей МЭ в волосах не коррелирует, тогда как уровень в волосах Cu имеет достоверные корреляционные соотношения с Ba, Cu и Pb, Bi и Ni — c Ni, Sb — c Li, Pb — c Ti. Выполненные дисперсионный, регрессионный и корреляционный анализы указывают на факт наибольшей связи с микроэлементным составом грунтовых вод таких МЭ в волосах больных ПА, как Cu, Ni и Pb.
Несколько неожиданными оказались прямые связи ОА с Mn в почве, так как у кролей с моделью заболевания аскорбат Mn положительно влияет на процессы деградации хряща. Mn, как эссенциальный (необходимый) МЭ, необходим для функционирования гликозилтрансферазы, участвующей в биосинтезе хондроитин-сульфата (основного компонента суставного хряща), а его дефицит в организме способствует развитию ОП и дегенеративным изменениям периартикулярных тканей.
По нашим данным, уровень истинных металлов в волосах больных ОА не зависит от содержания в почве Hg, Sn и Zn, а щелочных и щелочно-земельных металлов — от Ва, Be, Co и Li. В свою очередь, по данным регрессионного анализа, концентрация Zn в волосах обратно связана с содержанием в почве Ва, Bi, Mn, Ni и Pb. С уровнем Co, Cu, Mo и V в почве соотносится содержание в волосах Mn, c Ti и Li — Cu. Показатели Cd в волосах при ОА зависят от параметров в почве Be, Mg и Ni, Co — от Be, Bi и Cr, Cu — от Cr и Pb, Fe — от Bi и Mg, Mn — от Ва, Cr, Mg, Ni и Pb, Pb — от Ва, Bi, Cr, Mg, Mn и Ni.
Однофакторный дисперсионный анализ показывает влияние на содержание Cd в волосах уровней Be, Mg и Ni в почве, на Co — Be, Bi и Cr, на Cu — Li и Pb, на Fe — Bi, на Mn — Co и Ni, на Pb — Bi и Cr, на Zn — Ва, Bi, Ni и Pb. Содержание К в волосах зависит от уровней в почве Cr, Mn, Sn и V, Li — от Bi и Mg, Na — от Mn, Ni, Pb и V, Ва — от Cu, Mg Mn, Mo, Ti и V, Са — от Mg, Ni и Pb, Mg — от Cr, Hg, Mg, Mn, Ni, Pb, Sn, Ti и V, Sr — от Co, Cr, Cu, Hg, Mg, Mn, Mo, Ni, Pb, Sn и Zn. Необходимо отметить, что концентрация Mg в волосах со всеми металлами в почве имеет прямую связь, а Sr — обратную. Дисперсионный анализ свидетельствует о достоверном влиянии на показатели Mg и Sr в волосах всех металлов в почве, на К — Cr, Mn, Sn и V, на Li — Bi и Mg, на Na — Pb и V, на Ba — Mn и Mg, на Са — только Mg. Подчеркнем, что между концентрациями Mg в почве и волосах больных ОА существует прямая регрессионная зависимость.
Содержание щелочных и щелочно-земельных металлов в крови больных ОА не зависит от уровня Cu в почве. В свою очередь, показатели Сd в крови тесно связаны с концентрациями Cr, Cu, Mg и V, Co — c Be, Co, Hg, Mn, Mo, Ni и Zn, Cu — c Ва, Cr, Cu, Hg, Li, Mg, Mn, Sn, Zn, Fe — c Ва, Be, Cr, Cu, Hg, Li, Mg, Mn, Ni, Sn, Ti и Zn, Mn — c Pb и Mg, Pb — c Be, Cr, Cu, Hg, Mn, Ni, Pb, Sn и Zn, Zn — c Be, Bi и Cr, K — c Bi, Pb, Sn и Mg, Li — c Be, Co, Cr, Mn, Ni и Pb, Na — c Bi, Co, Sn и Ti, Ba — c Ва, Be, Bi, Co, Hg, Mo, Sn и Zn, Ca — c Ва, Hg, Mo, Ni, Pb, Sn и V, Mg — c Ва, Bi, Co, Cr, Mg, Mo, Ni, Pb и V, Sr — c Co, Hg, Mo и Sn. Связи одноименных металлов в крови больных ОА с уровнем их в почве более отчетливы. Так, имеет место зависимость Ва, Co, Cu, Mg и Pb. Обращает на себя внимание прямая зависимость содержания в крови Ва, Li, Co и Pb с показателями металлов в почве, а обратная касается Ca, Mg, Sr, Cu и Fe. На концентрацию в крови Ba, Ca, Co, Fe, Mg и Pb оказывают влияние все без исключения химические элементы в почве, на Cd — Cr и Cu, на Cu — Mn, Sn и Zn, на Mn — Pb, на Zn — Be, Bi и Cr, на K — Mg, на Li — Be, Mn, Ni и Pb, на Na — Ti, на Sr — Co, Hg, Mo и Sn.
От содержания Cu, Ni и Li в грунтовых водах уровень металлов в волосах больных ОА не зависит, тогда как концентрация Cd связана с показателями в воде Cu, Ni, Ti и Zn, Co — c Cu и Mn, Cu — с Pb и Ti, Fe — c Ni, Mn — c Ва, Ni, Pb и Zn, Pb — c Ва, Mn, Ti и Zn, Zn — c Ва, Cu, Pb и Zn, K — c Ва, Mn и Pb, Li — c Mn и Zn, Na — c Ва, Mn и Pb, Ba — Ва и Ti, Ca — c Pb и Zn, Mg — c Ва, Mn, Pb, Ti и Zn, Sr — c Ва, Mn, Pb и Ti. Дисперсионный анализ свидетельствует о влиянии всех химических элементов в грунтовых водах на показатели в волосах Cd, Zn, K, Mg и Sr при полном отсутствии такого воздействия на содержание Ва, Са и Cu. Кроме того, уровень в волосах Со зависит от Cu и Mn, Fe — от Ni, Mn — от Ni и Pb, Pb — от Ti, Li — от Mn и Zn, Na — от Mn. Параметры в волосах Cd и Sr с металлами в грунтовых водах имеют отрицательную связь.
Содержание в крови Cu, Fe и Na от показателей макро- и микроэлементов в воде не зависит, а уровень Cu в воде определяет только параметры в крови щелочных и щелочно-земельных металлов. Концентрация в крови Cd связана с Ва, Mn, Ti и Zn, Co — c Ti и Li, Mn — c Pb и Li, Pb — c Ва, Mn и Ti, Zn — c Ва, Ni и Ti, K — Ва, Pb и Li, Li — c Cu, Mn, Ti и Zn, Ba — c Ni, Zn и Li, Ca — c Ва, Cu, Ni, Pb, Ti и Zn, Mg — c Ва, Pb и Zn, Sr — c Mn, Ni и Ti. Если влияние металлов в грунтовых водах на показатели натриемии у больных ОА отсутствует, то отмечается четкая связь со всеми химическими элементами в воде Са, Cd, Mg и Sr. Кроме того, на содержание Со воздействуют Ti и Li, на Mn — Pb и Li, на Pb — Ва, Mn и Ti, на Zn — Ni, на K — Ba, на Li — Mn и Zn, на Ba — Li. Уровень Pb в окружающей среде полностью определяет содержание Mg в волосах и крови больных ОА. Ni влияет на Mn в волосах, Ва — на Zn, Mn — на К, Mg и Sr, Ti — только на Mg, Pb — лишь на Sr, показатели Ве в почве — на содержание в организме Со, Cr — на Pb, Bi — на Zn, Cr, Ni, V и Mg — на Mg, Co, Hg, Mo и Sn — на Sr, параметры в грунтовых водах Ti и Zn — на Сd, только Ti — на Pb и Sr, Pb — на Mn, Ba — на К, Mn и Zn — на Li, Ва и Zn — на Mg.
Многофакторный дисперсионный анализ показывает, что условия окружающей среды проживания людей и характера их трудовой деятельности оказывают влияние на интегральный уровень металлов в волосах и крови больных ОА. Достоверное воздействие испытывают параметры в волосах Al, Ва, Са, Cd, Co, Fe, К, Li, Mo, Na, Pb, Sb, Sr и V. Среди значений содержания металлов в крови сказанное касается Са, Cd, Co, Cu, Fe, Mg, Pb, Sr и Zn. Среди токсичных элементов в окружающей среде Ва способствует повышению в организме токсичного Pb и снижению эссенциального Zn, показатели которого у больных ОА также обратно зависят от содержания в почве и грунтовых водах Bi и Pb, а Со — от Ве, Cu от Zn.
Экологические условия окружающей среды оказывают влияние на клиническое течение ОА и рентгенологические признаки поражения суставов. От указанных факторов зависят распространенность ОА, тяжесть периферического суставного синдрома и спондилоартроза, развитие синовита и остеофитоза. Тяжесть течения заболевания и спондилоартроза, а также выраженность синовита определяются уровнями выброса в атмосферу зон проживания людей химических веществ и степенью накопления промышленных отходов. Кроме того, первый фактор оказывает воздействие на распространенность периферического ОА, а второй — на развитие субхондрального склероза, остеофитоза и лигаментоза.
Уровень химических элементов в почве зон проживания больных ОА оказывает воздействие на характер суставного синдрома, а развитие реактивного синовита тесно связано с содержанием Ва, Be, Bi, Cu, Hg, Li, Mg, Mo, Ni, Pb, Sn и Zn. На появление узелков Гебердена и/или Бушара при ОА влияет содержание в почве Bi, Co, Hg и Ti, на рентгенологическую стадию патологического процесса — Ве, Co, Cr, Li и V, на тяжесть спондилопатии — Ве, Co, Cr, Mg и V. Все перечисленные факторы регрессионно зависят от концентраций в почве Hg, Li, V и Zn. Кроме того, стадия ОА определяется уровнями Co, Mo и Ti, а выраженность спондилопатии — Be, Co, Ni и Sn.
Развитие субхондрального склероза тесно связано с содержанием в почве Be, Bi, Hg, Li и Mg, эпифизарного ОП — с Li, Mo и Ti, остеофитоза — с Ва, Be, Cu, Pb, Ti и V, остеокистоза — только с Sn, узурации костей — с Cr, Mg, Mn и V, лигаментоза — с Ва, Bi, Cu, Hg, Mn, Mo, Sn и Zn. Появление реактивного синовита при ОА определяется концентрацией в грунтовых водах Li, Ni и Pb, наличие узелков Гебердена — Бушара — Mn и Zn, стадия болезни — Li, тяжесть спондилопатии — Pb. Распространенность периферического ОА обратно зависит от уровня в воде Ti и Zn, стадия заболевания — от Li, тяжесть спондилопатии — от Mn и Zn, выраженность периферического ОА прямо связана с содержанием в грунтовых водах Mn. На развитие субхондрального склероза влияет содержание в грунтовых водах Ва, Ni и Li, на эпифизарный ОП — Zn, на остеофитоз — Pb и Ti, на остеокистоз — Cu, на лигаментоз — Cu, Mn, Ti и Zn.
Влияние на распространенность РА концен-трации Zn в подземных водах согласуется с данными литературы. Как высокий, так и низкий уровень Zn в крови у больных РА способствует прогрессированию течения заболевания, причем гиперцинкемия часто ассоциируется с развитием системных проявлений и прямо коррелирует с концентраций в сыворотке провоспалительных цитокинов. Из-за повышенного уровня Zn в синовиальной среде суставов больных РА возрастает протеолитическая активность матриксной металлопратеиназы.
Факторами риска развития РА считаются высокие концентрации в атмосфере кремния. Сказанное подтверждается эпидемиологическими обследованиями людей, контактирующих с кремнеземом. На линейных мышах MRL, являющихся естественной моделью РА, показано ухудшение течения патологического процесса после пребывания животных в атмосфере, богатой кремнийсодержащей пылью. Как известно, крупномасштабное производство стройматериалов наиболее неблагоприятно в отношении выброса кремнезема в окружающую среду. Между тем, о чем речь шла выше, такая отрасль промышленности не оказывает существенного влияния на распространенность РА.
Обсуждается роль климата с длительной повышенной инсоляцией в отношении развития РА и АС. Длительность солнечного сияния в изученных нами климатических регионах составляет 1727,0 ± ± 78,4 ч/год, количество дней с температурой воздуха менее –10 °С — 41,0 ± 1,1, а число дней с междусуточной изменчивостью относительной влажности воздуха на 20 % и более — 23,0 ± 0,9. Только низкая температура и влажность воздуха влияют исключительно на распространенность РА.
В обобщенном виде можно сделать следующие заключения: распространенность заболеваний суставов зависит от мощностей энергетической промышленности и удельного веса в регионе сельского хозяйства, РА — от климатических условий (температура и влажность воздуха), химической (коксохимической) промышленности, концентраций в почвах и подземных водах Ba, Li, Mn, Тi и Zn, АС — от уровня накопления в окружающей среде неутилизированных промышленных отходов и содержания в зоне обитания человека Cu, ПА — от функционирования металлургической, химической и машиностроительной отраслей, влияния на организм Cr, Mo, Pb и V, ОА — от степени выброса в атмосферу вредных химических соединений, в частности диоксида серы, оксида углерода и сероводорода, воздействия Mn, Sn и Zn.
В целом эскалация нарушений естественных связей человека с природой и дальнейшая плохая экология становятся факторами роста численности больных и артрологического профиля. В связи с этим вспомним крылатое выражение Гиппократа: «Natura sanat, medicus curat» («Врач лечит, но здоровье приносит природа»). Бездумное отношение к последней через необузданную урбанизацию и неконтролированное уничтожение среды обитания людей может сделать деятельность врачей просто малозначимой для эффективной борьбы с заболеваниями суставов. Вместе с тем не все так печально, о чем свидетельствуют данные представленных исследований. Некоторые заболевания нашли какие-то свои «способы противодействия» катастрофическому состоянию неблагоприятной экологической обстановки в крупных промышленных регионах. Хочется надеяться, что общими усилиями властных структур, представителей разных отраслей промышленности, гигиенистов и ревматологов-артрологов будут разработаны конкретные, принципиально новые методы борьбы с болезнями опорно-двигательного аппарата.
