Газета «Новости медицины и фармации» Кардиология (439) 2012 (тематический номер)
Вернуться к номеру
Современные позиции индапамида SR 1,5 мг в лечении артериальной гипертензии
Авторы: Л.В. Богун, ГУ «Институт терапии им. Л.Т. Малой НАМН Украины», г. Харьков
Рубрики: Кардиология
Разделы: Справочник специалиста
Версия для печати
Тиазидные и тиазидоподобные диуретики сохраняют ключевые позиции в современных схемах антигипертензивной терапии: они принадлежат к антигипертензивным препаратам 1-го ряда и в то же время являются эффективной составляющей комбинированной антигипертензивной терапии, причем включение в схемы антигипертензивной терапии диуретиков улучшает кардиоваскулярный прогноз при артериальной гипертензии (АГ) [1–3]. Механизм действия тиазидоподобных диуретиков сходен с таковым тиазидов: обе группы лекарственных средств являются производными сульфаниламида, действуют в начальной части дистальных отделов собирательных канальцев, где в норме происходит реабсорбция 5–10 % профильтрованного в провизорную мочу натрия и хлора, подавляя реабсорбцию ионов натрия и хлора [4]. Хотя дискуссии о равноценности и взаимозаменяемости тиазидных и тиазидоподобных диуретиков в лечении АГ продолжаются, однако в настоящее время имеются многочисленные данные о превосходстве тиазидоподобных диуретиков, что нашло свое отражение, в частности, в рекомендациях британских экспертов, согласно которым при необходимости назначения диуретиков больным АГ предпочтение следует отдавать именно тиазидоподобным препаратам [5]. В настоящее время синтезировано четыре тиазидоподобных диуретика: хлорталидон, индапамид, метолазон и хинетазон, из которых на украинском рынке два последних препарата не зарегистрированы, а хлорталидон доступен только в виде фиксированных комбинаций [6, 7]. Индапамид зарегистрирован в Украине в виде как фиксированных комбинаций, так и монопрепарата [7].
Сохраняя все свойства своего класса, индапамид имеет и уникальные отличительные особенности, что делает его особенно привлекательным в лечении АГ. Начало клинического применения индапамида в качестве антигипертензивного препарата датируется 70ми гг. прошлого века, однако, несмотря на длительный опыт его использования, некоторые его фармакологические свойства изучены не до конца, хотя диуретический и вазоактивные механизмы четко определены [8, 9].
В исследованиях, проведенных у здоровых добровольцев, в ответ на разовый прием индапамида в дозе 2,5 мг в форме выпуска с немедленным высвобождением (IR) наблюдалось существенное увеличение натрийуреза [10], при разовом приеме более низких доз в форме IR (0,5 и 1,0 мг) такого эффекта не наблюдалось [11]. Длительный прием 2,5 мг индапамида IR однократно в сутки пациентами с АГ не оказывал существенного влияния на обмен натрия [12], однако небольшой дефицит натрия все же может иметь место, о чем свидетельствует активация ренинангиотензинальдостероновой системы (РААС) [13].
В экспериментальных и клинических исследованиях было доказано наличие у индапамида вазодилатирующего эффекта, который вносит свой вклад, по крайней мере частичный, в его гипотензивный эффект [14, 15]. Вазодилатирующий эффект индапамида связан с нормализацией повышенной реактивности сосудов к множеству вазопрессорных факторов (ангиотензин II, тромбоксан А2, норадреналин и др.), уменьшением количества свободных радикалов за счет подавления пероксидации липопротеинов низкой плотности, повышением активности эндотелиального фактора расслабления и предотвращением повреждения эндотелия, со снижением периферического сосудистого сопротивления у больных эссенциальной АГ [8, 16, 17].
Индапамид также в определенной мере обладает свойствами антагониста кальция [18]. Помимо ингибирования котранспортера Na+/Cl– и торможения реабсорбции натрия в дистальных извитых канальцах — свойства, присущего всему классу тиазидов, индапамид способен ингибировать карбоангидразу почек с константой диссоциации 24 нмоль/л и константой ингибирования 400 нмоль/л [19]. Подавление активности карбоангидразы приводит к повышению внутриклеточного рН, в результате чего активируются кальцийактивируемые калиевые каналы большой проводимости в гладкомышечных клетках сосудов и снижается приток кальция внутрь клетки через вольтажзависимые каналы, что сопровождается вазорелаксацией [20].
Важной особенностью индапамида, отличающей его от других тиазидных/тиазидоподобных диуретиков, является независимость его антигипертензивной активности от диуретической, о чем свидетельствует сохранение его антигипертензивной эффективности у больных с хронической болезнью почек [21, 22] и у больных с анефрией, находящихся на постоянном гемодиализе [10].
Липофильность индапамида в 5–80 раз выше липофильности других тиазидных диуретиков, в результате чего индапамид обладает способностью к выраженной аккумуляции в гладкомышечных клетках сосудов [23].
В 90е гг. XX в. были сформулированы требования к идеальному антигипертензивному препарату, которые заключаются в обеспечении длительного эффекта в течение 24 ч при однократном дозировании в сутки и стабильного антигипертензивного действия с наименьшими колебаниями концентрации в крови.
Для решения этой задачи при создании лекарственной формы индапамида с замедленным высвобождением (sustained release — SR) действующего вещества были использованы новейшие технологии производства лекарственных форм пролонгированного действия. Наибольшее значение для поддержания стабильного антигипертензивного эффекта имеет процесс всасывания лекарственного препарата в желудочнокишечном тракте. Антигипертензивный препарат не должен всасываться одномоментно, что повлечет резкие перепады его концентрации в крови и неустойчивость клинического эффекта в течение всего периода лечения. Чтобы добиться медленного высвобождения и всасывания препарата, при создании индапамида SR 1,5 мг были использованы сложные транспортные системы. Технология создания ретардной формы индапамида объединила влажную грануляцию, позволяющую равномерно распределять малые количества лекарственного вещества, и добавление гельобразующего полимера (целлюлоза), обеспечивающего эффект замедленного высвобождения. Соотношение этих компонентов в данной лекарственной форме обеспечивает высвобождение 70 % индапамида на протяжении около 16 ч, при этом период полувыведения индапамида существенно не изменяется [23].
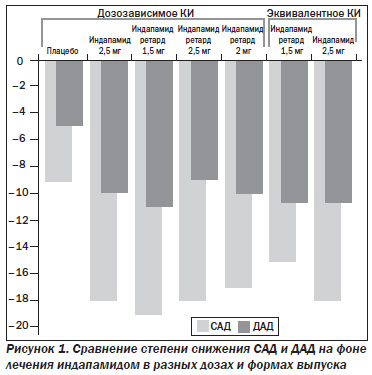
Сравнение клинической эффективности индапамида SR в дозе 1,5 мг/сут, индапамида SR в дозах 2,0 и 2,5 мг/сут и индапамида IR в суточной дозе 2,5 мг проведено в рандомизированном двойном слепом плацебоконтролируемом исследовании, включившем 285 больных с эссенциальной АГ в возрасте 18–70 лет [21]. Применение индапамида SR в дозировке 1,5 мг/сут оказывало гипотензивный эффект (–19/11 мм рт.ст.), сопоставимый с другими дозировками индапамида SR (2,0 и 2,5 мг) и с индапамидом IR 2,5 мг (–18/10 мм рт.ст.), но достоверно более выраженный по сравнению с плацебо (–19/11 мм рт.ст. против –9/5 мм рт.ст., р ≤ 0,01) (рис. 1).
В сравнительном исследовании на здоровых добровольцах проведено изучение фармакокинетики двух форм выпуска индапамида — индапамида IR 2,5 мг и индапамида SR 1,5 мг [25]. Результаты исследования показали, что время достижения пиковой концентрации препарата в крови возрастает с 0,8 до 11 ч, а максимальная концентрация препарата в крови снижается со 153 до 58 мкг/л, в то время как минимальная концентрация препарата в крови изменений не претерпевает. Таким образом, форма SR не только сглаживает колебания концентрации препарата в крови, но также снижает соотношение пиковой концентрации и конечной со 160 до 40 %, что уменьшает вероятность развития дозозависимых нежелательных лекарственных эффектов.
Согласно современным требованиям к антигипертензивной терапии, современный антигипертензивный препарат должен не только обеспечивать 24часовой контроль артериального давления (АД) при однократном применении в сутки [1], но и сохранять свою эффективность и переносимость при длительном применении. Индапамид SR 1,5 мг удовлетворяет этим требованиям, что было доказано в исследовании P. Weidmann, в котором прием препарата 324 пациентами на протяжении 12 месяцев вызывал нежелательные лекарственные явления, потребовавшие отмены препарата, только у 3 % больных — намного реже по сравнению с другими классами антигипертензивных препаратов [26].
Антигипертензивная эффективность индапамида SR сохраняется на протяжении суток при однократном приеме с благоприятным влиянием на суточный профиль АД, отсутствием резких подъемов АД и ортостатической гипотензии и высоким показателем соотношения Т/P (trough/peak ratio — соотношение конечного/пикового эффектов): 89 % для систолического АД (САД) и 85 % — для диастолического (ДАД), что удовлетворяет требованиям Управления по контролю качества пищевых продуктов и лекарственных препаратов США (US Food and Drug Administration (FDA)), согласно которым соотношение Т/Р должно составлять не менее 50 % [27]. Кроме того, проведенные исследования с применением 32часового периода суточного мониторирования АД (СМАД) показали, что лекарственная форма индапамида SR 1,5 мг способствует продлению гипотензивного действия, о чем свидетельствует высокий индекс Т/P даже через 32 ч после приема последней дозы индапамида SR 1,5 мг: 52 % — для САД и 54 % — для ДАД, что соответствует критериям FDA [28]. Данный результат имеет важное практическое значение для больных с АГ в случае несоблюдения 24часового интервала дозирования или пропуска доз [29].
Таким образом, форма выпуска индапамида SR обеспечивает длительный эффективный контроль АД при использовании более низких доз действующего вещества, позволяет избежать чрезмерных колебаний концентрации препарата в плазме крови, что сводит к минимуму риск нежелательных дозозависимых лекарственных явлений, в первую очередь гипокалиемии [30].
Сравнение антигипертензивной эффективности монотерапии индапамидом SR и монотерапии другими классами антигипертензивных препаратов представлено в метаанализе J.P. Baguet et al. [31]. В данном метаанализе, включившем 72 рандомизированных двойных слепых плацебоконтролируемых исследования c участием 9094 пациентов, сравнивалось влияние на уровень АД монотерапии основными классами антигипертензивных препаратов. Из всех проанализированных классов индапамид SR в дозе 1,5 мг/сут оказался наиболее эффективным в снижении САД (–22,2 мм рт.ст.) при сопоставимом с другими классами антигипертензивных препаратов действии на уровень ДАД (–11,7 мм рт.ст.).
Способность индапамида SR эффективно снижать АД была показана в исследовании XCELLENT [32]. В этом рандомизированном двойном слепом плацебоконтролируемом исследовании, включившем 1758 пациентов в возрасте от 40 до 80 лет с систолодиастолической или изолированной систолической АГ (ИСАГ), сравнивалась антигипертензивная эффективность индапамида SR 1,5 мг/сут, антагониста рецепторов ангиотензина II (АРА) кандесартана 8 мг/сут и антагониста кальция амлодипина 5 мг/сут. Дозировки кандесартана и амлодипина были выбраны с учетом действующих на момент планирования исследования рекомендаций по выбору стартовых доз антигипертензивных препаратов. Результаты исследования показали равную эффективность всех трех препаратов в снижении САД и ДАД и превосходство всех трех над плацебо.
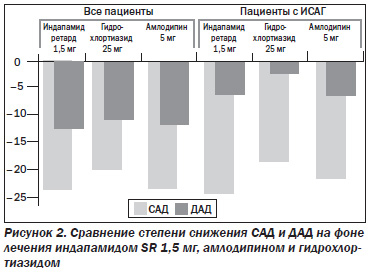
В исследовании J.P. Emeriau et al. была доказана антигипертензивная эквивалентность индапамида SR 1,5 мг/сут, амлодипина в дозе 5 мг/сут и гидрохлортиазида в суточной дозе 25 мг, при этом индапамид SR 1,5 мг превосходил амлодипин по безопасности за счет меньшего числа случаев развития претибиальных отеков [33] (рис. 2).
В исследовании LIVE у 411 больных с АГ и гипертрофией левого желудочка — ГЛЖ (по данным эхокардиографии индекс массы миокарда > 100 г/м2 для женщин и > 120 г/м2 для мужчин) двойным слепым методом сравнивали эффективность индапамида SR 1,5 мг и эналаприла 20 мг в регрессе ГЛЖ через 1 год лечения. Гипотензивная эффективность двух препаратов была сопоставимой: степень снижения САД/ДАД составила 25,2/12,8 мм рт.ст. в группе индапамида SR 1,5 мг и 24,5/12,4 мм рт.ст. в группе эналаприла, а число респондеров — 60 и 61 % соответственно. Таким образом, в исследовании LIVE было показано, что влияние индапамида SR 1,5 мг на уровни САД и ДАД сопоставимо с эналаприлом в суточной дозе 20 мг [34].
Эффективность и безопасность индапамида SR в дозе 1,5 мг изучались в нескольких крупных клинических исследованиях (КИ), показавших весь терапевтический спектр действия препарата, в том числе влияние на органымишени АГ в подгруппе пожилых пациентов.
Органопротективные свойства антигипертензивных препаратов являются важными характеристиками, обусловливающими их отдаленную эффективность и влияние на прогноз больных с АГ. К наиболее клинически значимым органопротективным эффектам относятся кардиопротективный и нефропротективный.
Кардиопротективный эффект обеспечивается влиянием антигипертензивных препаратов на гипертрофию миокарда левого желудочка: предупреждением развития ГЛЖ или возможным регрессом ГЛЖ. В 90е гг. ХХ в. были опубликованы результаты нескольких метаанализов КИ, посвященных эффективности различных классов антигипертензивных препаратов по влиянию на ГЛЖ с целью выявления преимуществ. Диуретики оказались менее эффективными, чем ингибиторы АПФ и антагонисты кальция, но превосходили класс бетаадреноблокаторов. Вместе с тем в крупных сравнительных КИ отдельные диуретики имели превосходство перед другими классами препаратов по снижению ГЛЖ.
Органопротективные эффекты индапамида SR 1,5 мг изучены и доказаны в двух крупных контролируемых КИ. В упоминавшемся выше исследовании LIVE, несмотря на одинаковую гипотензивную эффективность, индапамид SR 1,5 мг приводил к достоверно более выраженному уменьшению ГЛЖ: масса миокарда уменьшилась на 14,2 и 3 г соответственно в группе индапамида SR 1,5 мг и эналаприла, а индекс массы миокарда — на 8,4 и 1,9 г/м2, или 5,9 и 1,4 % соответственно. При этом толщина межжелудочковой перегородки и задней стенки левого желудочка уменьшилась на 1,8 и 2 % в группе индапамида SR 1,5 мг и на 0,1 и 1,6 % в группе эналаприла соответственно. Эффективность снижения ГЛЖ при приеме индапамида SR 1,5 мг не зависела от типа геометрии левого желудочка (концентрической или эксцентрической) [34].
В исследовании W. Bocker, в котором изучалось влияние высоких и низких доз индапамида на миокард, было установлено, что только низкие дозы индапамида уменьшают массу миокарда левого желудочка, подавляют активность альдостерона в плазме и активность ангиотензинпревращающего фермента (АПФ) в плазме и миокарде. На фоне приема высоких доз индапамида отмечена активация РААС и отсутствие эффекта уменьшения ГЛЖ [35].
Таким образом, ретардная лекарственная форма индапамида, сделавшая возможным уменьшение дозы активного вещества с 2,5 до 1,5 мг, позволяет в полной мере реализовать его органопротективные свойства.
Нефропротективный эффект антигипертензивных препаратов заключается в предупреждении развития хронической почечной недостаточности. Маркерами нефропротективного эффекта являются микропротеинурия — наиболее ранний признак нарушения функции почек, клиренс креатинина и индекс альбуминурия/креатинин (ИАК > 3,4). ИАК в 3 раза выше у больных с АГ и в 9 раз — у больных с сахарным диабетом (СД) и, как и микропротеинурия, является фактором риска сердечнососудистых осложнений.
Нефропротективный эффект индапамида SR 1,5 мг изучался в исследовании NESTOR [36].
У 570 больных с АГ и сахарным диабетом 2го типа сравнивалось влияние индапамида SR 1,5 мг и эналаприла на микроальбуминурию (МАУ) в течение 1 года лечения. Различий в гипотензивной эффективности между препаратами не было: степень снижения САД/ДАД составила 23,8/13 мм рт.ст. в группе индапамида SR 1,5 мг и 21/12,1 мм рт.ст. в группе эналаприла. ИАК у больных, включенных в исследование, составил 6,16, а скорость экскреции альбуминов — 58 мкм/мин, при этом нарушения клиренса креатинина не отмечалось. Через 1 год лечения наблюдалось снижение ИАК до 4,03 (на 35 %) в группе индапамида SR 1,5 мг и до 3,74 (на 39 %) в группе эналаприла, а скорость экскреции альбуминов снизилась на 37 и 45 % соответственно. Таким образом, нефропротективный эффект индапамида SR 1,5 мг оказался сопоставимым с таковым эналаприла.
Важнейшим свойством диуретиков является усиление антигипертензивного действия в составе в комбинированной терапии, особенно с препаратами, ингибирующими активность РААС. В последнее время комбинированная терапия в лечении больных АГ применяется все более часто. Это объясняется тем, что комбинированная терапия имеет много преимуществ: усиление антигипертензивного эффекта за счет разнонаправленного действия препаратов на патогенетические механизмы развития АГ, что увеличивает число пациентов со стабильным снижением АД; уменьшение частоты возникновения нежелательных эффектов за счет как меньших доз комбинируемых средств, так и взаимной нейтрализации этих эффектов; обеспечение наиболее эффективной органопротекции и уменьшение риска и числа сердечнососудистых осложнений.
Многие антигипертензивные препараты могут комбинироваться между собой, однако некоторые комбинации имеют преимущества не только с теоретических позиций основного механизма действия, но и с практических (доказанная высокая антигипертензивная эффективность). Ингибиторы АПФ (ИАПФ) в комбинации с диуретиком являются оптимальным выбором, при котором усиливаются преимущества и нивелируются недостатки. Данная комбинация является особенно популярной в терапии АГ благодаря высокой гипотензивной эффективности, защите органовмишеней, хорошей безопасности и переносимости, а также привлекательным фармакоэкономическим показателям. Препараты потенцируют действие друг друга за счет взаимодополняющего влияния на основные звенья регуляции АД и блокирования контррегуляторных механизмов. Снижение объема циркулирующей жидкости вследствие салуретического действия диуретиков приводит к стимуляции РААС, чему противодействуют ИАПФ. У пациентов с низкой активностью ренина плазмы ИАПФ обычно недостаточно эффективны, и добавление диуретика, приводящего к повышению активности РААС, позволяет ИАПФ реализовать свое действие. Это расширяет круг больных, отвечающих на терапию, и целевые уровни АД достигаются более чем у 80 % пациентов. ИАПФ предотвращают гипокалиемию и уменьшают возможное негативное влияние диуретической терапии на углеводный, липидный и пуриновый обмен.
В связи с этим интерес представляет работа J. Hashimoto и соавт. [37], которые добавляли индапамид в дозе 1 мг 76 пациентам, получавшим ИАПФ, АРА и антагонисты кальция в качестве монотерапии, но достичь целевых цифр АД у которых при таком лечении не удалось. В течение 4недельной комбинированной терапии в данных трех группах оценивалась динамика уровня АД путем СМАД, измерения АД в домашних условиях и случайного измерения АД. Во всех группах было отмечено достоверное снижение САД и ДАД. Снижение САД в вечернее время и пульсового АД было достоверно более выражено в группе «АРА + индапамид» по сравнению с группой «антагонист кальция + индапамид». Таким образом, добавление к антигипертензивной терапии индапамида приводило к дополнительному гипотензивному эффекту, продолжительность которого составляла 24 часа.
Влияние режимов антигипертензивной терапии, включающей индапамид SR, на кардиоваскулярный прогноз изучено в достаточно большом количестве КИ, в большинстве из которых он сочетался с ИАПФ.
Индапамид входил в состав комбинированной антигипертензивной терапии в трех крупных КИ, оценивающих жесткие конечные точки: PROGRESS (Perindopril pROtection aGainst REcurrent Stroke Study), ADVANCE (Action in Diabetes and Vascular disease: preterAx and diamicroNMR Controlled Evaluation) и HYVET (HYpertension in the Very Elderly Trial) [38–40].
В исследование PROGRESS вошло 2916 больных с АГ и 3189 лиц с нормотензией, имеющих в анамнезе инсульт или транзиторную ишемическую атаку (ТИА). Больным был назначен ИАПФ с возможностью дополнительного назначения диуретика индапамида 2,5 мг/сут или плацебо [40]. В общей сложности 58 % пациентов, находившихся на активной терапии, получали комбинацию периндоприла с индапамидом. Первичной оцениваемой конечной точкой (исходом) в исследовании PROGRESS было развитие любого инсульта (фатального или нефатального, ишемического или геморрагического). Вторичные (дополнительные) конечные точки включали: фатальный или ведущий к инвалидности инсульт; тяжелые сосудистые исходы (нефатальный инсульт или инфаркт миокарда, любая сосудистая смерть, в том числе внезапная); общую и специфическую смертность; необходимость госпитализации. Гипотензивная терапия, включающая ИАПФ (все пациенты) и индапамид (58 % пациентов), снижала АД в среднем на 9/4 мм рт.ст. и более чем на четверть уменьшала риск повторного инсульта. При этом особенно значимо снижался риск фатального или инвалидизирующего и геморрагического инсульта. Риск последнего уменьшался в 2 раза. Важное значение имеет и тот факт, что проводимая гипотензивная терапия снижала частоту инсульта не только при АГ, но и у больных, квалифицированных как нормотензивные. Помимо уменьшения риска инсульта, гипотензивная терапия снижала общий риск тяжелых сосудистых исходов на 26 %, в том числе нефатального инфаркта миокарда — на 38 %. Интерес представляет тот факт, что особенно выраженное уменьшение риска повторного инсульта (любых его разновидностей) и основных сосудистых исходов наблюдается в подгруппе пациентов, получавших активную гипотензивную терапию, включавшую комбинацию ИАПФ с индапамидом, у которых систолическое/диастолическое АД снизилось в среднем на 12,3/5,0 мм рт.ст. При применении комбинированной терапии частота тяжелого (фатального, инвалидизирующего) инсульта уменьшалась почти в 2 раза, а геморрагического — в 4 раза. На 2/5 снижалась суммарная частота основных сосудистых исходов. Напротив, в подгруппе больных, получавших один ИАПФ (снижение АД на 4,9/2,8 мм рт.ст.), гипотензивная терапия не приводила к существенному уменьшению риска тяжелых сосудистых исходов, включая инсульт. Такое различие в величине терапевтического эффекта между подгруппами комбинированной терапии и ИАПФ, очевидно, в первую очередь связано со значительным (более чем в 2 раза) различием в величине достигаемого гипотензивного эффекта. Еще одной причиной может быть достаточно произвольное назначение участникам исследования PROGRESS индапамида, при котором не осуществлялась рандомизация. Учитывая большое число включенных в исследование пациентов и его многоцентровой характер, а также длительность наблюдения, полученные данные служат прямым подтверждением необходимости проведения активной гипотензивной терапии в рамках вторичной профилактики инсульта вне зависимости от уровня АД. Анализ результатов исследования свидетельствует, что у пациентов с цереброваскулярной болезнью гипотензивная терапия, включающая ИАПФ и индапамид, эффективно предупреждает и развитие тяжелых коронарных исходов. Подсчитано, что ее назначение в течение 5 лет будет предотвращать один фатальный или тяжелый нефатальный сосудистый исход на 11 больных. По эффективности в качестве средства вторичной профилактики такая комбинация по крайней мере не уступает антитромбоцитарным препаратам [41] и статинам [42].
Кроме того, она характеризуется хорошей переносимостью и высокой безопасностью, практически не отличаясь от плацебо по частоте отмены [43].
В исследовании HYVET все пациенты получали индапамид SR 1,5 мг, к которому в последующем при необходимости добавлялся ИАПФ. Общий объем выборки, рассчитанный для достижения поставленной цели, а именно снижения риска инсульта на 35 %, составил 21 000 больных, которые должны были наблюдаться в течение 5 лет. Инсульт был выбран как первичная цель исследования (и первичная конечная точка), поскольку именно снижение риска инсульта в этой подгруппе больных было наиболее ожидаемым согласно перечисленным выше данным.
После двух недель вводного плацебопериода производилась рандомизация на группы пациентов, принимающих плацебо или индапамид SR 1,5 мг, к которому в последующем мог быть добавлен ИАПФ. В исследование включались больные с АГ старше 80 лет без верхнего возрастного предела с уровнем CАД 160–199 мм рт.ст. и ДАД менее 110 мм рт.ст. Помимо инсультов (исключая ТИА) в исследовании оценивались и другие важные конечные точки — поражения сетчатки, сердечная недостаточность, внезапная смерть, инфаркт миокарда, переломы. Через два года лечения среднее снижение АД в группе плацебо составило 14,5/6,8 мм рт.ст., а в группе активной терапии — 29,5/12,9 мм рт.ст. Соответственно значимые различия между группами составили 15,0/6,1 мм рт.ст. 48 % больных в группе активной терапии достигли целевого уровня АД при соответствующем показателе в группе плацебо 19,9 %.
В группе активного лечения отмечено снижение общей смертности на 21 % (на 23 % — смертности от сердечнососудистых причин). Что касается инсультов, то и по этому критерию исследование также показало положительные результаты. Число смертельных и несмертельных инсультов снизилось на 30 %, что означает 11 предотвращенных инсультов на 1000 пролеченных больных в течение двух лет. Риск фатального инсульта снизился на 39 %. Это очень большая цифра, особенно учитывая высокую долю смертности от инсульта среди лиц старческого возраста.
Еще одним важным результатом исследования, заслуживающим особого внимания, стало снижение фатальных и нефатальных событий, связанных с сердечной недостаточностью, на 64 %. Преимущества диуретиков в предотвращении сердечной недостаточности обсуждаются уже давно, особенно после результатов исследования ALLHAT. В настоящее время исследование HYVET еще раз подтвердило, что лечение АГ, основанное на диуретике индапамиде, позволяет существенно уменьшить заболеваемость и летальность, опосредованную хронической сердечной недостаточностью, распространенность которой у пожилых чрезвычайно высока [44].
Практический интерес представляют не только эффективность, но и переносимость и метаболические эффекты тиазидных диуретиков при длительном приеме. Неблагоприятное влияние тиазидных диуретиков на солевой, липидный, углеводный и пуриновый обмен является наиболее частой причиной развития осложнений, в том числе и жизнеугрожающих. Известно, что гипокалиемия, вызываемая тиазидными диуретиками, является причиной желудочковых аритмий и внезапной смерти; увеличение атерогенных фракций липидов, преимущественно триглицеридов, является фактором риска развития ишемической болезни сердца; нарушение толерантности к углеводам увеличивает риск развития СД 2го типа, а сочетание этих неблагоприятных метаболических нарушений с АГ усугубляет прогноз больных. В силу таких причин метаболические эффекты тиазидных диуретиков находятся под пристальным вниманием специалистов. Индапамид занимает особое место среди диуретиков. В рекомендуемых дозах (1,5–2,5 мг/сут) он не только обеспечивает адекватный антигипертензивный эффект, но и является метаболически нейтральным. Доказано, что индапамид не вызывает гипокалиемии, изменений в углеводном [46] и липидном профиле [47]. Особенно убедительное свидетельство метаболической нейтральности индапамида получено в результате проведения метаанализа трех исследований, включивших в общей сложности 1195 пациентов. По итогам лечения ретардной формой индапамида в течение 9–12 мес. не было выявлено влияния на углеводный и липидный профиль, а также уровень мочевой кислоты [48].
Оценка влияния индапамида SR 1,5 мг на экскрецию калия была проведена в эквивалентном исследовании. Применение малых доз препарата в течение 3 мес. достоверно меньше снижало уровень калия и реже вызывало гипокалиемию у больных с АГ. Дальнейшее длительное (в течение 9 мес.) лечение индапамидом SR 1,5 мг также не сопровождалось клинически значимым снижением уровня калия (до 3,88 ммоль/л) [49].
В современных условиях ограниченности финансирования здравоохранения при выборе антигипертензивной терапии учитываются не только клинические, но и экономические аспекты. Изучение затратной эффективности применения гипотензивных препаратов позволяет выявлять их экономические преимущества. Так, при ретроспективном фармакоэкономическом анализе нескольких крупных КИ (LIVE, TOHMS, PRESERVE, NESTOR) индапамид SR 1,5 мг показал лучшие коэффициенты затратной эффективности при оценке как степени снижения АД, так и регресса ГЛЖ и МАУ в сравнении с наиболее часто назначаемыми гипотензивными препаратами из разных классов [50].
Таким образом, индапамид SR 1,5 мг является представителем нового поколения современных антигипертензивных препаратов из класса диуретиков, имеет благоприятный профиль эффективности и безопасности, доказанный в крупных клинических исследованиях. Индапамид SR 1,5 мг является диуретиком выбора для начальной терапии АГ и эффективным компонентом комбинированной антигипертензивной терапии. Он обеспечивает эффективную органопротекцию у больных с ГЛЖ и микроальбуминурией, имеет наилучшее соотношение эффективность/безопасность в сравнении с другими диуретиками, не оказывает влияния на липидный и углеводный обмен.
1. Chobanian A.V., Bakris G.L., Black H.R. et al. Seventh report of the Joint National Committee on Prevention, Detection, Evaluation, and Treatment of High Blood Pressure // Hypertension. 2003; 42: 120652.
2. Mancia G., De Backer G., Dominiczak A. et al. 2007 Guidelines for the Management of Arterial Hypertension: the Task Force for the Management of Arterial Hypertension of the European Society of Hypertension (ESH) and of the European Society of Cardiology (ESC) // J. Hypertens. 2007; 25: 110587.
3. Ritchie L.D., Campbell N.C., Murchie P. New NICE guidelines for hypertension // BMJ. 2011; 343: d5644.
4. Seely J.F., Dirks J.H. Site of action of diuretic drugs // Kidney Int. 1977; 11: 18.
5. NICE. Hypertension Clinical Management of Primary Hypertension in Adults. National Institute for Health and Clinical Excellence 2011; Clinical guideline 127.
6. Sassard J., Bataillard A., McIntyre H. An overview of the pharmacology and clinical efficacy of indapamide sustained release // Fundamental & Clinical Pharmacology. 2005; 19: 637645. doi: 10.1111/j.14728206.2005.00377.x7.
7. http: //www.drlz.kiev.ua/
8. Campbell D.B., Brackman F. Cardiovascular protective properties of indapamide // Am. J. Cardiol. 1990 May 2; 65: 1127H.
9. Schaeffer P., Vigne P., Frelin C. et al. Identification and pharmacological properties of binding sites for the atypical thiazidediuretic, indapamide // Eur. J. Pharmacol. 1990 Jul 17; 182 (3): 5038.
10. Acchiardo S.R., Skoutakis V.A. Clinical efficacy, safety, and pharmacokinetics of indapamide in renal impairment // Am. Heart J. 1983; 106: 23744.
11. Onesti G., Pitone J.M., Lowenthal D.L. et al. Studies on the natriuretic effect and site of action of indapamide // Curr. Med. Res. Opin. 1977; 5: 183.
12. Isaac R., Witchitz S., Kamoun A. et al. A longterm study of the influence of indapamide on the exchangeable potassium and sodium pools in hypertensive patients // Curr. Med. Res. Opin. 1977; 5: 6470.
13. LeBel M., Grose J.H., Belleau L.J. et al. Antihypertensive effect of indapamide with special emphasis on renal prostaglandin production // Curr. Med. Res. Opin. 1983; 8 (Suppl. 3): 816.
14. Campbell D.B. The possible mode of action of indapamide: a review // Curr. Med. Res. Opin. 1983; 8 (Suppl. 3): 924.
15. Grimm M., Weidmann P., Meier A. et al. Correction of altered noradrenaline reactivity in essential hypertension by indapamide // Br. Heart J. 1981; 46 : 4049.
16. Bataillard A., Schiavi P., Sassard J. Pharmacological propertiesof indapamide: rationale for use in hypertension // Clin. Pharmacokinet. 1999; 37 (Suppl. 1): 712.
17. Velasco M., UrbinaQuintana A., HernandezPieretti O. Cardiovascular hemodynamic effects of indapamide and atenolol in hypertensive patients // Curr. Ther. Res. 1982; 31: 100717.
18. Hughes A.D. How do thiazide and thiazidelike diuretics lower blood pressure? // J. Renin Angiotensin Aldosterone Syst. 2004; 5: 15560.
19. Schaeffer P., Vigne P., Frelin C. et al. Identification and pharmacological properties of binding sites for the atypical thiazide diuretic, indapamide // Eur. J. Pharmacol. 1990 Jul 17; 182 (3).
20. Pickkers P., Garcha R.S., Schachter M. et al. Inhibition of carbonic anhydrase accounts for the direct vascular effects of hydrochlorothiazide // Hypertension. 1999 Apr; 33 (4): 10438.
21. Ambrosioni E., Safar M., Degaute J.P., Malin P.L., MacMahon M., Pujol D.R., de Cordoue A., Guez D. Lowdose antihypertensive therapy with 1.5 mg sustainedrelease indapamide: results of randomised doubleblind controlled studies. European study group // J. Hypertens. 1998; 16: 16771684.
22. Madkour H., Gadallah M., Riveline B., Plante G.E., Massry S.G. Indapamide is superior to thiazide in the preservation of renal function in patients with renal insufficiency and systemic hypertension // Am. J. Cardiol. 1996; 77 (suppl.): 23B25B.
23. Pruss T., Wolf P.S. Preclinical studies of indapamide, a new 2methylindoline antihypertensive diuretic // Am. Heart J. 1983 Jul; 106 (1, Pt 2): 20811.
24. Sassard J., Bataillard A., McIntyre H. Fundam. An overview of the pharmacology and clinical efficacy of indapamide sustained release // Clin. Pharmacol. 2005 Dec; 19(6): 63745.
25. Schiavi P., Jochemsen R., Guez D. Pharmacokinetics of sustained and immediate release formulations of indapamide after single and repeated oral administration in healthy volunteers // Fundam. Clin. Pharmacol. 2000; 14: 139146.
26. Leonetti G. Evaluation of longterm efficacy of indapamide SR in elderly hypertensive patients // Curr. Med. Res. Opin. 2005; 21: 3746.
27. Mallion J.M., Asmar R., Ambrosioni E. et al. Evaluation du rapport vallee:pic de l’indapamide 1,5 mg comprime enrobea liberation prolongee par la mesure ambulatoire de la pression arterielle // Arch. Mal. Coeur Vaiss. 1996; 89: 2738.
28. Jaillon P., Asmar R. et al. Доклад на Европейском обществе по артериальной гипертензии. Милан, 2001.
29. Jaillon P., Asmar R. Blood pressure reduction over 32 hours in hypertensive patients after 2 months of combination therapy with indapamide SR // J. Hypertens. 2001; 19 (Suppl. 2): S234.
30. Mallion J.M., Asmar R., Boutelant S. et al. Twentyfour hour antihypertensive efficacy of indapamide, 1.5mg sustained release: results of two randomized doubleblind controlled studies // J. Cardiovasc. Pharmacol. 1998; 32: 6738.
31. Baguet J.P., Robitail S., Boyer L. et al. A metaanalytical aproach to the efficacy of antihypertensive drugs in reducing blood pressure // Am. J. Cardiovasc. Drugs. 2005; 5: 13140.
32. London G., Schmieder R., Calvo C. et al. Indapamide SR versus candesartan and amlodipine in hypertension: the XCELLENT Study // Am. J. Hypertens. 2006; 19: 11321.
33. Emeriau J.P., Knauf H., Pujadas J.O. et al. A comparison of indapamide SR 1.5 mg, with both amlodipine 5 mg and hydrochlorothiazide 25 mg in elderly hypertensive patients: a randomized doubleblind controlled study // J. Hypertens. 2001; 19: 343350.
34. Gosse P., Sheridan D.J., Zannad F. et al. Regression of Left ventricular hypertrophy in hypertensive patients treated with indapamide SR 1.5 Versus Enalapril 20: the LIVE study // J. Hypertens. 2000; 18: 14651475.
35. Bocker W., Hupf H., Grimm D. et al. Effects of indapamide in rats with pressure overload left ventricular hypertrophy // J. Cardiovasc. Pharmacol. 2000; 36 (4): 4816.
36. Marre M., Puig J.G., Kokot F. еt al. Equivalence of indapamide SR and enalapril on microalbuminuria reduction in hypertensive patients with type 2 diabetes: the NESTOR Study // J. Hypertens. 2004; 22 (8): 161322.
37. Hashimoto J., Hirayama H., Hanasawa T., Watabe D., Asayama K., Metoki H., Kikuya M., Ohkubo T., Totsune K., Imai Y. Efficacy of combination antihypertensive therapy with lowdose indapamide: assessment by blood pressure selfmonitoring at home // Clin. Exp. Hypertens. 2005 May; 27 (4): 33141.
38. Patel A. Effects of a fixed combination of perindopril and indapamide on macrovascular and microvascular outcomes in patients with type 2 diabetes mellitus (the ADVANCE trial): a randomised controlled trial // Lancet. 2007; 370: 82940.
39. Beckett N.S., Peters R., Fletcher A.E. et al. Treatment of hypertension in patients 80 years of age or older // N. Engl. J. Med. 2008; 358: 188798.
40. 44. Group P.C. Randomised trial of a peridoprilbased bloodpressurelowering regimen among 6105 individuals with previous stroke or transient ischaemic attack // Lancet. 2001; 358: 103341.
41. Antiplatelet Trialists’ Collaboration. Collaborative overview of randomised trials of antiplatelet therapy, I: prevention of death, myocardial infarction and stroke by prolonged antiplatelet therapy in various categories patients // BMJ. 1994; 308: 81106.
42. Sacks F.M., Pfeffer M.A., Moye L.A. et al. The effect of pravastatin on coronary events after myocardial infarction in patients with average cholesterol levels // N. Engl. J. Med. 1996; 335: 10019.
43. PROGRESS Collaborative Group. Randomised trial of perindoprilbased bloodpressurelowering regimen among 6105 individuals with previous stroke or transient ischaemic attack // Lancet. 2001; 358: 103341.
44. Feigin V., Ratnasabapathy Y., Anderson C. Does blood pressure lowering treatment prevents dementia or cognitive decline in patients with cardiovascular and cerebrovascular disease? // J. Neurol. Sci. 2005; 229230: 1515.
45. Ninomiya T., Zoungas S., Neal B. et al. // J. Hypertens. 2010; 28 (6): 11411149.
46. Leonetti G., Rappelli A., Salvetti A. et al. Longterm effects of indapamide: final results of a twoyear Italian multicenter study in systemic hypertension // Am. J. Cardiol. 1990, 65: 6771.
47. Harrower A.D.B., McFarlane G., Donnelly T. et al. Effect of indapamide on blood pressure and glucose tolerance in noninsulindependent diabetes // Hypertension. 1985; 7 (Suppl. II): 1613.
48. Weidmann P. Metabolic profile of indapamide sustainedrelease in patients with hypertention // Drug Safety. 2001; 24: 115565.
49. Donnelly R. Clinical implications of indapamide sustained release 1,5 mg in hypertension // Clin. Pharmacokinet. 1999; 37 (suppl. 1): 2132.
50. Петров В.И., Недогода С.В., Сабанов А.В. Ретроспективный клиникоэкономический анализ результатов клинических исследований гипотензивных препаратов // Клин. исследования. 2004; 3–4: 3643.