Журнал «Медицина неотложных состояний» 6 (45) 2012
Вернуться к номеру
Стратегия диагностики при профессиональной бронхиальной астме
Авторы: Косарев В.В., Бабанов С.А., ГБОУ ВПО «Самарский государственный медицинский университет» Минздравсоцразвития России
Рубрики: Семейная медицина/Терапия, Медицина неотложных состояний
Разделы: Справочник специалиста
Версия для печати
В статье отражены современные представления об этиологии, патогенезе, лабораторной, функциональной диагностике профессиональной бронхиальной астмы, вопросы дифференциальной диагностики, лечения, профилактики данного заболевания в условиях промышленного и сельскохозяйственного производства, у медицинских работников.
У статті подані сучасні уявлення в області етіології, патогенезу, лабораторної, функціональної діагностики професійної бронхіальної астми, питання диференціальної діагностики, лікування, профілактики даного захворювання в умовах промислового і сільськогосподарського виробництва, у медичних працівників.
The article reflects the modern understanding of the etiology, pathogenesis, laboratory, functional diagnostics of occupational asthma, problems of differential diagnosis, treatment, prevention of this disease under the conditions of industrial and agricultural production, in health care workers.
профессиональная бронхиальная астма, феномены элиминации и реэкспозиции, диагностика.
професійна бронхіальна астма, феномени елімінації і реекспозиції, діагностика.
occupational asthma, the phenomena of elimination and re-exposition, diagnostics.
Профессиональная бронхиальная астма (ПБА) — хроническое заболевание дыхательных путей, характеризующееся обратимой обструкцией и/или гиперреактивностью бронхов, проявляющееся эпизодами затрудненного дыхания, свистами в груди, кашлем и этиологически обусловленное веществами, воздействующими на респираторный тракт на рабочем месте [1, 3]. Согласно Глобальной стратегии лечения и профилактики бронхиальной астмы (GINA, 2011), астма определяется как хроническое воспалительное заболевание дыхательных путей, в котором принимают участие многие клетки: тучные, эозинофилы, Тлимфоциты, альвеолярные макрофаги [5].
ПБА известна с начала XVIII века, когда была описана астма аптекарей (ипекакуановая астма), а также астма меховщиков при воздействии урсола.
Этиологические факторы и классификация
В соответствии с патогенезом выделяют следующие типы ПБA [2, 3].
1. Иммунологическая ПБА, или ПБА, связанная с гиперчувствительностью. При этом необходим промежуток времени для развития сенсибилизации к этиологическому фактору и, следовательно, должен быть латентный период между воздействием этого фактора и появлением симптомов заболевания. В соответствии с этиологическими факторами выделяют следующие подтипы иммунологической ПА:
— иммунологическая ПБА, вызванная высокомолекулярными соединениями. При этом задействованы иммунологические механизмы, включая иммуноглобулин Е (IgE);
— иммунологическая ПБА, вызванная низкомолекулярными соединениями. В этих случаях нет четкого подтверждения участия IgE.
2. Неиммунологическая ПБА, или ПБА, индуцированная ирритантами. Этот тип ПБА является результатом раздражения или токсического поражения дыхательных путей. Развитие данного типа ПБА возможно как в виде синдрома реактивной дисфункции дыхательных путей, который вызывается однократными воздействиями высоких доз ирритантов и развивается в течение 24 часов от момента воздействия, так и ПБА, вызванной низкими дозами ирритантов, которая развивается после повторных контактов с низкими дозами этиологического фактора.
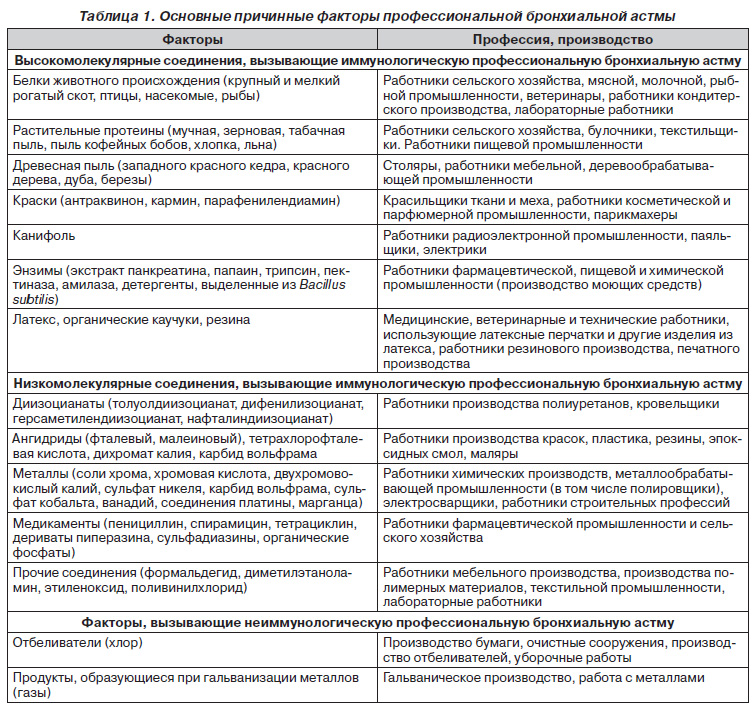
К высокомолекулярным соединениям, вызывающим иммунологическую ПБА, относятся белки животного происхождения, растительные протеины (мучная, зерновая, табачная пыль, пыль кофейных бобов). У работников хлебопекарной промышленности астму могут вызывать содержащиеся в муке белки злаковых, выявлены случаи сенсибилизации к продуктам переработки чая, чеснока, сои, а также к семенам клещевины, растительным клеям. Также к высокомолекулярным соединениям относятся древесная пыль, краски (кармин), канифоль, энзимы (экстракт панкреатина, папаин, трипсин, пектиназа, амилаза, детергенты, выделенные из Bacillus subtilis), латекс, органические каучуки, резина [2–4, 6].
К развитию иммунологической профессиональной бронхиальной астмы, обусловленной низкомолекулярными соединениями, приводят изоцианаты — соединения, которые широко используются для производства полиуретана, аэрозольных красок и защитных покрытий, клеев. Наиболее значимые в качестве этиологического фактора — толуолдиизоцианат, гексаметилендиизоцианат, дифенилметилдиизоцианат. Иммунологическая профессиональная бронхиальная астма возможна при воздействии низкомолекулярных ангидридов, воздействию которых подвержены работники, занятые на производстве этих консервантов, а также разнообразных полимеров и пластмасс, клеев, красок и материалов для антикоррозийных покрытий. Металлы (никель, платина, хром) и их соли способны вызывать ринит, конъюнктивит и бронхиальную астму, если поступают в зону дыхания в респирабельной форме [2, 3].
К факторам, приводящим к развитию неиммунологической ПБА, относятся хлор, продукты, образующиеся при гальванизации металлов, дым от сварки нержавеющей стали, от выплавки алюминия (табл. 1).
Существенная часть больных профессиональной бронхиальной астмой — медицинские работники (вызывают астму латекс, псилиум, дезинфекционные вещества (сульфатиазол, хлорамин, формальдегид, глутаральдегид; в анестезиологии — энфлюран), фармацевты (антибиотики, растительное лекарственное сырье), лаборанты (химические компоненты диагностических наборов, антибиотики, дезинфекционные вещества), работники вивариев (изза воздействия перхоти, слюны и белков мочи животных высокой молекулярной массы) и фармацевтических производств (антибиотики, метилдопа, циметидин, сальбутамол, пиперазин) [7–9].
Одна из причин бронхиальной астмы у медицинских работников — растительный продукт латекс, особенно его порошковая форма, используемая для припудривания резиновых перчаток. Первое описание перчаточной аллергии опбуликовано в 1927 году. За период с 1989 по 1993 год, по данным А. Heese, число случаев тяжелой аллергии на латекс возросло в 8,4 раза, при этом увеличилась доля тяжелых форм.
Патогенез. Сенсибилизирующие вещества с высоким молекулярным весом (5,000 дальтонов (Da) и более) часто действуют посредством IgEзависимого механизма. Сенсибилизирующие вещества с низким молекулярным весом (менее 5,000 Da), к которым относятся высокореактивные вещества типа эфиров изоциановой кислоты, могут действовать посредством IgEнезависимых механизмов либо вести себя как гаптены, соединяясь с протеинами организма. Если у рабочего выявляется сенсибилизация, то повторное воздействие сенсибилизирующего вещества (интенсивность которого часто бывает ниже того уровня, который вызвал сенсибилизацию) приводит к воспалительным процессам в дыхательных путях, часто сопровождаемым повышением непроходимости дыхательных путей и неспецифическими бронхиальными реакциями.
К высокомолекулярным соединениям, способным вызывать сенсибилизацию, относятся белки, которые являются полными антигенами [10, 11]. Кроме того, некоторые белки обладают ферментной активностью, облегчающей пенетрацию антигена [12]. В противоположность аллергенным белкам низкомолекулярные соединения, провоцирующие ПБА, обычно являются неполными антигенами (гаптенами) и для запуска иммунного ответа должны соединяться с другими молекулами. Эти вещества характеризуются высокой реактогенностью и могут связываться с определенными участками белковых молекул в дыхательных путях [13].
IgEзависимые механизмы. Большинство высокомолекулярных соединений, вызывающих ПБА, представляют собой белки или гликопротеины животного либо растительного происхождения, которые действуют через IgEопосредованные механизмы. Они являются полными антигенами и стимулируют выработку IgE. Тем не менее некоторые низкомолекулярные вещества (например, кислые ангидриды и соли платины) обладают свойствами гаптенов и соединяются с белкомносителем, образуя гаптенбелковый комплекс, который также стимулирует синтез IgE. При вдыхании этих веществ они связываются со специфическим IgE, находящимся на поверхности тучных клеток и базофилов, запуская последовательность клеточных реакций, что ведет к высвобождению и синтезу медиаторов и миграции и активации воспалительных клеток, формирующих воспалительную реакцию в дыхательных путях, характерную для астмы, к развитию процессов ремоделирования дыхательных путей, провоцирования бронхоконстрикции и гиперреактивности дыхательных путей [11].
IgEнезависимые механизмы. Большинство низкомолекулярных соединений, вызывающих ПБА, действуют через механизмы, которые, вероятно, являются иммунными, но не включают IgE [11]. Специфические IgG и IgG4антитела, повидимому, в большей степени связаны с уровнем воздействия, чем с заболеванием как таковым. Возможно, что в этих случаях задействована клеточная гиперчувствительность, или гиперчувствительность замедленного типа [14]. CD4лимфоциты играют поддерживающую роль в продукции IgE за счет Влимфоцитов и могут также индуцировать воспаление через секрецию ИЛ5. ИЛ5 является мощным стимулятором и активатором эозинофилов и основным цитокином, участвующим в миграции и активации эозинофилов во время отсроченной астматической реакции [15]. Повышение числа активированных Тлимфоцитов (которые экспрессируют рецептор для ИЛ2), активированных эозинофилов и тучных клеток обнаружено в бронхобиоптатах больных ПБА, вызванной низкомолекулярными соединениями [16, 17].
При ПБА ряд факторов роста, таких как фактор роста тромбоцитов (PDGF) и трансформирующий фактор роста b (TGFb), может стимулировать фиброгенез путем активации фибробластов и депозиции коллагеновых волокон в собственной пластинке слизистой оболочки бронхов.
Клиническая картина. ПБА часто проявляется внезапно. Для ПБА характерны зависимость возникновения болезни от интенсивности и длительности экспозиции причинного фактора, возникновение симптомов во время и после воздействия аллергенов и химических веществ на рабочем месте, отсутствие предшествующей респираторной симптоматики, сочетание астмы с другими клиническими проявлениями профессиональной аллергии (со стороны кожи, верхних дыхательных путей) [2–4, 8].
Так, по данным Е.В. Петровской [19], профессиональная бронхиальная астма, вызванная контактом с высокомолекулярными веществами, в 57,3 % случаев сочетается с аллергическим ринитом, в 16,6 % случаев — с аллергическим дерматитом. При контакте с низкомолекулярными соединениями аллергический ринит встречается в 31,3 %, аллергический дерматит — в 18,8 % случаев. При контакте с токсическими веществами в 28 % случаев выявлены поражения верхних дыхательных путей в виде ринофаринголарингита.
При обследовании у некоторых пациентов еще до развития приступа бронхиальной обструкции (во время выполнения работы) отмечаются затруднение дыхания, приступообразный кашель, нерезко выраженное удушье, наличие признаков аллергического ринита, чихание, чувство першения и щекотания в горле. В межприступном периоде — экспираторная одышка с характерным положением, занимаемым больным; при перкуссии выслушивается коробочный звук, подвижность нижних краев легких ограниченна, при аускультации легких определяются сухие хрипы на вдохе и на выдохе, меняющие свою интенсивность и локализацию. Во время приступа дыхательные шумы могут не прослушиваться. Кожные покровы бледные, сухие, вспомогательные мышцы напряжены; отмечаются тахикардия, глухость сердечных тонов, определение границ относительной сердечной тупости затруднено изза эмфиземы. Приступ удушья заканчивается отхождением вязкой, чаще прозрачной мокроты.
По наличию клинической симптоматики перед началом лечения ПБА разделяется:
— на интермиттирующую (cимптомы реже 1 раза в неделю, обострения кратковременные, ночные симптомы не чаще 2 раз в месяц, FEV1 или PEF ³ 80 % от должных значений, вариабельность PEF или FEV1 < 20 %);
— легкую персистирующую (симптомы чаще 1 раза в неделю, но реже 1 раза в день, обострения могут нарушать активность и сон, ночные симптомы чаще 2 раз в месяц, FEV1 или PEF ³ 80 % от должных значений, вариабельность PEF или FEV1 £ 30 %);
— персистирующую средней тяжести (симптомы ежедневно, обострения могут нарушать активность и сон, ночные симптомы > 1 раза в неделю, ежедневный прием ингаляционных b2агонистов короткого действия, FEV1 или PEF 60–80 % от должных значений, вариабельность PEF или FEV1 > 30 %);
— тяжелую персистирующую (симптомы ежедневно, частые обострения, ночные симптомы ПБА, ограничение физической активности, FEV1 или PEF £ 60 % от должных значений, вариабельность PEF или FEV1 > 30 %).
Для профессиональной бронхиальной астмы характерны: зависимость возникновения болезни от интенсивности и длительности экспозиции причинного фактора (возникновение симптомов во время и после воздействия аллергенов на рабочем месте); эффект элиминации (периодичность респираторных симптомов с улучшением состояния в выходные дни и в отпускной период); эффект реэкспозиции (ухудшение субъективного состояния и увеличение выраженности респираторных симптомов после возвращения на рабочее место — контакта с аллергенами); обратимый характер бронхиальной обструкции (кашля, одышки и свистящего затрудненного дыхания).
Следует отметить, что не всегда отмечается прямая зависимость между концентрацией профессиональных сенситизаторов в воздухе рабочих помещений и вероятностью развития ПБА, а также тяжестью ее обострений [9].
Близок по клинической картине к профессиональной бронхиальной астме биссиноз (от byssos — лен; впервые описан Greenbow, 1861) — своеобразное профессиональное заболевание, возникающее при длительном вдыхании волокнистой растительной пыли (пыли хлопка, льна и пеньки), клинически характеризующееся своеобразным быстро проходящим бронхоспастическим синдромом [3, 4].
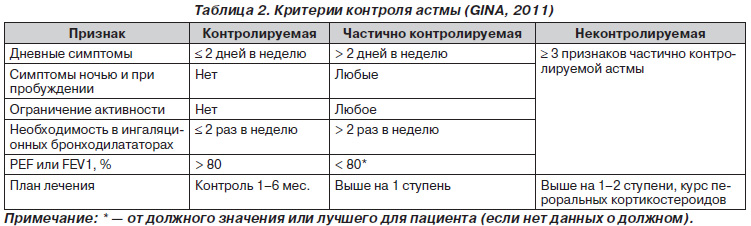
По уровню контроля профессиональная бронхиальная астма делится на контролируемую, частично контролируемую, неконтролируемую (табл. 2). По тяжести обострения — легкое, средней тяжести, тяжелое [5].
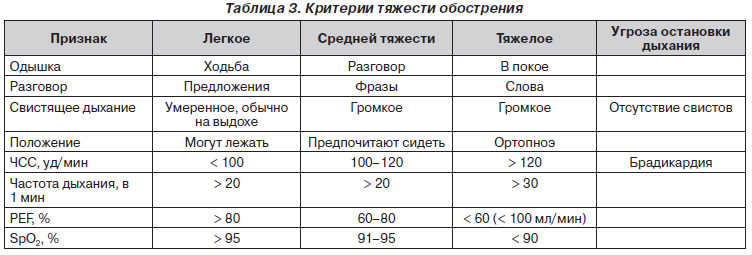
Тяжесть обострения определяется на основании выраженности клинических симптомов, наличия свистящего дыхания, положения больного, частоты дыхания, частоты сердечных сокращений, параметров пиковой скорости выдоха, SpO2 (табл. 3).
Как осложнение профессиональной бронхиальной астмы возможно развитие астматического статуса, эмфиземы легких, пневмосклероза, хронического легочного сердца, дыхательной недостаточности и бронхоэктазий.
Диагностика. Диагноз «профессиональная бронхиальная астма» может связать с профессией только специализированное профпатологическое учреждение (профцентр, НИИ профессиональных заболеваний, кафедра и клиника болезней медицинского вуза).
В диагностике учитываются субъективные данные (жалобы больного), данные объективного обследования, лабораторных, инструментальных и функциональных исследований — от общих до специальных (рентгенография органов грудной полости, исследование мокроты, функции внешнего дыхания). Также при необходимости проводятся компьютерная томография легких, магнитнорезонансная томография, консультации пульмонолога, фтизиатра, аллергологаиммунолога.
Степень выраженности бронхообструктивного синдрома оценивается по скоростным и объемным параметрам функции внешнего дыхания. Особенно ценная информация о состоянии бронхов может быть получена при изучении скоростных показателей пневмотахограммы и вязкостного дыхательного сопротивления — комплексного критерия бронхиальной обструкции. Применяется также динамическая пикфлоуметрия во время и после работы.
Одним из надежных способов специфической диагностики ПБА от химических гаптенов является провокационная ингаляционная проба с минимальными концентрациями водных растворов химических аллергенов, исключающими неспецифическое воздействие запаха и раздражающих свойств, присущих многим сенсибилизаторам [3, 4, 8]:
— через небулайзер, если вещество растворимо и иммунологические механизмы запускаются при участии IgE. Раствор антигена ингалируется в виде аэрозоля в возрастающих концентрациях. Через 10 мин после каждой ингаляции проводят форсированную спирометрию. Результат считается положительным, если FEV1 снижается не менее чем на 20 %. Если результат отрицательный, пациенту дают проингалировать максимальную концентрацию. Важно мониторировать FEV1 каждый час в течение 24 ч после ингаляции для выявления отсроченной реакции;
— в провокационной камере, если вещество нерастворимо. В этом случае пациент подвергается воздействию нераздражающих концентраций предполагаемого этиологического фактора. Если возможно, следует измерить концентрацию этого вещества. Длительность воздействия варьирует в зависимости от вещества и характеристик пациента. Результаты считаются положительными при снижении FEV1 более чем на 20 %. Если тест отрицательный, воздействие повторяют в течение более длительного времени или с более высокими концентрациями вещества.
При невозможности проведения провокационных проб изза тяжелого состояния больного рекомендуется использовать тест торможения естественной миграции лейкоцитов (полоскательный тест), принцип которого был разработан в 1980 году А.Д. Адо и основан на изменении миграции лейкоцитов в ротовую полость после полоскания слабым раствором аллергена. Особенно рекомендуется этот тест при подозрении на лекарственную аллергию [9, 18].
Для подтверждения профессионального генеза бронхиальной астмы необходимо определять в сыворотке уровень общего IgE и аллергенспецифические IgE (кожное тестирование, иммуноферментный анализ — ИФА, PACT). При ПБА чаще всего отмечается повышение концентрации общего IgE в 5–7 раз и отсутствие в сыворотке аллергенспецифических IgE на основные группы непрофессиональных аллергенов (бытовые, пыльцевые, грибковые) [19].
Также из иммунологических тестов определяются показатель специфического повреждения базофилов, специфические антитела в реакции связывания комплемента со специально подобранными дозами гаптенов.
Кожное или серологическое (например, РАСТ) тестирование может продемонстрировать иммунологическую сенсибилизацию в ответ на воздействие определенного вещества.
Лучше всего иммунологическая оценка подходит для веществ, для которых существуют стандартные тесты in vitro или покалывающие кожу реагенты, такие как соли платины и детергентные ферменты. Использование при тестировании растворов непромышленного производства часто вызывает тяжелые последствия, включая анафилактический шок, поэтому необходимо соблюдать осторожность.
Необходимо определять коэффициент сенсибилизации СD45+лимфоцитов к производственным аллергенам и уровни ИЛ4, ИЛ8 в сыворотке крови [19].
При ПБА в периферической крови обнаруживается абсолютный (или относительный) эозинофильный лейкоцитоз.
Также при обследовании больных ПБА могут быть использованы фибробронхоскопия (при возможности проведения исходя из клинического состояния), рентгенография легких, компьютерная томография легких и магнитнорезонансная томография (в целях дифференциальной диагностики для выявления интерстициальных процессов в легких как причины бронхообструктивного синдрома).
Для юридически обоснованной связи заболевания с профессией больной с подозрением на профессиональный генез бронхиальной астмы, кроме направления, должен представить в специализированное профпатологическое учреждение копию трудовой книжки (профессия, стаж), выписку из амбулаторной карты, карты периодических медицинских осмотров (подтверждают момент возникновения того или иного заболевания), санитарногигиеническую характеристику условий труда.
Санитарногигиеническая характеристика условий труда, составляемая Роспотребнадзором при получении из лечебнопрофилактического учреждения извещения о подозрении на профессиональное заболевание, описывает санитарногигиенические условия труда пациента; так называемый профессиональный маршрут (все места работы и ее продолжительность на том или ином участке); свойства, присущие данному виду аллергена (гидрофильность пыли или химического агента, раздражающее или сенсибилизирующее действие, наличие превышений предельно допустимой концентрации).
Лечение. При профессиональной бронхиальной астме даже на ранних стадиях болезни необходимо отстранение от работы, связанной с воздействием профессиональных аллергенов.
Патогенетическая терапия основывается на выявлении ведущего типа аллергической реакции и оказании блокирующего действия на развитие каждой стадии. Особое внимание при этом должно быть обращено на механизмы иммунологических реакций: торможение образования или высвобождения биологически активных веществ, угнетение образования антител, взаимодействие с рецепторами клеток, гипосенсибилизацию, стимуляцию образования блокирующих антител. Назначают такие десенсибилизирующие препараты, как супрастин, тавегил, цетиризин, фексофенадин и др.
В настоящее время в связи с появлением новых групп лекарственных препаратов, в том числе ингаляционных форм глюкокортикостероидов (ГКС), существенно изменились принципы рациональной фармакотерапии бронхиальной астмы, разработана и внедрена в клиническую практику ступенчатая терапия астмы (Глобальная стратегия лечения и профилактики бронхиальной астмы — GINA, 2011) с учетом этиологического фактора, данных иммунологического обследования, индивидуальных особенностей пациента [2, 5, 20, 21].
Первая ступень в первую очередь применяется у пациентов с эпизодическими, кратковременными приступами (кашель, свистящие хрипы £ 2 раз в неделю или более редкие ночные симптомы), что соответствует определению контролируемой бронхиальной астмы. В межприступный период — жалобы на ночные пробуждения и вышеупомянутые симптомы отсутствуют, а показатели внешнего дыхания в норме. При ухудшении состояния назначаются ингаляционные ГКС, что означает переход на вторую ступень. Если терапия, которую получает пациент, оказывается малоэффективной, то нужно перейти на ступень выше (например, если пациент находится на 2й ступени и лечение не дает должного эффекта, то нужно перейти на ступень 3 и так далее). И наоборот, если в течение 3 месяцев сохраняется хороший контроль над бронхиальной астмой, то можно перейти на ступень ниже (табл. 4).
Во время обострения астмы, развития астматического статуса пациенту показано применение препаратов, купирующих приступ бронхиальной обструкции. Это ингаляционные b2агонисты короткого действия — сальбутамол, фенотерол, подаваемые с помощью небулайзера; системные ГКС (парентеральное и пероральное введение), адреналин (эпинефрин). Иногда хороший эффект дает введение 2,4% раствора эуфиллина в вену в 10–20 мл изотонического раствора натрия хлорида.
Важное место в системе терапевтических мероприятий занимают специальное питание с исключением высокоаллергенных продуктов и проведение разгрузочнодиетических дней.
Профилактика. В системе профилактики особую роль играет проведение предварительных (при поступлении на работу) и периодических медицинских осмотров. Периодические медицинские осмотры проводятся 1 раз в год с обязательным участием профпатолога, терапевта, пульмонолога, аллергологаиммунолога, дерматовенеролога, оториноларинголога согласно Приказу МЗ и МП РФ № 302н от 12.04.2011 года «Об утверждении перечней вредных и (или) опасных производственных факторов и работ, при выполнении которых проводятся предварительные и периодические медицинские осмотры (обследования), и Порядка проведения предварительных и периодических медицинских осмотров (обследований) работников, занятых на тяжелых работах и на работах с вредными и (или) опасными условиями труда», с периодическим аллергологическим обследованием работающих.
Медицинскими противопоказаниями к работе в контакте с профессиональными аллергенами являются аллергические заболевания, тотальные дистрофические заболевания верхних дыхательных путей, хронические заболевания бронхолегочного аппарата, искривление носовой перегородки, врожденные аномалии органов дыхания, хронические очаги инфекции.
Большая роль в профилактике профессиональной бронхиальной астмы принадлежит дальнейшему совершенствованию технологических процессов, снижающих загрязнение воздуха рабочей зоны промышленными аллергенами, наличию, исправности и регулярному использованию коллективных средств защиты (прежде всего обеспечение эффективной работы проточновытяжной вентиляции), регулярному использованию индивидуальных средств защиты (масок, лепестков, респираторов).
Медикосоциальная экспертиза. Наличие хотя бы одного приступа удушья, доказательно связанного с воздействием профессиональных аллергенов, является показанием для немедленного прекращения контакта с потенциальными производственными аллергенами [1–4]. При подтверждении профессионального генеза бронхиальной астмы больной направляется на медикосоциальную экспертизу. Бюро МСЭ признает больного нетрудоспособным в своей профессии, определяет степень утраты общей трудоспособности (при наличии медицинских оснований — группа инвалидности), определяет нуждаемость в реабилитационных мероприятиях (реабилитационное, санаторнокурортное лечение, обеспечение лекарственными средствами для лечения ПБА и ее осложнений, обеспечение средствами доставки (небулайзер) и контроля эффективности лекарственных средств (пикфлоуметр), при необходимости кислородотерапии — обеспечение кислородным концентратором), нуждаемость в профессиональном переобучении. При этом все соответствующие расходы покрывает Фонд социального страхования.
При подготовке статьи использованы материалы, полученные при выполнении научных исследований по гранту Президента Российской Федерации для государственной поддержки молодых российских ученых — докторов наук (проект МД2790.2012.7 «Клиникопатогенетические особенности и прогнозирование течения обструктивных заболеваний легких профессиональной и непрофессиональной этиологии» / Бабанов С.А., 2012).
1. Артамонова В.Г., Мухин Н.А. Профессиональные болезни. — М.: Медицина, 2004. — 432 с.
2. Косарев В.В., Бабанов С.А. Профессиональные болезни. — М.: Гэотармедиа, 2010. — 368 с.
3. Профессиональная патология: Национальное руководство / Под ред. Н.Ф. Измерова. — М.: Гэотармедиа, 2011. — 784 с.
4. Саакадзе В.П., Степанов С.А. Профессиональная бронхиальная астма. — Саратов, 1989. — С. 1741.
5. GINA Report, Global Strategy for Asthma Management and Prevention. Published November 2011. http://www.ginasthma.org
6. Степанов С.А. К вопросу о природе так называемой «зерновой лихорадки» // Казанский медицинский журнал. — 1968. — № 8. — С. 813.
7. Макова Е.В. Клинические и иммунологические аспекты профессиональной аллергии к натуральному латексу: Автореф. дис... канд. мед. наук. — Самара, 2003. — 24 с.
8. Клинические рекомендации. Бронхиальная астма / Под ред. А.Г. Чучалина. — М.: Атмосфера, 2008. — 224 с.
9. Косарев В.В., Бабанов С.А. Профессиональные заболевания медицинских работников. — Самара: Офорт, 2009. — 232 с.
10. Tilles S.A., Jerath Tatum A. Differential diagnosis of occupational asthma // Immunol. Allergy Clin. N. Am. — 2003. — 23. — 167176.
11. Sastre J., Vandesplas O., Park H.S. Pathogenesis of occupational asthma // Eur. Respir. J. — 2003. — 22. — 364367.
12. Wan H., Winton H.L., Soeller C. et al. Der p1 facilitates transepithelial allergen delivery by disruption of tight functions // J. Clin. Invest. — 1999. — 104. — 123133.
13. Agius R.M., Nee J., Mc Govern B., Robertson A. Structure activity hypotheses in occupational asthma caused by low molecular weight substances // Ann. Occup. Hyg. — 1991. — 35. — 1291.
14. Maestrelli P., Saetta M., Mapp C., Fabri L.M. Mechanisms of occupational asthma // Clin. Exp. Allergy. — 1997. — 27 (Suppl. 1). — 4754.
15. Maestrelli P., del Prete G.F., de Carli M. et al. CD8 Tcell clones producing interleukin5 and interferongamma in bronchial mucosa of patients with asthma induced by toluene diisocyanate // Scand. J. Work Environ. Hlth. — 1994. — 20. — 376381.
16. Saetta M., Di Stefano A., Maestrelli P. et al. Airway mucos al inflammation in occupational asthma induced by toluene diisocyanate // Am. Rev. Respir. Dis. — 1992. — 145. — 160168.
17. Frew A.J., Chan H., Lam S., Chan Yeung M. Bronchial inflammation in asthma due to western red cedar // Am. J. Respir. Crit. Care Med. — 1995. — 151. — 340344.
18. Косарев В.В., Бабанов С.А. Справочник врачапульмонолога. — Ростов н/Д: Феникс, 2011. — 446 с.
19. Петровская Е.В. Клиникоиммунологические особенности профессиональной бронхиальной астмы: Автореф. дис... канд. мед. наук. — Самара, 2009. — 24 с.
20. Rabe K.F., Atienza T., Magyar P. et al. Effect of budesonide in combination with formoterol for reliever therapy in asthma exacerbations: a randomised controlled, double — blind study // Lancet. — 2006 Aug 26. — 368(9537). — 74453.
21. Vogelmeier C., D’Urzo A., Pauwels R., Merino J.M., Jaspal M., Boutet S., Naya I., Price D. Budesonide/formoterol maintenance and reliever therapy: an effective asthma treatment option? // Eur. Respir. J. — 2005. — 26(5). — 819828.