Журнал «Медицина неотложных состояний» 6 (45) 2012
Вернуться к номеру
Синдром удлиненного интервала QT и проблемы безопасности психофармакотерапии
Авторы: Лиманкина И.Н., Санкт-Петербургское общество кардиологов им Г.Ф. Ланга,
Федеральный центр сердца, крови и эндокринологии им. В.А. Алмазова,
ЗАО «Институт кардиологической техники», Россия
Рубрики: Семейная медицина/Терапия, Медицина неотложных состояний
Разделы: Руководства
Версия для печати
Рассматриваются особенности проявления приобретенного синдрома удлиненного интервала QT, развивающегося на фоне применения психофармакотерапевтических препаратов.
Розглядаються особливості прояву набутого синдрому подовженого інтервалу QT, що розвивається на фоні вживання психофармакотерапевтичних препаратів.
The peculiarities of manifestation of acquired long QT syndrome, developing secondary to administration of psychopharmacotherapeutic agents, are considered.
синдром удлиненного интервала QT, жизнеугрожающие желудочковые аритмии, психофармакотерапевтические препараты.
синдром подовженого інтервалу QT, життєзагрожуючі шлуночкові аритмії, психофармакотерапевтичні препарати.
long QT syndrome, life-threatening ventricular arrhythmias, psychopharmacotherapeutic agents.
Частота негативных кардиоваскулярных эффектов психотропной терапии, по данным масштабных клинических исследований, достигает 75 % [1]. Психически больные имеют достоверно более высокий риск внезапной смерти [1–4]. Так, в сравнительном исследовании (Herxheimer A., Healy D., 2002) показано 2–5кратное увеличение частоты внезапной смерти у пациентов с шизофренией в сравнении с двумя другими группами (больные глаукомой и псориазом) [5]. Американское агентство по контролю за продуктами питания и лекарствами (USFDA) сообщило об 1,6–1,7кратном повышении риска внезапной смерти при использовании всех современных антипсихотических препаратов (как классических, так и атипичных) [6]. Одним из предикторов внезапной смерти при терапии психотропными препаратами считают синдром удлиненного интервала QT (CУИ QT) [7].
Интервал QT отражает электрическую систолу желудочков (время в секундах от начала комплекса QRS до конца зубца Т). Его продолжительность зависит от пола (у женщин QT длиннее), возраста (с возрастом QT удлиняется) и частоты сердечных сокращений (ЧСС) (обратно пропорциональна). Для объективной оценки интервала QT в настоящее время пользуются корригированным (с поправкой на ЧСС) интервалом QT (QTc), определяемым по формулам Базетта (Bazett) и Фредерика (Friderici).
Формула Базетта:
QTс = QT / RК1/2 при RR < 1000 мс.
Формула Фредерика:
QTс = QT / RR1/3 при RR > 1000 мс.
В норме QTc составляет 340–450 мс для женщин и 340–430 мс для мужчин. Известно, что СУИ QT опасен развитием фатальных желудочковых аритмий и фибрилляции желудочков [7]. Риск внезапной смерти при врожденном СУИ QT в отсутствие адекватного лечения достигает 85 %, при этом 20 % детей умирают в течение года после первой потери сознания и более половины — в первое десятилетие жизни [8].
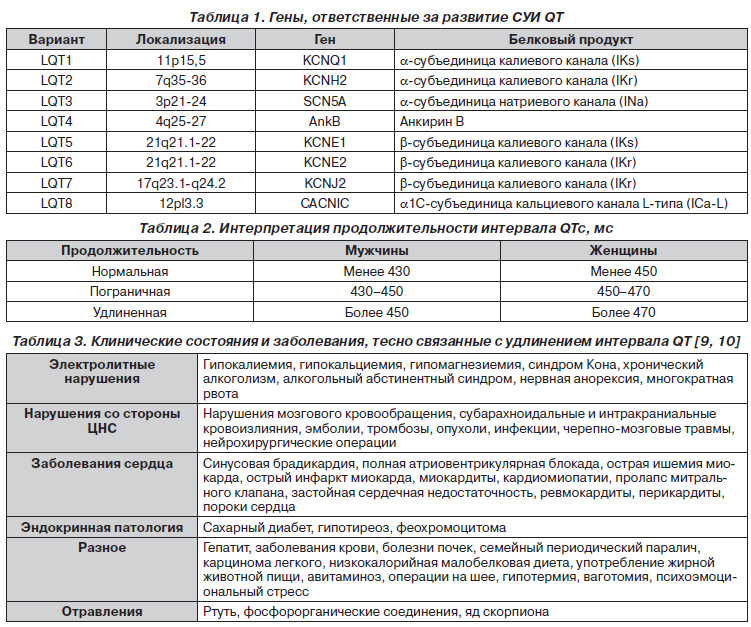
В этиопатогенезе заболевания ведущая роль отводится мутациям в генах, кодирующих калиевые и натриевые каналы сердца [7–10]. В настоящее время идентифицировано 8 генов, ответственных за развитие клинических проявлений СУИ QT (табл. 1). Кроме того, доказано, что у больных СУИ QT имеется врожденный симпатический дисбаланс (асимметрия иннервации сердца) с преобладанием левосторонней симпатической иннервации.
В клинической картине заболевания доминируют приступы потери сознания (синкопе), связь которых с эмоциональным (гнев, страх, резкие звуковые раздражители) и физическим стрессом (физическая нагрузка, плавание, бег) подчеркивает важную роль симпатической нервной системы в патогенезе СУИ QT.
Продолжительность потери сознания составляет в среднем 1–2 минуты и в половине случаев сопровождается эпилептиформными, тоникоклоническими судорогами с непроизвольным мочеиспусканием и дефекацией. Поскольку синкопальные состояния могут встречаться и при других заболеваниях, часто таких пациентов трактуют как больных с эпилепсией, истерией.
Особенности синкопальных состояний при СУИ QT:
— как правило, возникают на высоте психоэмоциональной или физической нагрузки;
— типичны предвестники (внезапная общая слабость, потемнение в глазах, сердцебиение, тяжесть за грудиной);
— быстрое, без амнезии и сонливости, восстановление сознания;
— отсутствие изменений личности, характерных для больных эпилепсией.
Синкопальные состояния при СУИ QT обусловлены развитием полиморфной желудочковой тахикардии типа «пируэт» (torsades de pointes) (TdP). TdP называют еще «сердечным балетом», «хаотической тахикардией», «желудочковой анархией», «сердечным штормом», что, по сути, является синонимом остановки кровообращения. TdP — неустойчивая тахикардия (общее количество QRSкомплексов при каждом приступе колеблется от 6 до 25–100), склонная к рецидивам (уже через несколько секунд или минут приступ может повториться) и переходу в фибрилляцию желудочков (относится к жизнеугрожающим аритмиям). К другим электрофизиологическим механизмам внезапной кардиогенной смерти пациентов с СУИ QT относят электромеханическую диссоциацию и асистолию.
ЭКГпризнаки СУИ QT:
— удлинение интервала QT, превышающее норму для данной ЧСС более чем на 50 мс, независимо от причин, лежащих в его основе, общепризнанно считается неблагоприятным критерием электрической нестабильности миокарда. Комитет по патентованным лекарственным средствам Европейского агентства по оценке медицинских продуктов (European Agency for the Evaluation of Medical Products) предлагает следующую интерпретацию продолжительности интервала QTc (табл. 2). Увеличение QTc на 30–60 мс у пациента, принимающего новые лекарственные средства, должно вызывать настороженность в отношении возможной связи с препаратом. Абсолютную продолжительность QTc свыше 500 мс и относительное увеличение более чем на 60 мс следует рассматривать в качестве угрозы TdP;
— альтернация зубца Т — изменение формы, полярности, амплитуды зубца Т свидетельствует об электрической нестабильности миокарда;
— дисперсия интервала QT — разница между максимальным и минимальным значением интервала QT в 12 стандартных отведениях ЭКГ. QTd = QTmax – QTmin, в норме QTd = 20–50 мс. Увеличение дисперсии интервала QT свидетельствует о готовности миокарда к аритмогенезу.
Отмечаемый в последние 10–15 лет растущий интерес к исследованию приобретенного СУИ QT расширил наши представления о внешних факторах, таких как различные заболевания, метаболические нарушения, электролитный дисбаланс, лекарственная агрессия, вызывающих нарушения функционирования ионных каналов сердца, аналогичные врожденным мутациям при идиопатическом СУИ QТ.
Клинические состояния и заболевания, тесно ассоциированные с удлинением интервала QT, представлены в табл. 3.
Согласно данным, приведенным в докладе Центров по контролю и предупреждению заболеваний (Centers for Disease Control and Prevention) от 2.03.2001 г., в США растет частота внезапной сердечной смерти среди людей молодого возраста. Высказывается мнение, что среди возможных причин этого роста важную роль играют лекарственные средства. Объем потребления лекарств в экономически развитых странах постоянно увеличивается. Фармацевтика давно стала таким же бизнесом, как и любой другой. Только на разработку нового продукта у фармацевтических гигантов в среднем уходит около 800 млн долларов, что на два порядка выше, чем в большинстве других областей.
Наметилась отчетливая негативная тенденция в проведении фармкомпаниями все большего числа препаратов как статусных, или престижных (lifestyle drugs). Такие лекарства принимают не потому, что они нужны для лечения, а потому что они соответствуют определенному образу жизни. Это виагра и ее конкуренты сиалис и левитра; ксеникал (средство для снижения веса), антидепрессанты, пробиотики, антигрибковые и многие другие препараты.
Другую тревожную тенденцию можно обозначить как Disease Mongering («торговля болезнями»). Крупнейшие фармкомпании, чтобы расширить рынок сбыта, убеждают вполне здоровых людей в том, что они больны и нуждаются в медикаментозном лечении. Количество мнимых недугов, искусственно раздуваемых до масштабов серьезных заболеваний, постоянно увеличивается. Синдром хронической усталости (синдром менеджера), климакс как заболевание, женская половая дисфункция, иммунодефицитные состояния, йододефицит, синдром беспокойных ног, дисбактериоз, «новые» инфекционные заболевания становятся брендами для наращивания продаж антидепрессантов, иммуномодуляторов, пробиотиков, гормонов.
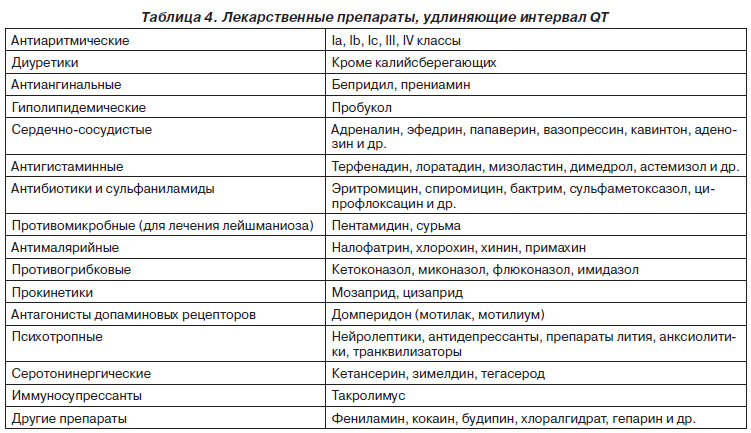
Самостоятельный и бесконтрольный прием лекарственных средств, полифармация, неблагоприятные комбинации препаратов и необходимость длительного приема лекарственных средств создают предпосылки для развития СУИ QT. Таким образом, индуцированное лекарствами удлинение интервала QT как предиктор внезапной смерти приобретает масштабы серьезной медицинской проблемы. Разнообразные лекарственные препараты самых широких фармакологических групп способны приводить к удлинению интервала QT [9–10] (табл. 4). Список препаратов, удлиняющих интервал QT, постоянно пополняется. Все лекарственные средства центрального действия удлиняют интервал QT, зачастую клинически значимо, и именно поэтому проблема лекарственноиндуцированного СУИ QT в психиатрии стоит наиболее остро [11].
В серии многочисленных публикаций доказана связь между назначением антипсихотиков (как старых, классических, так и новых, атипичных) и СУИ QT, TdP и внезапной смертью [1–6, 12–17]. В Европе и США предоставление лицензии для нескольких нейролептиков не допускали или откладывали, другие были сняты с производства. После сообщений о 13 случаях внезапной необъяснимой смерти, связанной с приемом пимозида, в 1990 году было принято решение об ограничении его суточной дозы до 20 мг в сутки и лечении под контролем ЭКГ. В 1998 году после публикации данных о связи приема сертиндола с 13 случаями серьезной, но нефатальной аритмии (36 смертельных случаев были предположительными) фирмапроизводитель добровольно временно прекратила продажу препарата на 3 года. В том же году по поводу удлинения интервала QT тиоридазин, мезоридазин и дроперидол получили предостережение в форме «черной вставки», а зипрасидон — полужирным шрифтом. К концу 2000 года после смерти 21 человека вследствие приема назначенного врачами тиоридазина этот препарат стал препаратом второй очереди в лечении шизофрении. Вскоре после этого дроперидол был отозван с рынка его производителями. В Соединенном Королевстве выпуск атипичного антипсихотического препарата зипрасидона откладывают, поскольку более чем у 10 % пациентов, принимающих этот препарат, возникло легкое удлинение интервала QT.
Из антидепрессантов кардиотоксический эффект в наибольшей степени проявляют циклические антидепрессанты [14, 18–22]. По данным исследования 153 случаев отравления трициклическими антидепрессантами (ТЦА) (из которых 75 % приходилось на амитриптилин), клинически значимое удлинение интервала QTс отмечалось в 42 % случаев [19]. Из 730 детей и подростков, получавших антидепрессанты в терапевтических дозах, удлинение интервала QTс > 440 мс сопровождало лечение дезипрамином в 30 %, нортриптилином — в 17 %, имипрамином — в 16 %, амитриптилином — в 11 % и кломипрамином — в 11 % [20]. Описаны случаи внезапной смерти, тесно ассоциированной с СУИ QT, пациентов, длительно получавших трициклические антидепрессанты [21–23], в т.ч. с посмертной идентификацией slowmetabolizer фенотипа CYP2D6 вследствие кумуляции препарата [24]. Новые циклические и атипичные антидепрессанты более безопасны в отношении кардиоваскулярных осложнений, демонстрируя удлинение интервала QT и TdP лишь при превышении терапевтических доз.
Большинство психотропных препаратов, широко используемых в клинической практике, относятся к классу В (по Haverkamp W., 2001), т.е. на фоне их применения имеется относительно высокий риск возникновения TdP [25]. По данным экспериментов in vitro, in vivo, секционных и клинических исследований, антиконвульсанты, антипсихотики, анксиолитики, нормотимики и антидепрессанты способны блокировать быстрые калиевые HERGканалы, натриевые каналы (вследствие дефекта гена SCN5A) и кальциевые каналы Lтипа, вызывая, таким образом, функциональную недостаточность всех каналов сердца [26–33].
Кроме того, в формировании СУИ QT принимают участие хорошо известные кардиоваскулярные побочные эффекты психотропных препаратов [1, 3, 34]. Многие транквилизаторы, нейролептики, препараты лития, ТЦА снижают сократимость миокарда, что в редких случаях может привести к развитию застойной сердечной недостаточности. Циклические антидепрессанты способны накапливаться в сердечной мышце, где их концентрация в 100 раз превышает уровень в плазме крови. Многие психотропные препараты являются ингибиторами кальмодулина, что приводит к нарушению регуляции синтеза протеинов миокарда, к структуральному повреждению миокарда и развитию токсической кардиомиопатии и миокардита [35, 36].
Следует признать, что клинически значимое удлинение интервала QT является грозным, но редким осложнением психотропной терапии (8–10 % при лечении антипсихотиками [37]). Повидимому, речь идет о латентной, скрытой форме врожденного СУИ QT с клинической манифестацией вследствие лекарственной агрессии. Интересна гипотеза о дозозависимом характере воздействия препарата на сердечнососудистую систему, согласно которой для каждого антипсихотика существует своя пороговая доза, превышение которой и приводит к удлинению интервала QT. Считается, что для тиоридазина это 10 мг/сутки, для пимозида — 20 мг/сутки, для галоперидола — 30 мг/сутки, для дроперидола — 50 мг/сутки, для хлорпромазина — 2000 мг/сутки. Высказывается предположение, что удлинение интервала QT также может быть связано с электролитными нарушениями (гипокалиемией). Имеет значение и способ введения препарата.
Положение усугубляется сложным коморбидным церебральным фоном психически больных, который сам по себе способен вызывать СУИ QT. Необходимо также помнить, что психически больные получают препараты годами и десятилетиями, а метаболизм подавляющего большинства психотропных средств осуществляется в печени, с участием системы цитохрома Р450 [38–42]. Лекарства, метаболизируемые определенными изомерами цитохрома Р450, представлены в табл. 5.
Кроме того, выделяют 4 статуса генетически детерминированного метаболического фенотипа:
— экстенсивные (быстрые) метаболизанты (Extensive Metabolizers или fast), имеющие две активные формы энзимов микросомального окисления; в терапевтическом плане — это пациенты стандартных терапевтических доз;
— промежуточные метаболизанты (Intermediate Metabolizers), имеющие одну активную форму энзима и вследствие этого несколько сниженный лекарственный метаболизм;
— низкие или медленные метаболизанты (Poor Metabolizers или slow), не имеющие активных форм энзимов, вследствие чего концентрация препарата в плазме крови может возрастать в 5–10 раз;
— сверхинтенсивные метаболизанты (Ultraextensive Metabolizers), имеющие три и более активные формы энзимов и ускоренный лекарственный метаболизм.
Многие психотропные препараты (особенно нейролептики, производные фенотиазина) оказывают гепатотоксическое действие (вплоть до развития холестатической желтухи), обусловленное комплексным (физикохимическим, аутоиммунным и прямым токсическим) воздействием на печень, что в ряде случаев может трансформироваться в хроническое поражение печени с нарушением ферментного метаболизма по типу poor metabolizing («бедного» метаболизма). Кроме того, многие нейротропные препараты (седативные, антиконвульсанты, нейролептики и антидепрессанты) являются ингибиторами микросомального окисления системы цитохрома Р450, главным образом, энзимов 2С9, 2С19, 2D6, 1A2, 3A4, 5, 7. Таким образом, создаются предпосылки для кардиоваскулярных осложнений при неменяющейся дозе психотропного препарата и неблагоприятных лекарственных комбинациях.
Выделяют группу высокого индивидуального риска кардиоваскулярных осложнений при лечении психотропными препаратами. Это пациенты пожилого и детского возраста, с сопутствующей сердечнососудистой патологией (заболевания сердца, аритмии, брадикардия менее 50 ударов в минуту), с генетическими повреждениями ионных каналов сердца (врожденный, в том числе латентный, и приобретенный СУИ QT), с электролитным дисбалансом (гипокалиемия, гипокальциемия, гипомагнеземия, гипоцинкемия), с низким уровнем метаболизма (poor, slow metabolizers), с дисфункцией автономной нервной системы, с выраженными нарушениями функции печени и почек, получающие одновременно препараты, удлиняющие интервал QT и/или ингибирующие цитохром P450. В исследовании Reilly (2000) факторами риска удлинения интервала QT признаны: возраст старше 65 лет (относительный риск (ОР) = 3,0), использование диуретиков (ОР = 3,0), галоперидола (ОР = 3,6), ТЦА (ОР = 4,4), тиоридазина (ОР = 5,4), дроперидола (ОР = 6,7), высоких (ОР = 5,3) и очень высоких доз нейролептиков (ОР = 8,2).
Перед современным врачом стоят сложные задачи правильного выбора препарата из огромного количества лекарств (в России это 17 000 наименований!) по критериям эффективности и безопасности. Грамотное мониторирование интервала QT позволит избежать серьезных кардиоваскулярных осложнений психотропной терапии [43].
1. Buckley N., Sanders P. Cardiovascular adverse effects of antipsychotic drugs // Drug. Safety. — 2000. — 23(3). — 215228.
2. Brown S. Excess mortality of schizophrenia, a metaanalysis // Br. J. Psychiatry. — 1997. — 171. — 502508.
3. O’Brien P., Oyebode F. Psychotropic medication and the heart // Advances in Psychiatric Treatment. — 2003. — 9. — 414423.
4. Abdelmawla N., Mitchel A.J. Sudden cardiac death and antipsychotics drugs // Advances in Psychiatric Treatment. — 2006. — 12. — 3544; 100109.
5. Herxheimer A., Healy D. Arrythmias and sudden death in patients taking antipsychotic drugs // BMI. — 2002. — 325. — 12531254.
6. FDA issues public health advisory for antipsychotic drugs used for treatment of behavioral disorders in elderly patients (FDA talk Paper) Rochvill (MD): US Food and Drug Adminstration, 2006.
7. Schwartz P.J. The Long QT Syndrome // Futura Publishing Company, Inc., Armonk, NY, 1997. — Vol. 7.
8. Schwartz P.J., Spazzolini C., Crotti L. et al. The Jervell and LangeNielsen Sundrome: natural history, molecular basis and clinical outcome // Circulation. — 2006. — 113. — 783790.
9. Бутаев Т.Д., Трешкур Т.В., Овечкина М.А. и др. Врожденный и приобретенный синдром удлиненного интервала QT (учебнометодическое пособие) // Инкарт. СанктПетербург, 2002.
10. Camm A.J. DrugInduced Long QT Syndrome // Futura Publishing Company, Inc., Armonk, NY, 2002. — Vol. 16.
11. Van de Kraats G.B., Slob J., Tenback D.E. Reduction of prolonged QTcinterval related risks with neuropharmacological drugs. Recommendations for clinical practice // Tijdschr Psychiatr. — 2007. — 49(1). — 4347.
12. Glassman A.H., Bigger J.R. Antipsychotic drugs: prolonged QTc interval, torsade de pointes and sudden death // American Journal of Psychiatry. — 2001. — 158. — 17741782.
13. Vieweg W.V.R. Neugeneration antipsychotic drugs and QTcinterval prolongation // Primary Care Companion J. Clin. Psychiatry. — 2003. — 5. — 205215.
14. Mehtonen O.P., Aranki K., Malkonen L. et al. A survey of sudden death associated with the use of antipsychotics or antidepressant drugs: 49 cases in Finland // Acta Psychiatrica Scandinavica. — 1991. — 84. — 5864.
15. Ray W.A., Meredith S., Thapa P.B. et al. Antipsychotics and the risk of sudden cardiac death // Archives of General Psychiatry. — 2001. — 58. — 11611167.
16. Straus S.M.J.M., Bleumink G.S., Dieleman J.P. et al. Antipsychotics and the risk of sudden cardiac death // Archives of Internal Medicine. — 2004. — 164. — 12931297.
17. Trenton A.J., Currier G.W., Zwemer F.L. Fatalities associated with therapeutic use and overdose of atypical antipsychotics // CNS Drugs. — 2003. — 17. — 307324.
18. Victor W., Wood M. Tricyclic Antidepressants, QT Interval and Torsade de Pointes // Psychosomatics. — 2004. — 45. — 371377.
19. Thorstrand C. Clinical features in poisoning by tricyclic antidepressants with special reference to the ECG // Acta Med. Scan. — 1976. — 199. — 337344.
20. Wilens T.E., Biederman J., Baldessarini R.J. et al. Cardiovascular effects of therapeutic doses of tricyclic antidepressants in children and adolescents // J. Am. Acad. Child. Adolesc. Psychiatry. — 1995. — 35. — 14741480.
21. Riddle M.A., Geller B., Ryan N. Another sudden death in a child treated with desipramine // J. Am. Acad. Child. Adolesc. Psychiatry. — 1993. — 32. — 792797.
22. Varley C.K., McClellan J. Case study: two additional sudden deaths with tricyclic antidepressants // J. Am. Acad. Child. Adolesc. Psychiatry. — 1997. — 36. — 390394.
23. Oesterheld J. TCA cardiotoxicity: the latest // J. Am. Acad. Child. Adolesc. Psychiatry. — 1996. — 34. — 14601468.
24. Swanson J.R., Jones G.R., Krasselt W. et al. Death of two subjects due to imipramine and desipramine metabolite accumulation during chronic therapy: a review of the literature and possible mechanisms // J. Forensic. Sci. — 1997. — 42. — 335339.
25. Haverkamp W., Breithardt G., Camm A.J. et al. The potential for QT prolongation and proarrhythmia by nonantiarrhythmic drugs: clinical and regulatory implications. Report on a policy conference of the European Society of Cardiology // Eur. Heart J. — 2000. — 21(5). — 12161231.
26. Ogata N., Narahashi T. Block of sodium channels by psychotropic drugs in single quineapig cardiac myocytes // Br. J. Pharmacol. — 1989. — 97(3). — 905913.
27. Crumb W.J., Beasley C., Thornton A. et al. Cardiac ion channel blocking profile of olanzapine and other antipsychotics. Presented at the 38th American College of Neuropsychopharmacology Annual Meeting; Acapulco, Mexico; December 12–16,1999.
28. Jo S.H., Youm J.B., Lee C.O. et al. Blocade of the HERG human cardiac K+channel by the antidepressant drug amitriptyline // Br. J. Pharmacol. — 2000. — 129. — 14741480.
29. Kupriyanov V.V., Xiang B., Yang L., Deslauriers R. Lithium ion as a probe of Na+channel activity in isolated rat hearts: a multinuclear NMR study // NMR Biomed. — 1997. — 10. — 271276.
30. Kiesecker C., Alter M., Kathofer S. et al. Atypical tetracyclic antidepressant maprotiline is an antagonist at cardiac HERG potassium channels // Naunyn Schmiedebergs Arch. Pharmacol. — 2006. — 373(3). — 212220.
31. Tarantino P., Appleton N., Lansdell K. Effect of trazodone on HERGchannel current and QTinterval // Eur. J. Pharmacol. — 2005. — 510(1–2). — 7585.
32. Jow F., Tseng E., Maddox T. et al. Rb+ efflux through functional activation of cardiac KCNQ1/mink channels by the benzodiazepine RL3 (L364,373) // Assay. Drug. Dev. Technol. — 2006. — 4(4). — 443450.
33. Rajamani S., Eckhardt L.L., Valdivia C.R. et al. Druginduced long QT syndrome: HERG K+ channel block and disruption of protein trafficking by fluoxetine and norfluoxetine // Br. J. Pharmacol. — 2006. — 149(5). — 481489.
34. Glassman A.H. Schizophrenia, antipsychotic drugs, and cardiovascular disease // J. Clin. Psychiatry. — 2005. — 66 (Suppl. 6). — 510.
35. Shamgar L., Ma L., Schmitt N. et al. Calmodulin is essential for cardiac IKS channel gating and assembly: impaired function in longQT mutations // Circ. Res. — 2006. — 98(8). — 10551063.
36. Hull B.E., Lockwood T.D. Toxic cardiomyopaty: the effect of antipsychoticantidepressant drugs and calcium on myocardial protein degradation and structural integrity // Toxicol. Appl. Pharmacol. — 1986. — 86(2). — 308324.
37. Reilly J.G., Ayis S.A., Ferrier I.N. et al. QTcinterval abnormalties and psychotropic drugs therapy in psychiatric patients // Lancet. — 2000. — 355(9209). — 10481052.
38. Andreassen O.A., Steen V.M. Pharmacogenetics and tailored drug treatment in schizophrenia // Tidsskr. Nor. Laegeforen. — 2006. — 126(18). — 24002402.
39. Kutscher E.C., Carnahan R. Common CYP450 interactions with psychiatric medicines: A brief review for the primary care physician // S. D. Med. — 2006. — 59(1). — 59.
40. Kropp S., Lichtinghagen R., Winterstein K. et al. Cytochrome P450 2D6 and 2C19 polymorphisms and length of hospitalization in psychiatry // Clin. Lab. — 2006. — 52(5–6). — 237240.
41. Daniel W.A. The influence of longterm treatment with psychotropic drugs on cytochrome P450: the involvement of different mechanisms // Expert. Opin. Drug. Metab. Toxicol. — 2005. — 1(2).— 203217.
42. KootstraRos J.E., Van Weelden M.J., Hinrichs J.M. et al. Therapeutic drug monitoring of antidepressants and cytochrome P450 genotyping in general practice // J. Clin. Pharmacol. — 2006. — 46(11). — 13201327.
43. Андреев Б.В., Лиманкина И.Н. Проблема интервала QT в психиатрической практике // Медицина ХХ век. — 2006. — 4. — 4144.