Газета «Новости медицины и фармации» 3 (444) 2013
Вернуться к номеру
Цефалоспорины при лечении респираторных заболеваний в амбулаторно-поликлинической практике педиатра
Авторы: Хайтович Н.В., Национальный медицинский университет имени А.А. Богомольца, г. Киев
Рубрики: Педиатрия/Неонатология
Разделы: Справочник специалиста
Версия для печати
В настоящее время большинство назначений антибиотиков у детей делается в амбулаторной практике. В 75 % случаев антибиотики назначаются при лечении детей с респираторной патологией или заболеваниями лорорганов.
В подавляющем большинстве случаев острые респираторные заболевания (ОРЗ) у детей вызываются вирусами (грипп, парагрипп, PCвирус и др.), неосложненные, при обычном течении они не требуют применения антибиотиков. Бактериальные осложнения острой респираторной вирусной инфекции (суперинфекция) развиваются, как правило, после 5–7го дня заболевания и изменяют классическое его течение [1].
Необходимо учитывать, что слизистогнойный ринит и отрицательный результат исследования на вирусы не являются подтверждением бактериальной этиологии ОРЗ и показанием к проведению антибактериальной терапии. Применение антибиотиков при рините может быть оправданно только при высокой вероятности наличия острого синусита, о чем говорит сохранение ринита в течение 10–14 дней в сочетании с лихорадкой, отеком лица или болью в проекции придаточных пазух.
Фарингит в большинстве случаев вызывается вирусами, сочетается с поражением слизистой других отделов дыхательных путей (ринит/ларингит/трахеит/бронхит) и не требует назначения антибактериальной терапии, кроме случаев с доказанной или высоко вероятной ролью бетагемолитического стрептококка в качестве возбудителя инфекции.
Для подтверждения или исключения бактериальной инфекции обычно используются так называемые маркеры бактериального воспаления — уровни лейкоцитоза > 15 × 109/л, Среактивного белка > 30 мг/л, в последнее время — также прокальцитонина > 2 нг/мл [2].
Абсолютными показаниями к назначению антибактериальной терапии являются: острый гнойный синусит; обострение хронического синусита; острый стрептококковый тонзиллит; острый средний отит (ОСО) у детей до 6 мес.; паратонзиллит; эпиглоттит; пневмония. Дифференцированного подхода к назначению антибактериальной терапии требуют: ОСО у детей старше 6 мес.; обострение хронического тонзиллита [1].
При назначении антибиотиков детям в амбулаторной практике используются такие принципы:
- назначать только при высоковероятной или доказанной бактериальной природе заболевания;
- выбирать антибиотики по возможности с учетом региональных данных о наиболее распространенных (вероятных) возбудителях и их резистентности;
- учитывать антибактериальную терапию, которую ребенок получал в предшествующие 2–3 мес., так как повышен риск носительства резистентной микрофлоры (S.pneumoniae, H.influenzae и др.);
- использовать пероральный путь приема антибиотиков;
- не применять потенциально токсичные препараты (аминогликозиды, хлорамфеникол, сульфаниламиды, фторхинолоны);
- учитывать возрастные ограничения применения антибиотиков (например, тетрациклины — с 8 лет, фторхинолоны — с 18 лет);
- проводить коррекцию стартовой антибактериальной терапии (при отсутствии клинических признаков улучшения в течение 48–72 ч от начала терапии; в более ранние сроки — при нарастании тяжести заболевания; при развитии тяжелых нежелательных реакций; при уточнении возбудителя инфекции и его чувствительности к антибиотикам по результатам микробиологического исследования);
- отменять антибиотики при появлении данных о том, что инфекция не является бактериальной, не ожидая завершения первоначально намеченного курса терапии;
- при проведении коротких курсов антибактериальной терапии не назначать антибиотики вместе с антигистаминными или противогрибковыми препаратами, иммуномодуляторами изза отсутствия доказательств преимуществ их совместного назначения;
- по возможности не использовать жаропонижающие средства вместе с антибиотиками, так как это может скрыть отсутствие эффекта и задержать смену препарата.
Существуют определенные различия при лечении детей в условиях поликлиники и стационара, связанные с характером возбудителей и тяжестью заболевания, но основной целью, которую преследует антибактериальная терапия, является эрадикация возбудителей. В последние годы установлены основные возбудители верхних и нижних дыхательных путей у детей (Streptococcus pneumoniae, Haemophilus influenzae, Moraxella catarrhalis) и обычно лечение детей с легкими и среднетяжелыми формами заболеваний осуществляется амбулаторно. Так, при остром среднем отите частота выделения пневмококка составляет 20–40 %, гемофильной палочки — 10–30 %, моракселлы — 5–15 %; при остром синусите пневмококки обнаруживаются в 41 % случаев, гемофильная палочка — в 35 %, моракселла — в 4 %, обычно в ассоциации с анаэробами (около 7 % выделенных штаммов); при обострении хронических лоринфекций этиологическая роль анаэробных бактерий увеличивается (67 % выделенных штаммов). По данным 15 североамериканских клинических исследований, наиболее значимыми возбудителями внебольничной пневмонии являются пневмококк (20–60 %) и гемофильная палочка (3–10 %). Атипичные возбудители (микоплазмы, хламидии, легионеллы) вне эпидемических вспышек вызывают инфекции нижних дыхательных путей в 1–8 % случаев [3]. Развитие тяжелых форм заболевания с осложнениями, в том числе нозокомиальных инфекций, которые обусловлены прежде всего грамотрицательной микрофлорой (Klebsiella pneumoniae, Pseudomonas aeruginosa, Acinetobacter spp., Escherichia coli), нередко устойчивой к большинству антибиотиков, требует госпитализации.
Достижение эрадикации возбудителей предотвращает переход острой инфекции в хроническую, уменьшает частоту рецидивов при хронических заболеваниях, увеличивает интервал между обострениями, т.е. разрывает порочный круг инфекционного процесса и улучшает качество жизни пациента. Непременными условиями надежной эрадикации микроорганизмов при лечении инфекций респираторного тракта являются: активность антибиотика в отношении основных возбудителей; достаточные концентрации антибиотика в очаге инфекции; поддержание подавляющей рост бактерий концентрации в течение необходимого времени. Активность в отношении основных возбудителей определяется природным спектром антибиотика и уровнем приобретенной резистентности к нему микроорганизмов. Лактамные антибиотики плохо проникают в клетки макроорганизма, поэтому наиболее высокие концентрации создаются в межклеточном пространстве, макролидные антибиотики главным образом концентрируются внутриклеточно, при этом их концентрации вне клеток могут быть недостаточными (ниже значений минимальной подавляющей концентрации (МПК) для пневмококка и гемофильной палочки). Для достижения адекватного клинического эффекта концентрации беталактамных антибиотиков в очаге инфекции должны превышать МПК, при которой происходит гибель более 90 % микроорганизмов (МПК90), в течение более 40 % времени между введениями препарата (Т > МПК90)
Наиболее часто в практике участкового педиатра выбор стартовой (эмпирической) антибактериальной терапии основывается на клинических проявлениях заболевания [4].
Среди современных антибиотиков разных групп цефалоспориновые антибиотики (в мире насчитывается около 70 [5]) занимают особенное место, с их применением связаны как большие надежды, так и определенное разочарование, что обусловлено неадекватным их применением.
В 1944 году итальянский исследователь Джузеппе Броту предположил, что периодическое самоочищение сточных вод в Сардинии обусловлено ингибирующей активностью особых микроорганизмов. В 1945 году был выделен гриб Cephalosporin acremonium, обладающий выраженной антибактериальной активностью в отношении грамположительных и грамотрицательных микроорганизмов. В последующем, с 1955 по 1962 г., рабочая группа под руководством H. Florey и E. Abraham ведет активное изучение этого гриба и продуктов его жизнедеятельности. Была выделена бактерицидная субстанция — цефалоспорин С, которая стала исходным веществом для получения 7аминоцефалоспориновой кислоты — структурной основы цефалоспоринов. В 1970 году врачебный мир знакомится с цефалексином, а в 1971 году появляется цефазолин [6].
Цефуроксим (ставший родоначальником так называемого II поколения цефалоспоринов) создан компанией Glaxo в 1970 году (патент США № 3.974.153), но использовался в парентеральной форме изза низкой биоабсорбции, затем Glaxo синтезировала цефуроксим для перорального применения (патент США № 4.267.320 от 12 мая 1981 года), разрешен FDA в 1987 году.
В 1980 и 1982 годах появляются цефотаксим и цефтриаксон — ключевые препараты III поколения цефалоспоринов, в 1983 году — цефтазидим (имеет еще антисинегнойную активность).
Антибактериальная активность цефалоспоринов обусловлена торможением синтеза пептидогликана — структурной основы микробной стенки. Важно подчеркнуть, что бактерицидный эффект цефалоспоринов реализуется только в процессе роста и размножения микроорганизмов, тогда как «покоящаяся» клетка неуязвима для действия антибиотиков.
К настоящему времени синтезировано 4 поколения цефалоспоринов. В основу деления цефалоспоринов на поколения, или генерации, положена их антимикробная активность, при этом каждая генерация имеет ключевой препарат, с которым ассоциируется то или иное поколение и который служит как бы образцом для создания лекарствпрототипов (табл. 1). В ряду от I к III поколению для цефалоспоринов характерна тенденция к расширению спектра и повышению уровня антимикробной активности в отношении грамотрицательных бактерий при некотором снижении активности в отношении грамположительных микроорганизмов.
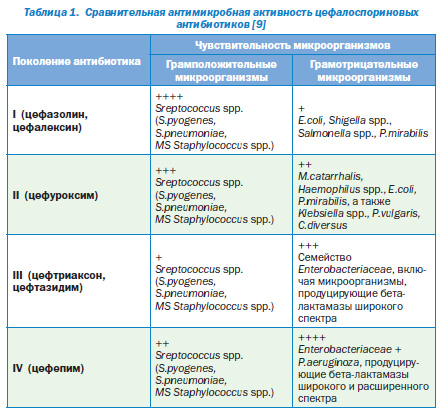
По уровню пневмококковой активности цефалоспорины I поколения уступают аминопенициллинам, хотя они активны в отношении S.pneumoniae, а также в отношении Staphylococcus spp., но лишь метициллинчувствительных. К этой группе относятся препараты как для парентерального введения (цефазолин, цефрадин), так и для приема внутрь (цефалексин, цефадроксил). Антимикробный спектр пероральных и парентеральных цефалоспоринов І поколения во многом схож, однако парентеральные превосходят по своей активности пероральные препараты.
Эти препараты стойкие к действию стафилококковой беталактамазы, но гидролизируются беталактамазами грамотрицательных бактерий (Escherichia coli, Salmonella spp., Schigella spp., Proteus mirabilis), в отношении которых активность значительно ограничена. Препараты этой группы не активны в отношении атипичных микроорганизмов.
Основным показанием для пероральных цефалоспоринов I поколения являются стрептококковые или стафилококковые инфекции. Цефадроксил и цефалексин являются альтернативой природным пенициллинам и аминопенициллинам при лечении стрептококкового тонзиллита, а также основными средствами для лечения неосложненных инфекций кожи и мягких тканей в амбулаторных условиях. Эти препараты эффективны также при лечении острого гнойного артрита, в этиологии которого доминируют стафилококки. Из пероральных цефалоспоринов I поколения предпочтение отдается цефадроксилу, так как при равной антимикробной активности in vitro он имеет преимущество по сравнению с цефалексином в удобстве дозирования (с интервалом 12 часов в отличие от цефалексина, который назначается каждые 6 часов).
Устойчивость микроорганизмов к действию цефалоспоринов может быть связана с одним из следующих механизмов: видоизменением (модификацией) пептидогликана, снижением эффективности цефалоспоринов; гидролизной активацией антибиотиков (беталактамазами); нарушением проницаемости внесенных структур микробной клетки и затруднением связывания антибиотика с пептидогликанами.
Цефалоспорины II поколения имеют более высокую активность в отношении грамотрицательных бактерий (в сравнении с препаратами предыдущей группы), особенно H.influenzaе, а также более устойчивы к действию беталактамаз. При этом сохраняется высокая активность к грамположительным бактериям. К препаратам этой группы для парентерального введения относятся цефуроксим, цефокситин, цефамандол, для перорального введения — цефуроксима аксетил, цефаклор.
Безусловным лидером II поколения среди пероральных препаратов является молекула цефуроксима. При сходном с цефаклором антимикробном спектре цефуроксим более активен в отношении Strеptococcus spp. и Staphylococcus spp. Цефуроксим также более активен в отношении M.catarrhalis и Haemophylus spp., так как устойчив к гидролизу их беталактамазами, цефаклор этими ферментами разрушается.
Цефуроксима аксетил является пролекарством и при приеме внутрь метаболизируется в стенке кишки до активного соединения — цефуроксима. Биодоступность цефуроксима аксетила увеличивается после приема пищи.
Показания к использованию: фарингит (тонзиллит); острый средний отит; синусит; острый бронхит; пневмония, неосложненная инфекция кожи (фолликулит, импетиго, эризипелас, целлюлит, фурункул, карбункул); неосложненная инфекция мочевой системы (пиелонефрит, цистит); болезнь Лайма.
При лечении стрептококкового тонзиллита цефуроксима аксетил показан в случае наличия бактерий, которые продуцируют беталактамазу; если недавно использовалась антибиотикотерапия; при рецидивирующем стрептококковом тонзиллите и в случае неудачи эрадикации бетагемолитического стрептококка группы А или отсутствия эффекта от пенициллина; при наличии сопутствующих заболеваний, аллергии на пенициллины [7].
Цефуроксим рекомендуется в лечении хронического аденоидита в случае аллергии на пенициллины [8].
Базовыми препаратами ІІІ поколения являются цефотаксим и цефтриаксон, спектр их антибактериальной активности практически идентичен. Для них характерна высокая активность в отношении Streptococcus spp., причем та часть пневмококков, которые устойчивы к пенициллину, чувствительны к цефотаксиму и цефтриаксону. Важно, что они активны в отношении S.aureus, кроме MRSAштаммов. Другие актуальные для заболеваний органов дыхания патогены — H.influenzae и M.сatarrhalis абсолютно беззащитны перед цефалоспоринами III поколения, так же как и все представители семейства Enterobacteriacaeae, включая те, что продуцируют беталактамазы широкого спектра. Представители III поколения активны в отношении менингококков. При этом они способны проникать через гематоэнцефалический барьер, создавать терапевтические концентрации в спинномозговой жидкости. Цефалоспорины III поколения активны в отношении гонококков. Цефтазидим и цефоперазон стоят особняком в группе цефалоспоринов III поколения. Их отличает от вышеназванных препаратов активность (особенно цефтазидима) в отношении Р.aeruginoza, что чрезвычайно важно при курации больных с госпитальными инфекциями. Они также создают клинически значимые концентрации в спинномозговой жидкости. Говоря о представителях III поколения цефалоспоринов, следует обратить внимание на наличие в их семействе ингибиторозащищенных цефалоспоринов — цефоперазона/сульбактама и цефтриаксона/сульбактама. Благодаря соотношению двух компонентов удается достичь инактивации большинства беталактамаз расширенного спектра, которые в первую очередь выделяют Enterobacteriaceae, Acinetobacter spp., B.fragilis.
В связи с расширенной антимикробной активностью представителей III поколения цефалоспоринов их применение в педиатрической практике не всегда оправданно.
При внебольничных респираторных инфекциях верхних и нижних дыхательных путей значение пероральных цефалоспоринов III поколения ограниченно.
Говоря о побочных эффектах цефалоспоринов III поколения, следует учитывать их способность повышать активность трансаминаз, а высокие дозы цефтриаксона могут вызвать холестаз и псевдохолелитиаз. Цефтриаксон, цефотаксим нарушают выработку и всасывание витамина К изза подавления кишечной микрофлоры, что вызывает нарушение свертывания крови, поэтому пациентам, принимающим ацетилсалициловую кислоту, антикоагулянты, это следует учитывать [10, 11].
Все пероральные цефалоспорины III генерации характеризуются более длительным (по сравнению с препаратами I–II генерации) периодом полувыведения, поэтому могут приниматься каждые 12–24 ч.
Цефалоспорины IV поколения по сравнению с тремя предыдущими генерациями имеют сбалансированный антимикробный спектр: объединение активности цефалоспоринов I–II генераций к грамположительным бактериям (метициллинчувствительным стафило, стрепто, певмококкам) и некоторым анаэробам с высокой активностью цефалоспоринов III генерации. Эта группа представлена парентеральными препаратами цефепимом, цефпиромом. Ключевой препарат IV поколения — цефепим. Главными отличительными чертами от цефалоспоринов III поколения являются повышенная способность проникать через внешнюю мембрану грамотрицательных бактерий и определенная устойчивость к гидролизу хромосомными беталактамазами класса С. Цефепим, сохраняя антимикробное свойство предыдущего поколения, проявляет значительно большую активность в отношении Р.аeruginoza. Его логичнее всего применять при тяжелых нозокомиальных инфекциях, вызванных полирезистентной флорой, инфекциях на фоне иммунодефицитных состояний, тяжелых инфекциях дыхательной системы — абсцессе легкого, эмпиеме плевры.
Цефалоспорины всех генераций имеют преимущественно почечный путь элиминации, поэтому при нарушении функции почек следует уменьшать дозу препаратов.
Таким образом, создание и внедрение в клиническую практику антибиотиков класса цефалоспоринов явилось одним из важнейших событий в истории химиотерапии бактериальных инфекций. Представители этого класса остаются одними из самых назначаемых во многих странах мира.
Сравнительное изучение бактериологической активности цефалоспоринов разных генераций по отношению к бактериям, выделяемым при бронхолегочных заболеваниях у детей, позволило установить высокую бактериологическую активность цефалоспоринов II поколения. При этом отсутствует существенная разница в активности парентеральных и пероральных форм антибиотиков по отношению к основным этиологически значимым микроорганизмам при данной патологии. Все это обосновывает применение пероральных форм цефалоспориновых антибиотиков II генерации при бронхолегочных заболеваниях, в том числе при неосложненных острых пневмониях у детей. Цефуроксима аксетил эффективен при лечении острого среднего отита у детей в 93 % случаев, синусита — в 89 %, тонзиллофарингита — в 97 %, негоспитальной пневмонии — в 92 % [12, 13].
Цефуроксима аксетил (Зиннат™) — это единственный цефалоспорин II поколения, устойчивый к беталактамазам, поэтому активен в отношении не только E.coli, но и Klebsiella spp., которые активно продуцируют беталактамазы широкого спектра, следовательно, он высокоэффективен при инфекциях мочевыводящих путей.
Применяя цефуроксим в лечении тяжелых форм заболевания, можно использовать так называемую ступенчатую (этапную) терапию. При этом в период выраженного токсикоза цефуроксим назначается парентерально (Зинацеф™), а при снижении интенсивности инфекционновоспалительных проявлений терапия продолжается пероральной формой препарата (Зиннат™).
Цефуроксима аксетил отличается хорошим профилем безопасности. В сравнении с цефалоспоринами III поколения (цефподоксима проксетил и цефиксим) с ним связано наименьшее количество побочных эффектов со стороны желудочнокишечного тракта [12].
Для детей в амбулаторных условиях следует использовать суспензию ЗиннатТМ, которую легко можно приготовить из гранул, расфасованных специально для одного приема в пакетики (саше) по 125 мг или во флаконы (125 мг/5 мл, 100 мл).
Применение форм антибиотиков для 1–2кратного приема в сутки оказывает положительное влияние на соблюдение пациентами предписаний врача. Однодвукратный прием антибиотика удобен и для родителей ребенка: чаще соблюдается правильный режим дозирования, ниже вероятность пропуска приема препарата.
Статья печатается при поддержке
компании ГлаксоСмитКляйн
1. Баранов А.А., Богомильский М.Р., Волков И.К. Практические рекомендации по применению антибиотиков у детей в амбулаторной практике // Здоров’я України. — 2008. — 10 (1). — 2124.
2. Таточенко В.К. Антибиотики в арсенале участкового педиатра для лечения болезней органов дыхания // Лечащий врач. — 2009; http://www.lvrach.ru/2009/06/9784082/?format=print
3. Bartlett J.G., Mundy L.M. Communityacquired pneumonia // New England Journal of Medicine. — 1995. — 333. — 161824.
4. Белобородова Н.В. Алгоритмы антибиотикотерапии рецидивирующих инфекций дыхательных и мочевыводящих путей у детей // Здоровье ребенка. — 2009. — 1(16); http://www.mifua.com/archive/article/7952
5. Cамсыгина Г.А. Цефалоспорины в педиатрии // В мире лекарств. — 2000. — № 1; http://medi.ru/doc/7200104.htm
6. Мостовой Ю.М. Цефалоспорины: разочарования и оптимизм // Новости медицины и фармации. — 2011. — 19 (391); http://www.mifua.com/archive/article/22886
7. Brook I. Overcoming penicillin failures in the treatment of Group A streptococcal pharyngotonsillitis // International Journal of Pediatric Otorhinolaryngology. — 2007. — V. 71, 10. — 15011508.
8. Marzouk H., Aynehchi B., Thakkar P. et al. The utility of nasopharyngeal culture in the management of chronic adenoiditis // Int. J. Pediatr. Otorhinolaryngol. — 2012 Oct. — 76(10). — 14135.
9. Periti P. Introduction: cephalosporin generations // J Chemother. — 1996 Feb. — 8 (Suppl. 2). — 36.
10. Инструкция к медицинскому применению препарата Цефтриаксон.
11. Инструкция к медицинскому применению препарата Цефотаксим.
12. Scott L.J. et al. Cefuroxime Axetil An Updated Review of its Use in the Management of Bacterial Infections // Goa Drugs. — 2001. — 61 (10). — 14551500.
13. Brook I. Use of oral cephalosporins in the treatment of acute otitis media in children // International Journal of Antimicrobial Agents. — 2004. — 24. — 1823.

