Газета «Новости медицины и фармации» Гастроэнтерология (451) 2013 (тематический номер)
Вернуться к номеру
Стан фіброзування печінки та його наслідки у хворих на неалкогольний стеатогепатит із коморбідним ожирінням та гіпертонічною хворобою у динаміці лікування препаратами Гепадиф®, езетиміб та фозиноприл
Авторы: Хухліна О.С., Мандрик О.Є., Антонів А.А., Буковинський державний медичний університет, м. Чернівці
Рубрики: Гастроэнтерология, Кардиология, Эндокринология
Разделы: Клинические исследования
Версия для печати
Актуальність дослідження коморбідного перебігу неалкогольного стеатогепатиту (НАСГ) у хворих на ожиріння та гіпертонічну хворобу (ГХ) обумовлена каскадом реакцій взаємообтяження, що призводять до прогресування усіх захворювань [1–3]. На тлі ожиріння прогресує метаболічний синдром (МС) із метаболічною інтоксикацією (оксидативний стрес), істотною дис- та гіперліпідемією та накопиченням насичених жирів у печінковій паренхімі, що активує систему прозапальних цитокінів із прискоренням апоптозу клітин, формуванням асептичного запалення, некрозу гепатоцитів, а також активної реакції сполучної тканини з розвитком перицелюлярного, перисинусоїдального, центролобулярного фіброзу печінки [4–6]. Згідно з нашими дослідженнями, за фонового МС та ГХ перебіг НАСГ супроводжується раннім розвитком фіброзування печінкової тканини та внутрішньопечінкової портальної гіпертензії внаслідок зростання артеріальної квоти синусоїдального кровообігу, наслідком чого є розвиток спленомегалії, початкових явищ гіперспленізму (тромбоцитопенія, тенденція до лейкоцитопенії, зниження осмотичної та пероксидної резистентності еритроцитів — ПРЕ), флебектазії гемороїдальних вен) [3, 6]. За адекватного лікування зазначені зміни мають оборотний характер [2], водночас загальноприйняті методи лікування не завжди враховують патогенетичний підхід до проблеми і тому не завжди ефективні.
Метою дослідження було з’ясування ймовірного впливу комплексу засобів (Гепадиф®, езетиміб та фозиноприл) на ступінь стеатозу печінки, фіброзування печінкової тканини, стан печінкового кровообігу та формених елементів крові за коморбідності НАСГ, ожиріння І ступеня та ГХ ІІ стадії.
Матеріал та методи дослідження
Обстежено 60 хворих на НАСГ м’якої та помірної активності з коморбідним перебігом ГХ ІІ стадії та ожирінням І ступеня. Для визначення ефективності лікування було сформовано 2 групи пацієнтів, які були рандомізовані за віком, статтю, ступенем ожиріння та активністю цитолітичного синдрому.
Контрольна група (К) (30 осіб) отримувала гіпокалорійну дієту, метформін по 500 мг 2 рази на день для усунення проявів МС, ессенціалє Н як гепатопротекторний препарат (по 1 капсулі 3 рази на день), аторвастатин по 10 мг 1 раз на день як гіполіпідемічний середник та еналаприлу малеат по 10 мг на добу під контролем артеріального тиску (АТ) упродовж 30 днів.
Основна група (О) (30 осіб) отримувала гіпокалорійну дієту, метформін по 500 мг 2 рази на день для усунення проявів МС, Гепадиф® як гепатопротекторний препарат (по 2 капсули 3 рази на день), езетиміб по 10 мг 1 раз на день як гіполіпідемічний середник та фозиноприл по 10 мг на добу для контролю АТ упродовж 30 днів. Протягом дослідження випадків побічної дії ліків не було встановлено.
Комплексне ультрасонографічне дослідження (УСД) виконували на ультразвуковому сканері AU4 Idea (Biomedica, Італія) конвексним датчиком із частотою 3,5 МГц, воно включало ультразвукове дослідження у реальному масштабі часу у Врежимі та імпульсну допплерографію судин черевної порожнини за методикою Г.І. Кунцевич із співавт. Визначали діаметр (D, мм), максимальну систолічну швидкість кровотоку (Vmax, см/с), кінцеву діастолічну швидкість кровотоку (Vmin, см/с), середню лінійну швидкість кровотоку (Vсер, см/с), об’ємну швидкість кровотоку (Q, мл/хв) ворітної, селезінкової, нижньої порожнистої вен, загальної печінкової та селезінкової артерій. Для ворітної вени обчислювали конгестивний індекс (КІ) за формулою:
КІ = піR2/Vсер,
де R — радіус судини (см), Vсер — середня лінійна швидкість (см/с). ПРЕ вивчали за методикою Н.О. Григорович, О.С. Мавричева.
Стадію фіброзування печінкової тканини вивчали за допомогою ФіброТесту, ступінь жирової дистрофії печінки — за допомогою СтеатоТесту (BioPredictive, Франція). Стан компонентів сполучної тканини вивчали за вмістом у сироватці крові вільного оксипроліну (ВОП) за С.С. Тетянець, білковозв’язаного оксипроліну (БЗОП) — за М.А. Осадчуком, гексозамінів — за О.Г. Архіповою. Колагенолітичну активність (КЛА) плазми крові досліджували за інтенсивністю лізису азоколу методом імуноферментного аналізу.
Статистичну обробку матеріалу здійснювали за допомогою параметричних та непараметричних методів варіаційної статистики.
Результати дослідження
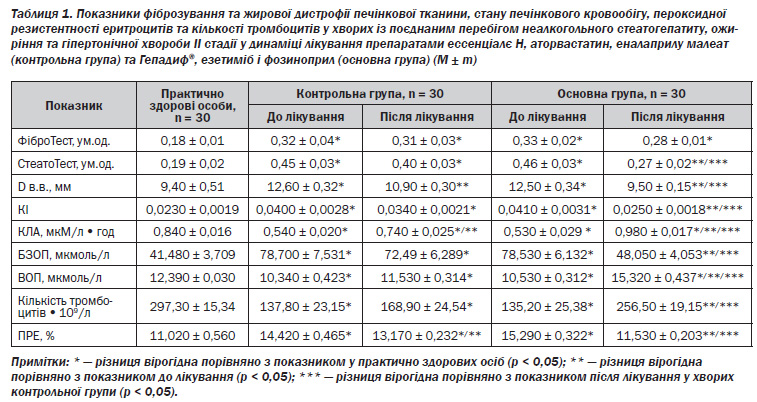
Аналіз впливу препаратів Гепадиф®, езетиміб, фозиноприл при курсовому призначенні хворим на НАСГ (О група) на перебіг захворювання порівняно з К групою виявив такі результати. УСД печінки через 1 місяць лікування хворих на НАСГ О групи виявило вірогідне зниження ступеня гепатомегалії (вертикальний розмір правої частки печінки 151,0 ± 2,3 мм проти 167,3 ± 3,2 мм до лікування), водночас через 1 місяць після лікування даний параметр вже становив 142,0 ± 2,1 мм (17,0 % (р < 0,05)), трансформацію середньозернистої структури паренхіми у дрібнозернисту та більш однорідну, а також істотне зниження ступеня стеатозу печінки (зменшення ступеня дорзального згасання ехосигналу). Вказані дані підтверджувались результатами проведеного СтеатоТесту (табл. 1). Зокрема, показник інтенсивності стеатозу гепатоцитів, який був істотно підвищений до лікування, після лікування істотно знизився у хворих О групи на 41,3 % (р < 0,05), у той час як у групі К — лише мав тенденцію до зниження. Отже, застосування езетимібу у комбінації з препаратом Гепадиф® у лікуванні хворих на НАСГ з ожирінням та ГХ унаслідок нормалізації ліпідного обміну [2] привело до вірогідного зменшення ступеня стеатозу печінки. Проведений ФіброТест в обстежених хворих до лікування виявив вірогідний розвиток фіброзування печінкової тканини, середні показники якого вказували на F1 (табл. 1). Зміни показників ФіброТесту у динаміці лікування були статистично невірогідні в обох групах (р > 0,05), однак у хворих О групи показник фіброзування зменшився на 15,2 % (р > 0,05), що вказує на спроможність запропонованої терапії гальмувати процес фіброзування печінки за умов продовження терапії. На цей факт також вказує динаміка показників обміну компонентів колагену. Так, підвищений до лікування маркер анаболізму колагену БЗОП після лікування вірогідно знизився у О групі на 38,8 % (р < 0,05), маркер катаболізму колагену ВОП зріс на 45,5 % (р < 0,05), що виникло, на нашу думку, внаслідок посилення КЛА плазми крові у 1,8 раза (р < 0,05).
Слід зазначити, що до лікування перебіг НАСГ м’якої та помірної активності на фоні ГХ ІІ стадії супроводжувався початковими проявами портальної гіпертензії (зростання діаметра ворітної вени (D в.в.) в межах 30,0–36,0 %, КІ ворітного кровообігу — у 1,6–1,7 раза (р < 0,05), тромбоцитопенії — у 2,2–2,6 раза (р < 0,05), підвищення здатності еритроцитів до пероксидного гемолізу — у 26–40 % (р < 0,05)).
Як результат проведеної терапії протизапального, мембраностабілізуючого, гіполіпідемічного, системного гіпотензивного та антифібротичного спрямування нами був зареєстрований гіпотензивний ефект на систему портального кровообігу. В обох групах було встановлено зменшення D в.в.: у К групі — на 13,5 % (р < 0,05), в О групі — на 24,0 % (р < 0,05), однак КІ ворітного кровообігу вірогідно знизився лише у О групі хворих: на 39,0 % (р < 0,05) із нормалізацією показника. Наслідком досягнутого ефекту, на нашу думку, стало підвищення після лікування кількості тромбоцитів у периферичній крові в 1,9 раза (р < 0,05), а також зростання ПРЕ на 24,6 % (р < 0,05), що може свідчити як про зниження інтенсивності оксидативного стресу та метаболічної інтоксикації, так і про усунення явищ гіперспленізму.
Висновки
1. У хворих на ожиріння І ступеня та гіпертонічну хворобу ІІ стадії неалкогольний стеатогепатит м’якої та помірної активності перебігає з раннім розвитком фіброзування печінкової тканини (у межах F1 — 0,28–0,36), cередня інтенсивність стеатозу при цьому становить S2 (0,42–0,49), із початковими проявами портальної гіпертензії (зростання діаметра ворітної вени у 30,0–36,0 %, конгестивного індексу ворітного кровообігу — в 1,6–1,7 раза (р < 0,05), тромбоцитопенії — у 2,2–2,6 раза (р < 0,05), підвищення здатності еритроцитів до гемолізу — у 26–40 % (р < 0,05)).
2. Комплексна терапія із включенням препаратів Гепадиф®, фозиноприл та езетиміб була ефективніша за традиційну комбінацію — ессенціалє Н, еналаприл та аторвастатин — щодо швидкого усунення гепатомегалії, зниження ступеня стеатозу гепатоцитів, гальмування фіброзування печінкової тканини, покращення печінкового кровообігу: зниження гемодинамічних показників, що вказують на тиск у системі ворітної вени, відновлення кількісних показників тромбоцитарної ланки гемостазу та стабільності мембран еритроцитів.
1. Буеверов А.О. Неалкогольная жировая болезнь печени: обоснование патогенетической терапии / А.О. Буеверов, П.О. Богомолов // Клинические перспективы в гастроэнтерологии, гепатологии. — 2009. — № 1. — С. 39.
2. Патогенетическое обоснование применения препарата «Гепадиф» у больных неалкогольным стеатогепатитом / Н.В. Харченко, Г.А. Анохина, В.В. Харченко [и др.] // Сучасна гастроентерол. — 2011. — № 6(62). — С. 6671.
3. Хухліна О.С. Неалкогольна жирова хвороба печінки та інсулінорезистентність: патогенез, клініка, діагностика, лікування глутаргіном / О.С. Хухліна, М.Ю. Коломоєць. — Чернівці, 2008. — 318 с.
4. Bohinc B.N. Mechanisms of disease progression in NASH: new paradigms / B.N. Bohinc, A.M. Diehl // Clin. Liver Dis. — 2012. — Vol. 16, № 3. — Р. 549565.
5. Chakraborty J.B. Mechanisms and biomarkers of apoptosis in liver disease and fibrosis / J.B. Chakraborty, F. Oakley, M.J. Walsh // Int. J. Hepatol. — 2012. — Vol. 2012. — P. 648915.
6. Fujii H. Inflammation and fibrogenesis in steatohepatitis / H. Fujii, N. Kawada // J. Gastroenterol. — 2012. — Vol. 47, № 3. — P. 215225.
7. NASH is an inflammatory disorder: pathogenic, prognostic and therapeutic implications / G.C. Farrell, D. van Rooyen, L. Gan, S. Chitturi // Gut. Liver. — 2012. — Vol. 6, № 2. — P. 149171.
8. Pagadala M.R. The relevance of liver histology to predicting clinically meaningful outcomes in nonalcoholic steatohepatitis / M.R. Pagadala, A.J. McCullough // Clin. Liver Dis. — 2012. — Vol. 16, № 3. — Р. 487504.
9. Torres D.M. Features, diagnosis, and treatment of nonalcoholic Fatty liver disease / D.M. Torres, C.D. Williams, S.A. Harrison // Clin. Gastroenterol. Hepatol. — 2012. — Vol. 10, № 8. — P. 837858