Международный неврологический журнал 2 (56) 2013
Вернуться к номеру
Центральний понтинний мієліноліз: діагностика, особливості перебігу
Авторы: Шульга Л.А., Білецька О.В., Ящук Н.М., Шульга О.Д., Луцька міська клінічна лікарня, Волинська обласна клінічна лікарня, м. Луцьк
Рубрики: Неврология
Разделы: Справочник специалиста
Версия для печати
Розглядається клінічний випадок центрального понтинного мієлінолізу, причини, що зумовлюють його виникнення, труднощі при діагностиці даного захворювання.
Рассматривается клинический случай центрального понтинного миелинолиза, причины, обусловливающие его возникновение, трудности при диагностике данного заболевания.
The paper deals with a clinical case of central pontine myelinolysis, considers the causes induced its development, difficulties in diagnosing this disease.
центральний понтинний мієліноліз, гіпонатріємія.
центральный понтинный миелинолиз, гипонатриемия.
central pontine myelinolysis, hyponatremia.
/161/161.jpg) Центральний понтинний мієліноліз (ЦПМ) — це рідкісна форма демієлінізуючого процесу в ділянці мосту мозку, що виникає як ускладнення при швидкій корекції вираженої та, як правило, хронічної гіпонатріємії будьякої етіології.
Центральний понтинний мієліноліз (ЦПМ) — це рідкісна форма демієлінізуючого процесу в ділянці мосту мозку, що виникає як ускладнення при швидкій корекції вираженої та, як правило, хронічної гіпонатріємії будьякої етіології.
ЦПМ уперше був описаний у 1959 р. R. Adams і співробітниками як особлива форма демієлінізуючого ураження, що розвивається в ділянці мосту мозку при алкоголізмі та порушенні харчування [1]. У 1962 р. було встановлено, що вогнища демієлінізації можуть зустрічатися поза межами мосту (мозочок, латеральні колінчасті тіла, зовнішня капсула, гіпокамп, покришка, таламус, хвостате ядро) як у поєднанні з ЦПМ, так і ізольовано, таке ураження було назване екстрапонтинним мієлінолізом (ЕПМ). У 1976 р. Tomlinson і співавт. установили, що етіологічним чинником ЦПМ є швидка корекція рівня Na в пацієнтів із гіпонатріємією. Частіше за все ЦПМ та ЕПМ розвивається в пацієнтів при алкоголізмі [1–5], хронічній печінковій недостатності, після трансплантації печінки [2, 4, 6], при хронічній нирковій недостатності [6, 7], цукровому діабеті [6, 7], після тривалого застосування діуретиків [2, 4, 6]. До рідкісних причин розвитку цього стану відносять полідипсію, синдром Шихана, булімію, видалення аденоми гіпофіза й астроцитоми мозочка, системний червоний вовчак [6, 7]. Морфологічна основа ЦПМ — розпад мієліну в центральній частині варолієва мосту біля серединного шва, що далі поширюється ніби язики полум’я на провідні шляхи [2]. Вентролатеральні відділи мосту залишаються інтактними.
В експерименті на моделі ЦПМ у щурів було показано, що хронічна гіпонатріємія веде до внутрішньоклітинного набряку мозку, а швидке введення гіпертонічного сольового розчину (із метою корекції гіпонатріємії) переводить його в позаклітинний набряк, провокуючи набухання та загибель олігодендроцитів, пошкодження олігодендромієлінового комплексу, інтрамієліновий набряк і врештірешт — розрив і розпад мієлінової оболонки [8].
Клінічний перебіг ЦПМ класично описується як двофазний [5, 7]. ЦПМ починається з розладів свідомості, судомних нападів, рідше — гострих психозів та інтелектуальних порушень (пов’язаних із хронічною гіпонатріємією), після чого спостерігається тимчасове покращення стану (пов’язане з початковим підвищенням рівня Na), а через 2–3 дні розвивається вторинний неврологічний синдром, безпосередньо спричинений мієлінолізом. Ця пізня фаза найчастіше характеризується розвитком тетрапарезу чи тетраплегії, псевдобульбарного синдрому внаслідок ураження кортикоспінального та кортикобульбарного шляхів, синдромом «закритої людини», рідше повідомляється про мутизм, дистонію та кататонію.
Діагностика
Діагностика ЦПМ та ЕПМ стала можливою завдяки методам нейровізуалізації. Комп’ютерна томографія (КТ) виявляє вогнища зниженої щільності білатерально в мості та інших ділянках мозку, які не накопичують контраст. Слід зазначити, що КТ не завжди здатна виявити вогнища ураження при даній патології, особливо в ранніх стадіях [10].
Магнітнорезонансна томографія (МРТ) є найінформативнішим методом діагностики ЦПМ. МРТдослідження виявляє гіпоінтенсивний сигнал у зонах ураження мозку (як правило, в центральній частині мосту) в Т1режимі та гіперінтенсивний сигнал у зонах ураження мозку без ознак перифокального набряку чи об’ємного впливу в Т2режимі. Типова зона ураження мосту описується як овальна зона на сагітальних, трикутна — на аксіальних зрізах і у формі крил летючої миші — на коронарних зрізах. Покришка мосту та його вентролатеральні відділи не уражаються [11, 12]. Час появи типових для ЦПМ змін при МРТобстеженні та клінічних симптомів може не збігатися, розрив у часі може становити до 10–14 днів [2], що обмежує використання Т1 та Т2режимів МРТ для ранньої діагностики ЦПМ. Проте МРТ DWI є чутливішим методом щодо руху води, а тому може бути використаним для ранньої діагностики ЦПМ та ЕПМ [2, 5]. Розміри вогнища на МРТ не корелюють із вираженістю неврологічної симптоматики [2].
Диференціальна діагностика
Оскільки ЦПМ є рідкісною патологією, диференціальна діагностика повинна проводитись з захворюваннями, що мають схожі клінічні прояви: інсультом, пухлинами мозку (гліоми, метастази), розсіяним склерозом, енцефалітами [6, 7] — та іншими формами ураження центральної нервової системи при алкоголізмі: енцефалопатією Верніке, алкогольною мозочковою дегенерацією [2].
Вищевказані захворювання звичайно візуалізуються у вигляді більш дифузних вогнищ, не бувають настільки симетричними і відрізняються від ЦПМ і ЕПМ клінічно.
Наводимо клінічний випадок пацієнтки Д., 49 років, яка знаходилась на стаціонарному лікуванні у відділенні екстракорпоральних методів детоксикації та неврологічному відділенні ЛМКЛ з 28.12.2009 по 19.01.2010 р., якій було встановлено діагноз центрального понтинного мієлінолізу.
Пацієнтка направлена з наркодиспансеру з діагнозом: «підозра на внутрішньочерепну гематому. Глибокий сопор — кома I. ППР унаслідок вживання алкоголю. Стан після перенесеного алкогольного делірію».
Згідно з анамнезом зловживала алкоголем протягом останніх 2 років. Перед надходженням у наркодиспансер протягом 3 днів знаходилася на обстеженні в нашому відділенні із приводу серії генералізованих тонікоклонічних судомних нападів, що виникли вперше. Проведена КТ головного мозку виявила гідроцефалію середнього ступеня, атрофічні зміни кори обох півкуль; БАК виявив: гіпокаліємію, гіпербілірубінемію (64,8 мкмоль/л). На 3й день у хворої розвинувся деліріозний синдром, із приводу якого для подальшого лікування пацієнтка переведена в наркодиспансер. Деліріозний стан був купіруваний, але на 5й день виникла слабкість у ногах, порушилась хода, з’явилися розлади мови за типом дизартрії та дисфагії, протягом 3 днів наросли розлади свідомості. Для подальшого дообстеження та лікування направлена в Луцьку міську клінічну лікарню.
При огляді шкірні покриви та склери субіктеричні, обличчя набрякле. АТ 120/80 мм рт.ст. Ps — 90 уд/хв, ритмічний. Живіт м’який, дещо збільшений у розмірі. Печінка виступає зпід краю реберної дуги на 3–4 см. У неврологічному статусі: сопор, відкриває очі на прохання. На больові подразники реагує стогоном. Очні щілини, зіниці D = S, фотореакції мляві. Вертикальний та горизонтальний парез погляду. Симптом очей ляльки. Двобічний парез жувальної та мімічної групи м’язів. Анартрія. Знижений глотковий рефлекс. Активні рухи в кінцівках відсутні. Квадриплегія. Тонус м’язів кінцівок знижений. Сухожилкові рефлекси не викликаються. Паталогічних стопних та менінгеальних знаків не виявлено.
На КТ головного мозку попередні зміни, вогнищевого ураження не виявлено. На УЗД органів черевної порожнини ознаки хронічного гепатиту, асцит. КТ ОГК — двобічна гіпостатична пневмонія, пневмофіброз зліва. ЕКГритм синусовий, правильний, дифузні зміни міокарда. Загальний аналіз крові — помірний лейкоцитоз 12,5 •10/л. Біохімічний аналіз крові: гіпонатріємія — Na 131 ммоль/л, гіпербілірубінемія — 43,39 ммоль/л. Люмбальна пункція: ліквор у межах норми.
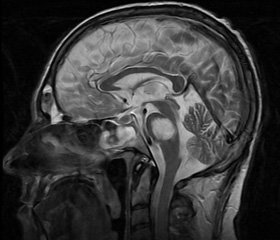
На 3й день госпіталізації проведено МРТ головного мозку: На серії МРтомограм, виконаних у режимі Т2Flair, у мості візуалізується гіперінтенсивне вогнище 28 мм. Враховуючи дані анамнезу, підгострий перебіг захворювання, результати неврологічного огляду (синдром закритої людини), дані МРТ головного мозку, хворій установлено діагноз: «центральний понтинний мієліноліз із тетраплегією, двобічним над’ядерним паралічем жувальної та бульбарної групи м’язів».
Алкогольна хвороба печінки: хронічний алкогольний гепатит із трансформацією в цироз. Асцит. Метаболічна (токсична) кардіоміопатія. СН IIA NYHA II. Двобічна гіпостатична пневмонія. Пролежні сідничної ділянки, п’яткових кісток».
Проведено лікування ноотропами (церебролізин, цераксон, пірацетам, актовегін), препаратами для покращення реологічних властивостей крові (сорбілакт, реосорбілакт, трентал), вітамінотерапію (вітаміни В1, В6, В12, С), протинабрякову терапію (Lлізину есцинат, манітол), вводили дексаметазон, антихолінестеразні препарати (нівалін, прозерин), проводили антибіотикотерапію та застосовували препарати для симптоматичного лікування цирозу печінки. Хворій проводився масаж кінцівок, електрофорез із прозерином та електростимуляція нижніх кінцівок. На фоні проведеного лікування у хворої була відмічена позитивна неврологічна динаміка, наросла сила в правих кінцівках до 3 балів, з’явились мінімальні рухи в лівих кінцівках, сухожилкові рефлекси, зріс об’єм рухів очними яблуками, почала розмовляти (мова дизартрична), самостійно ковтати. Незважаючи на позитивну неврологічну динаміку, у пацієнтки прогресували явища печінкової недостатності та асцит. На 22й день перебування в стаціонарі помирає на фоні поліорганної недостатності.
При встановленні діагнозу в нашої пацієнтки в першу чергу розглядалась можливість ішемічного інсульту в мості. Проте відсутність факторів ризику (артеріальної гіпертензії, церебрального атеросклерозу), підгострий розвиток захворювання, переважання в клінічній картині загальномозкової симптоматики і характерні зміни на МРТ головного мозку (наявність гіперінтенсивного вогнища в мості зі збереженням вентролатеральних його відділів у режимі Т2Flair) дозволили правильно поставити діагноз. Для інсульту характерне асиметричне вогнище в мості, можливе також симетричне вогнище в медіодорзальних відділах, переважно у формі трикутника з вершиною до покришки, часто уражається і покришка, що діагностується в режимі Т1, Т2 з першої доби.
Лікування та профілактика
Немає досліджень щодо ефективності різних методів лікування при ЦПМ [2]. Лікування має симптоматичний характер. В окремих роботах повідомляється про ефективність великих доз кортикостероїдних препаратів [2, 3, 6], доцільність інтравенозного введення імуноглобулінів [2, 3], проведення плазмаферезу [2]. У пацієнтів із виявленою гіпонатріємією та пацієнтів із групи ризику ЦПМ найкращим лікуванням є адекватна корекція гіпонатріємії.
Гіпонатріємія за ступенем вираженості поділяється на помірно виражену (125 < Nа < 135 ммоль/л), виражену гіпонатріємію (Na < 125 ммоль/л) або різке зниження рівня Na плазми (> 0,5 ммоль/год). За тривалістю поділяється: на гостру гіпонатріємію < 48 годин, хронічну гіпонатріємію > 48 годин (хронічною вважається і гіпонатріємія, тривалість якої невідома).
Для запобігання демієлінізуючим синдромам принципово важливим є темп корекції гіпонатріємії. Темп корекції гострої гіпонатріємії не більше 24 ммоль/добу. Темп корекції хронічної гіпонатріємії ≤ 1–2 ммоль/л/год, але не більше 8 ммоль/л/добу [12, 13].
Тривалий час прогноз при ЦПМ вважався вкрай несприятливим (оскільки до запровадження методів нейровізуалізації цей діагноз був посмертним). Проте останнє дослідження серії 34 випадків ЦПМ показало такий результат: у 2 пацієнтів — смерть, 11 пацієнтів — наявність неврологічного дефіциту, що потребував стороннього догляду, 10 пацієнтів — наявність неврологічного дефіциту, проте хворі залишились самостійними, в 11 — повне видужання [2, 14]. Індивідуальний прогноз — тяжкий, слід зазначити, що результат не залежить від вираженості неврологічної симптоматики, рівня гіпонатріємії чи МРТзмін [4, 14].
Висновки
При встановленні діагнозу ЦПМ виникають значні труднощі. МРТ є золотим стандартом у діагностиці даної патології. Раннє виявлення цієї патології дозволяє адекватно проводити терапію з використанням сучасних методик, але найбільш ефективною є профілактика цього захворювання, що полягає в правильній корекції гіпонатріємії.
1 Adams R.D., Victor M., Mancall E.L. Central pontine myelinolysis: a hitherto undescribed disease occurring in alcoholic and malnourished patients // Arch. Neurol. Psychiatry. — 1959. — 81. — 154172.
2. Martin R.J. Central pontine and extrapontine myelinolysis: the osmotic demyelination syndromes // J. Neurol. Neurosurg. Psychiatry. — 2004. — 75(suppl. 3). — iii22iii28.
3. Bakst R.L., Kasper M.E., Greene R.E. Central Pontine Myelinolysis in a Patient Admitted for Alcohol Withdrawal Hospital // Physician. — May 2008. — Vol. 44, № 5. — Р. 2328.
4. Pearce J.M.S. Central Pontine Myelinolysis // Eur. Neurol. — 2009. — 61. — 5962.
5. Kimberly A. Ruzeka, Norbert G. Campeaua and Gary M. Millera. Early Diagnosis of Central Pontine Myelinolysis with DiffusionWeighted Imaging AJNR // Am. J. Neuroradiol. — February 2004. — 25. — 210213.
6. Cтaxовская Л.В., Ерохина Л.Г., Лескова Н.Н., Губский Л.В. Центральный понтинный и экстрапонтинный миелинолиз // Журн. неврол. и психиат. — 2000. — 100, 2. — 5558.
7. Волкова Э.Ю., Бобылова М.Ю., Алиханов А.А., Михайлова С.В., Пилия С.В., Карманов М.Е., Дунаевская Г.Н., Глухарева Е.Ф. Центральный понтинный и экстрапонтинный миелинолиз у підростка // Журнал неврологии и психиатрии им. С.С. Корсакова. — 2008. — 2.
8. Norenberg M.D., Papendick R.E. Chronicity of hyponatremia as a factoir in experimental myelinolysis // Ann. Neurol. — 1984. — 15. — 544547.
9. Laureno R., Illowsky Karp B. Myelinolysis after correction of hyponatremia // Ann. Intern. Med. — 1997. — 126. — 5762.
10. Rosenbloom S., Buchhlolz D., Kumar A.J. et al. Evolution of central pontine myelinolysis on CT // Am. J. Neuroradiol. — 1984. — 5. — 110112.
11. Thompson P.D., Miller D., Gledhill R.F., Rossor M.N. Magnetic resonance imaging in central pontine myelinolysis // J. Neurol. Neurosurg. Psychiatry. — 1989. — 52. — 675677.
12. Kumar S., Fowler M., GonzalezToledo E., Jaffe S.L. Central pontine myelinolysis, an update // Neurol. Res. — 2006. — 28. — 360366.
13. Horacio J. Adrogué, Nicolaos E. Madias. Hyponatremia // New England Journal of Medicine. — 2000. — Vol. 342, № 21. — 15811589.
14. Menger H., Jörg J. Outcome of central pontine and extrapontine myelinolysis // Journal of Neurology. — 1999. — 246. — 700705.

/163/163.jpg)