Газета «Новости медицины и фармации» Антимикробная терапия (223) 2007 (тематический номер)
Вернуться к номеру
Сравнительная эффективность лечения пиелонефритов цефтриаксоном и цефтриаксоном в комбинации с сульбактамом
Авторы: И.Г. БЕРЕЗНЯКОВ, Е.В. ПЕТРЕНКО, Харьковская медицинская академия последипломного образования; А.Ф. МИХАЙЛЮТА, А.Н. ВАСЮК, А.А. МИХАЙЛЮТА, Городская многопрофильная клиническая больница № 25 г. Харькова
Рубрики: Нефрология
Разделы: Клинические исследования
Версия для печати
Введение
Инфекции мочевых путей (ИМП) являются самыми частыми бактериальными инфекциями. В самом общем виде ИМП можно охарактеризовать как наличие бактерий в моче (бактериурия) в сочетании с воспалительной реакцией в мочевых путях макроорганизма. В соответствии с современными представлениями, ИМП подразделяют на группы в зависимости от условий возникновения заболеваний (внебольничные и нозокомиальные), локализации (инфекции верхних и нижних мочевых путей) и фона, на котором они развились (осложненные и неосложненные).
Пиелонефрит (острый и обострение хронического) относится к инфекциям верхних мочевых путей. Под термином «острый пиелонефрит» понимают бактериальное поражение паренхимы почек. Его не следует использовать для обозначения каких-либо тубулоинтерстициальных нефропатий, если инфекция не была документирована. Около 20 % внебольничных бактериемий у женщин обусловлены пиелонефритом.
Хронический пиелонефрит (хронический инфекционный интерстициальный нефрит) представляет собой хроническое очаговое, часто двустороннее инфекционное поражение почек, которое вызывает атрофию и деформацию чашечек с выраженным рубцеванием паренхимы. Заболевание развивается только у больных со значительными анатомическими аномалиями (например, с обструктивной уропатией или чаще — пузырно-мочеточниковым рефлюксом). Среди больных с терминальной хронической почечной недостаточностью 2–3 % случаев обусловлены хроническим пиелонефритом.
Эмпирическая терапия пиелонефрита зависит от того, где именно будет лечиться больной: амбулаторно или в стационаре. Амбулаторное лечение возможно у больных с нетяжелым острым или обострением хронического пиелонефрита при отсутствии тошноты и рвоты, признаков обезвоживания при условии соблюдения пациентом предписанного режима лечения. Антимикробный препарат целесообразно назначать внутрь. Препаратами выбора являются фторхинолоны, альтернативными средствами — бета-лактамы (защищенные аминопенициллины или пероральные цефалоспорины II–III поколения). Длительность лечения при остром пиелонефрите — 7–14 дней [1, 2]. В отсутствие улучшения в течение 48–72 ч от начала адекватной антибактериальной терапии больного необходимо обследовать на предмет наличия обструкции или абсцессов почки (ультразвуковое исследование почек или компьютерная томография). При персистировании возбудителя в конце лечения оправдано продление курса терапии на 2 недели. Вопрос о целесообразности антибактериальной терапии обострений хронического пиелонефрита до сих пор остается дискуссионным. Принято считать, что нарастание степени бактериурии, выделение диагностически значимых количеств микробов-возбудителей из мочи на фоне соответствующих клинических проявлений (лихорадка, ознобы, боли в области поясницы) являются достаточным основанием для назначения антимикробных средств. Антибиотики в подобных случаях назначаются сроком на 2–3 недели [3].
Если больной госпитализируется в стационар, антибиотики применяются парентерально. Допускается проведение ступенчатой терапии, когда вначале антибиотик вводится парентерально в течение 3–5 дней (до нормализации температуры тела), а затем лечение продолжается антибиотиком для перорального применения. Препаратами выбора являются фторхинолоны (предпочтительны те из них, которые имеют лекарственные формы для парентерального и перорального применения), альтернативными средствами — бета-лактамы (цефалоспорины III поколения или защищенные аминопенициллины) [2].
При нозокомиальных пиелонефритах и при госпитализации пациента в отделение реанимации и интенсивной терапии значительно возрастает опасность инфицирования синегнойной палочкой. Поэтому средствами выбора в терапии таких больных являются карбапенемы (имипенем, меропенем), антипсевдомонадные цефалоспорины III поколения (цефтазидим, цефоперазон), фторхинолоны. Учитывая высокую частоту бактериемии и трудно предсказуемый характер чувствительности к антибиотикам возбудителей госпитальных инфекций, обязательно следует проводить посевы мочи и крови до начала и на фоне терапии.
В современных условиях для лечения острого пиелонефрита не следует использовать аминопенициллины, цефалоспорины I поколения и нитроксолин, поскольку резистентность E.coli (основного возбудителя заболевания) к этим препаратам превышает 20 %. Не рекомендуется применение и некоторых других антибактериальных средств: тетрациклинов, хлорамфеникола, нитрофурантоина, нефторированных хинолонов (например, налидиксовой кислоты). Концентрации этих препаратов в крови или почечной ткани обычно ниже значений минимальных подавляющих концентраций основных возбудителей заболевания [3].
В этиологии неосложненного острого пиелонефрита доминирует Escherichia coli. Основным механизмом устойчивости данного микроорганизма к антибиотикам является выработка плазмидных бета-лактамаз широкого спектра действия, чувствительных к ингибиторам бета-лактамаз. Появление на фармацевтическом рынке Украины нового ингибиторозащищенного цефалоспорина III поколения — цефтриаксон/сульбактама открывает перспективы совершенствования антибактериальной терапии больных с пиелонефритом.
В настоящее время известно более 300 бета-лактамаз, и их список постоянно пополняется. Добавление ингибитора бета-лактамаз к цефтриаксону позволяет преодолевать устойчивость, вызванную бета-лактамазами расширенного спектра действия группы 2be, цефалоспориназами группы 2e и даже карбапенемазами, не содержащими ионы цинка в активном центре (группа 2f) [4]. В то же время добавление сульбактама не позволяет предотвратить разрушение цефтриаксона цефалоспориназами 1-й группы (класс С). Они, как правило, кодируются хромосомами. Однако для штаммов E.coli характерен низкий уровень продукции цефалоспориназ, который не обеспечивает устойчивость к цефалоспоринам, хотя его можно обнаружить с помощью чувствительных тестов [5].
Фармакологическая совместимость цефтриаксон/сульбактама изучалась в нескольких исследованиях, в которых было установлено отсутствие фармакокинетического взаимодействия компонентов [6, 7]. Сходные результаты были получены и в исследованиях комбинации сульбактама с другими бета-лактамными антибиотиками: цефоперазоном, ампициллином, амоксициллином, пиперациллином [8–11]. Поэтому дозирование ингибиторозащищенных бета-лактамов определяется, исходя из крат ности введения антибиотика. Если ампициллин/сульбактам применяется 4 раза в сутки, то амоксициллин/сульбактам — 3, цефоперазон/ сульбактам — 2, цефтриаксон/сульбактам — 1–2 раза.
Целью настоящего исследования стало сравнение клинической эффективности цефтриаксона и цефтриаксон/сульбактама у больных с внебольничными пиелонефритами.
Материал и методы
Диагноз пиелонефрита устанавливали при наличии не менее 3 из нижеследующих признаков:
— острое начало заболевания с температурой тела > 38 °С;
— боль в боку (в области проекции почки);
— болезненность при пальпации в костовертебральном углу;
— жажда, сухость во рту;
— тошнота, рвота;
— пиурия;
— лейкоцитоз (> 10 × 109/л) [2, с дополнениями].
Все больные обследовались по общепринятому плану. В перечень обязательных диагностических мероприятий входили: сбор жалоб и анамнеза заболевания, объективное исследование, клинико-лабораторные (определение лейкоцитоза, количества нейтрофилов, СОЭ в периферической крови, клинический анализ мочи) и инструментальные (ультразвуковое исследование почек) методы исследования. По показаниям проводились микробиологическое исследование мочи (посев, определение чувствительности потенциальных возбудителей к антибиотикам) и экскреторная урография. Предварительная оценка эффективности терапии производилась через 48–72 ч от начала лечения. В случаях снижения температуры тела до менее чем 37,5 ºС или на ≥ 1 ºС по сравнению с исходной, уменьшения симптомов интоксикации и улучшения самочувствия пациента динамика заболевания расценивалась как позитивная. При недостаточном снижении температуры тела дальнейшая тактика лечения (изменение режима или продолжение прежней антибактериальной терапии, применение уроантисептиков, симптоматических средств — спазмолитиков, антигистаминных препаратов и т.д.) оставлялась на усмотрение лечащего врача. Повторная оценка перечисленных выше симптомов и признаков производилась на 5–6-е, 9–10-е и 12–15-е сутки от начала терапии.
Эффективность лечения оценивали по следующим критериям. Если через 12–15 сут. от начала терапии клиническая симптоматика отсутствовала, а показатели клинических анализов крови и мочи возвращались к норме, результаты лечения расценивались как выздоровление (в случаях острого пиелонефрита) или купирование обострения (при обострениях хронического пиелонефрита). Сохранение жалоб или клинических симптомов в отсутствие отклонений в лабораторных показателях либо персистирование отклонений в результатах лабораторных исследований у лиц, у которых жалобы и клинические симптомы отсутствовали, расценивались как улучшение. Под клиническими неудачами понимали: 1) клиническое ухудшение на фоне лечения; 2) изменение антибактериальной терапии во время лечения в связи с появлением побочных эффектов либо в связи с неэффективностью стартовой антибактериальной терапии; 3) возникновение осложнений (абсцедирование, суперинфекция и т.д.); 4) смерть пациента.
Критериями исключения из исследования были следующие:
— возраст < 17 лет;
— анамнестические указания на аллергические реакции на цефалоспорины или ингибиторозащищенные бета-лактамы;
— наличие тяжелых сопутствующих заболеваний: выраженная хроническая почечная недостаточность, хроническая сердечная недостаточность, цирроз печени, декомпенсированный сахарный диабет, опухоли любой локализации, психические заболевания, алкоголизм, наркомания, иммунодефицитные состояния (включая терапию глюкокортикостероидами).
Больных рандомизировали (методом конвертов) в группы лечения цефтриаксон/сульбактамом (производства Mili Healthcare Ltd.) по 1,5 г 1–2 раза в сутки внутривенно или внутримышечно либо цефтриаксоном по 1,0 г 1–2 раза в сутки внутривенно или внутримышечно. Назначение других медикаментов (уроантисептики, антигистаминные препараты, нестероидные противовоспалительные средства и т.д.) оставляли на усмотрение лечащего врача.
Результаты и обсуждение
В исследовании приняли участие 30 пациентов обоих полов (5 мужчин и 25 женщин) в возрасте от 17 до 78 лет, находившиеся на стационарном лечении в урологическом отделении городской многопрофильной клинической больницы № 25 г. Харькова и соответствовавшие заранее оговоренным критериям включения/исключения. Больные случайным образом были распределены в группы лечения цефтриаксоном/сульбактамом (15 человек) и цефтриаксоном (15 человек).
В группу лечения цефтриаксон/сульбактамом вошли 4 мужчины (26,6 %) и 11 женщин (73,3 %), средний возраст больных составил 43,9 ± 21,9 года. В группу лечения цефтриаксоном вошли 1 мужчина (6,6 %) и 14 женщин (93,3 %), средний возраст — 45,2 ± 22,5 года, то есть обе группы по половым и возрастным характеристикам были сопоставимы (табл. 1).
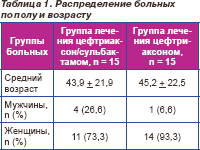
В исследование включали больных с острым пиелонефритом и обострением хронического пиелонефрита (как самостоятельное заболевание или как осложнение основного диагноза) (табл. 2).

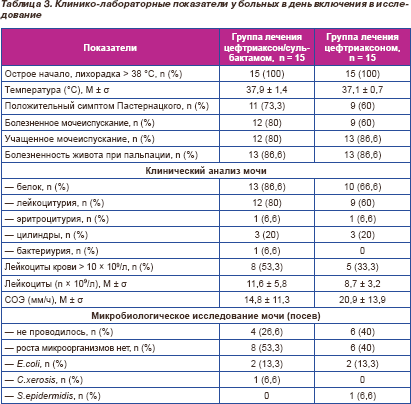
В день включения в исследование (день «0») у всех пациентов определяли основные клинические и лабораторные параметры, которые представлены в табл. 3. Приведенные данные свидетельствуют, что обе группы больных были сопоставимы по основным клинико-лабораторным показателям. У каждого третьего пациента микробиологическое исследование мочи не производилось, что, с одной стороны, объясняется нетяжелым состоянием включенных в исследование больных (в каждой из групп в день «0» состояние 8 человек (53,3 %) расценивалось как удовлетворительное, 7 (46,7 %) — как средней тяжести), с другой — низкой информативностью подобных исследований в условиях больничной микробиологической лаборатории. Из 20 микробиологических исследований мочи, выполненных в 0-й день, в 14 случаях (70 %) рост микроорганизмов отсутствовал, еще в 2 (10 %) выделены бактерии (C.xerosis и S.epidermidis ), которые не являются возбудителями пиелонефрита и, скорее всего, указывают на нарушение правил сбора, хранения, транспортировки мочи в лабораторию и/или задержку с началом собственно микробиологического исследования в самой лаборатории. Только у 4 пациентов (20 %) был выделен возбудитель пиелонефрита (E.coli ) в диагностически значимом титре.
В течение первых 48 часов всем пациентам было проведено ультразвуковое исследо вание почек. Наряду с типичной ультразвуковой картиной (цисто)пиелонефрита, были выявлены следующие находки: в группе лечения цефтриаксон/сульбактамом — аденома простаты у 2 человек (13,3 %), опущение почки (почек) — у 3 (20 %), пие лоэктазия — у 1 (6,6 %), камень в мочевом пузыре — у 1 (6,6 %), киста почки — у 1 (6,6 %), камень в почке — у 1 (6,6 %); в группе лечения цефтриаксо-ном — опущение почки (почек) у 2 человек (13,3 %), пиелоэктзия — у 1 (6,6 %), киста поч-ки — у 1 (6,6 %), камень в почке — у 1 (6,6 %).
Динамика ряда клинических и лабораторных показателей представлена на рис. 1–5.
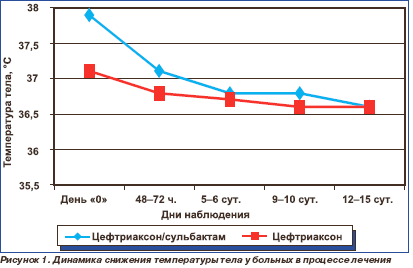
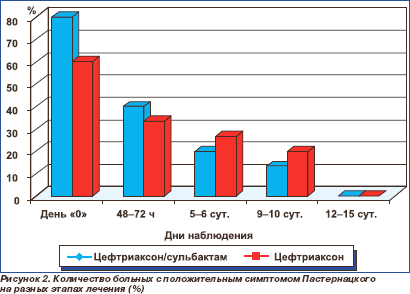
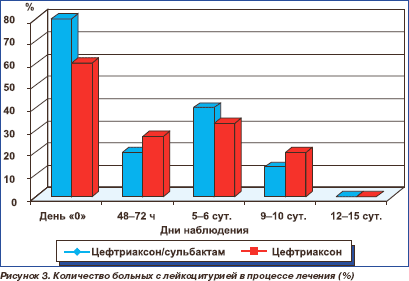
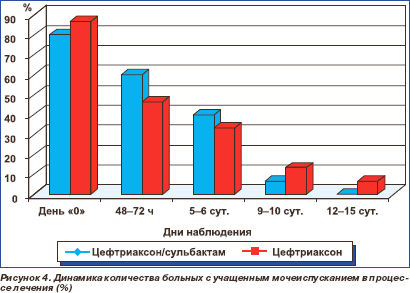
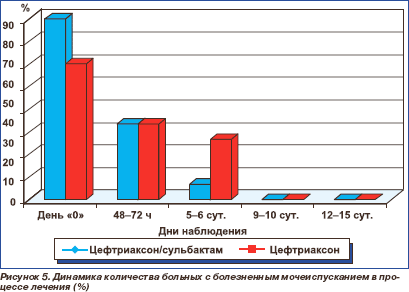
Спустя 48–72 ч от начала терапии у больных обеих групп отмечена позитивная динамика показателей клинического анализа крови. Так, в группе лечения цефтриаксон/сульбактамом число лейкоцитов снизилось с 11,6 ± 5,8 до 6,5 ± 2,7 (× 109/л), в группе лечения цефтриаксоном — с 8,7 ± 3,2 до 5,2 × 1,3 (× 109/л). В последующем анализы крови производились по мере необходимости.
Эффективность лечения больных с острым и обострением хронического пиелонефрита в условиях стационара оценивалась по приведенным выше критериям (табл. 4). Единственная клиническая неудача зарегистрирована у 1 пациента (6,7 %) из группы лечения цефтриаксоном/сульбактамом, у которого течение заболевания осложнилось присоединением нозокомиальной пневмонии. Нежелательных лекарственных явлений (побочных эффектов) за время исследования зарегистрировано не было.

Продолжительность антибактериальной терапии больных с пиелонефритами в сравниваемых группах представлена в табл. 5. Несмотря на то что в группе лечения цефтриаксон/сульбактамом антибиотик вводился в среднем почти на двое суток меньше, статистически значимых различий между сравниваемыми группами по длительности лечения антибиотиками не выявлено. Вероятными объяснениями выявленной тенденции могут быть небольшое число включенных в исследование пациентов и большее количество больных с обострениями хронического пиелонефрита в группе лечения цефтриаксоном, оптимальная длительность антибактериальной терапии которых в настоящее время точно не определена.

Выводы
1. Ингибиторозащищенный цефалоспорин III поколения — цефтриаксон/сульбактам является эффективным средством монотерапии больных с нетяжелыми внебольничными пиелонефритами (неосложненными и осложненными) в условиях стационара.
2. Цефтриаксон/сульбактам (производства Mili Healthcare Ltd.) характеризуется благоприятным профилем безопасности, сопоставимым с таковым цефтриаксона.
3. Клиническая эффективность, безопасность, удобство применения (1–2 раза в день внутривенно или внутримышечно), способность преодолевать основной механизм резистентности ключевых возбудителей внебольничных пиелонефритов (выработку бета-лактамаз) позволяют рекомендовать цефтриаксон/сульбактам в качестве препарата выбора для лечения больных с нетяжелыми внебольничными пиелонефритами (неосложненными и осложненными) в условиях стационара.
4. Выявлена тенденция к сокращению сроков антибактериальной терапии больных с нетяжелыми внебольничными пиелонефритами при использовании цефтриаксон/сульбактама по сравнению с цефтриаксоном (p < 0,1). Данное наблюдение нуждается в подтверждении в ходе последующих исследований.
1. Лоран О.Б., Рафальский В.В., Шевелев А.Н. Инфекции мочевыводящих путей // Практическое руководство по антиинфекционной терапии / Л.С. Страчунский, Ю.Б. Белоусов, С.Н. Козлов. — Смоленск: МАКМАХ, 2007. — С. 285-9.
2. Naber K.G., Bishop M.C., Bjerklund-Johansen T.E. et al. Guidelines on the management of urinary and male genital tract infections. — European Association of Urology, 2006.
3. Березняков И.Г. Инфекции и антибиотики. — Харьков: Константа, 2004.
4. Эйдельштейн М.В. β-лактамазы аэробных грамотрицательных бактерий: характеристика, основные принципы классификации, современные методы выявления и типирования // Клин. микробиол. антимикроб. химиотер. — 2001. — № 3 (3). — С. 223-42.
5. Livermore D.M. β-Lactamases in laboratory and clinical resistance // Clin. Microbiol. Rev. — 1995. — № 8. — Р. 557-84.
6. Fantin B., Pangon B., Potel G., Caron F., Vallee E., Vallois J.-M. et al. Activity of sulbactam in combination with ceftriaxone in vitro and in experimental endocarditis caused by Escherichia coli producing SHV-2-like β-lactamase // Antimicrob. Agents Chemother. — 1990. —№ 34 (4). — Р. 581-6.
7. Caron F., Gutmann L., Bure A., Pangon B., Vallois J.-M., Pechinot A. et al. Ceftriaxone-sulbactam combination in rabbit endocarditis caused by a strain of Klebsiella pneumoniae producing extended-broad-spectrum TEM-3 β-lactamase // Antimicrob. A gents Chemother. — 1990. — № 34 (11). — Р. 2070-4.
8. Bauernfeind A. Perspectives of beta-lactamases inhibitors in therapy of infections caused by Escherichia coli or Klebsiella with plasmidic resistance to third generation cephalosporins // Infection. — 1990. — № 18 (1). — Р. 48-52.
9. Alexov M., Lister P.D., Sanders C.C. Efficacy of ampicillin-sulbactam is not dependent upon maintenance of a critical ratio between components: sulbactam pharmacokinetics in pharmacodynamic interactions // Antimicrob. Agents Chemother. — 1996. — № 40 (11). — Р. 2468-77.
10. Bantar C., Nicola F., Arenoso H.J., Galas M., Soria L., Dana D. et al. Pharmacokinetics and pharmacodynamics of amoxicillin-sulbactam, a novel aminopenicillin- b -lactamase inhibitor combination, against Escherichia coli // Antimicrob. Agents Chemother. — 1999. — № 43 (6). — Р. 1503-4.
11. Lister P.D., Prevan A.M., Sanders C.C. Importance of beta-lactamase inhibitor pharmacokinetics in the pharmacodynamics of inhibitor-drug combinations: studies with piperacillin-tazobactam and piperacillin-sulbactam // Antimicrob. Agents Chemother. — 1997. —№ 41 (4). — Р. 721-7.
