Газета «Новости медицины и фармации» Неврология (469) 2013 (тематический номер)
Вернуться к номеру
Рассеянный склероз: современный взгляд на старую проблему
Авторы: Каменова С.У., д.м.н., - профессор, завкафедрой неврологии, КазНМУ им. С.Д. Асфендиярова, Институт последипломного образования, Республика Казахстан
Разделы: Справочник специалиста
Версия для печати
Рассеянный склероз (РС) — одно из распространенных заболеваний центральной нервной системы, поражающее преимущественно лиц молодого трудоспособного возраста, имеющее прогрессирующее течение и неизбежно приводящее к инвалидности. Без надлежащего лечения РС может привести к смертельному исходу.
История развития знаний о РС насчитывает около двух столетий. Особое медикосоциальное значение РС обусловливает огромный интерес к его изучению. Впервые эта болезнь была описана в 1830 году Крювелье и Карсвеллом, которые выделили ее в самостоятельную нозологическую форму, описали классическую клиническую картину и патоморфологические изменения. Затем в 1868 году ЖанМартен Шарко, профессор неврологии университета в Париже, изучил наиболее часто встречающиеся симптомы РС, включая скандированную речь и аномальные движения глаз, мозжечковую атаксию, и сравнил их с другими неврологическими заболеваниями. Он описал характерные «бляшки» в головном мозге при вскрытии умерших больных с подобными заболеваниями.
Развитие и внедрение в медицину патологоанатомических, гистологических методик, микроскопии, различных способов окраски срезов тканей приводит к углублению представлений о сути неврологических заболеваний. Так, в 1878 году Луи Ранвье впервые обнаружил миелин, описал такую его функцию, как охват и защита нервов, и тем самым доказал участие миелиновой оболочки в проведении импульса между мозгом и остальными частями тела. В этот же период сформировались представления о демиелинизации.
В 1916 году доктор Джеймс Доусон в Эдинбургском университете выполнил детальные микроскопические исследования мозга больных, которые умерли от РС, и описал воспаление вокруг сосудов, приводящее к повреждению миелиновых оболочек. Важным вкладом в изучение проблемы является разработка критериев диагностики РС европейской экспертной комиссией в 1965 году. В 1969–1970 гг. обоснована роль адренокортикотропного гормона (АКТГ) в лечении обострений РС, при этом были использованы новые стандартизированные диагностические критерии и оценочные шкалы для оценки эффективности лечения.
В 1981 году впервые использован метод магнитнорезонансной томографии (МРТ) для изучения РС, что привело к революции в его диагностике. Характерные для этого заболевания изменения в головном и спинном мозге регистрируются с помощью МРТ у более чем 90 % пациентов с предположительным диагнозом РС.
Достижением современной неврологии в области РС явилось создание и применение лекарственных препаратов, тормозящих повреждающее воздействие иммунной системы на ткани головного и спинного мозга. В 1993 году бетаинтерферон1b утвержден в качестве препарата первого ряда для лечения РС.
Несмотря на многолетнюю историю изучения РС, это заболевание является одной из современных проблем клинической неврологии. Хорошо известно, что движение науки вперед обеспечивают новые идеи и методы. Так, обзор современных научных исследований, проведенных в мире, показывает, что к настоящему времени исследователи этиологии РС условно выделяют три направления поиска этиологических факторов: изучение наследственной предрасположенности и генетических факторов; изучение влияния внешних факторов, среди которых особое место занимают инфекционные агенты; исследование участия географических и климатических факторов риска, свидетельствующих о различных уровнях заболеваемости РС в различных регионах планеты [1–3].
Специалисты по вопросам генетической предрасположенности к РС предполагают, что генетические факторы могут проявляться под влиянием внешних воздействий и определять течение заболевания, но не являются обязательным условием развития РС у человека, т.е. наследственной болезнью [4, 5]. Многие эпидемиологические исследования подтверждают большую частоту случаев развития болезни в последующих поколениях, при этом предрасположенность к РС выше у женщин, чем у мужчин [5, 6].
В поисках причин развития демиелинизирующих процессов многие исследователи признавали ведущую роль иммунопатологических реакций организма человека. Было установлено, что наблюдаемая в эксперименте демиелинизация нервных корешков является следствием иммунных процессов и имеет сходную картину с РС у человека. Исследователи большинства стран мира пытались найти связь заболевания с вирусными и бактериальными инфекциями, воздействием экзотоксинов или травм головного мозга. Большое количество исследований было посвящено выяснению механизмов развития и течения РС, исследованию различных сторон обмена веществ у длительно болеющих этим заболеванием.
В настоящее время доказано, что при обострении РС повышается активность гидролитических ферментов, участвующих в деструкции миелина, повышается содержание холестерина, отмечено нарушение водносолевого баланса, углеводного обмена. Однако полученные данные пока не позволяют говорить об установлении четкой зависимости расстройств обмена от стадии заболевания и причинах, ведущих к обострениям или ремиссиям, и требуют дальнейших исследований.
Стремление ученых ряда стран подойти к решению вопроса об инфекционной причине РС методами эпидемиологических обследований позволило создать достаточно подробную картину географической распространенности болезни, согласно которой распространенность РС растет во многих странах мира, что связано не только с удлинением жизни больных, но и с истинным увеличением заболеваемости.
Так, распространенность РС в России составляет в среднем 25–40 случаев на 100 тыс. населения, и отмечается некоторый рост заболеваемости среди лиц молодого и среднего возраста, что связывают с улучшением средств ранней диагностики [7, 8]. На севере Европы частота РС составляет 140–150 случаев на 100 тыс. населения, в то время как в центре Европы эти показатели составляют 26,5–30,1 на 100 тыс. населения, в Японии, по материалам этих же авторов, заболевание встречается в 8–10 случаях на 100 тыс. населения [9, 10].
В последние годы в разных странах мира активно проводятся эпидемиологические и генетические исследования, позволяющие выявить факторы, определяющие повышенную предрасположенность к РС и особенности его клинического течения, а также разрабатываются новые подходы к лечению этого высокоинвалидизирующего заболевания.
РС — это непредсказуемое заболевание центральной нервной системы, клинические проявления могут варьировать от относительно легких до значительных. Особенностью РС является одновременное поражение нескольких отделов нервной системы, что приводит к появлению разнообразной неврологической симптоматики. Большинство людей испытывают свои первые симптомы в возрасте от 20 до 40 лет, начальные симптомы РС зачастую размыты, часто это или двоение в глазах, или искажения в восприятии цветовых образов, или даже слепота на один глаз.
Чаще всего у больных с РС самыми первыми признаками являются преходящие патологические сенсорные проявления в виде парестезии, онемения, покалывания, ощущения «иголки» или «прохождение электрического тока» в конечностях или по ходу позвоночника. Наиболее частыми жалобами у больных с РС являются нарушение речи, тремор, головокружение. Примерно у половины пациентов с РС выявляются когнитивные нарушения, такие как трудности концентрации внимания, памяти и недальновидность, но такие симптомы, как правило, упускаются из виду. Очень часто одним из проявлений РС является депрессия.
Многие больные с РС жалуются на мышечную слабость в конечностях и нарушение координации. Эти симптомы могут быть достаточно серьезными, нарушается походка, иногда даже устойчивость в вертикальном положении. В худшем случае РС может привести к частичному или полному параличу.
В связи с тем, что обычно РС начинается моносимптомно, диагностика значительно затруднена. После первой атаки часто наступает длительная ремиссия, поэтому диагноз в большинстве случаев ставится ретроспективно, когда возникает обострение с развернутой картиной многоочагового поражения нервной системы. Большинство больных, имея одну атаку, протекающую под маской другого заболевания, длительно находятся на лечении у разных специалистов.
Наиболее трудным является дифференциальный диагноз РС с одноочаговыми поражениями нервной системы, при которых возникают множественные и разнообразные симптомы. К числу одноочаговых многосимптомных поражений, с которыми приходится дифференцировать РС, относятся опухоли головного мозга, в первую очередь ствола головного мозга, опухоли спинного мозга, ограниченные церебральные и спинальные арахноидиты, краниовертебральные аномалии, нарушения кровообращения, особенно хронические, в головном и спинном мозге, гранулемы базальной и спинальной локализации [11].
Главным отличием РС от этих заболеваний является многоочаговость процесса, кроме того, каждое из этих заболеваний имеет признаки, не встречающиеся при РС. Так, при РС не бывает синдрома внутричерепной гипертензии, в отличие от опухолей. В случаях РС компьютерная томография (КТ) или МРТ выявляет лишь признаки гидроцефалии и единичные очаги пониженной плотности без перифокального отека и дислокации мозга [11,12].
РС отличает от ограниченных церебральных и спинальных арахноидитов отсутствие признаков внутричерепной гипертензии и воспалительных изменений ликвора, признаков поражения корешков черепных и спинальных нервов, деформации соответствующих ликворных пространств на МРТ [11]. При РС отсутствуют аномалии развития костей краниовертебрального стыка и позвоночника, как правило, сопутствующие врожденным аномалиям ствола мозга, мозжечка и спинного мозга.
Множественные симптомы РС обычно не удается уложить в какойлибо стволовой или спинальный сосудистый бассейн, что позволяет дифференцировать РС и сосудистые поражения; при РС отсутствуют признаки системного поражения сосудов [11,12].
Отсутствие воспалительных изменений крови и ликвора в ряде случаев, а также серологические и иммунологические исследования позволяют дифференцировать РС и инфекционные гранулемы.
Среди многоочаговых поражений нервной системы, с которыми приходится дифференцировать РС, следует указать, в первую очередь, воспалительные заболевания нервной системы:
— острый рассеянный энцефаломиелит;
— оптикомиелит Девике;
— острые энцефаломиелиты при общих инфекциях;
— параинфекционные и поствакцинальные энцефаломиелиты.
РС отличают от острого рассеянного энцефаломиелита отсутствие признаков острой вирусной инфекции, менее острое начало, хроническое прогрессирующее течение, отсутствие общеинфекционных симптомов и признаков поражения вещества головного и спинного мозга [13]. Многоочаговое поражение нервной системы при системных васкулитах, как первичных (гигантоклеточный артериит, узелковый полиартериит, гранулематоз Вегенера), так и вторичных (ревматизм, системная красная волчанка, сифилис и др.), отличается от РС наличием системного поражения сосудов (т.е. сочетанного поражения сосудов нервной системы, внутренних органов и периферических сосудов).
Заболевания, сходные с РС по клиническим критериям, но имеющие четкие отличия на МРТ:
— гранулематоз Вегенера;
— болезнь Уиппла;
— мальформация Арнольда — Киари;
— изолированные синдромы поражения спинного мозга;
— экстра и интрамедуллярные компрессионные поражения;
— дефицит витамина В12;
— внутричерепное новообразование.
При проведении дифференциальной диагностики с заболеваниями, сходными с РС по клиническим и МРТкритериям, очень часто для подтверждения диагноза необходимы соответствующие исследования:
— СПИД — антитела к ВИЧ в сыворотке;
— протромботические состояния — экстракраниальная допплерография и эхокардиография, коагулограмма;
— спиноцеребеллярные дегенерации — клиническое течение и отсутствие изменений других лабораторных тестов;
— церебральная аутосомнодоминантная артериопатия с субкортикальными инфарктами и лейкоэнцефалопатией — клиническое течение, анализ генетического сцепления, артериопатические проявления.
Наиболее сложно дифференцировать РС с заболеваниями, сходными по всем трем критериям — клиническим, МРТ и ликворным, где необходимы дополнительные методы исследования и тщательное наблюдение за динамикой клинических проявлений [11,13]:
— васкулиты — синдром Шегрена, узелковый полиартериит, системная красная волчанка (при необходимости проводят церебральную ангиографию, определение антикардиолипиновых антител, антинуклеарного фактора и т.д.);
— болезнь Бехчета — клинические проявления, кожнослизистые изъязвления;
— нейроборрелиоз — определение антител к Borrelia burgdorferi в сыворотке и ликворе;
саркоидоз — тест Квейма, биопсия любого доступного очага;
— адренолейкодистрофия — определение длинноцепочечных жирных кислот;
— зрительная атрофия Лебера — анализ митохондриальной ДНК;
— острый диссеминированный энцефаломиелит — повторная МРТ, клиническое течение.
Таким образом, в связи со сложностью клинической диагностики РС только комплексный подход с использованием современных методов обследования позволит проводить раннюю диагностику, адекватное лечение, соблюдение режима, необходимого для пациента с данным заболеванием, чтобы предупредить прогрессирование процесса и ухудшение состояния больного.
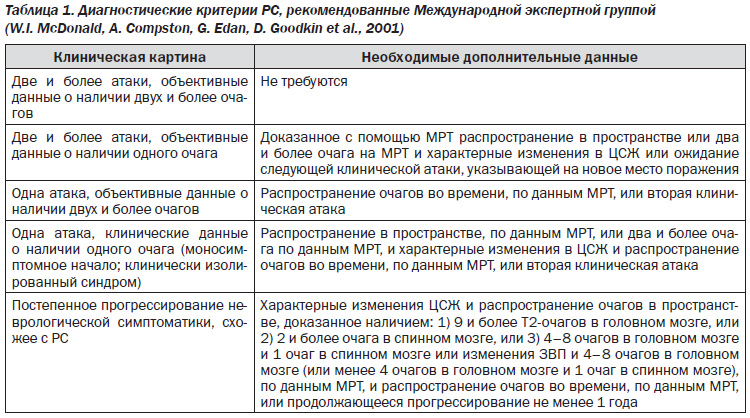
Международная экспертная группа, созданная в Лондоне в июле 2000 г. при поддержке Национального общества РС (США) и Международной Федерации обществ РС, разработала диагностические критерии РС (табл. 1).
Изменения диагностических критериев приняты с учетом особой роли магнитнорезонансной томографии (МРТ) в подтверждении диагноза РС, решения главной задачи — выявления очагов демиелинизации во времени и в пространстве, а также с целью облегчить постановку диагноза у больных с различным началом заболевания, включая «моносимптоматический» вариант, типичный ремиттирующий и постепенно прогрессирующий.
Критерии предназначены главным образом практическим врачам, поэтому желательно их иметь под рукой. Основным положением является доказательство распространения очагов во времени и пространстве. Здесь указана важность параклинических исследований, особенно МРТ. Однако диагностика РС остается отчасти объективным и отчасти субъективным процессом. Диагноз может быть выставлен специалистом, хорошо знающим это заболевание, дифференциальную диагностику и способным интерпретировать параклинические методы исследования.
Кроме того, до недавнего времени имели место только две категории диагноза РС — «достоверный» и «вероятный». После принятия новых критериев стало возможным использование таких терминов, как «возможный РС» (когда риск РС достаточно высок, а имеющихся клинических данных недостаточно) или «не РС».
Среди итогов обсуждения необходимо выделить следующие:
1. Важность подтверждения распространения очагов демиелинизации в пространстве и во времени для правильной постановки диагноза, особенно когда клинических данных недостаточно.
2. Клиническая картина определяется прежде всего клинической симптоматикой. Анамнестические сведения могут вызвать подозрение о возможном заболевании, но их недостаточно для верной постановки диагноза. Диагноз РС может быть выставлен только в случае, когда удается выявить очаги демиелинизации, разделенные в пространстве и во времени.
3. Радиологические и лабораторные исследования, включая МРТ, анализ цереброспинальной жидкости (ЦСЖ) и зрительные вызванные потенциалы (ЗВП) являются дополнительными методами, но могут быть и основными при недостаточности одной лишь клинической симптоматики. Перечисленные исследования имеют различную информативность, определенные границы чувствительности и специфичности. МРТ является наиболее информативным из указанных методов. Исследование ЦСЖ дает информацию о воспалительных и иммунологических нарушениях, что важно в тех случаях, когда клиническая картина атипична, а МРТкритерии неполные. Проведение исследования ЗВП особенно ценно в случаях, когда изменения на МРТ носят сочетанный характер (например, у больных с первичнопрогрессирующей формой РС в сочетании с прогрессирующей миелопатией) или патология на МРТ не является специфичной (например, у пожилых пациентов с факторами риска ишемической болезни). В других случаях исследование ЗВП диагностически менее значимо.
4. В дебюте РС, когда еще недостаточно необходимых критериев, принимают формулировку «возможный РС». Использование таких субкатегорий, как «клинически достоверный», «лабораторно подтвержденный» РС, нежелательно.
Международная экспертная группа, просмотрев формулировки терминов в прежней диагностической схеме, предложила свое понимание следующих определений.
Что называть атакой? Атака (экзацербация, обострение) определяется как эпизод появления неврологической симптоматики и при клиническом исследовании соответствует очагам воспаления и демиелинизации. Длительность обострения — не менее 24 часов. Меньший по времени промежуток расценивается как псевдоатака и может быть вызван повышением температуры тела или инфекцией. Единичный пароксизмальный эпизод не должен расцениваться как обострение, а вот множество отмеченных эпизодов с длительностью не менее 24 часов требует тщательного обследования.
Каков промежуток между атаками? Интервал между обострениями (т.е. время с момента восстановления после 1го обострения до начала 2го (Poser С.М. et al., 1983)) должен составлять 30 дней.
Что соответствует патологии при параклиническом тестировании? Определяющим при МРТисследовании является выявление очагов демиелинизации, разделенных во времени и в пространстве.
МРТкритерии распространения очагов во времени:
1. Если МРтомография проведена через 3 и более месяца от начала проявления клинической симптоматики, то наличия на данной томограмме очага, накапливающего парамагнитный контраст, достаточно для подтверждения распространения во времени, если этот очаг расположен в месте, связанном с предшествующим появлением клинических симптомов. Если такого очага нет, необходимо дальнейшее наблюдение с повторным обследованием, желательно через три месяца. Выявления на новой МРтомограмме очага, накапливающего контраст, или новых очагов, гиперинтенсивных на Т2изображениях, достаточно для подтверждения распространения очагов во времени.
2. Если МРтомография проведена в сроки менее чем три месяца от начала проявления клинической симптоматики, необходимо повторное исследование через три и более месяца. Если на второй МРтомограмме выявлен очаг, накапливающий парамагнитный контраст, то этого достаточно для подтверждения распространения во времени. Если на второй МРтомограмме нет таких очагов, то необходимо еще одно МРТисследование не раньше, чем через три месяца от первого, при этом выявление на этой МРтомограмме новых гиперинтенсивных очагов или очага, накапливающего контраст, является достаточным для подтверждения распространения во времени.
МРТкритерии распространения очагов в пространстве (Barkhof F. et al., 1997, Tintore М. et al., 2000)
1. Один очаг, контрастированный гадолинием, или девять Т2 гиперинтенсивных очагов (если очага, контрастированного гадолинием, нет).
2. Не менее одного инфратенториального очага.
3. Не менее одного юкстакортикального очага.
4. Не менее трех перивентрикулярных очагов.
Примечания: 1) очаги в поперечнике должны быть более 3 мм; 2) один очаг в спинном мозге может быть приравнен к очагу в головном мозге.
Для диагностики РС необходимо наличие 3 признаков из 4. Известно, что диагностическая роль очагов в спинном мозге недостаточно определена, хотя характеристики и распространение спинальных очагов при РС описаны в литературе. Установлено отсутствие таких очагов в контрольных группах и даже у пожилых лиц. В случаях, когда на Т2изображениях обнаруживаются гиперинтенсивные очаги размерами не менее 3 мм на протяженности двух сегментов, диагноз сомнений не вызывает. При клинически изолированном синдроме или медленно прогрессирующей форме выявление очагов демиелинизации в спинном мозге может служить дополнением к МРтомограммам головного мозга. Обнаружение 2 и более спинальных очагов, точно разделенных в пространстве и времени, при отсутствии очагов в головном мозге пока не считают соответствием принятым критериям.
Исследование ЦСЖ. Изменения в ЦСЖ подтверждают иммуновоспалительную природу РС, особенно в случаях недостаточности МРТкритериев или их специфичности (например, у пожилых пациентов) и при атипичной клинической картине. Правда, анализ ЦСЖ не может подтвердить распространение очагов в пространстве и времени. С диагностической целью используют метод изоэлектрического фокусирования ликвора, при котором определяют концентрацию в нем IgG, а затем соотносят результат с концентрацией IgG в сыворотке периферической крови. Лимфоцитарный плеоцитоз при этом должен быть менее чем 50/мм3. Характерным для РС является повышение индекса IgG. Известно, что качество проводимого исследования ЦСЖ различно среди лабораторий разных регионов и стран. В этом случае практический врач становится зависимым от технологических возможностей конкретного учреждения. А ненадежность при проведении этого исследования может привести к постановке неверного диагноза.
Исследование ЗВП. Для РС типично значительное увеличение латентности Р100, что позволяет получить дополнительную информацию при клиническом обследовании, особенно если очаги расположены в проекции зрительных путей. Как и при МРТ, и при исследовании ЦСЖ, необходима корректная интерпретация полученных данных.
Международная экспертная группа по РС подтверждает необходимость доказательства распространения (диссеминации) клинических эпизодов и очагов в пространстве и времени, подчеркивает этот основной критерий в предложенной диагностической схеме. Требование объективных данных об атаке или прогрессировании заболевания (единичные симптомы не учитываются) четко сформулировано; по мнению экспертной группы, клинические проявления РС являются основой при проведении лечения.
Предполагается, что в большинстве случаев у клиницистов будет возможность использовать методы, требующиеся при постановке диагноза. Однако в некоторых странах применение таких исследований, как МРТ, ограничено и нет даже возможностей использовать альтернативные методы (исследование ЗВП и ЦСЖ). В таких случаях разрешена формулировка диагноза «возможный РС». В последующем фиксируют не менее двух атак с клинически подтвержденными ограниченными очагами.
Кроме этого, специфичность и точность указанных выше параклинических методов различна. Экспертная группа утвердила наиболее высокотехнологичные исследования для своей схемы, но здесь возникает новая проблема. Например, при проведении МРТ с целью визуализации диссеминации очагов необходима точная установка ориентиров при регистрации, а это не всегда удается выполнить. В такой ситуации врач не может быть уверен в качестве и надежности полученной информации. И поэтому в крайних случаях основанием для диагноза остается клиническая симптоматика.
В большинстве случаев рекомендации экспертной группы позволяют поставить диагноз РС. При этом важно отметить, что предложенные критерии применимы для категории больных с типичными признаками РС и чей возраст ограничен 10–59 годами (наиболее подверженная заболеванию возрастная группа). Особое внимание стоит обратить на то, что у пациентов, чей возраст выходит за эти границы (моложе и старше), начало РС может быть атипичным (например, нарастающая деменция, эпилепсия или афазия). У таких пациентов дополнительные исследования (ЗВП и анализ ЦСЖ) оказываются более информативными, чем в типичных случаях. При постановке диагноза таким больным не требуется строгое следование критериям.
Некоторые заболевания и синдромы требуют проведения дифференциальной диагностики с РС. К ним относят случаи мультифокальной ишемии или инфаркта у молодых пациентов с такими заболеваниями, как антифосфолипидный синдром, системная красная волчанка, болезнь Такаясу, менинговаскулярный сифилис и даже каротидная диссекция. Различные инфекции, такие как HTLV1 и болезнь Лайма, могут дебютировать как РС. Паранеопластическая мозжечковая атаксия у пациентов молодого возраста может вызвать определенные сложности при дифференциальной диагностике, так как при этом заболевании часто выявляют повышенный уровень IgG в ЦСЖ. Монофазные демиелинизирующие заболевания (острый рассеянный энцефаломиелит, оптический нейромиелит), а также заболевания, генетически обусловленные нарушениями синтеза миелина (лейкодистрофии у детей и подростков), могут протекать по типу РС.
В последние годы отмечается неуклонная тенденция к росту заболеваемости РС и омоложению контингента больных в Республике Казахстан. Среди 192 больных с РС, находящихся на диспансерном учете в городских поликлиниках Алматы, 72,5 % составляют женщины и 38,3 % — лица молодого возраста до 30 лет, 81,7 % больных имеют различные группы инвалидности. Средняя длительность заболевания составляет от 5 до 20 лет, средний возраст больных 34,1 ± 3,5 года.
Несмотря на принимаемые меры, в организации помощи больным РС остается много нерешенных проблем. В нашей стране в недостаточном объеме ведутся научные исследования по демиелинизирующим заболеваниям, в том числе по эпидемиологии, с использованием отечественных приоритетов гетерогенности патологических процессов и мультифакторности их патогенеза.
Современная организация медицинской помощи невозможна без описательных эпидемиологических исследований, позволяющих оценить потребность в том или ином виде медицинской помощи и ее эффективность, сравнить различные регионы и временные периоды.
Работа государственных органов здравоохранения по всем вопросам данной проблемы существенно отстает от европейского и мирового уровня.
Отсутствуют мероприятия по ранней диагностике РС, его эффективному лечению, медицинской, социальной, профессиональной реабилитации и трудоустройству больных с РС, финансовой и социальной поддержке больных с РС и членов их семей.
Не разработано поэтапное и непрерывное обслуживание больных на амбулаторном и госпитальном этапах с целью продления ремиссий заболевания.
Не внедряются в плановом порядке новые способы медицинской реабилитации, современные приемы социальной адаптации, бытовой и общественно полезной независимости лиц с РС и членов их семей.
Неврологи и врачи других специальностей большинства городских поликлиник недостаточно информированы о современных возможностях диагностики и дифференциальной диагностики и лечения РС, об эффективных методиках профилактики и лечения осложнений заболевания, тогда как консультативная и лечебная помощь в клиниках для большинства пациентов оказывается недоступной.
Отсутствует преемственность между амбулаторным и стационарным звеном медицинской помощи, что обусловливает, с одной стороны, отсутствие адекватной терапии на догоспитальном этапе, а с другой — часто неоправданную госпитализацию больных.
Список литературы находится в редакции