Газета «Новости медицины и фармации» 15 (466) 2013
Вернуться к номеру
Особенности вакцинации детей, страдающих аллергическими заболеваниями
Авторы: Зайков С.В., д.м.н., профессор, Катилов А.В., к.м.н., Кириченко Л.Н., к.м.н. - Винницкий национальный медицинский университет им. Н.И. Пирогова
Рубрики: Семейная медицина/Терапия, Аллергология , Педиатрия/Неонатология, Иммунология
Разделы: Справочник специалиста
Версия для печати

Традиционно к наиболее актуальным проблемам медицины относится повышение эффективности иммунопрофилактики инфекционных болезней. Эпидемиологической безопасности в отношении инфекций, контролируемых средствами специфической профилактики, можно достичь только благодаря высоким показателям (не меньше 95 %) охвата населения профилактическими прививками и наличию адекватного иммунного ответа у 90 % вакцинированных. Эффективность вакцинации зависит от качества иммунобиологических препаратов, научно обоснованных схем иммунизации и состояния иммунной системы организма на момент проведения прививки, которая имеет особенности у лиц с аллергическими заболеваниями (АЗ). Вакцинация детей с аллергопатологией до сих пор остается предметом дискуссий как среди медицинских работников, так и среди населения. Неблагополучная эпидемиологическая ситуация по инфекционным заболеваниям в нашей стране, с одной стороны, диктует необходимость максимально полного охвата профилактическими прививками детского контингента, а у детей с атопией часто отмечаются признаки вторичной иммунной недостаточности. С другой стороны, высокая распространенность (10–35 % детского населения) АЗ и боязнь обострений аллергического процесса и возникновения тяжелых аллергических реакций часто приводят к отводам детей от прививок со стороны врачей и родителей, что не всегда обосновано. В связи с этим в рамках данной публикации мы остановимся на вопросах влияния вакцинации на течение АЗ, клиники и диагностики поствакцинальных аллергических осложнений, а также тактики вакцинации детей с АЗ.
По целому ряду причин у части детей компоненты вакцины могут стать причиной возникновения аллергических реакций. Так, некоторые вирусы, например вирус гриппа А, увеличивает выделение гистамина при попадании в организм привитого причиннозначимых для него аллергенов (пыльца растений, домашняя пыль, перхоть животных и др.), что может провоцировать обострение АЗ. Компонентами ряда вакцин, которые могут вызвать развитие аллергических реакций, являются антигены самих вакцин, протеины животного происхождения (белки куриных яиц), антибиотики (неомицин, канамицин), консерванты (формальдегид, тимеросал), стабилизаторы (желатин). Гидроокись алюминия относится к числу наиболее часто используемых при изготовлении вакцин адсорбентов и может стать депо для антигенов и усилить адъювантный эффект. С другой стороны, гидроокись алюминия сама является потенциальным аллергеном. Иногда наличие в вакцинах чужеродного белка (яичный альбумин, бычий сывороточный альбумин и пр.) может оказать сенсибилизирующее действие на организм ребенка, которое впоследствии клинически проявляется при введении этого белка с пищей. Исследованиями последних лет установлено, что возникающие в организме детей с АЗ изменения на фоне вакцинации, как правило, кратковременны, не ухудшают в дальнейшем течение основного процесса и не служат основанием для прекращения вакцинации. Имеются данные, что у детей, больных атопическим дерматитом с ремиссией заболевания три месяца и более, поствакцинальный период не отличается от такового у здоровых. Например, на фоне введения АДСанатоксина в крови у этих детей отмечаются умеренное снижение Тлимфоцитов, эозинофилия, повышение уровня циркулирующих иммунных комплексов, увеличение в 3–5 раз по сравнению с исходным уровня общего IgE, но без повышения уровня аллергенспецифических IgE. При этом в 10–20 % случаев развивается кратковременное обострение АЗ, не приводящее к ухудшению течения заболевания в дальнейшем.
В материалах масштабного исследования ISSAC (International Study of Asthma and Allergies in Childhood) в 2001 г. были опубликованы данные об отсутствии существенного влияния иммунизации вакцинами БЦЖ, а также против кори и коклюша на организм ребенка с АЗ. В литературе также обсуждаются вопросы эффективности и безопасности вакцинации от гриппа детей с бронхиальной астмой (БА). Так, в двух из трех групповых исследований было зафиксировано увеличение числа обострений БА у детей, вакцинированных от гриппа, но поскольку включение в группы не было рандомизировано, то эти исследования не могут считаться корректными. При ретроспективном анализе результатов исследования большой группы детей с БА P. Kramarz et al. (2000) не выявили доказательств увеличения числа ее обострений при контроле тяжести заболевания в период от 2 дней до 2 недель после прививки от гриппа. Наиболее обнадеживающие результаты были получены при рандомизированном двойном слепом плацебоперекрестном исследовании группы из 2032 пациентов, больных БА. При этом было выявлено крайне незначительное увеличение риска обострений в период между 3м и 14м днями после прививки от гриппа (абсолютная разница 1,1 %; 95% ДИ 1,4–3,6). Других побочных эффектов вследствие вакцинации пациентов с БА не отмечено. Окончательно результаты об отсутствии прямого влияния вакцинации против гриппа на увеличение частоты обострения БА нашли отражение в Кохрановском обзоре, выполненном C.J. Cates et al. (2008). Таким образом, у грудных детей и подростков не выявлено причинной связи между иммунизацией противовирусными вакцинами и развитием БА или атопии. Хотя исследования продемонстрировали безопасность противогриппозной вакцины для детей с БА, работы по изучению эффективности вакцинации при этом заболевании выполняются и в настоящее время. С целью снижения заболеваемости ОРВИ у детей с БА перспективной может быть вакцина против риновируса. К сожалению, изза наличия его многочисленных серотипов и нехватки доминирующего сезонного серотипа возможность получения эффективной вакцины против риновируса в ближайшее время далека от реальности. Такая вакцина могла бы потенциально снизить количество обострений БА, уменьшить стоимость лечения и улучшить качество жизни больных детей.
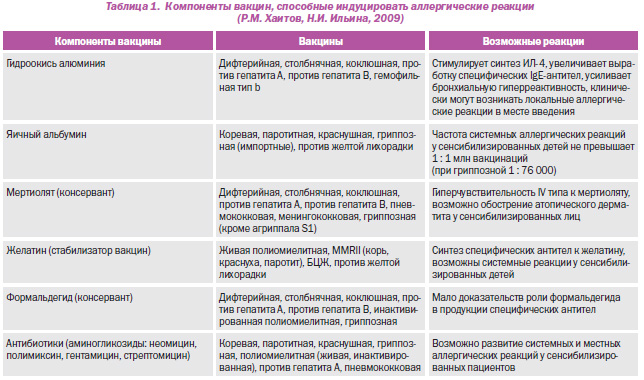
Существующее мнение о том, что вакцины могут сенсибилизировать организм детей, правомерно лишь в отношении некоторых содержащихся в них субстанций. Усовершенствованный процесс производства вакцин освобождает их в большей степени от балластных веществ, вследствие чего все включенные в Национальный календарь прививок вакцины содержат намного меньше потенциальных аллергенов, чем было ранее. Как живые, так и инактивированные вакцины практически не стимулируют стойкое повышение уровня IgE и продукцию специфических IgEантител, а также повышенное высвобождение гистамина. Кроме того, в условиях отсутствия широкой циркуляции возбудителей инфекционных заболеваний, постоянного контакта детей с патогенными микроорганизмами вакцины заменяют их и являются как бы «воспитателями» иммунной системы, так как переключают иммунные реакции с аллергического Th2типа иммунного ответа на инфекционный Th1тип, что позволяет сформировать противоинфекционную защиту организма ребенка. Следовательно, аллергия на компоненты вакцин возникает лишь у отдельных детей, страдающих АЗ. Чаще это бывает у детей, сенсибилизированных к аминогликозидам, белку куриного яйца, желатину, алюминию, пекарским дрожжам. Эти субстанции способны вызывать у сенсибилизированных лиц аллергические реакции немедленного типа. Перечень компонентов вакцин, способных индуцировать нежелательные реакции у вакцинированных детей (Р.М. Хаитов, Н.И. Ильина, 2009), приведен в табл. 1.
Этапы формирования иммунного ответа на вакцины включают в себя:
активацию антигенпрезентирующих клеток (дендритные клетки, макрофаги, Влимфоциты); 1)
дифференцировку наивных Тклеток в Th1, Th2, Treлимфоциты, специфичные к различным эпитопам вакцины; 2)
3) презентацию дендритными клетками и макрофагами антигена Влимфоцитам в фолликулах лимфоидных органов, активацию и пролиферацию антигенспецифических Вклеток и их дифференцировку в плазматические клетки, синтез антигенспецифических антител;
формирование Т и Влимфоцитов памяти. 4)
При этом следует отметить, что формирование поствакцинального иммунитета у детей с АЗ имеет некоторые особенности:
уровень протективных антител сравним у детей с атопией и у здоровых лиц; 1)
ряд вакцин (например, против гепатита В) индуцируют синтез цитокинов Th1 и Th2типа; 2)
у новорожденных преобладает Th2ответ, а не Th1 за счет снижения синтеза интерферона; 3)
у детей до 1 года Th2 4)> Th1ответа.
Указанные особенности могут несколько увеличивать частоту развития поствакцинальных осложнений у детей с атопией или повышать риск обострения АЗ, но в целом не влияют на эффективность вакцинации данного контингента, что подтверждается рядом клинических исследований.
В целом вакцинопрофилактика относится к наиболее безопасным и эффективным способам предупреждения инфекционных заболеваний, но все же вакцины могут вызывать побочные реакции и в очень редких случаях тяжелые осложнения. Так, в США с 1991 по 2001 г. было использовано 1,9 млрд доз вакцин, а частота осложнений при этом составила 0,00012 %, или 2281 случай. По данным K. Bohlke et al. (2003), частота анафилактических реакций, связанных с вакцинацией, колеблется от 0,65 до 1,53 случая на 1 млн доз вакцины. Однако последние данные, по их мнению, могут быть и завышенными, поскольку при детальном обследовании 5 детей с анафилактическим шоком после иммунизации только у 1 ребенка был подтвержден истинный характер анафилаксии. Согласно исследованиям N.A. Halsey (2008) и J.M.L. Brotherton (2008), в Австралии анафилаксия после применения вакцины против папилломавируса человека регистрировалась с частотой 1/1 млн — 2,6/100 тыс. вакцинаций. Следовательно, приведенные выше данные свидетельствуют в пользу низкой частоты поствакцинальных нежелательных реакций, особенно при сопоставлении их с риском возникновения инфекционных заболеваний и их осложнений, которые опасны для детей с АЗ, имеющих признаки вторичной иммунной недостаточности.
В большинстве стран мира все поствакцинальные события классифицируют на поствакцинальные реакции и поствакцинальные осложнения. К поствакцинальным реакциям относятся стереотипные доброкачественные реакции организма в ответ на иммунизацию, не выходящие за рамки нормы и обратимые в короткие сроки. Среди них выделяют местные (гиперемия, отек, инфильтрация в месте введения вакцины) и общие (повышение температуры тела, интоксикация, потеря аппетита, головная боль и пр.). Поствакцинальным же осложнением считаются выраженные функциональные и органические изменения со стороны отдельных органов и систем органов необратимого характера, возникающие в ответ на введение вакцины.
В перечень основныхпоствакцинальных осложнений внесены:
анафилактический шок; 1)
2) тяжелые генерализованные аллергические реакции (рецидивирующий ангионевротический отек, синдром Стивенса — Джонсона, синдром Лайелла, сывороточная болезнь и пр.);
энцефалит; 3)
вакциноассоциированный полиомиелит; 4)
5) поражения ЦНС с генерализованными или фокальными остаточными проявлениями (энцефалопатия, серозный менингит, неврит, полиневрит), приведшими к инвалидности, а также с клиническими проявлениями судорожного синдрома;
генерализованная инфекция, остеит, остит и остеомиелит, вызванные вакцинной БЦЖ; 6)
артрит хронический, вызванный вакциной против краснухи. 7)
Возникают поствакцинальные осложнения чаще в первые 24 часа после введения вакцины (реакции немедленного типа) или в период разгара вакцинального процесса (в первые 1–2 дня после применения инактивированных вакцин и с 5го по 14й день после введения живых вакцин). Для их диагностики используют клинический, лабораторный и эпидемиологический методы исследования.
Поскольку для детей с АЗ более характерны поствакцинальные аллергические осложнения (ПАО), то мы остановимся на их характеристике подробнее. Традиционно выделяют общие и местные аллергические осложнения. К общим ПАО относятся: анафилактический шок, сывороточная болезнь и сывороточный синдром, генерализованные аллергические дерматиты (крапивница, синдром Стивенса — Джонсона, синдром Лайелла), поражения нервной системы. К местным относятся реакции, локализованные на коже: аллергический дерматит по типу феномена Артюса — Сахарова, отек Квинке, крапивница, возникшие в зоне введения вакцины (часто наблюдаемые при введении АКДС, антирабической и др.). ПАО чаще возникают при повторном введении вакцины при проведении курсовой вакцинации или ревакцинации и обусловлены формированием гиперчувствительности организма привитого пациента к компонентам вакцины. Риск развития гиперчувствительных реакций на компоненты вакцин выше у детей с проявлениями в анамнезе анафилактических реакций на лекарственные средства и пищевые продукты. Анафилактический шок возникает сразу же после введения вакцины. К его характерным особенностям относятся сосудистая недостаточность (низкое артериальное давление, слабость, отсутствие пульса на магистральных сосудах, холодные конечности, гиперемия лица, повышенное потоотделение), дыхательная недостаточность (бронхо, ларингоспазм, отек гортани), нарушение сознания, возможен судорожный синдром. Помимо системных нарушений возможно развитие генерализованной крапивницы, ангионевротического отека, колики, рвоты, диареи. Рецидивирующий ангионевротический отек может возникать в области тыльной стороны кистей рук или ступней, век, губ, гениталий и дыхательных путей, что может привести к развитию бронхообструкции. Развитие синдрома Стивенса — Джонсона связано с экссудативной полиморфной эритемой с диффузным воспалением слизистых оболочек и их ишемией, а синдром Лайелла — с буллезным некротическим эпидермолизом. Сывороточная болезнь возникает обычно через 7–12 суток после вакцинации и характеризуется повышением температуры тела, различного характера и локализации высыпаниями на коже, гиперплазией лимфоузлов, артралгией.
В ряде клинических исследований была осуществлена попытка выявить зависимость между типом ПАО и видом использованных вакцин. Так, уртикарии или анафилактические реакции на АКДС, АДС или АС описываются редко. Наличие в вакцинах консерванта — тимеросала (АКДС, АДС, АктХиб, гепатит В, грипп) или алюминия может приводить к индукции гиперчувствительности замедленного типа с локальными ее проявлениями в форме контактного дерматита или обострения атопического дерматита у 5,7 % иммунизированных пациентов. Описана также аллергическая реакция в форме анафилаксии на желатин, входящий в вакцину MMR. Изредка отмечены случаи вакцинальных гранулем как проявление аллергии к алюминию на вакцины, содержащие его гидроокись. Некоторые бактериальные вакцины, такие как АКДС, холерная, тифозная, могут вызывать локальные реакции (гиперемия, болезненность в месте введения, лихорадка), которые трудно связать с гиперчувствительностью к компонентам вакцины, поскольку они скорее всего отражают ее токсическое действие. По имеющимся в настоящий момент данным, все вакцины, кроме БЦЖ и живой полиомиелитной вакцины, могут вызывать анафилактический шок, анафилактоидную реакцию и коллапс, синдром Стивенса — Джонсона, синдром Лайелла, рецидивирующие отеки Квинке, кожную сыпь, сывороточную болезнь. В целом же можно констатировать, что в принципе различные компоненты вакцин, хотя и не так часто, как думают многие родители и, к сожалению, ряд медицинских работников, могут вызывать разные клинические проявления ПАО, а также иногда провоцировать обострения имеющихся АЗ у вакцинированных детей.
Диагностика ПАО в настоящее время основана на комплексном анализе данных аллергологического анамнеза, физикального обследования, кожного (приктест) и лабораторного тестирования с компонентами вакцин, общелабораторного метода исследования. Высокоинформативным традиционно является сбор аллергологического анамнеза, при котором выясняются:
установление сроков вакцинации: первичная или повторная вакцинация; -
были ли нежелательные побочные реакции на предыдущие введения вакцин; -
имеется ли у вакцинируемого отягощенный анамнез по АЗ; -
страдает ли ребенок аллергическими, аутоиммунными или какимилибо другими хроническими заболеваниями; -
какова давность перенесенных острых инфекционных заболеваний, травм, операций; -
каков спектр фармакотерапии ребенка, особенно получал ли он ранее белковые препараты, глюкокортикостероиды, иммунодепрессанты. -
Далее следует тщательный врачебный осмотр детей перед предстоящей вакцинацией и после нее. Диагностика ПАО основывается на профессиональной интерпретации клинических симптомов. Лабораторные тесты для выявления сенсибилизации к вакцинам имеют вспомогательное значение (тест Шелли, реакция бластной трансформации лимфоцитов, торможения миграции лейкоцитов в капиллярах с соответствующими вакцинальными антигенами, иммунограмма с определением IgA, IgM, IgG, IgE). Изменения в гемограмме (лейкопения, нейтропения, лимфоцитоз, эозинофилия) или в иммунограмме (незначительная дизиммуноглобулинемия, угнетение реакции бластной трансформации лимфоцитов на митоген и соответствующий антиген менее 50 %) при наличии клинической картины подтверждают ПАО.
Главным методом диагностики ПАО традиционно считается клинический, основанный на данных личного и семейного анамнеза по АЗ, анализа временного промежутка и обстоятельств развития побочной реакции (чаще реакции немедленного типа), физикального исследования (наличие симптомов анафилактического шока, крапивницы и отека Квинке, сывороточной болезни, синдромов Лайелла и Стивенса — Джонсона, аллергического контактного дерматита, обострений бронхиальной астмы, аллергического дерматита, ринита, конъюнктивита и пр.). Необходимо отметить, что ПАО немедленного типа развиваются в течение от нескольких минут до нескольких часов и чаще представлены в форме крапивницы и ангионевротического отека, несколько реже — в виде бронхообструктивного синдрома, стридора, абдоминальных симптомов, гипотензии и анафилактического шока. Реже гиперчувствительные реакции вследствие вакцинации развиваются в течение нескольких дней или 2–3 недель после иммунизации и представлены в форме различных вариантов (макулопапулезная, уртикарная, многоформная эритема) кожной сыпи.
Кожное и лабораторное аллергологическое тестирование с компонентами вакцин, в т.ч. со стабилизаторами и консервантами, показано детям с отягощенным аллергологическим анамнезом, но оно пока по разным причинам не нашло широкого применения в Украине. В литературе имеются данные о достаточно высокой информативности приктеста для диагностики гиперчувствительности к вакцинам у детей с АЗ. Проведение приктеста рекомендуется начинать с разведения вакцины и ее компонентов 1 : 10 с использованием позитивного и негативного контроля. Результаты приктеста считаются позитивными при превышении размеров папулы в опыте над контролем на 3 мм и более. Если результаты приктеста в разведении 1 : 10 отрицательны, то его повторяют с неразведенной вакциной. Если результаты и этого теста отрицательны, то проводится внутрикожное введение вакцины в разведении 1 : 100, а потом 1 : 10 при отрицательном результате предыдущего теста. K. Sugai et al. (2007) установили, что внутрикожное тестирование с разведением вакцины 1 : 10 более информативно, чем приктест с неразведенной вакциной. При отрицательных результатах кожного тестирования ребенку без анафилаксии в анамнезе проводят вакцинацию и наблюдают за ним в течение 1 часа. Если ребенок в анамнезе имеет симптомы анафилаксии, но результаты кожного тестирования отрицательны, то ему вводится 10 % от дозы вакцины. Остальная часть вакцины вводится после наблюдения за пациентом в течение 30–60 минут и при отсутствии у него признаков ПАО. После этого за ребенком наблюдают еще в течение 1 часа. При положительных результатах кожного тестирования с вакциной или ее компонентами результаты обследования вносятся в медицинскую документацию, а остатки вакцины утилизируются.
Кожное тестирование с вакцинами и их компонентами должно проводиться аллергологами. Так, R.S. Zeiger (2002) рекомендует детям с возможной их сенсибилизацией к белку куриного яйца проведение кожного приктеста как с соответствующим аллергеном, так и с противогриппозной вакциной, если первый тест дал положительный результат. Высокую информативность показал приктест с АКДС, АДС и АС у детей, сенсибилизированных к соответствующим вакцинам. Кроме того, таким детям рекомендуется проведение серологического исследования для выявления антител к АС, хотя его информативность в этом случае не слишком высока. В ряде случаев положительные результаты приктеста с компонентами вакцин не коррелируют с особенностями формирования ПАО. Так, гиперчувствительность к тимеросалу обычно проявляется локальными реакциями замедленного типа, поэтому у большинства пациентов не развиваются реакции немедленного типа, хотя у части из них выявляется положительный результат приктеста к этому консерванту вакцин. Внутрикожное тестирование с компонентами вакцин используется реже. Проведение патчтеста возможно для диагностики гиперчувствительности замедленного типа к гидроксиду алюминия и мертиоляту.
При обследовании ребенка с любым поствакцинальным осложнением также проводится клинический анализ крови и мочи, биохимический анализ крови и по показаниям — рентгенологическое, электрофизиологическое, вирусологическое и серологическое исследования биологических жидкостей, анализ фекалий и пр.
Проводить дифференциальную диагностику ПАО следует с обострением соответствующих АЗ, предшествовавших вакцинации или совпавших по времени с нею, но имеющих другую этиологию (пищевая, лекарственная, инсектная, пыльцевая аллергия и пр.), а также поствакцинальных реакций, не обусловленных иммунологическими механизмами (например, ирритантный контактный дерматит, вызванный алюминием). В этом случае важное значение имеют указания на наличие проявлений аллергопатологии до введения вакцины, а также контакт с причиннозначимыми аллергенами помимо вакцинации. Успешной дифференциальной диагностике помогает наличие положительных результатов кожных проб с аллергенами и/или увеличение уровня специфического IgE в сыворотке крови при проведении лабораторных тестов.
В процессе принятия решения о проведении вакцинации, ее сроках, объеме медикаментозной подготовки и выборе вакцинного препарата необходимо учитывать спектр сенсибилизации, нозологическую форму и стадию АЗ, что предполагает индивидуальный подход к каждому ребенку. При легкой форме АЗ вакцинация ребенка осуществляется по общему плану в лечебнопрофилактическом или дошкольном учреждении. В случае среднетяжелой формы АЗ вакцинация проводится в лечебнопрофилактическом учреждении под наблюдением семейного врача или врача кабинета иммунопрофилактики, а патронаж ребенка в поствакцинальный период осуществляет медсестра семейной амбулатории. При тяжелой форме АЗ вакцинация проводится в лечебнопрофилактическом учреждении под наблюдением аллерголога и врача кабинета иммунопрофилактики, а в поствакцинальный период патронаж осуществляет медсестра этого кабинета. Перед вакцинацией по вышеуказанным правилам может быть рекомендовано проведение приктеста с соответствующей вакциной и ее компонентами, особенно у лиц с отягощенным анамнезом по аллергии на желатин, куриный белок, хотя отечественные специалисты предлагают ориентироваться на клинические проявления АЗ, длительность его ремиссии, наличие ПАО, назначать или усиливать базисную терапию АЗ в момент иммунизации, включать в план базисной терапии антимедиаторные (чаще антигистаминные) препараты, бронходилататоры и пр. Подобную медикаментозную подготовку рекомендуют начинать за 5–7 дней до проведения вакцинации и продолжать в течение 2 недель после нее. Детям, имеющим повышенный риск развития IgEзависимых аллергических реакций, за 30–40 мин до прививки один из антигистаминных препаратов вводят также парентерально.
Следует отметить, что эффективность и необходимость проведения такой антимедиаторной профилактической терапии в последнее время рядом авторов оспариваются. Так, в рамках исследования, проведенного в Российском НИИ детских инфекций при вакцинации против кори детей с БА, получавших и не получавших антигистаминные средства, было установлено, что через месяц после прививки отмечалась тенденция к снижению уровня IgE, что свидетельствовало об отсутствии не только неспецифического сенсибилизирующего эффекта вакцины, но и влияния дополнительной терапии на уровень IgE. Кроме того, антигистаминная терапия у детей с АЗ замедляла антителообразование при первичной иммунизации. Следовательно, применение антимедиаторной терапии у детей с БА перед их вакцинацией нецелесообразно как с точки зрения профилактики обострения основного заболевания, так и в связи с негативным влиянием препаратов на формирование иммунного ответа на вакцину. Также было определено, что у детей с АЗ процесс специфического антителообразования замедлен, даже если вакцинация не сопровождается применением антигистаминных препаратов. В дальнейшем результаты проведенного наблюдения были экстраполированы и на группу детей с атопическим дерматитом. Поскольку он в большинстве случаев ассоциирован с ферментативными нарушениями пищеварения, дисбиозом, пищевой аллергией, то в качестве медикаментозной поддержки при вакцинации этим детям назначались биопрепараты и ферменты. Наблюдение в поствакцинальный период при введении как живых вакцин, так и неживых (против гепатита В, АКДС, АДС, гриппа) показало позитивное влияние этой терапии (без дополнительного введения антигистаминных средств) на течение поствакцинального периода. Опыт иммунизации детей с атопическим дерматитом против кори показал, что с 3–4го по 11–14й дни после прививки у 19–20 % из них развивались общие поствакцинальные реакции с катаральным синдромом, лихорадкой, иногда геморрагическими проявлениями и у 5–10 % — с местными реакциями. Все эти реакции укладывались в течение нормального вакцинального процесса. Следовательно, введение антимедиаторных препаратов (желательно современных неседативных) в качестве подготовки к прививкам оправдано и необходимо только в случаях, когда у детей ранее были острые аллергические реакции в виде крапивницы, отека Квинке, дерматита, анафилактических реакций или АЗ у них протекают в тяжелой форме.
Естественно, что важное значение при вакцинации детей с АЗ придается профилактическим мероприятиям. Для этого ряд авторов рекомендуют:
использовать комбинированные вакцины, что позволяет сократить аллергенную нагрузку и снизить риск сенсибилизации; -
- проводить плановые прививки не ранее чем через месяц после последнего обострения АЗ под наблюдением врача иммунологааллерголога;
- отводить детей от последующей иммунизации той вакциной, на которую у них возник анафилактический шок. Вопрос о продолжении иммунизации детей, имеющих в поствакцинальном периоде системные проявления аллергии в виде крапивницы и отека Квинке, решать в каждом конкретном случае индивидуально, после консультации аллерголога. По эпидемиологическим показаниям такие дети могут быть ревакцинированы в период ремиссии АЗ на фоне превентивной противоаллергической терапии (парентеральное введение антигистаминных препаратов, глюкокортикостероидов, адреналина непосредственно перед введением вакцины);
- проводить профилактические прививки детям с АЗ в кабинетах иммунопрофилактики, в прививочных кабинетах, фельдшерскоакушерских пунктах или в стационарах при наличии средств противошоковой терапии. После каждой вакцинации ребенок должен находиться под наблюдением медицинского персонала не менее 30 минут, поскольку в этот период могут развиться системные аллергические реакции немедленного типа;
- соблюдать в период вакцинации элиминационные мероприятия и диету с исключением облигатных аллергенов и гистаминолибераторов (рыба, яйца, мед, шоколад, орехи, какао, цитрусовые, клубника, земляника), а также воздержаться от приема других продуктов, на которые ранее отмечались аллергические реакции, не включая при этом в рацион питания новые продукты. Диета соблюдается в течение не менее 1 недели до вакцинации и 1–3 месяцев после нее (в зависимости от вида вакцинного препарата и течения поствакцинального периода);
- проводить кожные пробы с неинфекционными и инфекционными аллергенами не ранее чем за 1,5 недели до введения вакцинных препаратов или спустя 1–1,5 месяца после него;
при - проведении аллергенспецифической иммунотерапии вакцинацию следует осуществить не ранее чем через 1–1,5 месяца после завершения курса лечения, за исключением ситуации, обусловленной эпидемическими показаниями. После введения вакцинных препаратов курсы терапии могут быть начаты не ранее чем через 1 месяц (при введении живых вирусных вакцин — через 1,5–2 месяца);
после - постановки пробы Манту введение вакцинных препаратов (за исключением БЦЖ и БЦЖМ) рекомендуется проводить не ранее чем через 10–12 дней, поскольку у большинства детей с АЗ наблюдается положительная реакция на туберкулин. После введения АКДСвакцины, АДС, АДСМанатоксинов, живой коревой вакцины и вакцины против эпидемического паротита пробу Манту можно ставить не ранее чем через 1,5 месяца;
не прививать детей с поллинозом в момент цветения причиннозначимых растений; -
- при неблагоприятной эпидемической ситуации проводить вакцинацию можно и при отсутствии ремиссии АЗ на фоне активной противоаллергической терапии и под наблюдением аллергологаиммунолога. При этом вакцинация имеет преимущества перед введением иммуноглобулина (белкового препарата), который может вызвать более серьезные осложнения основного заболевания;
расширить для детей с - респираторными АЗ календарь профилактических прививок за счет ежегодной вакцинации против гриппа, а также против пневмококковой и гемофильной инфекций. Вакцинация против этих инфекций не только приводит к снижению частоты и тяжести интеркуррентных заболеваний, но и способствует положительной динамике течения основного заболевания, позволяя добиться уменьшения объема базисной терапии и удлинения периода ремиссии. Введение дополнительных вакцинных препаратов можно сочетать с введением вакцин основного календаря прививок;
проводить детям с высоким риском развития ПАО кожное тестирование с вакцинами и их компонентами по вышеуказанным методикам; -
- не иммунизировать коревой и паротитной вакцинами детей с наличием в анамнезе указаний на системные аллергические реакции на антибиотики, содержащиеся в вакцинах, на антигены субстрата культивирования. Выявление выраженной аллергии к белкам куриного яйца является противопоказанием для прививок вакцинами от гриппа и клещевого энцефалита, приготовленными на курином субстрате. Тяжелые аллергические реакции на пекарские дрожжи могут служить противопоказанием для вакцинации против вирусного гепатита В;
- проводить изучение каждого случая развития поствакцинального осложнения с фиксацией всех полученных данных в медицинской документации.
Таким образом, вакцинация детей с аллергопатологией не только возможна, но и необходима. Эффективность вакцинации данного контингента достаточно высока, а риск развития умеренного обострения аллергического заболевания или поствакцинального осложнения незначителен. Главным и необходимым условием эффективной и безопасной иммунизации данного контингента детей является индивидуальный подход к ним.
Список литературы находится в редакции