Газета «Новости медицины и фармации» Неврология (490) 2014 (тематический номер)
Вернуться к номеру
Метаанализ клинических исследований бетагистина при болезни Меньера и вестибулярном головокружении
Авторы: Jozef J.P., Nauta - Department of Clinical Development, Abbott EPD, CP Weesp, The Netherlands
Разделы: Клинические исследования
Версия для печати
Статья опубликована на с. 5-14
Введение
Головокружение определяется как ощущение движения в то время, когда никакого движения по отношению к земной гравитации не происходит [1]. Головокружения разделяют на вестибулярные или невестибулярные. Вестибулярные головокружения делятся на периферические (связанные с патологией лабиринта или вестибулярного нерва) или центральные (связанные с патологией мозгового ствола или мозжечка) [2]. Наиболее распространенным типом периферического вестибулярного головокружения является доброкачественное пароксизмальное позиционное головокружение [3]. Болезнь Меньера (БМ) является второй наиболее частой причиной вестибулярного головокружения [4]. Для нее характерны периодически повторяющиеся приступы головокружения, шум в ушах, потеря слуха и заложенность уха. Центральное вестибулярное головокружение встречается реже и является следствием дисфункции центральной нервной системы [5]. Невестибулярное головокружение может быть вызвано неврологическими или сердечными заболеваниями, а также может являться побочным эффектом некоторых лекарственных средств.
Лечение головокружения включает медикаментозную терапию, физиотерапию, когнитивно-поведенческую терапию, интратимпанальную терапию гентамицином и хирургические методы. Цель медикаментозной терапии состоит в том, чтобы помочь пациентам справиться с острой симптоматикой и остановить ощущение вращательного движения [6]. В долгосрочной перспективе важно предотвратить или уменьшить дальнейшие приступы головокружения и устранить основную причину заболевания [6, 7].
Бетагистин зарегистрирован с 1968 года и широко используется при купировании головокружения. Несмотря на то, что механизм его действия до конца неизвестен, на основе выводов доклинических и клинических исследований было предположено, что он обладает несколькими различными потенциальными эффектами. Во-первых, бетагистин модулирует гистаминергическую передачу нервных импульсов посредством частичного агонистического действия в отношении H1-гистаминовых рецепторов в сочетании с мощными антагонистическими Н3-гистаминовыми свойствами [8]. Во-вторых, сосудистые эффекты бетагистина были зарегистрированы как в улитке, так и в головном мозге [9–14]. В-третьих, полагают, что бетагистин влияет на возбудимость нейронов, оказывая ингибирующее, зависимое от дозы действие на отростки нейронов в латеральном и медиальном вестибулярных ядрах [15, 16]. Вполне возможно, что эффект бетагистина, оказываемый на головокружение, прежде всего достигается самим бетагистином, а затем поддерживается аминоэтилпиридином [17, 18]. Наконец, данные свидетельствуют о том, что H3-гистаминовые рецепторы играют ключевую роль в вестибулярной компенсации, восстановлении поведения и уменьшении симптоматики. Бетагистин потенциально может воздействовать на механизмы восстановления с целью обеспечения клинических преимуществ, помогая улучшить поведенческую адаптацию. Полагают, что, вместе взятые, эти свойства способствуют наступлению полезных терапевтических эффектов бетагистина при болезни Меньера и вестибулярном головокружении.
Хотя эффект бетагистина на головокружение был оценен во многих исследованиях, остается неясным, в какой степени данное вещество улучшает симптоматику при болезни Меньера и вестибулярном головокружении.
В последнее десятилетие был опубликован только один систематический обзор и один метаанализ плацебо-контролируемых исследований бетагистина, посвященных данной тематике. Это был последний Кокрановский обзор, посвященный эффективности бетагистина при болезни Меньера [19], и исследователи пришли к выводу о том, что бетагистин приемлем для тех, кто его использует. Тем не менее при этом не было найдено достаточно доказательств того, чтобы показать, оказывает ли бетагистин какой-либо эффект при лечении болезни Меньера. Исследователями Della Pepa и соавт. был проведен метаанализ [20]. Авторы провели оценку клинических исследований у больных с головокружением и подтвердили терапевтический эффект бетагистина при позиционном пароксизмальном головокружении и головокружении, возникшем вторично на фоне артериальной недостаточности. Эти неубедительные результаты могут быть связаны с методологией, выбранной для выполнения анализа.
Большинство исследований, включенных в Кокрановский обзор, а также в метаанализ Della Pepa и соавт., для оценки мнения исследователя по поводу эффективности лечения использовали упорядоченную категорийную (или порядковую) шкалу. Методология для метааналитического подхода, сочетающего упорядоченные категорийные данные, была описана Whitehead and Jones [21], и недавно эта же методология была снова использована Sutton и соавт. [22] в их учебнике по метаанализу, применяемому в клиническом исследовании.
В данной статье мы представляем метаанализ плацебо-контролируемых клинических исследований бетагистина у пациентов, страдающих вестибулярным головокружением или болезнью Меньера, который основан на таком подходе, а затем двух субанализов, проведенных по каждой из этих болезней в отдельности. Кроме того, в отличие от метаанализа, проведенного Della Pepa и соавт., и Кокрановского обзора наш метаанализ основан не только на опубликованных, но и на неопубликованных данных.
Материалы и методы
Стратегия поиска
Для рассмотрения были выбраны клинические исследования, в которых в качестве терапии применялся бетагистин и которые либо соответствовали данным компании Abbott (ранее: Solvay Pharmaceuticals, Duphar), либо были опубликованы в медицинской литературе. Для этой цели был проведен поиск литературы, содержащей клинические исследования с бетагистином и имевшей дату завершения сбора данных 1 февраля 2012 года. В поиск включались материалы клинических исследований с бетагистином, находящиеся в открытом доступе (на всех языках), в которых принимали участие пациенты с диагнозом «головокружение» или «болезнь Меньера». Были проработаны следующие базы данных: MEDLINE (начиная с 1966 года), EMBASE (начиная с 1974 года), BIOSIS (начиная с 1970), SCISEARCH (начиная с 1974 года), DERWENT DERWENT (начиная с 1983 года).
Критерии включения в наш метаанализ были следующими: 1) участники исследования должны были испытывать вестибулярное головокружение; 2) исследование должно быть плацебо-контролируемым рандомизированным двойным слепым; 3) оно должно было или быть проведено в параллельных группах, или иметь перекрестный дизайн. Если исследование имело перекрестный дизайн, то к рассмотрению и оценке принимались только данные первого периода лечения, то есть до момента, когда оно стало перекрестным.
Статистические методы
Цель нашего метаанализа состояла в анализе, основанном на полном анализируемом множестве. Это множество определялось как совокупность всех пациентов, которые были рандомизированы для лечения и получили хотя бы одну дозу назначенного препарата [23]. Критерии исключения из полного анализируемого множества были следующими: пациенты, нарушившие критерии включения или исключения; пациенты, выпадающие во время фазы введения плацебо; а также пациенты, у которых имела место путаница с исследуемым препаратом. Если пациент исключался из анализа, то причина его исключения (при наличии показаний) подвергалась тщательной проверке. Если причина была связана с эффективностью лечения (например, отсутствием эффекта), категориальная оценка, отражающая его, осуществлялась косвенным путем.
Искомой переменной была та, которая в основном оценивалась во всех испытаниях, а именно — решение исследователя в целом об эффективности лекарственной терапии. Тем не менее классификация ответов в разных испытаниях была различной. Для объединения упорядоченных категориальных данных был применен метааналитический метод, описанный Whitehead и Jones [21]. Для каждого отдельного исследования модель пропорциональных шансов приспосабливалась к данным с использованием процедуры SAS PROC Logistic. Показатель терапевтического эффекта, связанный с этим подходом, являлся отношением шансов улучшения. Он представлял собой отношение шансов улучшения у пациентов, которые получали терапию бетагистином, к шансам улучшения у пациентов, получавших плацебо. Предполагалось, что модель пропорционального отношения шансов кумулятивных коэффициентов являлась постоянной по категориям используемой шкалы. Максимальные оценки вероятности того, что отношение шансов в реестре с соответствующими стандартными ошибками, были объединены как для фиксированного эффекта, так и для модели случайных эффектов [24]. Оценки соотношения шансов (средние) фиксированных эффектов и случайных эффектов рассчитывались в соответствии с подходом DerSimonian и Laird [25]. Анализ фиксированных эффектов основывался на предположении о том, что неоднородность между исследованиями отсутствовала или была незначительной. При оценке доверительного интервала (ДИ) в процессе анализа случайных эффектов принималась во внимание неоднородность, следовательно, ДИ был, как правило, шире. Конечным результатом являлись взвешенные (пропорциональные) шансы, отображающие вероятность улучшения по сравнению с отсутствием улучшения.
Результаты
Публикации и отчеты
В общей сложности для анализа было взято 29 публикаций и внутренних неопубликованных отчетов о плацебо-контролируемых клинических исследованиях с применением бетагистина при вестибулярном головокружении или болезни Меньера: 21 публикация (шесть из которых основаны на отчетах компании Abbott) и 8 неопубликованных отчетов компании Abbott [26–61]. Самая старая публикация датируется 1966 годом, самая свежая — 2010 годом.
Пятнадцать публикаций и отчетов были исключены из нашего метаанализа: Watanabe [26], Frew [27], Wilmot [28], Oosterveld [29], Mak [31], Kastein [32] и Meyer [33], результаты которых до перекрестного дизайна были недоступны. Hicks [34], Wolfson [35] и Martins [36] являются перекрестными исследованиями с фиксированной терапевтической последовательностью. Singarelli [37] не является рандомизированным исследованием. В исследованиях Okamato [38] и Salami [39] для оценки степени тяжести головокружения используется упорядоченная категориальная шкала, но эти данные не являются извлекаемыми из публикаций. В исследовании Schmidt [40] изучалась форма препарата бетагистина с длительным высвобождением, которая никогда не присутствовала на рынке. В исследовании Le Gourrierec [41] принимали участие пациенты, которым в качестве терапии болезни Меньера была проведена невротомия вестибулярного нерва.
Следующие 14 публикаций и докладов соответствовали критериям включения нашего метаанализа: Elia [42], Burkin [43], Canty [44], Kastein [46], Nury [47], Fischer [48], Ricci [50], Legent [51], Conraux [53], Oosterveld [55], Maisonneuve [57], Salden [58], KirkPatrick [59], Mira [61]. Этот отбор включает в себя пять неопубликованных исследований. Нам неизвестно о каких-либо других неопубликованных рандомизированных двойных слепых плацебо-контролируемых исследованиях, посвященных применению бетагистина. Общее число пациентов, включенных в эти неопубликованные исследования, составляло 479 (242 принимали бетагистин и 237 — плацебо).
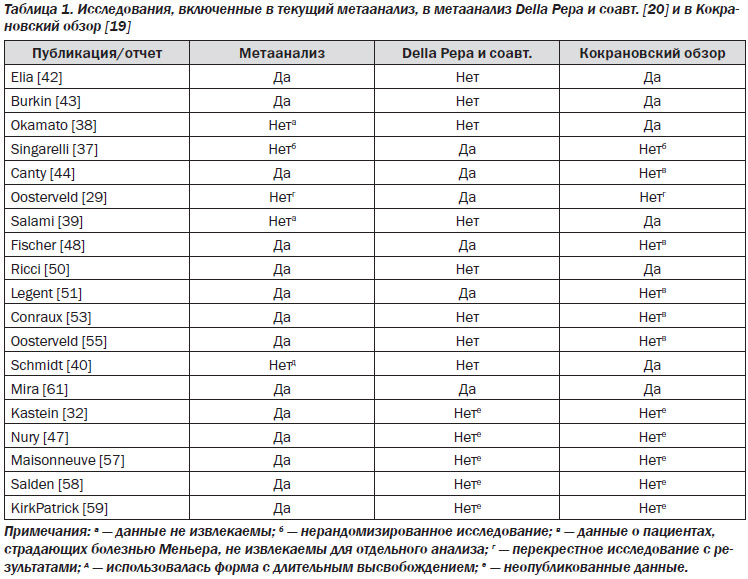
В табл. 1 представлен обзор публикаций и докладов, которые были включены в наш метаанализ, метаанализ Della Pepa и соавт. и Кокрановский обзор.
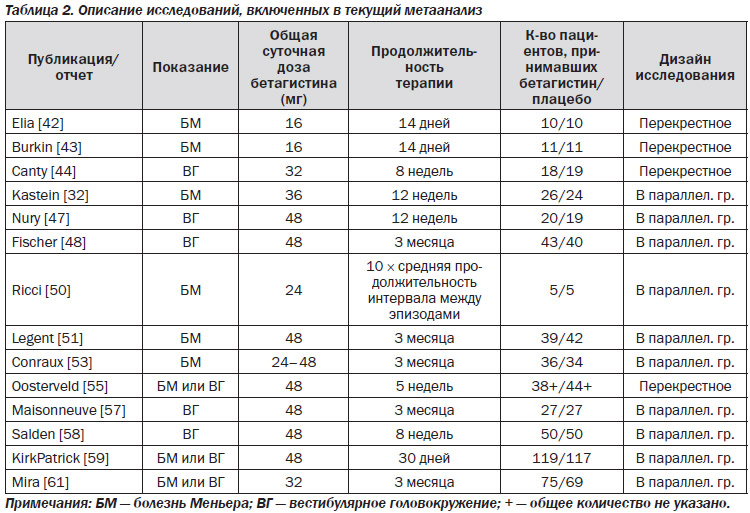
В табл. 2 приведены 14 клинических исследований, включенных в наш метаанализ.
Среди препаратов, используемых в исследовании, были или бетагистина гидрохлорид, или бетагистина дигидрохлорид. Общая суточная доза бетагистина варьировала между 16 и 48 мг. Продолжительность лечения колебалась от 14 дней до 3 месяцев. Десять исследований имели дизайн проведения в параллельных группах и четыре — перекрестный дизайн. В общей сложности в эти 14 исследований было рандомизировано 1038 пациентов: 506 принимали бетагистин, 500 — плацебо; по 32 пациентам, получавшим терапию, данные отсутствуют.
Шкалы
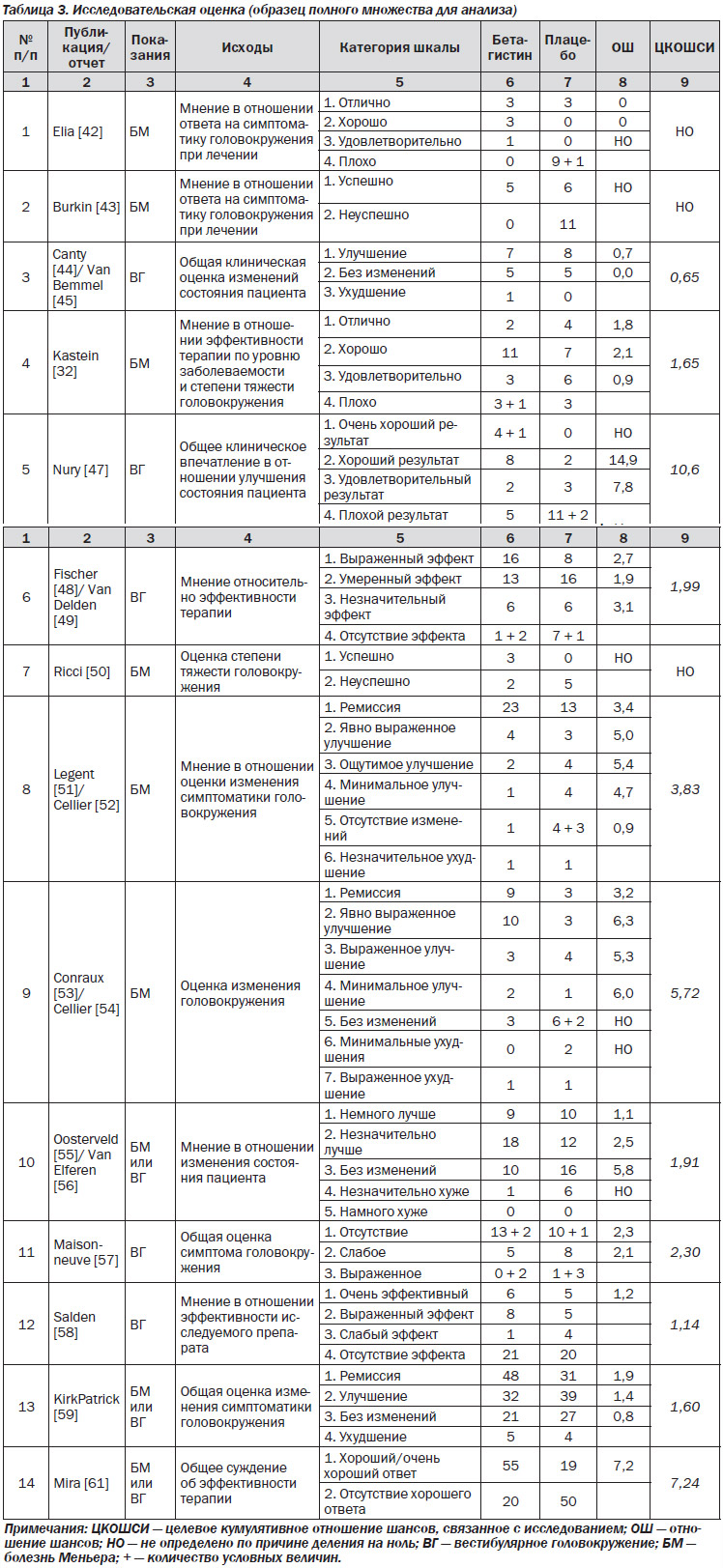
Шкалы, используемые исследователями, приведены в табл. 3. Исследователь Elia [42] оценил реакцию симптомов головокружения на лечение с использованием шкалы с четырьмя упорядоченными категориями: отлично, хорошо, удовлетворительно и плохо. В целом, за исключением одного исследования, исследовательская шкала оценивала изменение по сравнению с исходными данными. Elia [42], Kastein [32], Ricci [50], Legent [51], Conraux [53] и KirkPatrick [59] осуществляли оценку либо изменений симптомов и степени тяжести, либо уменьшения головокружения. Canty [44], Nury [47], Fischer [48] и Oosterveld [55] осуществляли оценку изменений состояния пациента; Salden [58] и Mira [61] оценивали эффективность терапии, а Burkin [43] — изменение симптоматики головокружения. Единственным исследованием, в котором изменения не оценивались по исследовательской шкале, было Maisonneuve [57]. В этом испытании исследователь осуществлял оценку симптомов головокружения спустя 3 месяца терапии.
Типы пациентов
Основываясь на критериях включения и исключения из исследования, мы использовали следующие условные группы пациентов: страдающие болезнью Меньера, вестибулярным головокружением или группа «БМ или ВГ».
В исследование Elia [42] были включены пациенты, страдающие БМ. В исследование Burkin [43] были включены пациенты с диагнозом БМ. В исследование Kastein [32] были включены пациенты, страдающие БМ, лабиринтной ишемией или другими формами периферического головокружения неясной этиологии; из 36 пациентов, включенных в статистический анализ, у 33 была диагностирована БМ и у 3 — периферическое головокружение. В исследовании Ricci [50] все пациенты были амбулаторными и страдали БМ. В исследование Legent [51] были включены пациенты, страдающие повторяющимися пароксизмальными головокружениями с кохлеарным синдромом, характерным для БМ, или без него, однако одним из критериев исключения было наличие доброкачественного пароксизмального позиционного головокружения, которое предполагает отсутствие у пациентов БМ. В исследование Conraux [53] были включены пациенты, страдающие хроническим головокружением; критерием исключения здесь также было наличие доброкачественного пароксизмального позиционного головокружения, которое предполагает отсутствие у пациентов БМ. Пациенты в этих исследованиях были отнесены к условной группе «БМ».
В исследование Canty [44] были включены пациенты, страдающие эпизодическим вращательным головокружением периферического происхождения; пациенты с диагнозом классической БМ были исключены из исследования. В исследование Nury [47] были включены пациенты с головокружением центрального происхождения. В исследование Fischer [48] были включены пациенты, страдающие пароксизмальными приступами вращательного головокружения. В исследование Maisonneuve [57] были включены пациенты, страдающие рецидивирующим пароксизмальным головокружением с наличием или отсутствием кохлеарного синдрома. В исследование Salden [58] были включены пациенты с доброкачественным пароксизмальным позиционным головокружением. Мы отнесли этих пациентов к условной группе «ВГ».
В исследование Oosterveld [55] были включены пациенты, страдающие хроническим или пароксизмальным головокружением; из 25 пациентов, включенных в статистический анализ, у 9 была диагностирована БМ, у 15 — пароксизмальное головокружение и у 1 — шейное головокружение. В исследование KirkPatrick [59] были включены две нозологии: рецидивирующее головокружение или периодическое головокружение и рецидивирующее головокружение или периодическое головокружение без типичного кохлеарного синдрома, характерного для БМ. В исследование Mira [61] были включены пациенты, страдающие рецидивирующим головокружением, связанным либо с БМ, либо с пароксизмальным позиционным головокружением, вероятно, сосудистого происхождения. Мы отнесли этих пациентов к условной группе «БМ или ВГ».
Анализы
В табл. 3 подведены итоги исследовательской оценки. Число, следующее за символом «+», является условно начисленным числом по причине пропущенных значений. Например, в исследовании Elia [42] в группе принимавших плацебо один пациент прекратил лечение вследствие отсутствия эффекта; для этого пациента было условно принято мнение в отношении эффективности терапии как «плохое». А также в табл. 3 показаны отношения шансов, если таковые определялись.
В исследовании Kastein [32] использовалась 4-точечная упорядоченная категорийная шкала. Это означает, что имеются три кумулятивных отношения шансов: одно для категории с оценкой «отлично» по отношению к совокупности категорий с оценками «хорошо», «удовлетворительно» или «плохо» ([2 • 16]/[18 • 1] = = 1,8); одно для совокупности категорий с оценкой «отлично» или «хорошо» по отношению к совокупности категорий с оценкой «удовлетворительно» или «плохо» ([13 • 9]/[7 • 8] = 2,1); и одно для совокупности категорий с оценками «отлично», «хорошо» или «удовлетворительно» по отношению к категории «плохо» ([16 • 3]/[4 • 14] = 0,9). Отношения шансов, выделенные курсивом, представляют собой отношения шансов, оцененные на основании проведенных исследований. Если предположить, что эти отношения шансов одинаковы (пропорциональны), то можно получить общее соотношение пропорциональных шансов в исследовании. В исследовании Kastein [32] оцененное отношение пропорциональных шансов составило 1,65.
В трех исследованиях не получилось вычислить отношения шансов [42, 43, 50] в связи с делением на ноль. В первых двух из них применялась низкая общая суточная доза (16 мг) и краткосрочная терапия (14 дней). Таким образом, эти исследования не были учтены. В остальных 12 исследованиях использовалась стандартная общая суточная доза (24–48 мг), а также продолжительность лечения была не менее 1 месяца (1–3 месяца), в том числе в исследовании Ricci [50]. Таким образом, это исследование не было проигнорировано, и при оценке отношения шансов был применен следующий подход. Для группы принимавших плацебо данные «0 успешных результатов/5 безуспешных» были изменены на «1 успешный результат/4 безуспешных». Таким образом, в данном случае была введена небольшая стандартная погрешность в пользу плацебо.
Из 1038 пациентов, рандомизированных в 14 исследований (раздел «Публикации и отчеты»), 117 (11,3 %) были исключены из нашего метаанализа; это было связано либо с тем, что они были включены в исследование Elia [42] или Burkin [43], либо с тем, что они выпали из исследования во время приема плацебо в последующей вводной фазе исследования, либо вследствие нарушения критериев включения, либо вследствие отсутствия данных после рандомизации. Таким образом, количество пациентов, включенных в наш метаанализ полного анализируемого множества, составило 921; 469 принимали бетагистин и 452 принимали плацебо. Из 921 пациента 179 (19,4 %) были отнесены к условной группе «БМ», 281 (30,5 %) — к условной группе «ВГ», а 461 (50,1 %) — к группе «БМ или ВГ». Шестнадцать результатов (1,7 %) были условными, а для 39 пациентов, принимавших бетагистин (8,3 %), и 36 пациентов, принимавших плацебо (8,0 %), результаты отсутствовали.
Общая эффективность бетагистина при лечении вестибулярного головокружения
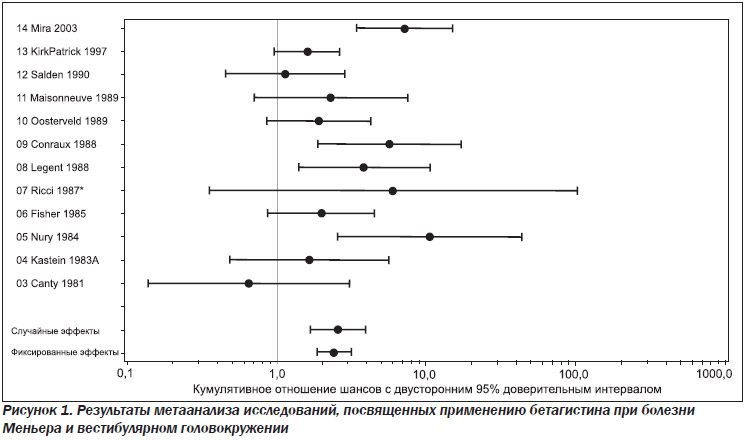
Рис. 1 отображает результаты метаанализа 12 исследований. На нем показаны отношения шансов, оцененные на основании проведенных исследований, с двусторонним 95% доверительным интервалом, а также результаты анализов фиксированных и случайных эффектов.
Отношения шансов, оцененные на основании проведенных исследований, варьировали от 0,65 [44] до 10,6 [47]. Все исследования, кроме Canty [44], продемонстрировали положительный эффект в пользу бетагистина по сравнению с плацебо. Этот эффект был статистически значимым в четырех исследованиях, поскольку нижняя граница двустороннего 95% доверительного интервала для отношения шансов была > 1,0. Анализ фиксированных эффектов показал оценку отношения шансов 2,42 (95% ДИ 1,86–3,16). Анализ случайных эффектов, осуществляемый путем оценки среднего отношения шансов 2,58 (95% ДИ 1,67–3,99), означает, что у пациентов, получавших бетагистин, шансы на благоприятный исход по сравнению с плацебо выше в 2,58 раза. Рис. 1 показывает, что гетерогенность между исследованиями является значительной, следовательно, анализ случайных эффектов в данном случае является анализом выбора. Однако следует отметить, что взаимодействие имеет выраженную количественную природу. А это означает, что, несмотря на имеющиеся различия между исследованиями, почти во всех случаях бетагистин показывает лучшие результаты по сравнению с плацебо. Оба анализа представили статистически значимый результат, что свидетельствует о положительном общем эффекте бетагистина на клиническую картину вестибулярного головокружения.
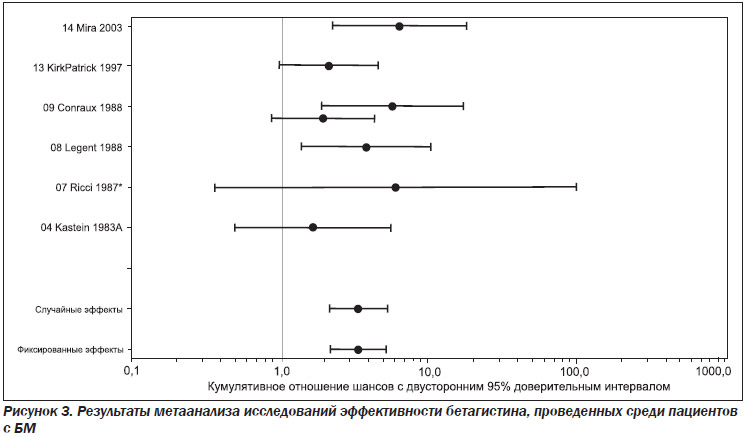
На рис. 2 показана интерпретация модели с точки зрения вероятности благоприятного исхода. Данный рисунок демонстрирует следующее:
— у пациентов, получавших плацебо, вероятность наиболее благоприятного исхода составляла 25,0 % («значительное улучшение»), а среди пациентов, получавших бетагистин, вероятность того же результата составляла 46,2 %, то есть была в 1,85 раза выше;
— у пациентов, получавших плацебо, вероятность благоприятного исхода составляла 30,0 % («значительное улучшение/незначительное улучшение»), а среди пациентов, получавших бетагистин, вероятность благоприятного исхода составляла 52,5 %, то есть была в 1,75 раза выше.
После данного общего метаанализа было проведено два субанализа: отдельно для каждой из нозологий — БМ и головокружения.
Эффективность применения бетагистина при болезни Меньера
Среди 12 исследований 4 было проведено в условной группе пациентов «БМ» и 3 — в группе «БМ или ВГ». В двух из трех исследований [59, 61], которые включали пациентов, страдающих как БМ, так и ВГ, данные подгруппы «БМ» были доступны для отдельного анализа. В исследованиях Van Elferen и Essers [60] описаны результаты обследования пациентов с БМ, которые были включены в отдельный отчет KirkPatrick [59].
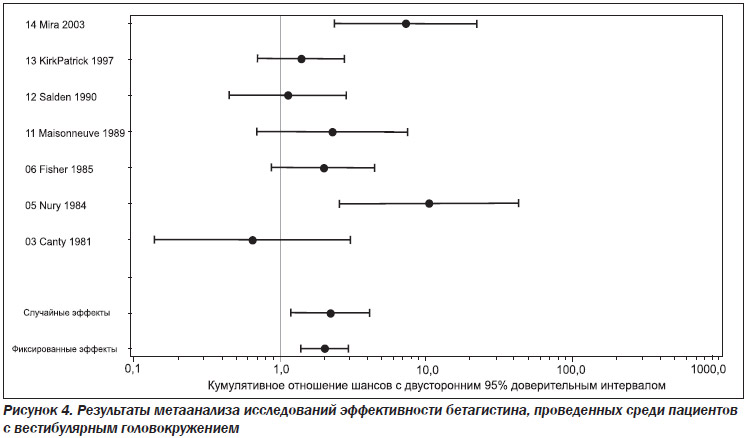
В исследовании Mira [61] принял участие в общей сложности 81 пациент (41 принимал бетагистин и 40 — плацебо). Исследователи оценили эффективность лечения как «хорошо/очень хорошо» у 30 пациентов в группе принимавших бетагистин и у 11 пациентов в группе принимавших плацебо. Поскольку в отчете говорится, что, «по мнению врача, эффективность терапии была хорошей/очень хорошей у 73,5 % пациентов в группе принимавших бетагистин и у 27,6 % в группе принимавших плацебо, без расхождений между обеими группами», было предположено, что этот процент применим как для условной группы «БМ», так и для «ВГ». (То же предположение имело место и в Кокрановском обзоре.) Поскольку в исследовании Oosterveld [55] не было возможности извлечь данные о пациентах, страдающих БМ, для отдельного анализа, при проведении субанализа этим исследованием пренебрегли. Таким образом, количество исследований, включенных в наш метаанализ, которые вошли в условную группу «БМ», составило шесть. Общее число пациентов с БМ в этих исследованиях составило 344 (полное анализируемое множество): 178 принимали бетагистин и 166 — плацебо. Общее число пациентов с БМ, данные по которым не были утеряны, составило 333 человека, среди которых 168 принимали бетагистин и 165 — плацебо. Результаты данного субанализа показаны на рис. 3.
При этом анализ как фиксированных, так и случайных эффектов дает статистически значимый результат. Оценка отношения шансов фиксированных эффектов составляла 3,35 (95% ДИ 2,16–5,19); оценка среднего отношения шансов случайных эффектов составляла 3,37 (95% ДИ 2,14–5,29).
Субанализ условной группы пациентов «БМ» включал в себя два исследования, которые были исключены из Кокрановского обзора: Conraux [53] и Legent [51] (табл. 1). Применение в данном случае критериев Кокрановского обзора с исключением обоих исследований показало, что анализ как фиксированных, так и случайных эффектов также был статистически значимым (оценка отношения шансов фиксированных эффектов составляла 2,83 (95% ДИ 1,64–4,87); оценка среднего отношения шансов случайных эффектов составляла 2,90 (95% ДИ 1,50–5,60)).
Эффективность применения бетагистина при вестибулярном головокружении
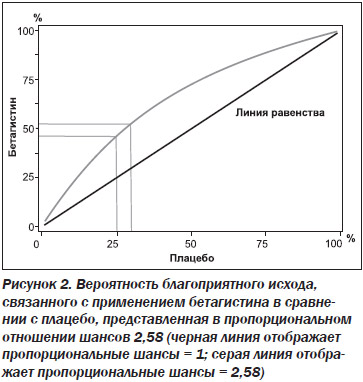
Пять из 12 исследований были посвящены головокружению. В двух исследованиях условной группы пациентов «БМ или ВГ» была возможность извлечь данные о пациентах с ВГ для проведения отдельного анализа, в результате чего число субисследований, проведенных в условной группе пациентов «ВГ», стало равным семи. Результаты данного субанализа показаны на рис. 4.
Опять-таки, анализ как фиксированных, так и случайных эффектов продемонстрировал статистически значимый результат. Оценка отношения шансов фиксированных эффектов составила 2,02 (95% ДИ 1,40–2,93); оценка среднего отношения шансов случайных эффектов составляла 2,23 (95% ДИ 1,20–4,14), что показало общее полезное влияние бетагистина.
Обсуждение
Насколько нам известно, наш метаанализ является первым, в котором был использован новый подход к объединению упорядоченных категорийных данных, предложенный Whitehead и Jones [21] для клинических исследований с бетагистином. Сильная сторона данного подхода заключается в том, что он демонстрирует (1) различия в цифрах эффективности и в определениях категорий, а также (2) в использовании данных в их первоначальном виде. При этом число шкальных категорий варьирует от двух до восьми. Поскольку данные могут быть проанализированы в их первоначальном виде, нет необходимости использовать возможный субъективный характер и, следовательно, применять преобразования смещения.
Также сильной стороной нашего анализа является то, что конечная точка, представляющая собой решение исследователя в целом об эффективности медикаментозной терапии, была выбрана потому, что она была единственной конечной точкой, которая измерялась последовательно почти во всех исследованиях.
Результаты нашего метаанализа 12 рандомизированных двойных слепых плацебо-контролируемых клинических исследований подтверждают терапевтический эффект бетагистина в отношении симптома головокружения как при болезни Меньера, так и при вестибулярном головокружении. Этот вывод основан на анализе мнения исследователей об эффективности лечения в плане клинических аспектов головокружения. Одиннадцать из 12 исследований показали положительное влияние бетагистина, в 4 исследованиях эффект был статистически значимым, а расчетные средние шансов были высоко значимыми. В данном метаанализе конечная точка была выбрана потому, что она являлась единственной эффективной конечной точкой, которая последовательно оценивалась почти во всех исследованиях. Кроме того, были проанализированы данные в их первоначальном виде и не применялись никакие возможные субъективные преобразования. В предыдущих анализах, которые выполнялись Cochrane и Della Pape и соавт., анализ данных по полученным результатам не являлся априорным, точно установленным анализом, который бы мог привести к предвзятости.
Бетагистин назначали перорально разделенными дозами; общая суточная доза обычно находилась в пределах от 24 до 48 мг. В 12 исследованиях общая суточная доза варьировала от 24 мг (1 исследование), 32 мг (2 исследования), 36 мг (1 исследование), 24–48 мг (1 исследование) и до 48 мг (7 исследований), тем самым представляя современные стандарты клинической практики.
Наш метаанализ является обновленным (содержит дополнительные исследования) и расширенным (более широкая популяция пациентов) по сравнению с метаанализом, проведенным исследователями Della Pape и соавт. в 2006 году в отношении эффектов бетагистина на симптоматику головокружения, а также с Кокрановским обзором, проведенным в 2011 году в отношении эффективности бетагистина при болезни Меньера.
Della Pape и соавт. включили в свой метаанализ семь клинических исследований (табл. 1). Исследование Singarelli [37] (20 пациентов) было исключено из анализа по той причине, что оно не было рандомизированным, а исследование Oosterveld [29] (27 пациентов) было исключено из анализа по причине отсутствия результатов перед последующей фазой исследования после перекреста.
Метаанализ Della Pape и соавт. имеет несколько существенных ограничений. Во-первых, авторы объединили различные результаты, используемые во включенных исследованиях для оценки эффективности бетагистина (такие как, например, общее мнение, основанное на мнении пациента или исследователя, количество эпизодов головокружения и их продолжительность), в новый бинарный исход: «улучшение» или «отсутствие улучшения». Очевидным недостатком этого подхода при применении постфактум является субъективность, которая, возможно, приводит к предвзятости. В частности, недостаток данного подхода состоит в том, что результаты не являются воспроизводимыми, поскольку они не предоставляют определение улучшенной категории. Во-вторых, отсутствует описание статистической методологии, на которой базируется анализ. В-третьих, метаанализ является неполноценным, поскольку включенные перекрестные исследования анализируются, как если бы это были исследования, проведенные в параллельных группах с независимыми терапевтическими группами, что явно неверно.
Следовательно, метаанализ Della Pape и соавт. следует интерпретировать с осторожностью в связи с имеющимися недостатками данного статистического анализа.
В Кокрановский обзор вошли семь изданий. Включение исследования Schmidt [40] является спорным, поскольку в нем использовалась форма бетагистина, которая никогда не была в продаже (бетагистин замедленного высвобождения). По этой причине мы не включили это исследование в наш метаанализ.
Бетагистин имеет хорошо обоснованный профиль безопасности с более чем 35-летним опытом клинического использования и постмаркетингового надзора, проводимого по всему миру [62]. Учитывая хороший профиль безопасности и эффективности бетагистина, мы приходим к выводу о том, что его соотношение польза/риск является положительным и что он является безопасным и эффективным для лечения головокружения при БМ и вестибулярного головокружения.
Список литературы находится в редакции