Журнал «Медицина неотложных состояний» 2 (57) 2014
Вернуться к номеру
Ацетилцистеїн як засіб детоксикації ендотоксемії на тлі хронічного генералізованого пародонтиту
Авторы: Лук’янчук В.Д., Гордійчук Д.О. - Кафедра фармакології ДЗ «Луганський державний медичний університет»; Шейман Б.С. - Український центр дитячої токсикології, інтенсивної та еферентної терапії НДСЛ «Охматдит» МОЗ України, м. Київ
Рубрики: Медицина неотложных состояний, Стоматология
Разделы: Клинические исследования
Версия для печати
Актуальна проблема сучасної стоматології — поширення пародонтопатій різного генезу, результатом яких є розвиток ендотоксикозу. Мета дослідження — визначити ступінь ендотоксемії при пародонтиті за умов застосування ацетилцистеїну. Для досягнення мети досліджували низку лейкоцитарних індексів (ядерний індекс інтоксикації, індекс співвідношення нейтрофіли/лімфоцити, лімфоцитарний індекс та індекс імунореактивності), а також показники циркулюючих імунних комплексів, молекул середньої маси і продукти ліпідопереокислення на тлі експериментального пародонтиту із застосуванням ацетилцистеїну. Результати експериментального дослідження дозволили встановити підвищення рівнів ядерного індексу інтоксикації, індексу співвідношення нейтрофіли/лімфоцити, циркулюючих імунних комплексів, ТБК-реактантів і молекул середньої маси, що свідчить на користь розвитку запалення й виділення токсичних метаболітів при хронічному пародонтиті. У цей же час спостерігається зниження лімфоцитарного індексу та індексу імунореактивності, що підтверджує зрив детоксикуючої системи на тлі пародонтиту. При застосуванні ацетилцистеїну як пародонтопротекторного засобу визначається нормалізація всіх досліджуваних показників. Таким чином, ацетилцистеїн сприяє активації детоксикуючої системи за умов синдрому ендогенної інтоксикації на тлі хронічного генералізованого пародонтиту.
Актуальная проблема современной стоматологии — распространение пародонтопатий различного генеза, результатом которых является развитие эндотоксикоза. Цель исследования — определить степень эндотоксемии при пародонтите в условиях применения ацетилцистеина. Для достижения цели исследовали ряд лейкоцитарных индексов (ядерный индекс интоксикации, индекс соотношения нейтрофилы/лимфоциты, лимфоцитарный индекс и индекс иммунореактивности), а также показатели циркулирующих иммунных комплексов, молекул средней массы и продукты липидопереокисления на фоне экспериментального пародонтита с применением ацетилцистеина. Результаты экспериментального исследования позволили установить повышение уровней ядерного индекса интоксикации, индекса соотношения нейтрофилы/лимфоциты, циркулирующих иммунных комплексов, ТБК-реактантов и молекул средней массы, что свидетельствует в пользу развития воспаления и выделения токсических метаболитов при хроническом пародонтите. В это же время наблюдается снижение лимфоцитарного индекса и индекса иммунореактивности, что подтверждает срыв детоксицирующей системы на фоне пародонтита. При применении ацетилцистеина как пародонтопротекторного средства определяется нормализация всех исследуемых показателей. Таким образом, ацетилцистеин способствует активации детоксицирующей системы в условиях синдрома эндогенной интоксикации на фоне хронического генерализованного пародонтита.
The actual problem of modern dentistry — prevalence of periodontopathies of various origins, which result in the development of endotoxemia. The purpose of the study — to determine the degree of endotoxemia in periodontitis in acetylcysteine use. To achieve the objective we studied a number of leukocyte indices (nuclear toxicity index, index of neutrophils/lymphocytes ratio, lymphocytic index and immunoreactivity index), as well as indicators of circulating immune complexes, the average-weight molecules and products of lipid peroxidation on the background of experimental periodontitis using acetylcysteine. The results of experimental studies revealed increased levels of nuclear intoxication index, index of neutrophils/lymphocytes ratio, circulating immune complexes, TBA-reactants and average-weight molecules, that indicate the development of inflammation and release of toxic metabolites in chronic periodontitis. At the same time there is observed a decrease in lymphocyte index and index of immunoreactivity, which confirms the failure of the detoxifying system against the background of periodontitis. When acetylcysteine is administered as a drug for periodontium protection, normalization of all studied parameters is being determined. Thus, acetylcysteine helps activate detoxifying system in terms of endogenous intoxication with chronic generalized periodontitis.
ендотоксикоз, детоксикація, хронічний генералізований пародонтит, ацетилцистеїн.
эндотоксикоз, детоксикация, хронический генерализованный пародонтит, ацетилцистеин.
endotoxemia, detoxification, chronic generalized periodontitis, acetylcysteine.
Статья опубликована на с. 20-24
Вступ
Актуальною проблемою сьогодення є стрімке поширення пародонтопатій різного генезу, серед яких особливе місце посідає хронічний генералізований пародонтит (ХГП) [14, 32]. ХГП негативно впливає не тільки на стан зубощелепної системи, але й супроводжується порушенням загального стану, причиною чого є розвиток ендотоксикозу [8, 18].
Унаслідок запальної реакції при ХГП спостерігається вивільнення літичних ферментів, що чинять мембранопошкоджуючу дію, відбувається надлишкова продукція перекисних речовин, медіаторів, цитокінів, які потрапляють у систему кровообігу [30]. У результаті місцеві запальні процеси в тканинах пародонта сприяють розвитку так званого синдрому ендогенної інтоксикації (СЕІ) [2, 26].
Сучасна концепція щодо ролі мембранодеструктивних процесів у патогенезі СЕІ визначає можливість фармакокорекції даного патологічного процесу шляхом застосування засобів з антиоксидантним та детоксикуючим типом дії [10, 27]. Згідно з даними [1, 9] та результатами власних досліджень [20], одним із засобів, що поєднує детоксикуючий та мембраностабілізуючий ефекти, є ацетилцистеїн.
Мета дослідження — аналіз динаміки розвитку й перебігу СЕІ на тлі ХГП за умов застосування ацетилцистеїну.
Матеріали та методи дослідження
Досліди виконані на 92 білих нелінійних щурах масою 180–200 г обох статей у повній відповідності до вимог ДП «Державний експертний центр МОЗ України» [13]. ХГП відтворювали за власною методикою [24].
Тварини були розподілені на 4 групи: інтактна, контрольна (ХГП без лікування), дослідна (ХГП + ацетилцистеїн) та референтна (ХГП + метилурацил). Дослідним щурам упродовж експерименту 1 раз на добу натще перорально вводили ацетилцистеїн у дозі 100 мг/кг у вигляді 2% водного розчину (виробництво Луганського хімфармзаводу). Як препарат порівняння використовували метилурацил (ЗАТ «Фармацевтична фірма «Дарниця») [23, 25].
Усі показники визначали в динаміці: через 2, 4, 6 і 8 тижнів. Перебіг СЕІ та детоксикуючі властивості ацетилцистеїну оцінювали за низкою параметрів (індексів), що ґрунтуються на даних клінічного аналізу крові і є показовими вже на ранніх стадіях захворювання [28]. Розраховували такі індекси: ядерний індекс інтоксикації (ЯІІ) [19]; індекс співвідношення нейтрофіли/лімфоцити (ІСНЛ) [31]; лімфоцитарний індекс (ЛІ) [16], індекс імунореактивності (ІІР) [33].
Показником ступеня тяжкості перебігу ендогенної інтоксикації при ХГП за умов експерименту, що вивчається, слугували циркулюючі імунні комплекси (ЦІК), уміст яких у сироватці крові визначали за методом [15].
Також як маркери СЕІ досліджено концентрацію продуктів ліпідпереокислення, що реагують з 2-тіобарбітуровою кислотою (ТБК-реактанти), та молекули середньої маси (МСМ) [17]. Концентрацію МСМ визначали у сироватці крові за спектрофотометричним методом [29], а ТБК-реактанти — за методикою [21].
Отримані результати обробляли статистично за допомогою t-критерію Стьюдента, оцінюючи вірогідність на рівні значимості не менше 95 % (р ≤ 0,05) [11].
Результати та їх обговорення
Отримані результати дослідження ЯІІ наведені на рис. 1.
/21/21.jpg)
Установлено, що в контрольній серії (ХГП без лікування) показник ЯІІ впродовж експерименту вірогідно (Р < 0,001) більше, ніж в інтактних тварин, у середньому на 6–55 %. Це можна пояснити доволі раннім формуванням СЕІ, уже починаючи з 2-го тижня моделювання ХГП. Виявлені при цьому зміни при ХГП характеризуються ядерним зсувом нейтрофілів вліво, що вказує на регенеративні зрушення, тобто збільшення кількості паличкоядерних та юних нейтрофілів на тлі загального підвищення лейкоцитів. Така ситуація має місце при запальних та гнійно-септичних захворюваннях, зокрема і ХГП, що власне має своє підтвердження в літературі [5].
У цей же час показники ЯІІ при ХГП за умов застосування ацетилцистеїну впродовж усіх термінів дослідження реєструються на рівні здорових та референтних щурів (Р > 0,05; рис. 1).
Отримані результати, на нашу думку, свідчать про здатність ацетилцистеїну чинити пародонтопротекторну дію, в основі якої лежать детоксикуючі властивості, а отже, й попереджати нейтрофільний зсув лейкоцитарної формули, що цілком збігається з динамікою клінічних змін перебігу ХГП у дослідній групі тварин.
Іншим розрахунковим індексом СЕІ, що вивчається, є ІСНЛ. Отримані дані (рис. 1) свідчать, що величина цього показника в контрольній серії вірогідно зростає вже через 2 тижні від початку моделювання ХГП та зазнає максимального підвищення на 6-му тижні дослідження (перевищує рівень інтактних щурів на 35 %), що може бути обумовлено значною активацією нейтрофілів та зниженням кількості лімфоцитів у крові. Це ще раз свідчить на користь активації продукції нейтрофілів на фоні зниженого гуморального імунітету на тлі ХГП.
При застосуванні ж ацетилцистеїну показник, що аналізується, вірогідно не відрізняється (Р > 0,05) не лише від референтної, а й від інтактної серії тварин упродовж всіх термінів дослідження. Отримані результати варто оцінювати як запобігання розвитку гранулоцитозу, що є характерною ознакою запальної реакції при ХГП за умов фармакокорекції ацетилцистеїном.
Результати вивчення ЛІ, які наведені на рис. 1, вказують, що у щурів із ХГП величини цього індексу в середньому в 1,21 раза нижчі, ніж в інтактній групі у всі строки спостереження. Це, як свідчать дані літератури [7], пов’язане зі збільшенням кількості нейтрофілів, що спостерігається вже з 2-го тижня дослідження внаслідок запалення тканин пародонту та надлишкового утворення ендотоксинів.
Інша динаміка значень ЛІ визначається у групі тварин із ХГП при застосуванні ацетилцистеїну, коли цей показник вірогідно (Р < 0,05–0,001) вищий, ніж у контролі, на 6, 10, 12 і 37 % відповідно через 2, 4, 6 та 8 тижнів експерименту. Варто наголосити, що ці величини ЛІ вірогідно не відрізняються у всі терміни дослідження від аналогічних у інтактній серії, але вірогідно перевершують зареєстровані в референтній групі. Це, швидше за все, свідчить на користь стабілізації стану клітинного імунітету при ХГП під впливом ацетилцистеїну.
Наступний розрахунковий показник крові, що вивчається, — це ІІР, який відображає стан основних клітин — продуцентів цитокінів та дисбаланс в цитокіновому профілі [3]. Установлено (рис. 1), що в контрольній групі рівень ІІР протягом 8 тижнів у середньому в 1,5 раза нижчий, ніж у здорових щурів. Ці дані вказують на низьку імунологічну реактивність організму при ХГП, що, як нам здається, є наслідком зменшення кількості лімфоцитів, які є головними клітинами імунної системи, що забезпечують адекватну імунну відповідь організму на надмірну кількість ендотоксинів запального генезу.
При застосуванні ацетилцистеїну на тлі індукованого ХГП відмічається чітка тенденція до нормалізації ІІР впродовж всього терміну дослідження. Доведено, що даний показник в дослідній групі вірогідно (P < 0,001) вище щодо контролю у середньому на 25 %, що свідчить про здатність ацетилцистеїну попереджати деградацію відносного вмісту лімфоцитів та викликати активацію гуморального імунітету при запаленні. Останнє, у свою чергу, пояснює зниження ступеня розвитку ендогенної інтоксикації при застосуванні ацетилцистеїну. Примітною є та обставина, що показники ІІР дослідної і референтної серій не мають вірогідної різниці впродовж дослідження, хоча є дещо нижчими відносно норми.
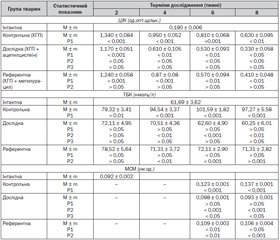
Результати дослідження іншого високоінформативного показника ступеня тяжкості ендогенної інтоксикації — ЦІК наведені в табл. 1.
Отримані результати показали, що в контрольній серії вже з 2-го тижня експерименту відбувається вірогідно різке зростання цього показника щодо інтактної групи. У подальшому (через 4–8 тижнів) в контролі зберігається збільшення рівня ЦІК у середньому в 4 рази від аналогічного показника у здорових тварин.
Отримані дані можуть бути пояснені порушенням балансу між утворенням й елімінацією ЦІК, а це в підсумку призводить до їх надлишкового накопичення за наявності запального процесу в умовах ХГП, що узгоджується з даними літератури [12].
При індукованому пародонтиті на тлі застосування ацетилцистеїну спостерігається тенденція до нормалізації рівня ЦІК з 4-го тижня дослідження (табл. 1). Спираючись на відомості літератури [4], цей факт можна пояснити тим, що введення з лікувальною метою ацетилцистеїну щурам із ХГП сприяє виведенню імунних комплексів з організму. Варто також наголосити, що вміст ЦІК у дослідній та референтній групах вірогідно не відрізняється впродовж дослідження (Р > 0,05).
Отже, за результатами даного фрагменту комплексного дослідження є підстави стверджувати, що застосування ацетилцистеїну суттєвим чином зменшує ступінь ендогенної інтоксикації, яка розвивається в умовах запального процесу тканин пародонту.
Надалі визначали вплив ацетилцистеїну на рівень кінцевих продуктів ПОЛ в організмі щурів із ХГП — ТБК-реактантів, що є маркерами СЕІ, оскільки вони відносяться до токсичних метаболітів, які утворюються в процесі мембранодеструкції [22]. Отримані при цьому результати (табл. 1) вказують, що вже через 2 тижні від початку моделювання ХГП рівень ТБК-реактантів у контрольній групі тварин вірогідно (Р < 0,01) в 1,3 раза перевищує аналогічний показник в інтактних тварин. У більш пізні терміни дослідження (4–8 тижнів) у цій групі тварин відзначається тенденція до зростання кількості досліджуваних продуктів ПОЛ.
При оцінці детоксикуючого впливу ацетилцистеїну на рівень ТБК-реактантів звертає увагу та обставина, що вже з 4-го тижня дослідження препарат знижує рівень кінцевих продуктів ПОЛ на 25,4–38,4 % (Р < 0,01–0,001) порівняно з контролем та не має вірогідної різниці впродовж експерименту з інтактною і референтною серіями (табл. 1).
Таким чином, застосування ацетилцистеїну знижує утворення агресивних перекисних продуктів із мембранопошкоджуючою дією, що, на нашу думку, можна розцінювати як один із механізмів детоксикуючої активності цього лікарського засобу.
Не менш важливим універсальним маркером СЕІ, що ідентифікується, є МСМ. Отримані результати (табл. 1) свідчать, що в контрольній групі (ХГП без лікування) у найбільш показові терміни дослідження (6 і 8 тижнів) рівень цього показника в 1,40 раза вищий, ніж в інтактній серії щурів (р < 0,001). Така надлишкова кількість МСМ вказує на беззаперечний розвиток ендотоксикозу за умов форми запального процесу пародонту, що моделюється, і підтверджується даними літератури [6].
Інша динаміка концентрації МСМ у щурів із ХГП спостерігається на фоні застосування ацетилцистеїну (табл. 1). Установлено, що ацетилцистеїн вірогідно (Р < 0,001) знижує продукцію МСМ (через 6 і 8 тижнів дослідження) у 1,25–1,47 раза відповідно порівняно з контрольною групою. Більше того, рівень МСМ при застосуванні ацетилцистеїну в умовах ХГП протягом експерименту не має вірогідної різниці (Р > 0,05) з показниками інтактної та референтної серій. Це свідчить про здатність ацетилцистеїну попереджати генерацію токсичних продуктів порушеного обміну білків і ліпідів, що розвиваються на тлі ХГП.
Аналіз отриманих результатів дозволяє констатувати, що концентрація МСМ віддзеркалює ступінь розвитку ендогенної інтоксикації за умов ХГП, а також здатність ацетилцистеїну гальмувати розвиток СЕІ запального генезу, що обумовлено детоксикуючими властивостями цього засобу.
Висновки
Отримані результати досліджень інтегральних індексів лейкоцитарної формули крові, а також маркерів СЕІ — МСМ та ТБК-реактантів дозволяють стверджувати, що за їх рівнями можна судити про ступінь розвитку СЕІ на тлі ХГП, а також об’єктивно оцінити ефективність застосування засобу фармакотерапії детоксикуючої дії — ацетилцистеїну.
1. Cotgreave I.A. N-acetylcysteine: pharmacological considerations and experimental and clinical applications / I.A. Cotgreave // Adv. Pharmacol. — 1997. — Vol. 38. — P. 205-227.
2. Experimental endotoxemia in humans: analysis of cytokine release and coagulation, fibrinolytic, and complement pathways / S.J. van Deventer, H.R. Buller, J.W. ten Cate [et al.] // Blood. — 1990. — Vol. 76, № 12 (December 15). — P. 2520-2526.
3. Gemmell E. Cytokines and prostaglandins in immune homeostasis and tissue destruction in periodontal disease / E. Gemmell, R.I. Marshall, G.J. Seymour // Periodontol. — 2000. — 1997 Jun. — 14. — P. 112-143.
4. Gemmell E. The role of T cells in periodontal disease: homeostasis and autoimmunity / E. Gemmell, K. Yamazaki, G.J. Seymour // Periodontol. — 2000. — 2007. — № 43. — P. 14-40.
5. Periodontal disease immunology: ‘double indemnity’ in protecting the host / J.L. Ebersole, D.R. 3rd Dawson, L.A. Morford [et al.] // Periodontol. — 2000. — 2013 Jun. — 62(1). — P. 163-202.
6. Reynolds J.J. Mechanisms of connective tissue matrix destruction in periodontitis / J.J. Reynolds, M.C. Meikle // Periodontol. — 2000. — 1997 Jun. — 14. — Р. 144-157.
7. Serhan C.N. Controlling the resolution of acute inflammation: a new genus of dual anti-inflammatory and proresolving mediators / C.N. Serhan // Journal Periodontol. — 2008 Aug. — 79(8 Suppl.). — P. 1520-1526.
8. Артюшкевич А.С. Заболевания периодонта. — М.: Медицинская литература, 2006. — 306 с.
9. Беляева Л.Е. Редокс-зависимые механизмы действия N-ацетилцистеина / Л.Е. Беляева, В.И. Шебеко, А.П. Солодков // Вестник ВГМУ. — 2008. — Том 7, № 4. — С. 1-14.
10. Липидмодифицирующий компонент в патогенетической терапии / А.П. Власов, В.Г. Крылов, Т.В. Тарасова [и др.]. — М.: Наука, 2008. — 374 с.
11. Гланц С. Медико-биологическая статистика / С. Гланц; пер с англ. — М.: Практика, 1999. — 459 с.
12. Громашевская Л.Л. Метаболическая интоксикация в патогенезе и диагностике патологических процессов / Л.Л. Громашевская // Лабораторная диагностика. — 2006. — Т. 35, № 1. — С. 3-13.
13. Доклинические исследования лекарственных средств: Методические рекомендации / Под ред. член.-корр. АМН Украины А.В. Стефанова. — К.: Авиценна, 2002. — 567 c.
14. Иванова Ж.В. Распространенность и интенсивность и особенности клинического течения заболевания пародонта у лиц молодого возраста / Ж.В. Иванова // Современная стоматология. — 2008. — № 1. — С. 15-21.
15. Иммунный статус, принципы его коррекции и оценки иммунных нарушений: Монография / В.Г. Передерий, А.М. Земсков, Н.Г. Бычкова, В.М. Земсков. — К.: Здоров’я, 1995. — 211 с.
16. Исследование системы крови в клинической практике / Под ред. Г.И. Казинца и В.А. Монрова. — М.: Триада-Х, 1997. — 301 с.
17. Карякина Е.В. Молекулы средней массы как интегральный показатель метаболических нарушений: обзор литературы / Е.В. Карякина, С.В. Белова // Клиническая и лабораторная диагностика. — 2004. — № 3. — С. 3-8.
18. Клинико-патогенетические подходы к совершенствованию терапии пародонтита у больных хроническими инфекционными заболеваниями / Л.А. Соболева, Е.Н. Блинникова, Р.Р. Сякин и др. // Вестник Санкт-Петербургской государственной медицинской академии им. Мечникова. — 2009. — № 1. — С. 101-104.
19. Клиническая гематология / Даштаянц Г.А. — К., 1978. — 230 с.
20. Лукьянчук В.Д. Влияние ацетилцистеина на динамику состояния прооксидантно-антиоксидантного гомеостаза при хроническом генерализованном пародонтите / В.Д. Лукьянчук, Д.А. Гордийчук // Загальна патологія та патологічна фізіологія. — 2011. — Т. 6 (№ 4). — С. 129-136.
21. Метод определения малонового диальдегида с помощью тио–барбитуровой кислоты // Современные методы в биохимии / Под ред. Ореховича В.И. — М.: Медицина, 1977. — С. 57-59.
22. Невельский М.Я. Вільнорадикальне окислення — ведучий фактор в стоматологічній патології та обґрунтування методів його корекції / М.Я. Невельский // Вестник проблем биологии и медицины. — 1998. — № 1. — С. 17-24.
23. Опарин С.В. Применение мексидола в композиции лекарственных препаратов, иммобилизированных на желатиновых шинах, для местной активной патогенетической терапии начальных стадий воспалительных заболеваний пародонта / С.В. Опарин // Бюллетень экспериментальной биологии и медицины. — 2006. — Прил. 1. — С. 209.
24. Патент на полезную модель 10110, Украина, МПК G09В 23/28. Способ моделирования хронического генерализованного пародонтита / В.Д. Лукьянчук, О.О. Шпулина. — № 20041210839; Заявл. 27.12.2004; Опубл. 15.11.05, Бюл. № 11. — 10 с.
25. Рациональная фармакотерапия / Под ред. Г.М. Барера, Е.В. Зорян, В.С. Агапова [и др.]. — М.: Литтерра, 2006. — 119 с.
26. Синдром ендогенної інтоксикації: етіологія, патогенез, клініка, фармакотерапія (методичні рекомендації) [Лук’янчук В.Д., Шейман Б.С., Рисухіна Н.В. та ін.] / Під ред. д.м.н., проф. Лук’янчука В.Д. — Київ; Луганськ, 2011. — 46 с.
27. Соколова Н.А. Антиоксиданты — новая эра в стоматологии / Н.А. Соколова // Дискус Дентал. — 2004. — С. 55.
28. Сперанский И.И. Общий анализ крови — все ли его возможности исчерпаны? Интегральные индексы интоксикации как критерии оценки тяжести течения эндогенной интоксикации, ее осложнений и эффективности проводимого лечения / И.И. Сперанский, Г.Е. Самойленко, М.В. Лобачева [и др.] // Острые и неотложные состояния в практике врача. — 2009. — № 6 (19). — С. 37-45.
29. Способ определения «средних молекул» / В.В. Николайчик, В.В. Моин, В.В. Кирковский [и др.] // Лабораторное дело. — 1991. — № 10. — С. 13-18.
30. Чайковская И.В. Влияние маркеров эндогенной интоксикации на патогенез генерализованного пародонтита / И.В. Чайковская, Л.В. Яворская // Вісник ВДНЗУ «Українська медична стоматологічна академія». — 2012. — Т. 12, № 4 (40). — С. 63-67.
31. Черний В.И. Нарушения иммунитета при критических состояниях: особенности диагностики / В.И. Черний, А.Н. Нестеренко // Внутренняя медицина. — 2007. — № 2 (2). — С. 12-15.
32. Чумакова Ю.Г. Генерализованный пародонтит: структура нуждаемости в специализированной стоматологической помощи / Ю.Г. Чумакова // Вісник стоматології. — 2007. — № 6. — С. 24-31.
33. Шабалов Н.П. Гетерогенность системного воспалительного ответа при неонатальном сепсисе / Н.П. Шабалов, Д.О. Иванов, Н.Н. Шабалова // Медицинский академический журнал. — 2001. — Т. 1, № 3. — С. 81-90.

/23/23.jpg)