Газета «Новости медицины и фармации» Гастроэнтерология (493) 2014 (тематический номер)
Вернуться к номеру
Современные подходы в терапии лямблиоза и H.pylori-инфекции у детей
Авторы: Галина Бут
Рубрики: Гастроэнтерология
Разделы: Медицинские форумы
Версия для печати
Статья опубликована на с. 28-31
 27–28 ноября 2013 года в г. Киеве в центральном зале Центра культуры и искусств СБУ состоялся научно–практический конгресс с международным участием «Актуальные вопросы детской гастроэнтерологии». В рамках мероприятия состоялось пленарное заседание «Вопросы фармакотерапии в детской гастроэнтерологии». С докладом «Диагностика и лечение лямблиоза» выступила заведующая кафедрой медицинской паразитологии и тропических заболеваний ХМАПО, главный внештатный паразитолог МЗ, доктор медицинских наук, профессор Е.И. Бодня.
27–28 ноября 2013 года в г. Киеве в центральном зале Центра культуры и искусств СБУ состоялся научно–практический конгресс с международным участием «Актуальные вопросы детской гастроэнтерологии». В рамках мероприятия состоялось пленарное заседание «Вопросы фармакотерапии в детской гастроэнтерологии». С докладом «Диагностика и лечение лямблиоза» выступила заведующая кафедрой медицинской паразитологии и тропических заболеваний ХМАПО, главный внештатный паразитолог МЗ, доктор медицинских наук, профессор Е.И. Бодня.
Лямблиоз — это паразитарное заболевание, при котором его возбудитель (лямблия)* колонизирует все полости тела человека. Лямблии распространены повсеместно, поражаемость ими крайне высокая. Они распространены в тех местах, где социальные условия и образ жизни человека способствуют их передаче. Речь идет в первую очередь о детских коллективах, где не всегда соблюдаются правила личной гигиены.
Еще недавно, 5–10 лет назад, считалось, что лямблии являются условно-патогенными паразитами, которые при определенных условиях приобретают патогенные свойства, а вызываемые ими заболевания имеют тяжелые клинические проявления. В организме человека лямблиоз может протекать не только в форме носительства, но и вызывать вторичный иммунодефицит. Лямблиоз усугубляет эпидемически неблагоприятную ситуацию по кишечным дисбиозам и ухудшает эффективность вакцинопрофилактики. Одним из наиболее проблемных вопросов современной педиатрии является аллергизация с развитием нейродермитов и экзем, которые ассоциируются с паразитированием простейших в детском организме, в первую очередь лямблий.
На сегодняшний день рост числа больных лямблиозом обусловлен не столько улучшением выявляемости заболевания, сколько ухудшением качества водообеспечения. В настоящее время считается, что лямблии — причина около 20 острых кишечных заболеваний, фактором передачи которых является вода. По данным ВОЗ, ежегодно в мире регистрируется около 500 млн случаев заболевания лямблиозом.
Giardia lamblia — практически единственное простейшее, которое обитает в человеческом организме в просвете тонкой кишки. Лямблии существуют в двух отдельных морфологических формах — цисты и трофозоиты, причем одна циста дает два первичных трофозоита, которые очень быстро делятся, колонизируя всю поверхность слизистой оболочки тонкой кишки. Они очень устойчивы к действию факторов внешней среды, а также кислот и щелочей. Их инактивация возможна только при кипячении. Способы заражения лямблиозом — фекально-оральный и контактный, наиболее частым источником является вода. Для заражения лямблиозом достаточно 10 цист. От больного человека во внешнюю среду выделяется до 12 млн цист в 1 г фекалий — этого достаточно для заражения всего коллектива, в котором находится такой больной. Следует подчеркнуть, что при выявлении больного лямблиозом его следует немедленно изолировать. В детских дошкольных учреждениях число зараженных может достигать 70 %, также могут формироваться семейные очаги.
При лямблиозе происходит поражение микроструктуры тонкого кишечника, хотя простейшие не внедряются внутрь слизистой оболочки. Происходит уплощение ворсинок, гипертрофия крипт, уплотнение мононуклеарного инфильтрата в подслизистом слое. Одновременное заселение тощей кишки лямблиями и энтеробактериями приводит к поражению кишечных эпителиальных клеток щеточной каймы, а в дальнейшем — к развитию синдрома мальабсорбции.
Вследствие бурного размножения лямблий в кишечнике, особенно при нерациональном питании, резко изменяется микробный пейзаж кишечника:
1) появляются микроорганизмы (Helicobacter pylori) и грибы, которых не бывает в кишечнике в обычных условиях и которые, в свою очередь, стимулируют процесс размножения простейших;
2) резко снижается количество кишечной палочки, бифидо-, лактобактерий, обеспечивающих физиологический процесс пищеварения и всасывания.
На сегодняшний день доказано поражение поджелудочной железы лямблиями, в клинической практике довольно часто встречаются больные с клиническими проявлениями билиарно-панкреатической формы лямблиоза. По данным ВОЗ, при лямблиозе частота носительства — 20 %, 55 % составляют латентные формы заболевания, когда имеющиеся жалобы у пациента не ассоциируются с лямблиозом и поэтому не являются поводом к обращению за медицинской помощью. Удельный вес инфицирования лямблиозом с явно выраженной клинической симптоматикой составляет 22 %. По данным Американской ассоциации педиатров, у 80 % инфицированных обнаруживаются клинические проявления лямблиоза с разной степенью тяжести.
На основании личных результатов исследования и данных литературы можно представить общие и частные механизмы патогенного действия простейших:
— механическое повреждение слизистой;
— раздражение нервных окончаний слизистой и стимуляция патологических рефлексов, выделение нейропептидов;
— воспаление слизистой оболочки (высвобождение протеолитических ферментов, гиалуронидазы);
— нарушение процессов пищеварения, всасывания;
— развитие дисбиоза кишечника;
— формирование гиповитаминоза и гипоферментоза (лактазы, инвертазы и др.);
— сенсибилизация организма хозяина антигенными субстанциями;
— развитие аллергических и аутоаллергических реакций в органах и тканях (в том числе в слизистой кишечника);
— усугубление местной и общей иммуносупрессии (метаболиты паразитов обладают иммуносупрессивным действием);
— формирование эндогенной интоксикации;
— потенцирование аллергических реакций на продукты питания (непищевая аллергия);
— задержка роста, развития нередко с потерей массы тела у детей.
Наслоение лямблиоза на внутрибольничную инфекцию любой этиологии увеличивает сроки выздоровления.
Диагностика лямблиоза основывается прежде всего на учете клинических проявлений заболевания, обязательной также является лабораторная диагностика с выделением возбудителя или цист в фекалиях или дуоденальном содержимом. В некоторых случаях лямблии выявить очень трудно, так как существуют «немые» промежутки, когда цисты не выделяются с фекалиями. Необходимо учитывать этот факт и при получении отрицательного результата повторять исследование через 2 недели. Признано высокоинформативным исследование кала на антигены лямблий.
Лечение заболевания длительное, но появление в Украине новых препаратов позволило сократить его сроки и оптимизировать результаты. Лечение должно быть комплексным, направленным на ликвидацию эндотоксикоза, механическое удаление лямблий, улучшение ферментативной активности кишечника и коррекцию иммунологической защиты. Его основа — специфическая терапия, потому что патогенетическая терапия направлена на устранение клинических проявлений заболевания и не влияет на возбудителя. При выборе препарата для лечения лямблиоза у детей наряду с эффективностью главным требованием является безопасность. Рекомендуется также назначение диеты, препятствующей размножению лямблий (ограничение употребления углеводов). Необходимо назначать желчегонные препараты, энтеросорбенты, ферментотерапию и антигистаминные препараты. Только применение такого комплекса будет гарантировать успех лечения и отсутствие осложнений.
В настоящее время препаратом, обеспечивающим высокую эффективность специфической терапии, является Макмирор (нифуратель). Его применение — новый терапевтический подход, гарантирующий быстрый, надежный и безопасный терапевтический эффект.
Макмирор (нифуратель) обладает широким спектром антипротозойного и антимикробного действия.
Препарат эффективен в отношении Trichomonas vaginalis, Gardnerella vaginalis, анаэробов Enterococcus faecalis, Enterococcus faecium, Staphylococcus aureus, Bacillus subtilis, Escherichia coli, Shigella flexneri, Shigella sonnei, Salmonella typhi, Salmonella typhimurium, Salmonella enteritidis, Klebsiella spp., Enterobacter spp., Serratia spp., Citrobacter spp., Morganella spp., Rettgerella spp., Pragia fontium, Budvicia aquatica, Rachnella aquatilis, Acinetobacter spp., прочих атипичных энтеробактерий, а также простейших (амебы, лямблии) и др.
Кроме высокой эффективности, показана безопасность и хорошая переносимость нифурателя как у взрослых, так и у детей.
К преимуществам Макмирора следует отнести отсутствие резистентности к нему, практически полную элиминацию почками без вовлечения дезинтоксикационных резервов печени, способность восстанавливать нормальный биоценоз кишечника благодаря стимуляции роста лакто– и бифидобактерий. Период полувыведения препарата достаточно продолжительный — это позволяет применять его 2 раза в сутки. Взрослым назначают по 400 мг 2–3 раза в сутки, детям — из расчета по 15 мг/кг 2 раза в сутки, курс лечения — в среднем до 7 дней. Контрольное обследование, как правило, проводят через 3 и 6 недель после проведения специфической терапии. После применения нифурателя через 3 недели не обнаруживали вегетативных форм и цист лямблий.
На сегодняшний день Макмирор включен в «Протокол лечения детей с заболеваниями органов пищеварения» (Приказ МЗУ № 59), что еще раз подтверждает его эффективность, безопасность и переносимость в лечении не только острых, но и хронических форм лямблиоза.
 Доклад «Современные схемы лечения НР-инфекции у детей: обзор клинических протоколов медицинской помощи детям с хроническим гастритом, хроническим гастродуоденитом и язвенной болезнью желудка и двенадцатиперстной кишки» представил заведующий отделением проблем питания и соматических заболеваний детей раннего возраста ГУ «ИПАГ НАМН Украины», главный внештатный детский гастроэнтеролог МЗ Украины, доктор медицинских наук, профессор О.Г. Шадрин.
Доклад «Современные схемы лечения НР-инфекции у детей: обзор клинических протоколов медицинской помощи детям с хроническим гастритом, хроническим гастродуоденитом и язвенной болезнью желудка и двенадцатиперстной кишки» представил заведующий отделением проблем питания и соматических заболеваний детей раннего возраста ГУ «ИПАГ НАМН Украины», главный внештатный детский гастроэнтеролог МЗ Украины, доктор медицинских наук, профессор О.Г. Шадрин.
Helicobacter pylori изучается необычайно интенсивно: компьютерная сеть PubMed содержит более 21 тыс. упоминаний. Лишь кишечной палочке посвящено большее число публикаций по бактериологии.
«Проблемы важнее решения. Решения могут устареть, а проблемы остаются…» (Нильс Бор)
В настоящее время существуют различные эпидемио–логические модели НР-инфекции, они отличаются в развитых и развивающихся странах. По имеющимся данным, детское население наиболее быстро инфицируется в развивающихся странах, а длительное персистирование НР-инфекции повышает риск развития рака желудка. Из документов, согласно которым проводится эрадикационная терапия, на сегодняшний день самым последним является Совместное соглашение Европейской ассоциации педиатров-гастроэнтерологов и нутрициологов и Североамериканской ассоциации педиатров-гастроэнтерологов и нутрициологов.
Основные протоколы ведения Helicobacter pylori-инфекции у детей в мире:
— Current concepts in the management of Helicobacter pylori infection: the Maastricht III Consensus Report;
— Helicobacter pylori infection in children: ESPGHAN/NASPGHAN Guidelines (2010);
— Evidence-based Guidelines from ESPGHAN and NASPGHAN for Helicobacter pylori infection in children (2011).
Согласно этому документу, основной целью проведения клинического обследования является не выявление H.pylori, а определение основных причин и симптомов заболевания. Не рекомендуется обследование на хеликобактерную инфекцию у детей с функциональными болями в брюшной полости. Обследование и лечение НР-инфекции показано при наличии у родственников первой линии рака желудка и железодефицитной анемии неизвестной этиологии.
Guidelines from ESPGHAN and NASPGHAN for Helicobacter pylori infection in children (2011)
Кто должен быть проверен?
— Основная цель клинического исследования желудочно–кишечных симптомов — определение основных причин заболевания, а не только наличия инфекции Helicobacter pylori.
— Диагностическое исследование на определение H.pylori–инфекции не рекомендуется проводить у детей с функциональными болями в животе.
— У детей с родственниками первой степени, имеющими рак желудка, а также у детей с рефрактерной железодефицитной анемией может проводиться исследование на определение H.pylori–инфекции.
Для диагностики НР-инфекции золотым стандартом остается биопсия при проведении эндоскопического исследования. У детей достаточным считается использование стул-теста и дыхательного теста — неинвазивных и достаточно точных методов диагностики НР-инфекции.
Guidelines from ESPGHAN and NASPGHAN for Helicobacter pylori infection in children (2011)
Какие исследования необходимо проводить?
— Для диагностики хеликобактерной инфекции во время ЭГДС рекомендуется проводить биопсию желудка (антрального отдела и тела) для выявления гистопатологии.
— Иммуноферментный анализ для определения H.pylori-антигена в кале и 13С-уреазный дыхательный тест — надежное неинвазивное исследование для определения эрадикации H.pylori.
— Рекомендуется подождать не менее 2 недель после прекращения терапии ингибиторами протонной помпы и 4 недель после прекращения приема антибиотиков для проведения исследований (уреазный дыхательный тест, исследование кала) для определения H.pylori.
Guidelines from ESPGHAN and NASPGHAN for Helicobacter pylori infection in children (2011)
Кого лечить?
— При подтверждении H.pylori-позитивной язвенной болезни необходимо начать эрадикационную терапию.
— Когда H.pylori обнаруживается методом гистологии при отсутствии язвенной болезни, может быть рассмотрен вопрос о начале антихеликобактерной терапии.
— Стратегия «исследование и лечение» не рекомендуется.
У детей необходимо определять наличие антибиотикорезистентности H.pylori, а эффективность проведения эрадикационной терапии рекомендуется оценивать через 4–8 недель после ее завершения.
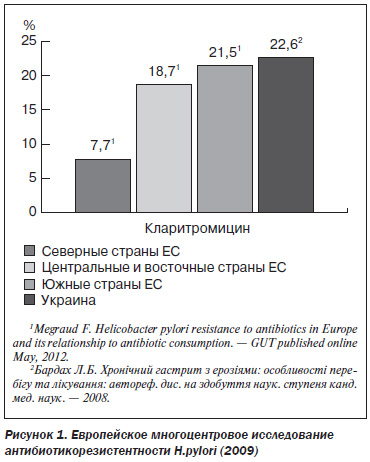
Классической в настоящее время признана схема тройной терапии: ингибитор (омепразол) + амоксициллин + кларитромицин, однако во всем мире сегодня врачи говорят о том, что ее эрадикационный потенциал существенно снизился по сравнению с прошлыми годами. Во многом это связано с формированием антибиотикорезистентных штаммов H.pylori. Так, в странах Центральной и Восточной Европы, в том числе и в Украине, резистентность H.pylori к кларитромицину превышает 20 %, что свидетельствует о снижении эффективности эрадикационных схем с включением кларитромицина.
В целом на сегодняшний день резистентность H.pylori к кларитромицину у детей гораздо выше, чем у взрослых.
Протоколы ведения H.pylori-инфекции у детей в Украине
1. Уніфіковані клінічні протоколи медичної допомоги дітям із захворюваннями органів травлення (Наказ МОЗ України № 59 від 29.01.2013):
— Уніфікований клінічний протокол медичної допомоги дітям із хронічним гастритом.
— Уніфікований клінічний протокол медичної допомоги дітям із хронічним гастродуоденітом.
— Уніфікований клінічний протокол медичної допомоги дітям із виразковою хворобою шлунка та дванадцятипалої кишки.
2. Додаток 2. Сучасні схеми лікування H.pylori-інфекції в дітей.
В результате проведенных исследований, в которых проанализировано применение антихеликобактерных схем у детей, был подготовлен Приказ № 59. В нем приведены современные ориентировочные схемы антихеликобактерной терапии, включающие коллоидный субцитрат висмута, амоксициллин и нифуратель (Макмирор).
Однонедельная тройная терапия препаратом висмута (преимущественно для детей до 12 лет):
1. Коллоидный субцитрат висмута + амоксициллин (рокситромицин) или кларитромицин (азитромицин) + нифуратель (фуразолидон).
2. Коллоидный субцитрат висмута + амоксициллин (рокситромицин)/кларитромицин (азитромицин) + фамотидин (ранитидин).
Однонедельная тройная терапия с блокаторами Н+/К+-АТФазы (преимущественно детям после 12 лет):
1. Омепразол (пантопразол) + амоксициллин (рокситромицин) или кларитромицин (азитромицин) + нифуратель (фуразолидон).
2. Омепразол (пантопразол) + амоксициллин (рокситромицин)/кларитромицин (азитромицин) + коллоидный субцитрат висмута.
Однонедельная квадротерапия (терапия усиления 2-го звена, преимущественно детям после 12 лет):
Коллоидный субцитрат висмута + омепразол (пантопразол) + амоксициллин (рокситромицин) или кларитромицин (азитромицин) + нифуратель (фуразолидон).
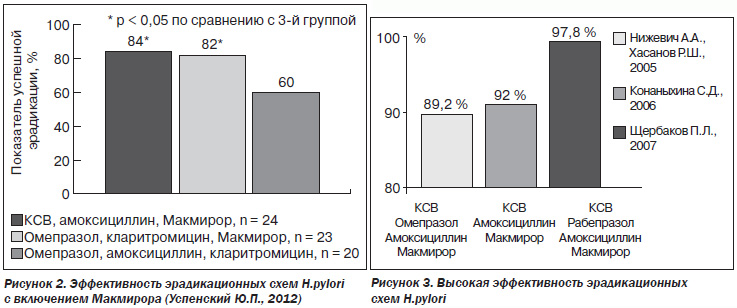
Применение коллоидного субцитрата висмута обеспечивает создание защитной пленки на поверхности эрозии, улучшает регенерацию слизистой оболочки, оказывает противовоспалительный эффект, стимулирует выработку желудочного сока. Ингибиторы протонной помпы также обладают целым рядом положительных свойств, благодаря которым уменьшаются сроки проведения эрадикации H.pylori вследствие пролонгации действия антибиотиков, угнетения скорости деления H.pylori, которая становится более уязвимой к воздействию эрадикационной терапии. Нифуратель, таблетки 200 мг — оригинальный препарат, синтезированный компанией Polichem (Италия), обладает широким спектром антибактериального и антипротозойного действия. Эффективен также против грибков рода Candida. На сегодняшний день практически отсутствует резистентность H.pylori к нифурателю. В исследованиях с нифурателем показаны преимущества его включения в вышеприведенные схемы антихеликобактерной терапии. Например, при квадротерапии эффективность эрадикационных схем с включением Макмирора достигает 97,8 %, а в терапии с препаратами висмута и амоксициллина — 92 % (рис. 3). Такая же высокая эффективность схем антихеликобактерной терапии с включеним Макмирора показана в исследованиях проф. Успенского Ю.П.: замена кларитромицина на нифуратель в схемах антихеликобактерной терапии позволила значительно повысить эрадикационный эффект (рис. 2).
Таким образом, имеющиеся на сегодняшний день данные убедительно свидетельствуют о том, что использование Макмирора (нифурателя) в схемах эрадикационной терапии позволяет наиболее эффективно проводить эрадикацию H.pylori у детей и подростков.